海泡石负载离子液体制备高热稳定性抗菌剂
(中国科学院过程工程研究所多相复杂系统国家重点实验室, 北京100190)
随着我国民众对生物安全重要性认识的不断提高,抗菌材料在减少疾病和应对突发生物污染事件中的作用被日益凸显出来,常见的抗菌材料分为有机和无机2类。有机抗菌材料包括天然抗菌化合物及香醛类、 氯酚类、 季铵类、 咪唑类合成化合物、 乙内酰脲类、 聚胍类、 吡啶硫酮类等[1-10],其抗菌谱广、 起效迅速、 灭菌能力强大,但往往耐热性能不佳,故很难用于塑料、粉末涂料等需要热加工或热固化的领域; 无机抗菌材料主要包括银系抗菌材料[11-13]、 锌系抗菌材料[14]、 铜系抗菌材料[15]和二氧化钛类抗菌材料[16],该类抗菌材料有耐热性好的优点,相比于有机抗菌剂,作用速度较慢,杀菌效能略低。在发挥有机抗菌材料高效的灭菌性能的基础上,通过有机、 无机复合有望获得兼具高效抑菌性和耐热性的新型抗菌材料。本团队曾经将三氯生负载于SiO2之中获得了耐热性和耐溶出性能均较好的抗菌材料[2-3],然而SiO2的前驱体为昂贵的硅酸四乙酯,难以工业化制备。另外,由于三氯生具有亲脂性、耐久性和生物积累性,已经被很多国家列为限用甚至禁用抗菌剂[17]。
咪唑类离子液体因具有独特的抗菌活性引起了相关领域研究人员的广泛关注[6,18-19],分子由强正电性的咪唑头基和长链疏水烷基构成,咪唑头基通过静电作用强烈吸附于带负电的细菌细胞膜上,同时其长链疏水烷基可以刺入细胞膜使细菌破裂死亡[19]。此外, 相比于具有类似抗菌机理的季铵盐抗菌剂,如CTAB,离子液体咪唑头基的双氮五元杂环的热稳定性显著优于季铵头基,因此咪唑类离子液体是制备高热稳定性抗菌剂的优良选择。根据本团队以前的研究经验,将有机抗菌剂与无机颗粒相复合是提高抗菌热稳定性的有效途径,同时因为咪唑类离子液体和天然无机矿物材料复合的研究相对较少,所以本团队考虑将咪唑类离子液体和具有天然孔道的矿物材料相复合,以期获得具有良好热稳定性的新型有机-无机杂化抗菌材料。海泡石是一种纤维状多孔富镁质的硅酸盐黏土矿物,具有沿着纤维径向的丰富孔道结构,耐热性好,价格低廉,非常适合与咪唑类离子液体相复合而提高后者的热稳定性。
1 实验
1.1 主要试剂材料和仪器设备
材料:海泡石(河北省易县海泡石开发有限公司);盐酸(氯化氢质量分数为30%,国药集团化学试剂有限公司);二次去离子水(电阻为18.2 MΩ)。
仪器设备: Nova2000e型孔径比表面分析仪(美国Quantachrome公司); Philips PANanalytical X’ Pert Pro型X射线衍射分析仪(XRD, 荷兰Philip公司); Netzsch Sta 499 F3型热重分析仪(TGA, 德国耐驰公司); SU8020 型扫描电子显微镜(日本HITACHI公司); Nabertherm LH30/13型马弗炉(德国纳博热公司)。
1.2 方法
1.2.1 样品制备
海泡石粉末在质量分数为1%的稀盐酸中,液固质量比为1∶6的条件下酸洗后离心洗涤,在温度为90 ℃条件下烘干,备用。离子液体(十四烷基-3-甲基咪唑溴盐)按照文献[20]合成,文中命名为IL。
取烘干后的海泡石2 g, 称取不同质量的IL溶于水中, 溶液体积控制为2.2 mL, 将溶有IL的溶液和海泡石粉末混合, 按照文献[21]的方法进行干法浸渍,实验中IL的负载量选择0.1、 0.2、 0.3、 0.4、 0.5、 0.7、 0.9 g等7个水平,分别对应IL的负载质量分数为4.8%、 9.1%、 13.0%、 16.7%、 20.0%、 25.9%、 31.0%, 7个样品分别命名为sep-IL-1—sep-IL-7, 不负载IL的空白海泡石样品命名为sep-IL-0。 由于IL溶解度的限制, sep-IL-5—sep-IL-7样品中IL需要在热水中溶解,负载结束后各样品在温度为90 ℃的条件下烘干过夜,研磨后封存备用。样品的耐热性能在马弗炉中检测,实验中灼烧温度选择250、 300、 350 ℃ 3个水平,首先将长方形瓷舟在马弗炉中灼烧1 h,保证瓷舟温度完全达到灼烧温度,然后立刻打开马弗炉炉门,将0.1 g负载有IL的海泡石样品放入瓷舟中,然后关闭炉门,开始计时,灼烧过程持续1 h,而后取出瓷舟,将灼烧样品保存于自封袋中预备检测其抑菌性能。
1.2.2 样品分析
采用比表面分析仪测定海泡石样品的比表面积和孔分布信息; 采用X射线衍射分析仪分析样品的X射线衍射图(测试条件: Cu Kα辐射, Ni滤波, 管电压为40 kV, 管电流为30 mA, 波长为0.154 18 nm, 2θ=5°~90°, 步长为0.02°); 采用热重分析仪表征样品的加热失质量情况, 升温速率为5 ℃/min, 气氛为空气; 采用扫描电子显微镜在加速电压为15 kV、 电流为10 mA条件下观察样品颗粒形貌, 并采用能谱扫描的方法分析其表面元素组成。 需要测试抗菌性能的粉末样品取10 mg,在压力为14 MPa下压片, 样片直径5.5 mm, 每个样品压制2个平行样片, 采用革兰氏阳性芽孢杆菌和革兰氏阴性大肠杆菌为测试菌种, 通过抑菌圈法研究抗菌能力, 芽孢杆菌的菌液浓度每毫升细菌群落数为108, 大肠杆菌的菌液浓度每毫升细菌群落数为109, 依照中国人民共和国卫生部《消毒技术规范(2017版)》[22]的方法进行抑菌环测试。
2 结果和讨论
2.1 海泡石样品的比表面分析

(a)吸附等温线

(b)孔径分布曲线(DFT方法)图1 空白海泡石(预处理前后)和sep-IL-7的孔结构分析结果
对空白海泡石样品sep-IL-0和样品sep-IL-7进行了低温氮吸附分析以表征孔结构信息, 结果如图1所示。 样品sep-IL-0分别在不预处理的情况下和抽真空、 温度为200 ℃、 预处理2 h的情况下进行分析, 因为样品sep-IL-7负载有IL, 在不预处理的情况下进行分析(以免IL逸出污染设备)所得结果如图1(a)所示。 可知sep-IL-0在预处理和不预处理2种情况下吸附等温线的形状比较类似, 但预处理后的样品在整个相对压力范围内吸附量均更高, 而样品sep-IL-7的吸附等温线仅在相对压力较大(p/p0=0.8~1.0)时有较微弱吸附。 利用密度泛函理论(density function theory, DFT)方法分析样品的孔分布如图1(b)所示。 由图可知, 对于sep-IL-0而言, 在大于2 nm的孔径范围内样品是否前处理几乎不影响其孔分布曲线形状, 但是预处理使sep-IL-0在1.6 nm附近的孔容大大增加, 经过预处理的海泡石样品的BET比表面积为238.7 m2/g, 而未经脱水前处理的样品的BET比表面积仅为114.8 m2/g, 说明空白海泡石具有大量孔径为1.6 nm左右的微细亲水孔道, 这些孔道极易吸收空气中的水分而导致其孔容和比表面积显著减小。 由图1(b)中样品sep-IL-7的孔分布曲线可知, 负载IL后样品孔径为1.6 nm附近的微孔完全消失, 甚至孔径为8 nm以下的孔道完全消失, 在大于8 nm的范围内的孔道的孔容有所减小, 样品的BET比表面积降低至20.1 m2/g, 说明在负载过程中IL成功进入海泡石的微孔孔道中, 甚至将其完全填充, 导致负载样品失去了全部的微孔和一部分介孔, 比表面积也剧烈减小, 可以推断: 由于IL分子和海泡石微孔(介孔)壁面具有强烈的相互作用, IL分子很可能优先填充海泡石的微孔并铺展在孔道内壁面上, 因此海泡石是IL的优良负载材料, 二者之间的强相互作用很可能为材料带来更好的热稳定性。
2.2 负载IL海泡石的XRD分析
将不同IL负载量的海泡石样品以及纯IL进行了XRD分析,结果如图2所示。由图可知,样品sep-IL-0由海泡石和少量滑石组成, 其他各负载IL的样品均表现出和sep-IL-0相同的XRD衍射峰,纯IL的XRD衍射峰在各样品中均没有出现,原因很可能是因为IL的分子经负载后完全铺展并粘附于海泡石微观孔道内壁,已经不再象纯离子液体一样在室温下发生成盐结晶过程,因此即使IL负载量为31%的样品sep-IL-7依然没有表现出室温下纯离子液体的XRD衍射峰。在IL的负载过程中,IL以溶液的形式进入海泡石孔道,在随后的烘干过程中,孔道内的IL并没有因为水分脱除而发生自身的结晶,原因可能在于酸洗后的海泡石孔道内表面存在大量活性硅酸表面,在中性条件下表现出负电性,很容易与IL正电性的咪唑头基发生静电结合,再次证明海泡石是咪唑类离子液体的优良负载材料。由于IL在水中的溶解度限制,因此实验没有尝试更高的IL负载量。鉴于各样品中IL都在海泡石样品中均匀分散,后面的测试重点关注IL负载量较高的样品。
2.3 负载IL海泡石的热重分析
为了表征各个样品的热稳定性,对纯IL和各样品sep-IL-3—7进行了空气气氛下的热重分析,其分析结果如图3所示。从分析结果可知,纯IL在温度为50~250 ℃缓慢失质量,这是因为IL吸附的水分在加热条件下不断失去,IL在温度为200 ℃开始快速分解挥发,在温度为300 ℃几乎彻底分解完毕,这是因为其有机分子在空气条件下氧化、 分解甚至闪燃导致的剧烈失质量。 空白海泡石在50~650 ℃的温度范围内不断缓慢失质量,这源于其丰富的孔道内的吸附水和结合水不断因加热而释放排出,导致平缓的失质量曲线。负载IL的各样品的显著失质量温度在250 ℃左右,在温度为350 ℃时各样品才进入相对平缓的失质量状态,因此可以推断,海泡石中负载的IL的热分解温度有所提高,根据该热重结果,在样品热稳定分析时选择250、 300和350 ℃ 3个灼烧温度。
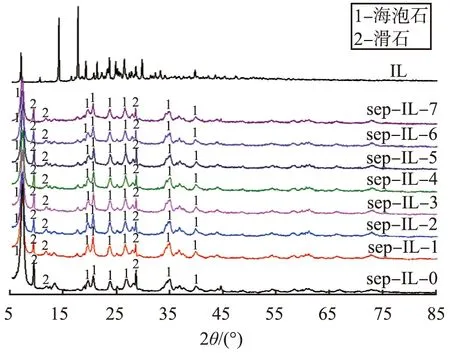
图2 不同离子液体负载量下海泡石样品的XRD衍射谱图Fig.2 XRD patterns of sepiolite samples with various ionic liquid doping amount
负载IL的海泡石样品在50~200 ℃温度范围的失质量小于纯海泡石和纯离子液体的,其原因很可能在于IL的亲水咪唑头基和海泡石孔道内壁紧密结合,其另一侧的疏水烷基长链减小了海泡石孔道对空气中水分子的吸附,因此负载IL的海泡石各样品在50~200 ℃的温度范围内的脱水失质量有所减弱,这也一定程度上证明了IL分子与海泡石孔道内壁的硅酸位点的结合较为牢固。

图3 不同离子液体负载量下海泡石样品的热重分析Fig.3 Thermogravimetric analysis results of sepiolite samples with various ionic liquid doping amount
2.4 负载IL海泡石的扫描电镜和能谱分析
对没有负载IL的海泡石样品sep-IL-0和IL负载最大的样品sep-IL-7进行了扫描电子显微镜分析,结果如图4所示。由测试结果可知,空白海泡石样品sep-IL-0和sep-IL-7的颗粒形貌相同,均为长度为0.8~1 μm、 直径为50~100 nm的棒状或纤维状颗粒,形状符合常见的海泡石棒束状的样式,可知IL的添加没有改变海泡石的形貌,说明IL分子易于在海泡石颗粒表面或其内部孔道壁面上铺展,所以海泡石的颗粒形状不变,同时负载样品中没有IL颗粒单独存在。

(a)sep-IL-0

(b)sep-IL-7图4 样品sep-IL-0和sep-IL-7的SEM图像
对样品sep-IL-7进行了能谱分析,结果如图5所示。对sep-IL-7进行能谱扫描的颗粒形貌如图5(a)所示。 由图可知,视野中sep-IL-7为一簇棒束状海泡石颗粒无规堆积而成的团粒。针对该团粒的能谱扫描结果如图5(b)—(f)所示,分别对应于Mg、 O、 Si、 N和Br 5个元素的扫描结果,由于海泡石为纤维状的硅酸镁颗粒,因此其元素扫描结果中Mg、 O、 Si 3种元素的强度很高,而且非常均匀,然而扫描结果中N元素的分布非常稀散(见图5(e)), 同时Br元素的分布明显多于N元素(见图5(f)), N和Br的分布都很均匀,没有局部富集和缺失的现象发生;从表面元素含量的结果可知:N元素的质量分数低于0.004%,而Br元素的质量分数为2.68%。从IL的分子结构来看,每个分子含有2个N原子和1个Br原子,考虑到Br和N的原子量差异,表面质量占比为2.68%的Br原子对应的N原子质量占比应该为0.94%。IL负载于海泡石内时N元素实际的能谱扫描丰度结果明显低于Br元素丰度下N元素相应的结果,原因很可能在于IL的2个N原子均在显正电的咪唑环上,该正电的咪唑环和海泡石显负电的硅酸表面结合强烈,导致IL分子的咪唑环倾向于钻进海泡石平行于c轴(平行于海泡石纤维轴向的晶轴)的孔道内部,因此暴露在颗粒表面的N原子较少。同时,IL的Br-因为受到硅酸表面的静电推斥而倾向于留在孔道外,很可能与孔道中置换出的Mg2+相结合,所以样品的表面元素中Br元素的相对含量明显高于N元素的。以上分析结果证实,IL分子易于受静电引力的作用而自发进入海泡石孔内部,并形成均匀的分散状态,这和XRD分析得到的结论相一致。这些均匀分散在海泡石孔道内部的IL分子很可能因为与海泡石硅酸表面的紧密结合而获得更好的热稳定性。至于离子液体分子如何能在海泡石狭长的微孔中运行以至将整个孔道填满,笔者认为文献[23]的研究给出了合理的解释:海泡石纤维不仅在平行c轴的方向上存在狭长的结构性微孔,同时在垂直纤维方向也存在大量短程的微孔,这些微孔将海泡石众多平行于纤维方向的结构性微孔互相连接,形成了巨大的空间网络孔道结构,因此,离子液体分子并非只能在海泡石平行纤维方向的微孔中一维扩散,而很可能同时借助那些垂直纤维方向的短程微孔在海泡石内部巨大的空间网络孔道结构中传输,最终填满了海泡石所有的微孔。

(a)选区照片(电子图像)

(b)Mg(Kα1-2)

(c)O(Kα1)
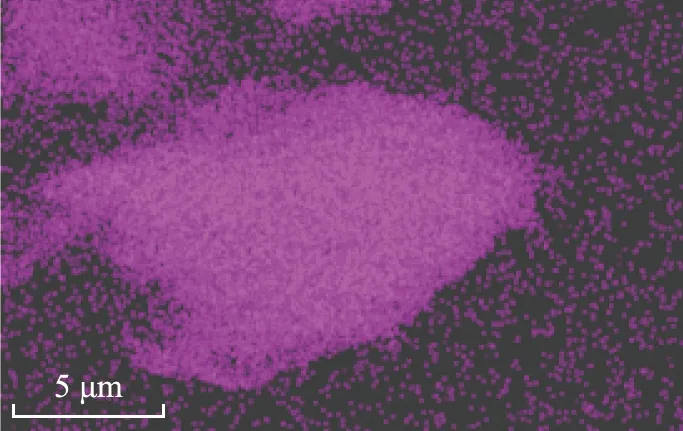
(d)Si(Kα1)

(e)N(Kα1-2)

(f)Br(Lα1-2)图5 样品sep-IL-7的SEM-EDX能谱分析结果
2.5 负载IL海泡石不同温度灼烧后抗菌性能分析
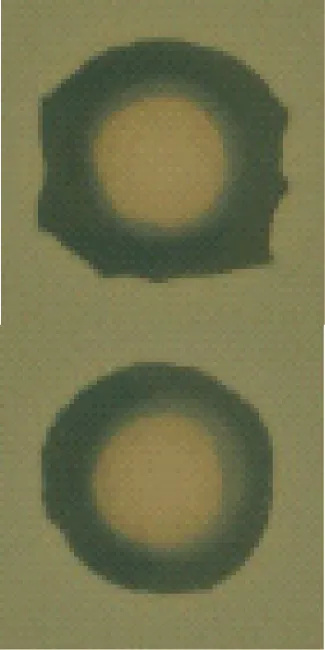
(a)sep-IL-5未烧

(b)sep-IL-6未烧

(c)sep-IL-7未烧

(d)sep-IL-5 250 ℃灼烧

(e)sep-IL-5 300 ℃灼烧

(f)sep-IL-5 350 ℃灼烧

(g)sep-IL-6 250 ℃灼烧

(h)sep-IL-6 300 ℃灼烧

(i)sep-IL-6 350 ℃灼烧

(j)sep-IL-7 250 ℃灼烧

(k)sep-IL-7 300 ℃灼烧

(l)sep-IL-7 350 ℃灼烧
根据前面的XRD分析可知,所有样品中离子液体分子均在海泡石中实现了均匀分散,故选择负载量最高的3个样品sep-IL-5—sep-IL-7进行灼烧前、后的抗菌性能分析,分别以芽孢杆菌和大肠杆菌为测试菌株、采用抑菌环的方法研究了sep-IL-5—sep-IL-7样品分别在温度为250、 300和350 ℃条件下灼烧后的抗菌性能。针对芽孢杆菌的抑菌环测试结果如图6所示。sep-IL-5—sep-IL-7样品在未经灼烧时均表现出显著的抗菌能力,随着IL的负载量增大,其抑菌环的尺寸略微增大,说明3个样品中IL的溶出速度差别不大,原因很可能是IL负载于海泡石的微细孔道中,二者之间存在较强的静电作用,因此IL在溶出过程中缓慢释放, 即使IL的负载量不同, 其溶出而导致的抑菌环的大小差别不大。 sep-IL-5—sep-IL-7样品经过灼烧后的抑菌效果如图6(d)—(l)所示, 3个样品在温度为250 ℃的条件下灼烧1 h后保留了大部分的抗菌能力, 其中样品sep-IL-7的抗菌能力最强, 因其IL负载量较大, 由纯IL的热重分析可知,温度为250 ℃下IL已经开始了剧烈分解,而负载于海泡石中的IL能在温度为250 ℃下灼烧1 h后保持大部分抗菌能力, 说明海泡石显著提高了IL的热稳定性; 3个样品在温度为300 ℃下灼烧后抑菌环尺寸有所下降, 但都保留了可辨识的抑菌能力, 纯IL的热重分析可知温度为300 ℃下IL已经分解完毕, 而负载于海泡石中的IL能在温度为300 ℃下灼烧1 h后保持一定的抑菌能力, 再次说明海泡石提高了IL的热稳定性; 3个样品在温度为350 ℃灼烧后均碳化变黑并完全失去了抑菌能力, 说明即使在温度为350 ℃的条件下灼烧1 h后海泡石中的IL分子没有完全热分解,但对其抑菌性能有益的咪唑环已经分解殆尽,因此样品不再具有任何抑菌性能。

(a)sep-IL-5未烧

(b)sep-IL-6未烧

(c)sep-IL-7未烧

(d)sep-IL-5 250 ℃灼烧

(e)sep-IL-5 300 ℃灼烧

(f)sep-IL-5 350 ℃灼烧

(g)sep-IL-6 250 ℃灼烧

(h)sep-IL-6 300 ℃灼烧

(i)sep-IL-6 350 ℃灼烧

(j)sep-IL-7 250 ℃灼烧

(k)sep-IL-7 300 ℃灼烧

(l)sep-IL-7 350 ℃灼烧图7 样品sep-IL-5—sep-IL-7在不同温度下灼烧后对大肠杆菌的抑菌环分析结果
以大肠杆菌为目标菌株的抑菌性能测试结果如图7所示。测试结果和使用芽孢杆菌的测试结果非常类似:sep-IL-5—sep-IL-7样品在未经灼烧时均表现出良好的抑菌性能,各样品在温度为250 ℃条件下灼烧1 h后抑菌性能略有下降,而在温度为300 ℃条件下灼烧1 h后各样品仍残留微弱的抑菌能力,在温度为350 ℃条件下灼烧1 h后各样品均丧失抑菌能力。之所以在温度为300 ℃条件下灼烧后样品抑菌圈相比芽孢杆菌的情况下更小,是因为该测试时使用的菌液浓度较高(每毫升细菌群落数为109)。从上述结果可知,样品对革兰氏阳性菌和革兰氏阴性菌均具有抑制和杀灭能力。
3 结论
1)咪唑类离子液体的分子很容易自发进入海泡石沿c轴的孔道内部并发生铺展,即使在IL质量分数为31%的高负载量下材料依然不显示离子液体的X射线衍射峰,原因很可能在于其正电性的咪唑头基和海泡石孔道内壁显负电的硅酸表面发生强相互作用, 从而使咪唑分子获得了更好的分散均匀性和热稳定性。
2)从耐热性能的研究可知,负载于海泡石孔道内的离子液体在空气中温度为300 ℃条件下灼烧1 h后仍能保留一定的抗菌性能, 大大拓展了有机抗菌剂的耐热温度范围, 有望应用在烧烤炉、 烤箱等电器的外层耐热涂料中, 使其获得持久的抗菌能力。 由目前的研究结果推测咪唑类离子液体和海泡石之间的强静电作用很可能赋予材料一定的耐溶出性和缓释效果, 这将在下一步的工作中进行研究。

