三元前驱体Ni0.88Co0.05Mn0.07(OH)2包覆氢氧化锌的研究
王金文,刘更好,李永光
(1.广东邦普循环科技有限公司,广东 佛山 528137; 2.广东省电池循环利用企业重点实验室,广东 佛山 528137; 3.湖南邦普循环科技有限公司,湖南 长沙 410600)
锂离子电池常用正极材料有锰酸锂、镍酸锂、钴酸锂、磷酸铁锂和三元材料等[1-2]。随着电动汽车和大规模储能技术的快速发展,人们对锂离子电池的容量、功率、成本、寿命及安全性等提出了更高的要求。LiNi0.8Co0.1Mn0.1O2(NCM811)作为三元正极材料的突出代表,极具研究前景。
离子掺杂可提高锂离子电池正极材料的电化学性能,掺杂用的非金属元素有F[3],金属元素有Al、Mg、Ti、Sn、Mo、Cr和La[4]等。正极材料的形貌和性能在很大程度上与前驱体相关,前驱体阶段包覆优化表面结构,也是改性方向之一。李永光等[5]在三元前驱体Ni0.82Co0.12Mn0.06(OH)2表面包覆氢氧化钴,pH=10.0时,包覆物沿基材外延结构继续生长;pH=11.5时,包覆物呈点状或片状均匀分布;反应温度为65 ℃、搅拌速度为350 r/min时,包覆形貌较好、振实密度较高。
理论和研究结果表明,包覆和掺杂是提高NCM811性能的有效手段,一方面是包覆材料能在材料表面提供良好的导电网络;另一方面是包覆能抑制材料与电解液发生反应。本文作者对高镍Ni0.88Co0.05Mn0.07(OH)2前驱体进行氢氧化锌包覆,研究以硫酸锌为原料,NaOH/氨水为沉淀剂时,NaOH量、氨水量、反应温度及包覆量对前驱体的影响。
1 实验
1.1 样品的制备
以NaOH(河北产,AR)和氨水(番禺产,AR)作为沉淀剂。将100 g前驱体Ni0.88Co0.05Mn0.07(OH)2(佛山产,98.99%)和500 ml去离子水加入1 L烧杯中,在加热搅拌(500 r/min)的条件下,往烧杯中并流加入硫酸锌溶液(广东产,AR)和沉淀剂,反应30 min完成沉淀后,陈化30 min,再将反应完全的浆料过滤、洗涤,在120 ℃下烘干6 h,得到待测样品,未进行包覆的基材记为Z。
研究NaOH量对包覆的影响时,以NaOH为沉淀剂,在55 ℃下,pH=9.0、10.0、11.0和12.0时,包覆1%(质量分数,理论值,下同)的锌。
研究温度对包覆的影响时,以NaOH为沉淀剂,在pH=12.0,温度分别为35 ℃、45 ℃、55 ℃、65 ℃和75 ℃的条件下,包覆1%的锌。
研究氨水量对包覆的影响时,以氨水为沉淀剂,在55 ℃下,pH=9.0、9.5、10.0、10.5和11.0时,包覆1%的锌。
研究锌包覆量对包覆的影响时,以NaOH为沉淀剂,在55 ℃下,pH=12.0时,分别包覆1%和2%的锌。
1.2 测试与分析
用NOVA SEM 450扫描电子显微镜(美国产)对样品形貌进行分析。用BSD3H-2000A物理吸附仪(北京产)测试样品的BET比表面积;用BT-302振实密度测试仪(丹东产)测定样品的振实密度(TD)。用Optima 2100DV电感耦合等离子发射光谱(ICP-AES)仪(美国产)测试颗粒包覆锌元素的含量(质量分数)。用Ultima Ⅳ X射线衍射仪(日本产)分析材料的物相,CuKα,λ=0.154 06 nm,管压40 kV、管流40 mA,扫描速度为5(°)/min,步长为0.03°。
2 结果与讨论
2.1 NaOH量对包覆的影响
硫酸锌与NaOH(适量)之间的化学反应见式(1):
ZnSO4+2NaOH=Zn(OH)2↓+Na2SO4
(1)
当NaOH过量时,发生如下反应:
Zn(OH)2+2NaOH=Na2ZnO2+2H2O
(2)
根据式(1)和(2),NaOH是强碱,而锌具有两性,NaOH加入量过多,会与氢氧化锌沉淀反应,生成可溶的锌酸钠,出现反溶现象。NaOH的不断加入,会导致OH-浓度上升,最终表现为pH值上升。NaOH为沉淀剂时,不同pH值下包覆前驱体的形貌如图1所示。
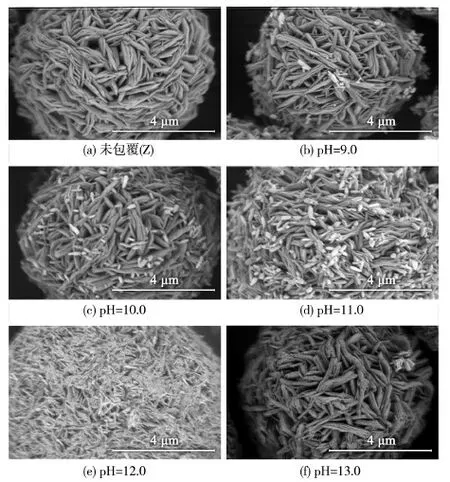
图1 NaOH为沉淀剂时不同pH值下包覆颗粒的SEM图
从图1可知,当pH值为9.0~11.0时,基料表面出现棒状包覆物;随着pH值的上升,包覆物数量增加。这是由于氢氧化锌发生非均匀形核,依附在容器壁或前驱体表面,而前驱体表面有较多的极性位点,表面张力较大,更适合氢氧化锌形核、生长。氢氧化锌结晶主要在前驱体表面,很少在容器壁上。包覆物数量上升,则是由于此时仍处于硫酸锌过量阶段。随着pH值的上升,NaOH增多,结晶析出的氢氧化锌也随之增加。不同的是在pH=9.0时,生成的棒状物有明显的棱状边角;pH=10.0和11.0时,包覆棒状物表面更圆滑,呈梭形,此时NaOH过少,形核速度小于生长速度,晶体生长得更粗大;当pH=12.0时,包覆物呈针状,材料表面已形成均匀且紧密的包覆层,基材表面原有空隙减少。这是由于在高pH值下,形核速度远大于生长速度,晶核越小表面能越高,越容易在缺陷位置进行填补,优先在具有不均匀性的点形核。pH=13.0时,表面包覆物呈零星点状,结合式(2)可知,是NaOH过量、析出氢氧化锌反溶所致。
NaOH为沉淀剂时,不同pH值下包覆颗粒的参数见表1。
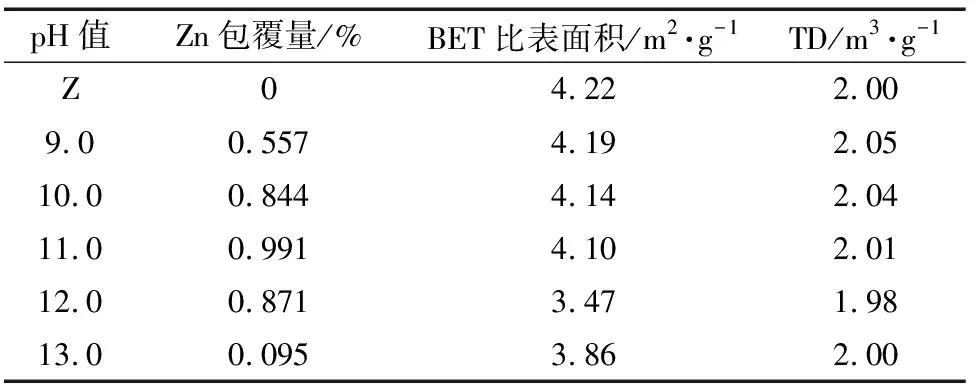
表1 NaOH为沉淀剂时不同pH值下包覆颗粒的参数
从表1可知,随着pH值增大,Zn的包覆量呈先上升、后下降的趋势,与氢氧化锌在不同pH值下的沉淀和反溶有关,也与图1的形貌一致。BET比表面积呈先下降、后上升的趋势,在pH=12.0时最低,此时的反应形核速度远快于生长速度,新核呈细小的针状,填入颗粒表面的缺陷中[图1(e)];pH=13.0时,由于Zn的反溶,导致BET比表面积回升。不同的包覆形貌,会导致包覆颗粒的TD变化。
综上所述,以NaOH为沉淀剂,若要在包覆材料表面形成均匀的棒状包覆,优选pH=11.0;若要形成均匀针状包覆,优选pH=12.0。
2.2 温度对包覆的影响
不同温度下包覆前驱体的SEM图见图2和图1(e)。

图2 NaOH为沉淀剂时不同温度下包覆颗粒的SEM图
从图2可知,当温度为35 ℃、45 ℃时,包覆物主要以晶核形式嵌入颗粒表面缺陷中,此时温度较低,形核和生长速度慢,晶体生长占据主导地位。当温度升高到65 ℃、75 ℃时,形核和生长速度都增大。升温有利于提高纳米粒子的自由能,从而填补进入晶片间隙这类能垒较高的位置。
不同反应温度下包覆颗粒的性能参数见表2。
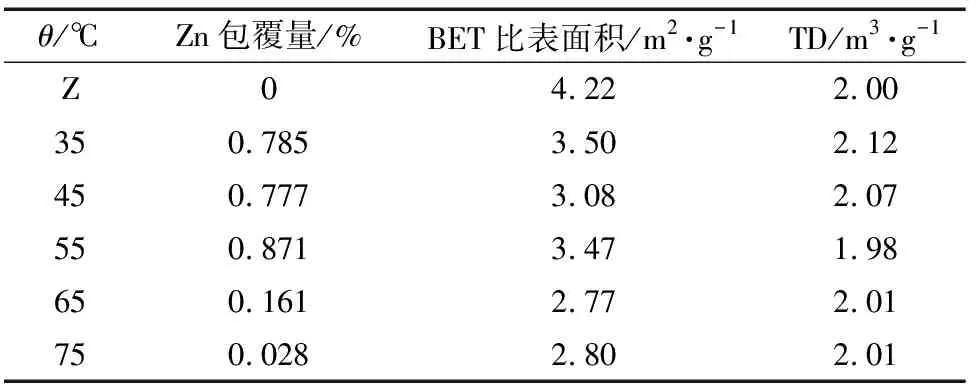
表2 NaOH为沉淀剂时不同温度下包覆颗粒的参数
从表2可知,在35 ℃、45 ℃和55 ℃时,Zn的包覆量相差不大,但在65 ℃、75 ℃时,Zn的包覆量迅速下降,原因是高温下水的电离常数增大,相同pH值时,NaOH含量更高,氢氧化锌发生反溶,检测的含量更低,包覆颗粒上无明显包覆物,仅部分晶核在基材表面间隙中[图2(c)、(d)]。包覆后颗粒的TD变化不大,BET比表面积降低,是因为部分氢氧化锌未沿基材方向生长,填入了颗粒表面的缺陷中,且形核速率随着温度的升高而增加,填入的包覆物相应增加,缺陷减少;在55 ℃时,BET比表面积有所回升,原因是此时形核速率远大于生长速率,颗粒表面形成大量的针状颗粒包覆;65 ℃与75 ℃时虽然部分氢氧化锌反溶,但由于温度较高,包覆物以细小的晶核嵌入基材表面缺陷,BET比表面积下降。
综上所述,以NaOH为沉淀剂,若要在包覆材料表面形成均匀包覆,则优选温度为55 ℃。
2.3 氨水量对包覆的影响
硫酸锌与氨水(适量)之间的化学反应见式(3):
(3)
当氨水过量时,发生如下反应:
4NH3+ZnSO4=Zn(NH3)4SO4
(4)
氨水与镍钴氢氧化物(M=Ni2+、CO2+)的反应为:

(5)
氨水为沉淀剂时,不同pH值下包覆前驱体的SEM图见图3。
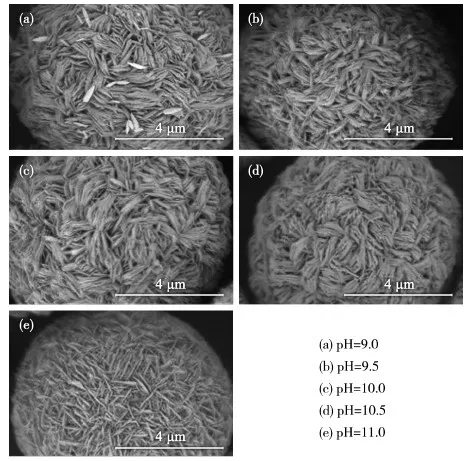
图3 氨水为沉淀剂时不同pH值下包覆颗粒的SEM图
与图1和图2相比,图3中颗粒的表面普遍形成更多的针状细长一次颗粒包覆,结合式(5)可知,原因是基材表面与氨水反应会生成金属离子和氨的配合物。这是一个可逆反应,调节pH值从9.0逐步上升到11.0,随着氨水的量不断增加,反应的正向作用增强,对比图1(a)与图3,基材的一次颗粒逐渐变细,是可逆反应的溶解和重结晶所致。
氨水为沉淀剂时,不同pH值下包覆颗粒的参数见表3。
工作室制具有“真实项目、真实环境、真正使用”的“三真”特性,即教学内容是基于真实的项目进行组织,教学环境应当模拟真实的企业环境,学习的成果能够推向社会真实使用[1]。电视制作类课程在项目设置、环境塑造和学习成果社会化等方面均容易实现,且从文献分析看,其成果也得到了很好的印证。
结合式(3)和(4)可知,实质上反应分两步进行,主要原因是随着氨水的量增加,溶液碱性增强。表3中TD波动不大,Zn的包覆量呈下降趋势。这是由于在pH=9.0时,氨水适量,随着pH值不断升高,氨水逐渐过量,生成的氢氧化锌逐渐反溶所致。BET比表面积呈先下降、后上升的趋势,与包覆颗粒的填充和一次颗粒的反溶有关。在pH值为9.0~10.0时,包覆颗粒对基材表面缺陷的填充作用更大,BET比表面积下降;pH>10.0后,氨水对一次颗粒的反溶、细化作用占主导,BET比表面积上升。

表3 氨水为沉淀剂时不同pH值下包覆颗粒的参数
综上所述,以氨水为沉淀剂,若要在包覆材料表面形成均匀包覆兼具较高的包覆量,则优选pH=9.5。
2.4 锌包覆量对包覆产物结构的影响
未包覆、包覆1%和2%锌后,材料的XRD结果见图4。包覆1%、2%锌的实际包覆量分别为0.871%、1.513%。

图4 不同锌包覆量下包覆颗粒的XRD图
从图4可知,基材颗粒与经过0.871%和1.513%锌包覆的颗粒,各峰对应良好,且未出现杂峰,说明包覆氢氧化锌后没有改变原基材的结构。
3 结论
本文作者在三元前驱体Ni0.88Co0.05Mn0.07(OH)2表面包覆一层氢氧化锌,研究NaOH量、氨水量、反应温度及包覆量对包覆产物的影响。以NaOH为沉淀剂时,若要在表面形成均匀紧密包覆,优选温度为55 ℃,进一步要在包覆材料表面形成均匀棒状包覆,则优选pH=11.0,要在包覆材料表面形成均匀针状包覆,则优选pH=12.0;以氨水为沉淀剂时,若要在包覆材料表面形成均匀紧密包覆,则优选pH=9.5,此时包覆颗粒兼具较高的包覆量;使用氢氧化锌在1%和2%的理论包覆量下,都没有改变原基材的结构。

