SARS-CoV-2变异株的遗传学特征和致病特点
王玉亮,龙艺尹,陈晓波
新型冠状病毒(SARS-CoV-2)感染引起的新型冠状病毒肺炎(conronavirus disease 2019,COVID-19)大流行对全球公共卫生及人类生命健康构成巨大威胁[1]。根据世界卫生组织(WHO)统计,截至2022年5月3日,全球COVID-19累计确诊病例已超5.1亿例,超624万人死亡[2]。在过去的2年中,世界各国通过对病毒样本进行基因组测序,见证了SARS-CoV-2不断进化及变异产生的多种变异株,相比原始毒株,新变异株具有更高的传染率,以致在全球快速传播,使COVID-19疫情防治复杂化并面临各种新的挑战[3]。本文就SARS-CoV-2变异株的遗传学特征,当前SARS-CoV-2新变异株奥密克戎(Omicron)流行病学特征、基因突变及临床特征,SARS-CoV-2样本采集方法及检测手段,疫苗接种以及COVID-19治疗等进行总结和分析,以期为SARSCoV-2的防治提供帮助。
1 SARS-CoV-2病毒概述
SARS-CoV-2基因组大小约为30 kb,编码9 860个氨基酸,是有包膜的单股正链RNA病毒,其病毒颗粒直径约100 nm,包括入侵宿主细胞所需的RNA遗传物质和结构蛋白。病毒一旦入侵宿主细胞,即会进行RNA的复制、转录和翻译,最后完成病毒颗粒的组装。SARS-CoV-2基因组包含14个功能性开放阅读框(ORF),编码4种主要结构蛋白,包括刺突蛋白(S蛋白)、包膜蛋白(E蛋白)、膜或基质蛋白(M蛋白)和核衣壳蛋白(N蛋白),以及16种构成复制酶复合物的非结构蛋白(NSP),见图1[4]。其中,S蛋白是病毒感染宿主细胞、新冠疫苗和治疗性中和抗体(Nab)研发的重要靶点[5]。在病毒入侵宿主细胞的过程中,首先通过位于S蛋白的氨基末端S1亚基的受体结合区域(RBD)识别并结合宿主细胞表面的血管紧张素转化酶2(ACE2),随后羧基末端S2亚基被跨膜丝氨酸蛋白酶2(TMPRSS2)切割,触发病毒与宿主细胞膜融合,随后病毒进入受感染细胞内进行复制及组装;此外,Furin蛋白酶可切割S1/S2亚基交界处多碱基Furin蛋白酶的切割位点(PRRAR),这有利于ACE2识别S蛋白的构象变化,且TMPRSS2与Furin蛋白酶对S蛋白的切割在病毒感染及高致病性中起协同作用[6]。

Fig.1 Schematic diagrams of SARS-CoV-2 genome structure图1 SARS-CoV-2基因组结构示意图
2 SARS-CoV-2变异株
为了便于研究人员向公众科普介绍病毒变异体系,提高公众健康意识,WHO(www.who.int/)、全球共享流感数据倡议组织(GISAID,www.gisaid.org/)、Nextstrain(nextstrain.org/)以及命名全球流行爆发谱系彭高命名系统(PANGOLIN,cov-lineages.org/)均免费共享基因组数据,并为所有新的和重要的变异株提供直接监测服务。WHO定期跟踪和调查SARS-CoV-2变异株,将新出现的变异株分类为值得关切的变异株(VOC)、待留意的变异株(VOI)及受监控的变异株(VUM)[7]。SARS-CoV-2-VOC是在符合VOI特征的基础上,还要有明确证据表明这些突变株对全球公共卫生造成巨大影响,使用于控制疾病传播的疫苗、治疗药物、诊断或公共卫生和社会措施的有效性严重削弱。SARS-CoV-2-VOI具有增强病毒传播能力、毒力的突变,影响病毒流行病学模式或疾病严重程度,具备社区传播或多点爆发,使公共卫生面临新的风险;SARS-CoV-2-VUM具有影响病毒特征的特定突变,并可能在未来构成潜在威胁,但目前尚无表型或流行病学影响的明确证据,需要加强监控和评估[8]。
根据WHO最近的流行病学更新,自大流行开始以来,已确定了5种SARS-CoV-2-VOC,包括B.1.1.7(Alpha)、B.1.351(Beta)、P.1(Gamma)、B.1.617.2(Delta)及最新出现B.1.1.529(Omicron),见表1[9-10];并描述了8种SARS-CoV-2-VOI,包括B.1.427/B.1.429(Epsilon)、P.2(Zeta)、B.1.525(Eta)、P.3(Theta)、B.1.526(Iota)、B.1.617.1(Kappa)、C.37(Lambda)及B.1.621(Mu),见表2[10]、图2。另外,WHO在其网站上公布了2种SARS-CoV-2-VUM,包括2021年9月多个国家报告的B.1.640谱系和2022年1月法国报告的XD(Delta与Omicron亚变种BA.1重组),但其特性尚未明确,相关信息较少,需要进一步监测。值得注意的是,之前有Delta亚变种AY.4与Omicron亚变种BA.1重组毒株“德尔塔克戎”(Deltacron)的报道[11],这种重组毒株起源于2种变异株感染了相同细胞后,病毒复制过程中相互交换遗传物质,由此产生2套遗传物质兼具的新毒株。GISAID提供的数据显示,欧洲多国及美国均相继报告了Deltacron相关病例,但样本数量依然非常有限。然而有研究人员表示,Deltacron可能是序列污染所
致的实验乌龙[12]。WHO卫生紧急项目技术负责人指出,目前没有发现这一毒株在流行病学和严重程度等方面带来任何变化,但许多研究正在进行。
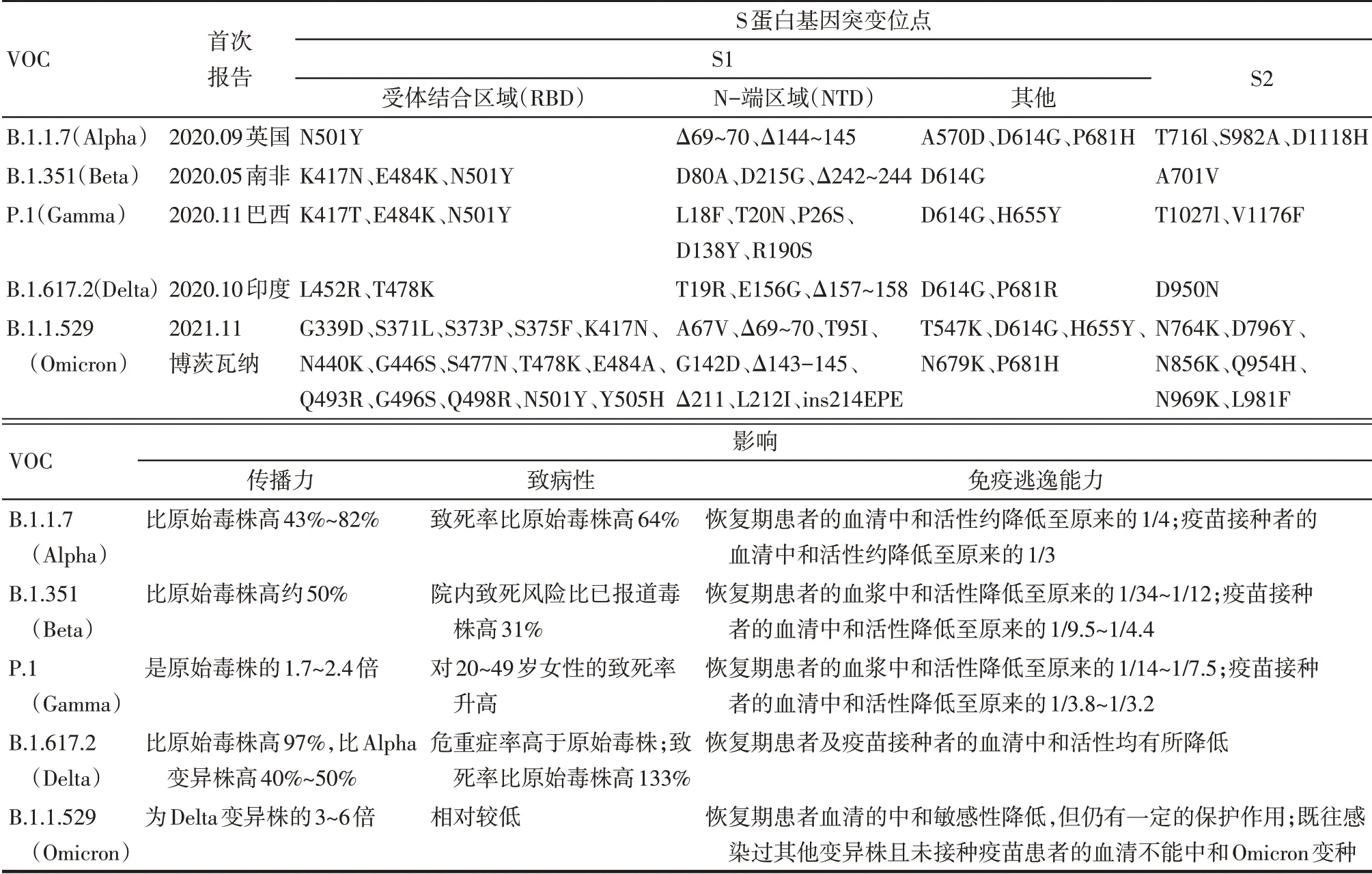
Tab.1 Genetic characteristics of SARS-CoV-2-VOC and their impacts表1 SARS-CoV-2-VOC的遗传学特征及其影响

Tab.2 Genetic characteristics of SARS-CoV-2-VOI and their impacts表2 SARS-CoV-2-VOI的遗传学特征及其影响

Fig.2 Global SARS-COV-2 variants图2全球SARS-COV-2变异株
3 Omicron变异株
3.1 Omicron流行病学特征2021年11月11日,在博茨瓦纳发现了一个SARS-CoV-2新变异株,其后南非多地报告了这种变异株。WHO于2021年11月26日将该突变株BA.1/B.1.1.529归类为VOC,并将其命名为Omicron,这是继Alpha、Beta、Gamma和Delta之后出现的第5个VOC。从12月开始,Omicron变异株已经传播到英国、美国、法国、荷兰、德国、丹麦、澳大利亚、以色列及印度等多国[13]。我国内地于2021年12月9日在对天津市入境闭环管控人员中筛查出一例Omicron变异株感染病例,为内地首次检出境外输入Omicron病例[14]。当前Omicron已在全球近180个国家/地区传播,并迅速取代Delta成为SARS-CoV-2感染优势流行毒株。
与之前流行的VOC相比,Omicron的传播性更强并呈现隐匿性传播。据英国卫生安全局报告,Omicron传播力为Delta的3~4倍。研究显示,Delta的基本传染数(R0)平均为5.8,而Omicron的R0可能在4~8之间,即每个感染者平均传染4~8个人。其中被称为“隐形Omicron”的BA.2亚变体传播速度比早前BA.1快75%左右[15]。我国本轮疫情主要由BA.2引起,R0可 能高 达9.5。2022年3月Nyberg等[16]在Lancet发表的英国150万Omicron病例流行病学特征研究显示,相比Delta,Omicron造成的住院和死亡风险显著下降,HR值分别为0.41(95%CI:0.39~0.43)及0.31(95%CI:0.26~0.37),由Omicron感染的内在死亡风险总体降低了80%。近日,英国科学家发布研究报告显示,英国1例男性患者自2020年感染SARS-CoV-2近一年半(长达505 d)后死亡,可能是世界上已知感染持续时间最长的病例,其免疫系统较弱,在对其死亡前的505 d持续观察中发现,SARS-CoV-2检测一直呈阳性[17]。伦敦国王学院及盖伊和圣托马斯国家医疗服务体系基金会的研究人员对9例顽固性COVID-19患者进行的跟踪调查发现,这些患者的免疫系统因器官移植、艾滋病、癌症等疾病的治疗而被削弱,特别容易长期感染SARS-CoV-2,其中有4例死亡;遗传分析显示,有5例患者体内的病毒至少完成了1种突变,感染505 d的患者体内SARS-CoV-2则携带了10种突变,包括Alpha、Gamma和Omicron在内的几个主要变异毒株;持续感染可能是新的变异株的来源,因为SARSCoV-2在患者体内也会不断进化,随时可能会获得新的突变[17]。Omicron变异株快速传播的另一特点是它在各种环境的物体表面上存活时间显著延长。当前,Omicron变异株已达到社区传播阶段且呈聚集性特征。与其他SARS-CoV-2-VOC相比,Omicron变异株再感染风险增加与之前接种的疫苗中和活性降低有关。
3.2 Omicron基因突变Omicron是迄今为止所有SARS-CoV-2变异中突变位点数量最多的变异株,基因组序列分析显示Omicron基因组中包含大约60个插入、替换及缺失,这显著超过了之前的4种VOC,其中32个突变位于S蛋白编码序列,包括T478K、N501Y、N655Y、N679K和P681H在内的一些突变,其与既往VOC流行株中的特征性氨基酸突变重叠,提示Omicron变异株经历了多发基因重组事件[18]。更令人担忧的是,其中15个突变位点位与ACE2具有更高的亲和力,可增强病毒感染/传播性,如N501Y(增强S蛋白和ACE2之间亲和力/增加病毒传播)、P681H(增强Furin蛋白酶与S蛋白的结合亲和力并促进病毒进入宿主细胞)、D614G(增加病毒适应性以增强病毒复制和传播)、H655Y/N679K(增强S亚基切割及病毒传播)。抗体结合区域内K417N、E484A、Q493K、Q498R、N501Y、Y505H或抗体 结 合 区 附 近S477N、T478K、G496S、G446S及N440K可能造成Nab抵抗,对单克隆抗体治疗表现出耐药性及免疫逃逸[19]。Ou等[20]对全球出现的Omicron变异株全基因组序列及其S蛋白基因序列进行了精细分析,发现部分Omicron变异株的S蛋白RBD区域出现了L452R和R346K突变,可能是Omicron与Delta及Mu变异株重组获得,从而导致对应区域的Nab结合效能下降,病毒免疫逃逸能力增强。Cameroni等[21]指出Omicron变异株S蛋白突变位点,见图3。另外,Omicron变异株具有许多疏水性氨基酸,如RBD区域的亮氨酸和苯丙氨酸,导致S蛋白局部构象、所带电荷和疏水性微环境发生改变,使其不被大多数以RBD和NTD为抗原结合表位的Nab识别,从而导致病毒具有了抗体免疫逃逸特性。
3.3 Omicron感染的临床特征Omicron的平均潜伏期约为3 d,确诊病例一般在首次出现症状前1~2 d就开始体外排出病毒。Omicron变异株感染以无症状和轻症感染为主,临床症状包括头痛、肌肉酸痛、流涕、干咳、咽痛、发热、呼吸急促、鼻塞、嗅觉/味觉减退或丧失、结膜炎、腹泻、盗汗、严重疲劳和血栓风险等,与之前流行的Delta相比更易感染中青年人群[16]。香港大学的研究团队通过使用手术切除的肺组织样本进行体外培养发现,在感染24 h后Omicron在人支气管细胞中的复制速度比Delta大约快70倍,而在肺组织内的复制速度仅为Delta的10%,这可能说明Omicron变异株感染患者的临床症状较轻。2022年4月Menni等[22]进行了前瞻性纵向观察研究,结果显示Omicron感染患者最常出现的症状有流涕(76.5%)、头痛(74.4%)、咽痛(70.5%)、打喷嚏(63.0%)、持续性咳嗽(49.8%)、声音嘶 哑(42.6%)。另有研究对Delta和Omicron感染的症状做了对比分析,结果显示,Omicron流行期间的感染者的嗅觉丧失仅有17%,而Delta感染者中为52.7%(OR=0.17,95%CI:0.16~0.19,P<0.01);Omicron出现咽痛、声音嘶哑的风险相比Delta感染者分别提高了55%(OR=1.55,95%CI:1.43~1.69,P<0.01)及24%(OR=1.24,95%CI:1.14~1.34,P<0.01),而其住院率低于Delta感染者(1.9%vs.2.6%,OR=0.75,95%CI:0.57~0.98,P<0.05);从症状出现到消失,Delta感染者平均经历8.89 d,而Omicron感染者则为6.87 d;同时,接种加强疫苗的Omicron患者症状持续时间平均为4.40 d,而Delta感染者为7.71 d[23]。尽管如此,Omicron高传染性对患有基础疾病的人群构成严重威胁,尤其是有合并症但尚未接种疫苗的人群,因为是否发展为重症不仅取决于病毒复制速度,还取决于自身的免疫机能;有些情况下Omicron可以逃脱免疫应答进而不会诱导有效的免疫反应,而在其他情况下,过激反应会诱发“细胞因子风暴”,导致急性呼吸窘迫综合征(ARDS)[24]。因此,全球卫生机构应尽快采取预防措施,以阻止这种新变异毒株在全球范围内的流行。

Fig.3 The spike glycoprotein mutations of Omicron variant图3 Omicron变异株S蛋白突变位点
3.4 Omicron新变体2022年1月19日,英国首先监测发现由Omicron BA.1亚变种及BA.2亚变种重组而成的一种新的SARS-CoV-2变异毒株,命名为XE。截至2022年3月底,XE的增长率/传播速度比BA.2亚变种高9.8%,社区传染率高出近10%,而BA.2已经是迄今为止已知传染性最高的SARSCoV-2变异毒株[25]。WHO发出警告,新变异毒株XE或比以前见过的任何SARS-CoV-2毒株都更具传染性,或是传播速度最快的SARS-CoV-2。目前WHO尚未将其列为VOC。韩国首次在境内发现由Omicron BA.1亚变种及BA.2亚变种重组而成新重组毒株XL感染病例,该确诊病例已接种完3剂新冠疫苗,患者于2022年3月23日确诊,目前暂无症状[26]。我国于2022年3月28日在江苏省常熟市核酸筛查发现1例轻型确诊病例,其感染病毒测序中发现为Omicron变异株BA.1.1亚变种,将其与本土病例和输入病例数据库及全球GISAID数据库进行对比,显示均未发现与之基因组高度同源的序列,需要进一步监测验证。Omicron亚变种BA.2继续进化,据GISAID数据,美国多地发现了BA.2的新分支BA.2.12和BA.2.12.1,其传播速度比BA.2提高23%~27%,与S蛋白L452Q突变有关;英国、印度、德国、加拿大等多国也发现了BA.2.12和BA.2.12.1的踪迹。当XE正在世界各地快速传播之际,Omicron再次变异出现了2个新亚变种BA.4和BA.5,4月11日WHO将这2个亚变种列为VOI。4月25日,山东烟台市召开疫情防控新闻发布会,通报国内首现Omicron亚变种BA.2.3进化分支。因此,Omicron变异株很可能不是SARS-CoV-2最后一个变异毒株,各国要提前做好准备,积极接种疫苗来应对SARSCoV-2变异。
4 SARS-CoV-2样本采集及检测
4.1 SARS-CoV-2样本采集方法根据SARSCoV-2的传播途径,SARS-CoV-2样本采集方法包括呼吸道采集及胃肠道采集。上呼吸道样本采集方式有鼻咽拭子、口咽拭子、鼻咽抽吸物、唾液等,下呼吸道样本采集方式有深咳痰、分泌物、支气管肺泡灌洗液及肺泡灌洗液,胃肠道样本可用肛拭子采集[27]。根据临床需要可留取全血标本和血清标本。对于确诊患者,下呼吸道样本检出率更高。总体而言,样本的选择对于准确检测SARS-CoV-2至关重要,也是判断疾病严重程度的重要因素。
4.2 SARS-CoV-2检测方法以分子生物学为核心的实验诊断技术是当前SARS-CoV-2临床实验诊断的重要手段。SARS-CoV-2分子检测方法有以下4类。(1)定量聚合酶链反应(PCR)技术:逆转录实时荧光定量PCR(RT-qPCR)、微滴式数字PCR(ddPCR)。(2)等温扩增技术:转录介导扩增(TMA)、切口酶扩增反应技术(NEAR)、逆转录环介导的等温扩增技术(RT-LAMP)、重组酶聚合酶扩增(RPA)。(3)分子杂交技术:成簇规律间隔短回文重复序列及其相关蛋白(CRISPR-Cas)系统、核酸微阵列分析。(4)二代测序(NGS)等[28]。目前,核酸检测仍然是判定感染SARS-CoV-2的“金标准”。源自Omicron变异株多处基因突变,特别是对于检测靶标为S蛋白编码基因的核酸检测试剂可能无法有效检出Omicron变异株,会引起漏检。我国核酸检测试剂主要选择了病毒序列保守性和特异性相对较高的ORF1ab和N基因作为靶标,Omicron仍然可以被核酸检出,目前尚未发现脱靶和漏检。NGS以相对无偏见的方式收集样本,通过全长病毒核酸序列测序分析,有助于精准判断SARS-CoV-2的突变类型、病毒溯源、流行病学调查、致病机制研究、药物及疫苗的研发等。此外,还可以使用免疫学诊断方法识别病毒抗原及机体针对病毒的免疫反应。根据《新冠病毒抗原检测应用方案(试行)》,在核酸检测基础上增加抗原检测作为补充,SARS-CoV-2抗原快速检测包括胶体金免疫层析法和荧光免疫层析法等[29]。SARS-CoV-2唾液/血清特异性抗体(sIgA、IgG和IgM)检测包括胶体金免疫层析法、酶联免疫吸附试验(ELISA)、化学发光免疫测定(CLIA)等[30],见图4。2022年4月14日,美国食品药品监督管理局(FDA)首次批准使用呼吸样本进行SARS-CoV-2检测,应用InspectIR COVID-19呼吸分析仪使用一种称为气相色谱-质谱(GC-MS)技术来分离和识别化学混合物,并能快速(3 min内)检测出呼出气体中5种SARS-CoV-2-VOC,当检测到标志物存在时,将返回一个推定(未经确认的)阳性检测结果,并通过分子检测予以确认。

Fig.4 The collecting and detection for SARS-CoV-2 specimen图4 SARS-CoV-2样本采集及检测
5 疫苗接种
鉴于Omicron变异株的过度突变和潜在的免疫逃逸机制,接种疫苗加强针(第3针)十分必要,因第3针疫苗能驱使体内记忆B细胞成为能产生抗体的效应B细胞,进而增加血清Nab水平以控制Omicron传播/感染并将发病率降至最低。接种的第3针疫苗建议使用异种疫苗作为序贯接种。笔者认为序贯接种可诱导机体免疫系统产生高效的“交叉免疫记忆”或称“互补免疫记忆”,以提升预防感染率。依据SARS-CoV-2的进化速度比流感等呼吸道病毒更快的特点,目前所提供的SARS-CoV-2疫苗可能需要及时更新,以确保疫苗继续提供保护水平,预防包括Omicron和未来变异毒株的感染。
6 COVID-19的治疗
2022年4月21日WHO更 新 了COVID-19治 疗的指南[31]:(1)对于轻症患者的治疗,重要推荐的治疗方法就是Paxlovid,有条件推荐的是Molnupiravir、Remdesivir及单抗药Sotrovimab和REGN-COV2;不推荐伊维菌素和皮质醇激素治疗;强烈反对使用康复者血浆、羟氯喹和克力芝。(2)对于有肺炎和缺氧表现的重症患者,强烈推荐皮质醇激素、白细胞介素(IL)-6抑 制 剂 或Janus激 酶(JAK)抑 制 剂Baricitinib;但 不 推 荐JAK抑 制 剂Ruxolitinib和Tofacitinib、伊维菌素及康复者血浆;强烈反对使用羟氯喹和克力芝。(3)对于出现ARDS的危重患者,强烈推荐皮质醇激素、IL-6抑制剂或Baricitinib。
7 结论
由于不同SARS-CoV-2变异株发生基因突变和(或)跨变种重组,从而促进了SARS-CoV-2的持续进化。新变体增强了病毒传播性、隐匿性和(或)增加再感染的风险,但随着疫苗接种和自然感染导致机体免疫力的增强,新变体所致疾病的严重程度有可能随着时间的推移而降低。目前世界各国针对SARS-CoV-2-VOC和SARS-CoV-2-VOI基 因 组 突变需保持足够详细和系统的监测,以便及时采取适当的公共卫生控制措施,同时亟需密切关注实验室诊断试剂的适用性(研发识别突变的特异性PCR检测方法以防止脱靶和漏检)及现有疫苗的有效性,以利于有效控制和尽早消灭COVID-19疫情。

