高强度聚焦超声消融术单用及联合GnRH-a治疗不同等级血供子宫肌瘤的效果对比
阳丽君,刘 君,黄 瑾,苏园园
(中山市人民医院妇科,广东 中山 528403)
子宫肌瘤是“妇科第一瘤”,是育龄女性发病率最高的一种妇科良性肿瘤。据统计,40 岁左右的女性子宫肌瘤的发病率高达50%,且近年来此病患者的发病年龄趋于年轻化。子宫肌瘤主要是由增生的子宫平滑肌细胞及纤维间质组成。当子宫肌瘤增大或引起临床症状时,需要及时进行治疗。以往临床上主要是采用子宫肌瘤剔除术或子宫全切术治疗此病。高强度聚焦超声(HIFU)消融术作为一种新的治疗方式,是将体外超声波聚焦于子宫肌瘤部位,通过热效应、空化效应、生物学效应及机械效应使子宫肌瘤细胞发生不可逆转的凝固性坏死,进而达到缩小肌瘤体积的作用。HIFU 消融术于2004 年开始正式应用于子宫肌瘤的治疗中。在过去10 余年的临床应用中,HIFU 消融术的有效性得到了大量学者的验证[1-3]。但该方法对于位置较深、血供丰富、体积大、组织成分较复杂的子宫肌瘤仍然存在治疗有效率低、患者术后并发症多等缺点[4-5]。研究指出,行子宫肌瘤手术前,用促性腺激素释放激素激动剂(GnRH-a)对患者进行预处理可缩小其子宫肌瘤的体积。本文主要是比较HIFU消融术单用及联合GnRH-a 治疗不同等级血供子宫肌瘤的效果。
1 资料与方法
1.1 一般资料
选取我院2018 年7 月至2020 年3 月期间收治的子宫肌瘤患者120 例作为试验对象。其纳入标准是:病情符合子宫肌瘤的诊断标准;病历资料完整;瘤体内部的血供等级为0 ~Ⅲ级(Adler 血流分级法);知晓本研究内容,并签署知情同意书。其排除标准是:合并有其他妇科疾病、恶性肿瘤或精神心理类疾病;对本研究中所用的药物过敏;对HIFU 消融术不耐受或存在禁忌证。按照随机数表法将其分为单独HIFU组(n=60)和GnRH-a 联合组(n=60)。两组患者的年龄、肌瘤个数、肌瘤体积、肌瘤内部血供等级等一般资料相比,差异无统计学意义(P>0.05)。详见表1。本研究已通过我院医学伦理委员会的批准。

表1 两组患者一般资料的比较
1.2 Adler 血流分级
采用Adler 血流分级法将患者子宫肌瘤内部的血供等级分为0 ~Ⅲ级。0 级:子宫肌瘤周边有半环状血流,瘤体内无血流信号。Ⅰ级:子宫肌瘤周边有半环状或短线状血流,瘤体内有少量血流,可见1 ~2个细棒状或点状的肿瘤血管。Ⅱ级:子宫肌瘤周边有半环状或环状血流,瘤体内有中量血流,可见3 ~4个点状血管或一个较长的血管穿入病灶,且其长度超过或接近肌瘤半径。Ⅲ级:子宫肌瘤的周边滋养血管呈网状包绕整个肌瘤,并有多个树枝状分支伸入肌瘤内部,可见不少于5 个点状血管或2 个较长的血管。
1.3 方法
单用HIFU 消融术对单独HIFU 组患者进行治疗,方法是:采用JC200 聚焦超声肿瘤治疗系统(由重庆海扶科技有限公司生产)对其进行治疗,治疗时对其实施常规的镇静镇痛,并使其俯卧于治疗台上。在超声的引导下对其子宫肌瘤进行消融治疗,采用点打的方式逐层覆盖肌瘤,将超声功率设为300 ~400W。对患者进行超声造影检查,若检查结果显示肌瘤内部的血供消失,则终止治疗。用HIFU 消融术联合GnRH-a 对GnRH-a 联合组患者进行治疗。对其进行HIFU 消融术的方法同上。本研究中所用的GnRH-a 为醋酸亮丙瑞林(生产厂家:TakedaPharmaceuticalCompany Limited ;批准文号:进口药品注册证号:J20090052),其用法是:在患者月经的第2 天为其皮下注射3.75 mg 的此药,28 d 后注射第2 针(剂量同上),56 d 后注射第3 针(剂量同上),在注射3 针后的4 周内对其实施HIFU 消融术。
1.4 观察指标
观察并记录GnRH-a 联合组患者治疗前及GnRH-a 注射3 针后瘤体内部的血供等级。比较两组患者治疗后子宫肌瘤的消融率及术中的能效因子。术后在增强MRI 的失状位、冠状位及横断位下采用相同的测量方法测量患者肌瘤内无灌注区的3 条径线(D1、 D2、D3),并采用椭圆的计算公式计算肌瘤体积(V)、无灌注区体积(non-perfused volume,NPV)。V=4π/3×(D1×D2×D3)。 肌 瘤 的 消 融 率=NPV/V×100%。能效因子F=η·Pt/V(J/mm3),η 为0.7,Pt 为治疗能量(J),P 为治疗功率,t 为超声辐照时间。比较两组患者术中不良事件的发生率及术后并发症的发生率。参照国际介入放射治疗协会(Society of Interventional Radiology,SIR)的分级标准将两组患者术中的不良事件分为A 级、B 级、C 级、D 级、E 级、F 级6 个级别。A 级:无需治疗,无不良后果。B 级:无不良后果,仅需临床观察。C 级:需要治疗,住院时间<48 h。 D 级:需要进一步治疗,包括意外增加护理水平或延长住院时间(>48 h)。E 级:出现永久性不良后遗症。F 级:患者死亡。术后对两组患者均进行12 个月的随访,比较其术前、术后3 个月、6 个月及12 个月的症状评分和子宫肌瘤症状和健康相关生活质量问卷(Uterine Fibroid Symptom and Healthrelated Quality of Life,UFS-QOL)评分,比较其术后3 个月、6 个月及12 个月子宫体积缩小率和病灶体积缩小率。症状评分的总分为100 分,患者的评分越高表示其临床症状越严重。UFS-QOL 包括月经量增多、下腹部不适、经血成块等指标,患者的评分越高表示其生活质量越好。
1.5 统计学方法
用SPSS 17.0(IBM,Amonk,NY)软件处理本研究中的数据,符合正态分布的计量资料用±s表示,组间比较采用单因素方差分析,两两比较采用LSD-t检验;计数资料用频数、频率表述,组间比较采用行×列表χ²检验,P<0.05 表示差异有统计学意义。
2 结果
2.1 GnRH-a 联合组患者治疗前及GnRH-a 注射3 针后瘤体内部血供等级的比较
GnRH-a 注射3 针后,GnRH-a 联合组患者瘤体内部的血供等级较治疗前明显下降,其中8 例患者瘤体内部的Ⅲ级血供下降至Ⅱ级或Ⅰ级。详见表2。
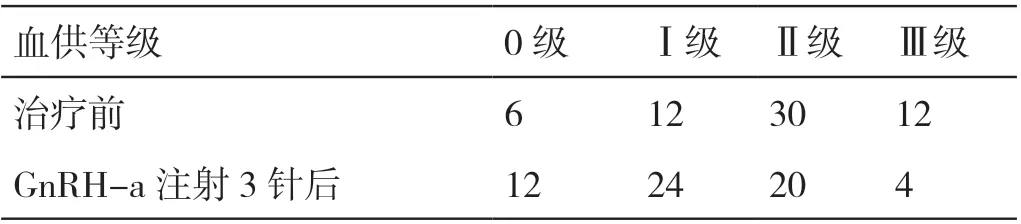
表2 GnRH-a 联合组患者治疗前及GnRH-a 注射3 针后瘤体内部血供等级的比较(例)
2.2 两组患者治疗后子宫肌瘤的消融率及术中能效因子的比较
随着两组患者子宫肌瘤血供级别的增加,其子宫肌瘤的消融率逐步下降。治疗后,GnRH-a 联合组患者子宫肌瘤的消融率高于单独HIFU 组患者,但组间相比差异无统计学意义(P>0.05)。GnRH-a 联合组患者术中的能效因子低于单独HIFU 组患者,差异有统计学意义(P<0.05)。详见表3。
表3 两组患者治疗后子宫肌瘤的消融率及术中能效因子的比较(± s)

表3 两组患者治疗后子宫肌瘤的消融率及术中能效因子的比较(± s)
注:* 与单独HIFU 组相比,P >0.05;#与单独HIFU 组相比,P <0.05。
组别 子宫肌瘤的消融率(%)能效因子(J·mm-3)单独HIFU 组(n=60) 74.66±14.6713.08±18.96 GnRH-a 联合组(n=60) 81.43±11.61*8.37±25.37#
2.3 两组患者术中不良事件的发生率及术后并发症发生率的比较
GnRH-a 联合组患者术中不良事件的发生率低于单独HIFU 组患者,差异有统计学意义(P<0.05)。两组患者术后并发症的发生率相比,差异无统计学意义(P>0.05)。详见表4。术中两组患者中共有58 例(占48.33%)患者出现不良事件,按照SIR 分类,其中发生A 类不良事件的患者有49 例(占40.83%),发生B 类不良事件的患者有7 例(占5.83%),发生C 类不良事件的患者有2 例(占1.67%),无患者发生D 类、E 类或F 类不良事件。A 类不良事件主要为下腹痛(占40.82%),发生此类不良事件的患者在术后3 d 内未经任何治疗自行恢复。在发生B 类不良事件的患者中,有3 例患者发生下腹痛(疼痛级别较重),有2 例患者发生骶骨疼痛,有2 例患者发生臀部其他部位疼痛,这7 例患者经对症处理后疼痛均得到缓解。在发生C类不良事件的2 例患者中,有1 例患者发生皮肤烧伤(浅Ⅱ度烧伤),经创面清洁换药处理后烧伤皮肤再生修复;有1 例患者出现腿部麻木和疼痛,考虑发生坐骨神经损伤,采用非甾体类抗炎药(NSAID)治疗后症状得到缓解。GnRH-a 联合组患者在采用GnRH-a治疗期间均出现了闭经症状(停药2 个月左右月经均恢复正常),其中有3 例患者出现不同程度的情绪波动、潮热、多汗、失眠等更年期症状,予以口服坤泰胶囊后症状好转。
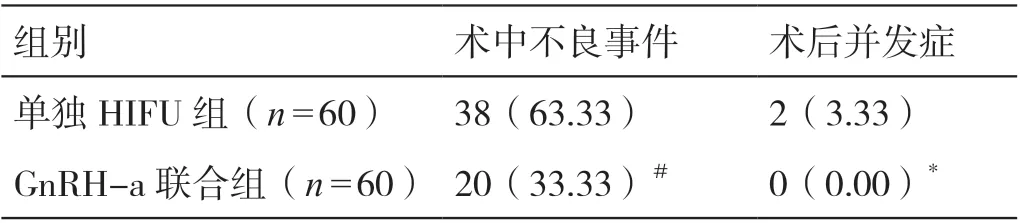
表4 两组患者术中不良事件的发生率及术后并发症发生率的比较[例(%)]
2.4 两组患者手术前后各项指标的比较
术前,两组患者的症状评分、UFS-QOL 评分相比,差异无统计学意义(P>0.05)。术后3 个月、6 个月及12 个月,两组患者的症状评分均低于术前,其QUL 评分均高于术前,差异有统计学意义(P<0.05)。术后3 个月、6 个月及12 个月,GnRH-a 联合组患者的症状评分均低于单独HIFU 组患者,其UFS-QOL评分均高于单独HIFU 组患者,差异有统计学意义(P<0.05)。术后6 个月及12 个月,两组患者的子宫体积缩小率和病灶体积缩小率均高于术后3 个月,差异有统计学意义(P<0.05)。术后6 个月及12 个月,GnRH-a 联合组患者的子宫体积缩小率和病灶体积缩小率均高于单独HIFU 组患者,差异有统计学意义(P<0.05)。详见表5。
表5 两组患者手术前后各项指标的比较(± s)
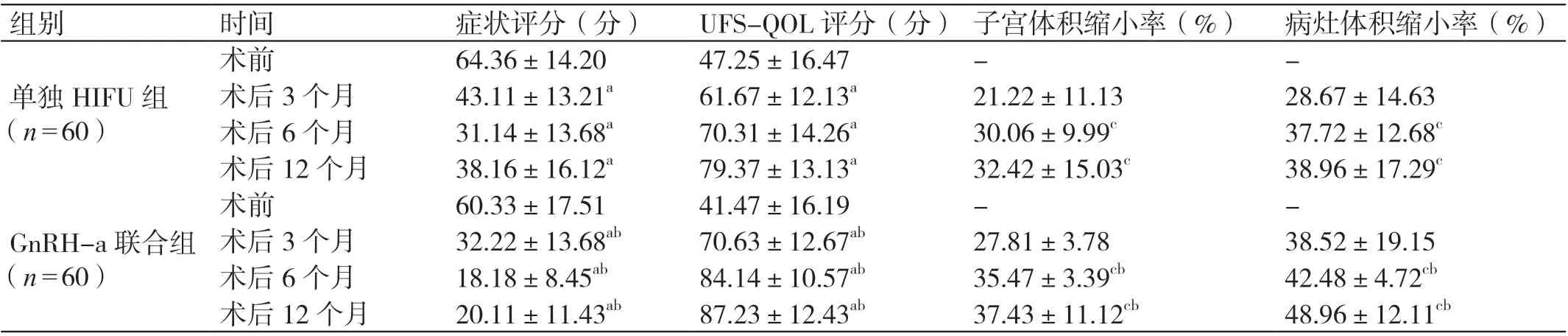
表5 两组患者手术前后各项指标的比较(± s)
注:a 与本组术前相比,P <0.05 ;c 与本组术后3 个月相比,P <0.05;b 与单独HIFU 组术后同一时间点相比,P <0.05。
组别 时间 症状评分(分)UFS-QOL 评分(分) 子宫体积缩小率(%) 病灶体积缩小率(%)单独HIFU 组(n=60)术前64.36±14.2047.25±16.47--术后3 个月43.11±13.21a61.67±12.13a21.22±11.1328.67±14.63术后6 个月31.14±13.68a70.31±14.26a30.06±9.99c37.72±12.68c术后12 个月38.16±16.12a79.37±13.13a32.42±15.03c38.96±17.29c GnRH-a 联合组(n=60)术前60.33±17.5141.47±16.19--术后3 个月32.22±13.68ab70.63±12.67ab27.81±3.7838.52±19.15术后6 个月18.18±8.45ab84.14±10.57ab35.47±3.39cb42.48±4.72cb术后12 个月20.11±11.43ab87.23±12.43ab37.43±11.12cb48.96±12.11cb
3 讨论
子宫肌瘤是育龄女性最常见的一种生殖器官良性肿瘤。从最近几年的报告来看,子宫肌瘤的发生率呈逐年增长的趋势。临床上治疗子宫肌瘤的方法有药物疗法、手术疗法及介入疗法等,但这些方法均有其各自的不足之处。近年来随着我国二胎及三胎政策的开放,很多子宫肌瘤患者都更倾向于选择对身体创伤较小的治疗方法。HIFU 消融术是通过将体外超声波聚焦于人体内的病灶部位,使病灶凝固性坏死,从而达到无创治疗目的的一种治疗手段。用HIFU 消融术治疗子宫肌瘤的安全性及有效性已得到了临床证实。但在治疗中发现,对于一些子宫肌瘤内部血供十分丰富的患者来说,由于其子宫肌瘤内部的血流速度较快,因此行HIFU 消融术时流动的血液会带走一部分的能量,使得治疗温度下降,从而导致超声治疗的效果降低[4-5]。本研究的结果显示,治疗后GnRH-a 联合组患者瘤体内部的血供等级较治疗前明显下降,其术中的能效因子、不良事件的发生率、术后的症状评分、UFS-QOL 评分、子宫体积缩小率和病灶体积缩小率均优于单独HIFU 组患者。提示用HIFU 消融术联合GnRH-a 治疗子宫肌瘤能有效减少肌瘤内部的血供,提高患者的疗效。随着子宫肌瘤内部血供的增加,其消融率会逐步下降。相关的研究表明,单纯的HIFU辐照只能破坏直径<2mm 的肿瘤滋养血管[6]。找到一种能够减少肌瘤内部血供的方法,就能增加超声能量的沉积,提高消融效率。GnRH-a 是GnRH 的合成类似物,可抑制子宫肌瘤的生长。《子宫肌瘤的诊治中国专家共识》中指出,GnRH-a 可缩小子宫肌瘤的体积。有研究发现,GnRH-a 缩小肌瘤是通过减少肌瘤中的血管数量和肌瘤的血供来实现的[7]。杨振华等[8]研究发现,行HIFU 消融术前使用曲普瑞林(一种GnRH-a)对子宫肌瘤患者进行辅助治疗,可明显缩短其手术的时间及辐照的时间,降低其并发症的发生率。这与本研究的结果大致相同。Yang 等[9]对18例T2WI 表现为均匀高信号的症状性子宫肌瘤患者进行研究,先采用GnRH-a 对其进行3 个月的治疗,再对其实施IFU 消融术,结果显示患者的疗效十分理想。本研究中GnRH-a 联合组患者术中的不良事件明显少于单独HIFU 组患者,考虑可能与GnRH-a 联合组患者术中消融的时间更短、能效因子更低有关[10]。
综上所述,用HIFU 消融术联合GnRH-a 治疗不同等级血供子宫肌瘤的效果显著,能有效减少肌瘤内部的血供及术中所需的能量,促使子宫和病灶的体积缩小,降低患者术中不良事件的发生率,减轻其临床症状,提高其生活质量。本研究也存的一定的不足之处,如不同等级血供子宫肌瘤术后的改变情况、消融率、能效因子等因本研究中的样本量较小而未详细进行分层对比,这有待于今后通过进一步扩大样本量来进行比较分析。

