自溶性微针基质材料的应用进展
姚碧金,刘冬榕,时军,庄泽槟
(广东药科大学中药学院,广东 广州 510006)
经皮给药系统(transdermal drug delivery systems,TDDs)是一类很有应用价值和市场潜力的制剂体系,具有控制药物释放、稳定血药浓度、无痛给药和减少剂量等优势,避免药物首过效应及给药过程的不适感,提高用药的安全性和适应性。近年来,TDDs在医药领域得到快速的发展,用于疾病预防、检测和治疗[1]。由于皮肤角质层(SC)的屏障作用,TDDs中药物的释放受限,因此有必要开发促进药物经皮渗透的方法,以增加药物在皮肤组织或血液中的浓度。
微针是一种经皮递药载体,能够机械穿透角质层屏障,几乎不触及真皮层血管及疼痛敏感的神经末梢,可促进大分子或亲水性药物的经皮传输。自溶性微针(dissolving microneedle,DMN)由药物与可溶解或生物降解的基质材料组成,其制备工艺及给药过程见图1。DMN用于皮肤给药后,基质材料吸收间质液便溶解或降解,释放的药物抵达真皮后随着血液循环到达病变部位发挥治疗作用,具有生物相容性、生物降解性、抗断裂强度和安全性等优点。与其他类型的微针相比,DMN避免了固体微针多步骤给药及生物锐器产生、中空微针制作成本高、涂层微针载药量低且剂量不准确、水凝胶微针给药速度慢等问题[2]。基质材料是DMN制造和使用的关键因素,必须满足生物稳定性、皮肤刺入率和用药安全性等要求。本文就自溶性微针基质材料的应用进展研究进行综述。
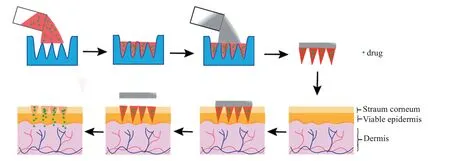
图1 微成型方法制备自溶性微针及自溶性微针给药的过程Figure 1 Preparation of dissolving microneedles by micro-forming method and the process of dissolving microneedles administration
1 天然水溶性基质材料
天然材料广泛来自动植物和微生物体内,具有可再生、可塑性、生物降解性和生物相容性,价廉易得,且不会对人体健康造成危害。自溶性微针的天然水溶性基质材料包括糖类和蛋白质类,这些材料与间隙液接触后迅速溶解,药物快速释放。
1.1 糖类
1.1.1 麦芽糖麦芽糖由两分子D-葡萄糖组成的天然碳水化合物,在皮肤内可被葡糖淀粉酶水解,具有生物相容性佳、稳定性高、成本低和安全性好等特点。麦芽糖有3种状态(液态、玻璃态、固态),活性化合物可以与液体状态下的麦芽糖混合,当麦芽糖处于玻璃态时形成微针,固体状态的麦芽糖可提供微针穿透皮肤所需的强度。Kolli等[3]采用微模压技术制造含盐酸尼卡地平的麦芽糖微针。该麦芽糖微针穿透皮肤深度约为160 μm,并很快在皮肤中溶解,增加药物的经皮透过率。Lee等[4]采用加热-拉伸法制备了载有抗坏血酸-2-葡萄糖苷和烟酰胺的自溶性麦芽糖微针。该微针稳定性好,且在刺入豚鼠皮肤20 min后完全溶解,动物实验证明可减少黑色素的沉积,抑制皮肤黑色素增多症。另外,麦芽糖可作为以聚乙烯吡咯烷酮或聚乙烯醇等为基质的自溶性微针的稳定剂[5]。
1.1.2 透明质酸透明质酸(HA),又名玻尿酸,是生物体内的非硫酸化糖胺聚糖,组成皮肤组织结构的亲水性成分,具有优异的保湿性、生物相容性和天然可降解性[6]。HA已被FDA批准用作皮肤填充剂,目前在微针中应用广泛。钦富华等[7]以透明质酸为基质材料,采用模具浇注法制备载有重酒石酸卡巴拉汀(RHT)的自溶性微针并对其经皮渗透性能进行考察。结果表明所制备的RHT自溶性微针贴片针长为500 μm,能有效穿透铝箔,在大鼠皮肤内的溶解时间为1 h;体外经皮试验中,1%RHT溶液和RHT自溶性微针的稳态透皮速率常数分别为3.08、8.04 μg/(cm2·h)。纯HA制备的微针,易脆且不易脱模。相较于HA的稳定性差、自由基敏感、机械强度差,透明质酸钠(SH)的力学强度和稳定性均增强。另外,可在配方中添加聚(马来酸烷基乙烯基醚),可增加HA-DMN的硬度[8]。为了改善抗疟疾药lumefantrine(LUM)口服利用率低的缺点,Volpe等[9]将LUM载于以SH为基质的微针中,制得的DMN-LUM具有强大的机械强度,能够穿透角质层释放药物,并能延长药物的作用时间。
1.1.3 硫酸软骨素硫酸软骨素(CS)是5种糖胺聚糖之一,是由D-葡萄糖醛酸和N-乙酰-D-半乳糖胺以β-1,3糖苷键连接而成,广泛分布于动物组织的细胞外基质和细胞表面,主要存在关节软骨中,是软骨修复和再生的重要分子,也是一种抗氧化和抗炎分子。硫酸软骨素已被证明是促进真皮成纤维细胞附着、生长和增殖的优良支架,在没有细胞毒性的情况下促进伤口愈合[10]。CS溶解在水中,在环境温度下形成高黏度凝胶,无需加热即可生产DMN。Naito等[11]证实,由CS组成的负载卵清蛋白(OVA)的自溶性微针锋利且强度足以穿透小鼠皮肤角质层,在短时间内有效地将负载的卵清蛋白输送到皮肤中,并在小鼠血清中诱导强烈的抗原特异性抗体反应,且其剂量-反应效率与皮内注射相当。为了提高干扰素-α-2b(IFN)的生物利用度,Chen等[12]以硫酸软骨素为基质材料,制成含有干扰素-α-2b的DMN,得到的IFN-DMN有利于提高IFN的稳定性。但由纯CS制成的IFN-DMN易碎。在此基础上,通过考察发现以质量浓度5%CS和45%聚乙烯吡咯烷酮(PVP)作为基质材料,得到的微针的药动学特征和肌肉注射组差异无统计学意义,且稳定、安全和不易碎。詹燕珊等[13]以硫酸软骨素和PVP为基质材料,制备装载丹参酮ⅡA固体分散体的自溶性微针并研究该微针对瘢痕增生的抑制作用及机制。实验表明,该微针穿透性强、安全稳定,可促进增生性瘢痕皮肤质地变软,降低皮肤增生厚度,消褪组织炎症。
1.1.4 壳聚糖壳聚糖(CH)是由天然多糖几丁质经过脱乙酰作用得到的,是一种直链阳离子多糖,具生物相容性、生物降解性、良好的机械强度和天然抗菌性等优良性能,被FDA普遍认为是安全的[14]。在体内,溶菌酶降解壳聚糖,产生无毒低聚糖,然后这些低聚糖可以结合到糖氨基多糖和糖蛋白中或被排泄。CH不溶于水中,仅在一定的酸性条件下才能完全溶解(pH≤6)。通过浇注法制备的载有美洛昔康的壳聚糖微针是一种成功的缓释剂,呈现出有序分布和均匀尺寸的微针,能成功地穿透牛尸体耳朵皮肤的角质层,建模等实验表明该DMN可能适用于牛常规手术后的疼痛管理[15]。Chi等[14]采用微模压方法制备了一种将血管内皮生长因子(VEGF)包裹在水凝胶中的壳聚糖微针阵列贴片。实验证明该微针可以在伤口闭合期间抑制炎症,促进胶原沉积、血管生成和组织再生。
1.2 蛋白质类
丝素蛋白(SF)是应用最多的蛋白质类DMN基质材料,为FDA批准的医疗设备,可为创面提供较理想的愈合条件,利于皮肤创面修复[16]。SF是从蚕丝中提取的具有规则疏水和亲水结构域天然高分子纤维蛋白,具有出色机械性(优良的韧性和延展性)、生物降解性、生物相容性、低免疫原性和缓释性。SF的体内降解产物无毒,且具有抗炎和抗氧化特性[17]。Yavuz等[16]使用聚二甲基硅氧烷(PDMS)模具制备载有避孕药左炔诺孕酮(LVN)的SF微针,得到的LVN-DMN性质稳定、无需冷藏且持续透皮给药超过3个月。在此基础上,当药物装入DMN内后,再将其装入微针贴片内,释放延长到1 a。Zhu等[18]将胰岛素/丝素蛋白的混合溶液倒入PDMS模具中制得微针尖端,丝素/脯氨酸/胰岛素混合溶液作为微针的底座,以获得复合载药微针。微针针尖具有良好的溶解性,能够快速溶解,促进胰岛素的释放。该底座具有膨胀而不溶解的特性,可作为药库携带胰岛素。动物实验表明,该微针具有明显的降血糖作用,并显示出缓释作用。
此外,胶原蛋白及其衍生物、蚕丝、明胶和玉米醇溶蛋白是少数用于制造DMN的蛋白质基质材料。据推测,此类材料能更好地与蛋白质类药物或疫苗相互作用,并有助于微针的高载药量和更好的稳定性[19]。
其他天然基质材料见表1。

表1 其他天然基质材料Table 1 Other natural substrate materials
2 合成可生物降解的高分子基质材料
可生物降解高分子材料在皮肤环境中可被皮肤微生物或其分泌物在酶或化学分解作用下发生降解,具有生物相容性、降解产物无毒性、生产成本低和结构及性能可调控的优势。该类材料主要包括有聚乙烯醇、聚乙烯吡咯烷酮、聚乳酸、聚乙醇酸、聚丙交酯-共-乙交酯、羧甲基纤维素、聚碳酸酯和聚甲基乙烯基醚-马来酸酐等。
2.1 聚乙烯醇
聚乙烯醇(PVA)是一种由醋酸乙烯单体聚合后醇解制成的水溶性聚合物材料,具有生物降解性、生物相容性、耐酸碱性、柔韧性好和成膜性能好等诸多优良特性。PVA在纳米抗菌材料、可降解材料、包装材料等领域均获得广泛的应用。PVA的醇解度和聚合度决定了其水溶性的大小。Liu等[22]通过溶液浇铸法制备以PVA为基质材料的DMN,在微针制造和干燥过程中,发现较高浓度的PVA有助于制备具有药物浓缩在尖端的DMN。该微针具有足够的机械性能,可以顺利刺入皮肤。Zhang等[27]制备并考察载有碳化艾草和前列腺素E2的PVA微针对受损骨骼肌的修复作用。结果表明,与经典艾灸治疗相比,该系统能更快地恢复肌肉损伤小鼠模型的肌肉力量和肌束纤维的横截面积。此外,它还可以成功诱导肌肉干细胞的增殖和分化,从而有效修复受损的肌肉组织。
2.2 聚乙烯吡咯烷酮
聚乙烯吡咯烷酮(PVP),也称聚维酮,是一种水溶性的乙烯基聚合物的衍生物,具有优良的生理惰性、生物相容性、吸湿性、增溶或凝聚作用,被FDA认为是安全的。PVP可调控药物的释放,提高水溶性差药物的生物利用度,并能掩盖不愉快的气味[28]。PVP平均分子量越大,黏接性越强,溶解越慢。李敏姝等[29]将布林佐胺溶于乙醇,加入PVP K90溶解后,灌注于微针模具中,干燥后脱模得到眼用角膜布林佐胺自溶性微针。该微针为圆锥形,高约750 μm,针尖距约500 μm,载药量高达7.3 mg/cm2;其机械强度较大(0.32 N/针),易插入大鼠角膜中,深度达200 μm,微针在2 min内就可快速溶解,受损角膜于24 h内可快速修复。此外,布林佐胺微针的体外释放率在2 h内高达93%,药物角膜渗透量为(877±105)μg。但是,PVP-DMN的快速溶解特性在一定方面限制了其应用,例如,在某些疾病条件下,立即给药可能会导致潜在的局部刺激或系统性过敏反应。因此,选用PVP作为基质材料时,可加入药用纤维素,如羟丙基甲基纤维素和甲基纤维素,作为微针的溶解改性剂,控制DMN的溶解速率[30]。
2.3 羧甲基纤维素
羧甲基纤维素(CMC)是一种阴离子型纤维素醚类的脱水葡萄糖的线性多糖,具有良好的溶解性和生物可降解性,可溶于水且成本低。欧洲食品安全局报告称,CMC是一种安全的食品添加剂。CMC有吸湿性,对光热稳定,黏度随温度升高而降低。在生物医学领域,CMC及其复合材料广泛应用于组织工程、伤口敷料和生物相容性植入物的3D支架制备等[31]。Yun等[32]将CMC作为基质材料来制备含有抗嗜水气单胞菌感染的疫苗DMN贴片。在皮肤插入实验中,DMN贴片被证实能够穿透鱼皮肤的角质层。通过凝集试验和对溶菌酶和超氧化物歧化酶等非特异性参数的分析,证实该微针贴片可诱导鱼类产生适应性和先天性免疫反应,且疗效与腹腔注射组几乎相似。陈欢欢等[33]开发了装载雷公藤甲素的CMC-CS双室自溶性微针,并进行质量评价及体外透皮性能的考察。制备的双室载药微针外观形态、机械性能良好;每片含药量为(218.88±0.10)μg;体外透皮实验表明,72 h内雷公甲素累积透皮率达98%。
2.4 聚乳酸-羟基乙酸共聚物
聚乳酸-羟基乙酸共聚物(PLGA)由2种单体—乳酸和羟基乙酸聚合而成的高分子有机化合物,具有良好的机械性能、生物相容性、生物降解性且降解速度可控的性能。PLGA被FDA批准为药用辅料和临床伤口敷料,可促进血管生成并加速伤口愈合[34],在人体内最终代谢为二氧化碳和水。PLGA的机械性能和降解性能可以通过丙交酯和乙交酯的不同比例进行调整,降解时间从几周到几个月不等,当两者的比例为50∶50时,降解速度最快。PLGA适用于骨修复,是一种具有良好生物相容性和可加工性的人工骨支架材料。Panda等[35]将溶菌酶分别包埋在PVP、HA和PLGA中,采用模具铸造技术制作了DMN。结果发现PLGA微针比PVP和HA微针需要更大的穿刺力,这可能是由于PLGA聚合物的刚性结构导致形成更宽的微针直径。PVP微针和HA微针的药物释放曲线显示瞬时释放,而PLGA微针相对缓释。另外,PVP和HA制造的微针表面光滑,而PLGA制造的微针具有粗糙的外观,这是PLGA聚合物的特征。Lee等[36]证明了PLGAMN输送系统长期输送左炔诺孕酮的可行性。
2.5 其他合成基质材料
自溶性微针的其他合成基质材料见表2。
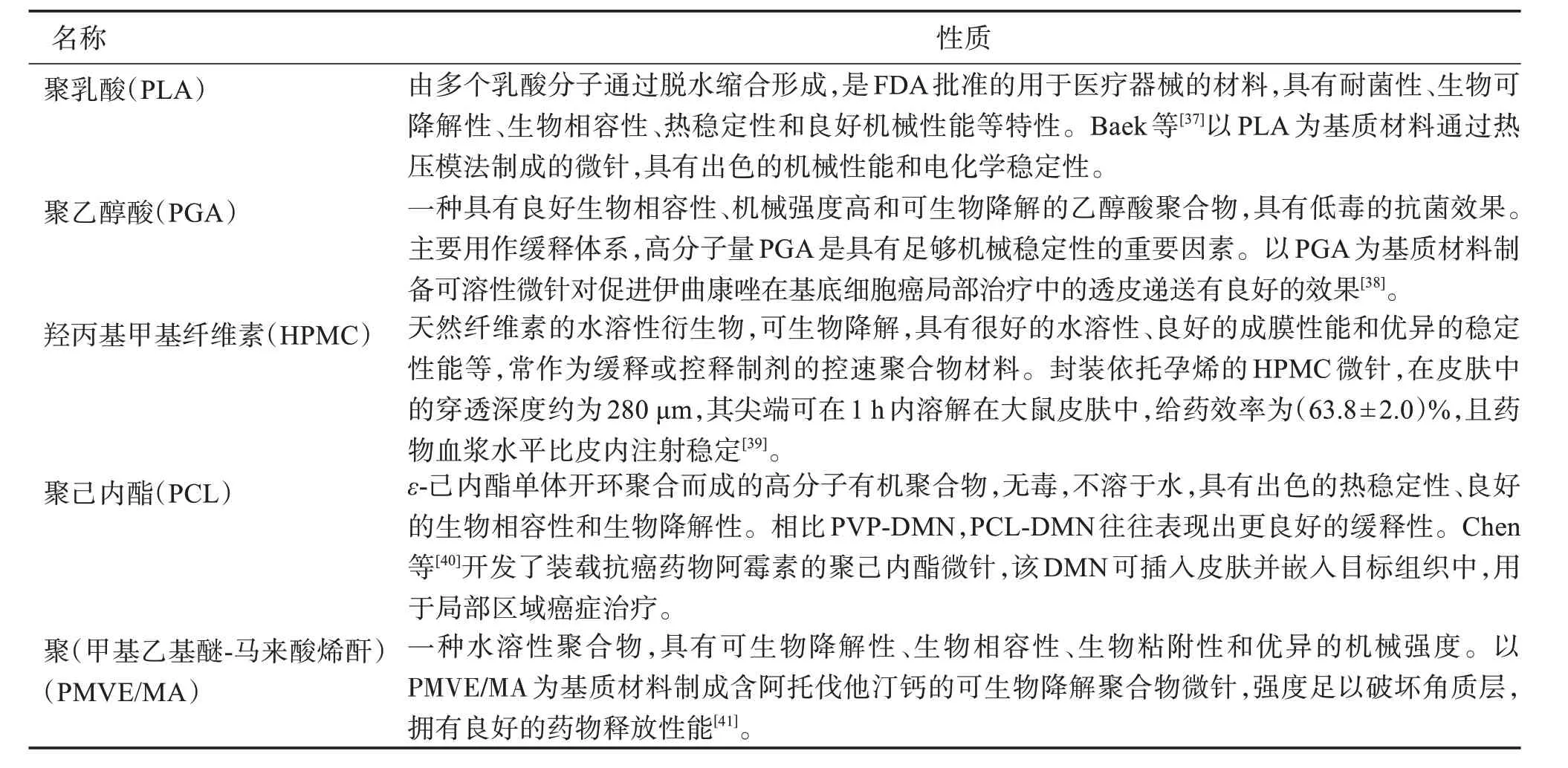
表2 其他合成聚合物基质材料Table 2 Other synthetic polymer substrate materials
3 自溶性微针基质材料应用面临的挑战
自溶性微针基质材料具有生物相容性好、可生物降解及可控制药物释放速率等优点,为DMN的广泛应用奠定了基础。但需关注的是,将自溶性微针进一步应用于临床给药还面临很多挑战。
3.1 稳定性
自溶性微针的稳定性对药物能否发挥药效或是否产生毒副作用至关重要。影响DMN的稳定性因素有很多。首先,部分DMN的基质材料有吸湿性,如PVP、CS和CMC等,这种吸湿性导致微针从生产过程中吸收水分,水分的存在很大可能对成品结构完整性、机械性能及药效产生负面影响。DMN在制造过程的高离心力、真空压力或高温等苛刻的加工条件也可能会降低药物的稳定性。另外,一些药物(如蛋白质和疫苗)在物理和生物环境中都极易降解,载于微针同样容易失效。已有研究表明:蚕丝和海藻糖可作为流感疫苗微针的稳定剂,在制造DMN是中掺入少量氧化石墨烯可显著提高微针的防潮性;使用双喷嘴喷雾沉积工艺制作DMN,可提高微针中蛋白质的稳定性[42-43]。因此,未来研究可以通过维持良好的生产环境、调整DMN配方比例或优化制备工艺等手段来保证其稳定性。
3.2 机械强度与载药量
基质材料机械强度是DMN能否穿透皮肤角质层的重要因素。首先,皮肤本身的弹性和韧性较大的基质材料(如PVA、CMC-Na)的使用,会导致DMN难以完全插入皮肤中;另外,部分脆性材料(如PVP、CS)单一使用时容易因为过脆而发生断裂。为了应对这一挑战,在制备DMN时往往选择两种或两种以上的基质材料混合使用,结合各材料之间的优势,以期使微针具有良好的机械性能,负载更多的药物含量。Xing等[44]优选PVA和PVP作为基体材料制备含有氨甲环酸的DMN,该微针能显著提高氨甲环酸的经皮透皮量,并减少黄褐斑豚鼠皮肤中黑色素的沉积。载药量小是DMN应用发展的一个限制因素。虽然可以在保证针体硬度的条件下,通过增加配方中药物的比例来增加载药量,但增加量还是比较微小的。未来可采用离心、再填充和蒸发等手段浓缩药物和载药纳米颗粒或开发具有较大药物负载能力的DMN的新型聚合物材料等方法来提高微针的载药量。
3.3 安全性
DMN的基质材料具有生物相容性和可生物降解性,在插入皮肤后完全溶解或降解,但关于用DMN反复穿透皮肤或聚合物沉积在皮肤中的长期影响知之甚少,且对于人体的长期毒性研究仍然有所欠缺。因此,在临床环境中常规使用DMN之前,需要充分考察基质材料在人体中的积累、生物分布以及长期毒性,确保DMN的安全性。
无痛、微创、安全、高效是DMN用于透皮给药的优势。同时,稳定性差、机械强度和皮肤穿刺能力不合适、载药量低和长期毒性研究有所欠缺,导致DMN无法规模化生产,是其在市场上应用的挑战。相信在这些问题得到妥善解决后,DMN在各类治疗药物输送中的应用将会越来越广泛。
4 小结
综上所述,用于制备自溶性微针的基质材料性质不尽相同,实际应用中,往往选择两种或两种以上的基质材料混合使用制备DMN,结合各材料之间的优势,以期获得合适的机械强度、释药速率和成型性能。自溶性微针由于其生物相容性好、患者依从性好、可生物降解、不产生针尖废弃物、可自主给药和安全性高等诸多优势在药物经皮给药领域具有巨大的潜力。相信随着微加工技术的不断发展和自溶性微针经皮递药系统的进一步研究,尤其是纳米粒、水凝胶、脂质体等微粒递药体系与基质的结合与应用,自溶性微针在抗肿瘤、降血糖、疫苗接种、临床检测和医学美容等领域将发挥越来越重要的作用,为广大病患者带来福音。

