古代经典名方芍药甘草汤基准样品的制备工艺研究
汤春花,梁凤友,林碧珊,高永坚,曾杉
(国药集团广东环球制药有限公司,广东 佛山 528305)
经典名方芍药甘草汤出自东汉张仲景的《伤寒论·辨太阳病脉证并治》第29条:“伤寒脉浮,自出汗,小便数,心烦,微恶寒,脚挛急……若厥愈足温者,更作芍药甘草汤与之,其脚即伸”。原处方为:白芍药、甘草(炙,各四两),上二味,以水三升,煮取一升五合,去滓,分温再服[1]。张仲景的芍药甘草汤被历代医家推崇,其加减组方一直沿用至今[2],是国家中医药管理局公布的《古代经典名方目录(第一批)》中的经典名方之一。主治津液受损、阴血不足、筋脉失濡所致诸证。方中芍药酸寒,养血敛阴,柔肝止痛;甘草甘温,健脾益气,缓急止痛。二药相伍,酸甘化阴,调和肝脾,有柔筋止痛之效。根据文献论著可知[3-8],芍药甘草汤基准样品的现代制备工艺为:取白芍、炒甘草饮片各12 g,加水600 mL,武火煮沸转文火煎煮至煎液约300 mL,过滤,即得。
据文献报道[9],芍药甘草汤含量测定指标主要是芍药苷、甘草苷、甘草酸等成分,且均已被证实为该方的药效成分。本研究在前人考证的基础上,通过试验考察确定浸泡时间、煎煮容器材质、煎煮时间、过滤方式对芍药甘草汤基准样品制备工艺的影响,以出膏率、浸出物和芍药苷、甘草苷、甘草酸含量作为评价指标,确定最佳制备工艺并进行了工艺验证,为芍药甘草汤进一步开发为复方颗粒提供依据。
1 仪器和材料
1.1 仪器
H-class UPLC色谱仪(PDA二极管阵列检测器,Waters公司);500瓦陶瓷锅(深圳市一枚王电子商务有限公司);不锈钢锅;SY-901多功能电磁炉(中山市南菱电子科技有限公司);HH-4型水浴锅(常州奥华仪器有限公司);HN101型电热鼓风干燥箱(上海苏进仪器设备厂);AL104型电子天平(梅特勒-托利多仪器(上海)有限公司);KQ5200DA型超声清洗仪(昆山市超声仪器有限公司);ST 16型高速离心机(Thermo)。
1.2 试药
芍药苷(批号:110736-201741)、甘草苷(批号:111610-201607)、甘草酸铵(110731-201720)由中国食品药品检定研究院提供。甲醇、乙腈为HPLC级,实验用其他试剂均为AR级。
1.3 药材
生白芍(安徽亳州,批号:H-BS01Y)、甘草(甘肃酒泉,批号:H-ZGC01Y),由广东一方制药有限公司鉴定分别为毛茛科植物芍药Paeonia lactifloraPall.的干燥根、豆科植物甘草Glycyrrhiza uralensisFisch.的干燥根和根茎,按2020年版《中国药典》[10]检验均合格。白芍饮片、炒甘草饮片分别按2020年版《中国药典》[10]和2008年版《上海市中药饮片炮制规范》[11]炮制而得。
2 试验方法
2.1 样品的制备方法
取白芍、炒甘草饮片各12 g,加水600 mL,武火煮沸转文火煎煮至煎液约300 mL,过滤,即得。
2.2 出膏率测定
取芍药甘草汤煎液10 g,精密称定,水浴蒸干后,105℃烘箱干燥3 h,置干燥器中放冷,精密称重,测得干固物质量,计算固含率(%)和出膏率(%),公式如下:
2.3 浸出物含量测定
取芍药甘草汤煎液50 g,精密称定,置分液漏斗中,加水饱和正丁醇萃取3次,每次50 mL,合并正丁醇层,置已称重的蒸发皿中,在水浴上蒸干溶剂,并在105℃烘箱中烘干3 h,取出放置于干燥器中放冷,精密称定,计算浸出物含量,公式如下:

2.4 含量测定
2.4.1 色谱条件
色谱柱:Waters BEH C18柱(1.7 µm,2.1×100 mm);流动相:乙腈(A)-0.1%磷酸(B),梯度洗脱(0~7 min,5%→15%A;7~15 min,15%→50%A;15~18 min,50%→100%A);流速为0.25 mL/min;柱温为30℃;进样量1 μL;检测波长为230 nm。
2.4.2 对照品溶液制备
取芍药苷、甘草苷、甘草酸铵对照品适量,精密称定,加甲醇制成每1 mL各含芍药苷80 μg、甘草苷20 μg、甘草酸铵200 μg的混合溶液,即得。
2.4.3 供试品溶液制备
取相当于0.12 g干固物的芍药甘草汤煎液,精密称定,置25 mL量瓶中,加入甲醇适量,超声处理(功率500 W,频率40 kHz)20 min,放冷,用甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。
2.4.4 含量测定方法学考察
2.4.4.1 专属性考察精密吸取供试品溶液(批号:SG200531)、混合对照品溶液与白芍、甘草阴性样品溶液各1 μL,按“2.4.1”项下色谱条件测定,结果见图1。结果表明,阴性样品溶液在供试品溶液色谱图相应位置上无对应色谱峰出现,说明该方法专属性较好。
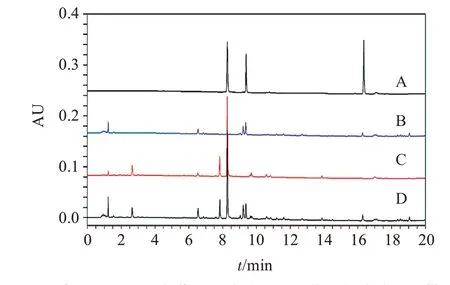
图1 专属性考察Figure 1 Exclusivity investigation
2.4.4.2 线性考察分别精密称定芍药苷对照品21.08 mg(纯度96.8%)、甘草苷对照品10.19 mg(纯度95.0%)、甘草酸铵对照品20.87 mg(纯度96.2%),置50 mL棕色量瓶中,加甲醇稀释至刻度,摇匀,分别制成每1 mL含芍药苷408.11 μg、甘草苷193.61 μg、甘草酸铵401.54 μg的对照品溶液。
分别精密量取芍药苷、甘草苷和甘草酸铵对照溶液适量,逐级稀释成质量浓度分别为50%、25%、12.5.%、6.25%、3.125%的溶液,按照“2.4.1”项中色谱条件测定,记录不同质量浓度(x)对照品的色谱峰面积(y),拟合得到线性回归方程为:芍药苷y=2 731.5x-5 538.7(r=0.999 6)、甘草苷y=4 777x-1 205.5(r=0.999 9)、甘草酸铵y=787x-487.3(r=0.999 9),结果表明芍药苷、甘草苷、甘草酸铵分别在12.75~408.11、6.05~193.61、12.55~401.54 μg/mL的范围内线性关系良好。
2.4.4.3 精密度试验精密吸取供试品溶液(批号:SG200531),按“2.4.1”项下色谱条件重复进样6次,测定芍药苷、甘草苷、甘草酸的峰面积和含量,计算芍药苷、甘草苷、甘草酸含量范围分别是4.81%~4.85%、1.39%~1.41%、1.75%~1.78%,RSD分别为0.46%、0.54%和0.77%,表明精密度良好。
2.4.4.4 稳定性试验精密吸取供试品溶液(批号:SG200531),按“2.4.1”项下色谱条件分别在0、4、8、12、16、20、24 h进样,测定芍药苷、甘草苷、甘草酸的峰面积和含量,计算芍药苷、甘草苷、甘草酸含量范围分别为4.82%~4.84%、1.39%~1.42%、1.72%~1.76%,RSD分别为0.27%、0.78%和0.85%,表明供试品溶液在24 h内稳定性良好。
2.4.4.5 重复性试验分别取相当于0.06、0.12、0.18 g干固物的芍药甘草汤煎液(批号:SG200531),精密称定,制备3种不同浓度的供试品溶液,每种浓度平行3份。按“2.4.1”项下色谱条件进样测定芍药苷、甘草苷、甘草酸含量,计算芍药苷、甘草苷、甘草酸含量范围分别是4.78%~4.91%、1.38%~1.43%、1.72%~1.78%,RSD分别为0.76%、1.01%和1.03%,表明该分析方法的重复性良好。
2.4.4.6 中间精密度考察由本项目组其他分析人员在不同日期和不同色谱仪下操作。分别取相当于0.06、0.12、0.18 g干固物的芍药甘草汤煎液(批号:SG200531),精密称定,制备3种不同浓度水平的供试品溶液,每种浓度平行3份。按“2.4.1”项下色谱条件分析测定芍药苷、甘草苷、甘草酸含量,计算芍药苷、甘草苷、甘草酸含量范围RSD分别为0.76%、0.66%、0.90%,表明中间精密度良好。
2.4.4.7 加样回收试验分别取相当于0.03、0.06、0.09 g干固物的芍药甘草汤煎液(批号:SG200531),精密称定,分别加入50%、100%和150%浓度的芍药苷、甘草苷、甘草酸对照溶液,制备成供试品溶液,按“2.4.1”项下色谱条件进样测定,计算芍药苷、甘草苷、甘草酸回收率(n=9)分别为97.76%、98.57%、98.63%,RSD分别为1.22%、0.86%、2.23%,均满足2020年版《中国药典》[10]要求。
2.4.4.8 耐用性考察
①不同色谱柱考察
精密吸取供试品溶液(批号:SG200531),按“2.4.1”项下色谱条件,分别考察了5种不同类型的色谱柱Agilent SB C18柱(1.8 µm,2.1 mm×100 mm)、Waters BEH C18柱(1.7 µm,2.1 mm×100 mm)、Agilent Bonus RP C18柱(1.7µm,2.1 mm×100 mm)、Waters CSH C18柱(1.7 µm,2.1 mm×100 mm)、YMC Triart C18柱(1.9 µm,2.1 mm×100 mm)对芍药苷、甘草苷、甘草酸色谱峰的分离情况,见图2。结果显示,Waters BEH C18色谱柱分离效果最佳,故选择Waters BEH C18色谱柱进行研究。

图2 不同色谱柱的考察Figure 2 Investigation of different chromatographic columns
②不同柱温考察
精密吸取供试品溶液(批号:SG200531),按“2.4.1”项下色谱条件,分别在不同柱温(25、30、35℃)平行进样2次,考察对芍药苷、甘草苷、甘草酸含量测定的影响。实验显示,25、30、35℃柱温下,芍药苷、甘草苷、甘草酸含量范围分别是4.82%~4.85%、1.39%~1.42%、1.71%~1.75%,RSD值分别为0.31%、0.86%、0.94%,表明不同柱温对指标含量的影响较小,本实验选择柱温30℃。
③不同流速考察
精密吸取供试品溶液(批号:SG200531),按“2.4.1”项下色谱条件,分别在不同流速(0.20、0.25、0.30 mL/min)平行进样2次,考察对芍药苷、甘草苷、甘草酸含量测定的影响。结果显示三种流速下芍药苷、甘草苷、甘草酸含量范围分别是4.84%~4.85%、1.37%~1.40%、1.72%~1.76%,RSD分别为0.17%、0.76%、0.81%,表明流速对含量测定影响较小,本实验选择流速0.25 mL/min。
3 基准样品制备工艺研究
3.1 预实验(得液量的考察)
取同一批白芍、炒甘草饮片各12 g,分成两组,每组平行6份,置陶瓷锅中,加水600 mL,浸泡30 min,武火煮沸后,第一组选用功率200 W分别煎煮20、40、60 min,第二组选用功率300 W分别煎煮20、40和60 min,趁热过滤考察得液量,结果见表1。结果表明功率200 W煎煮60 min和300 W煎煮40 min,得液量在300 mL±10%之间,符合试验目标。
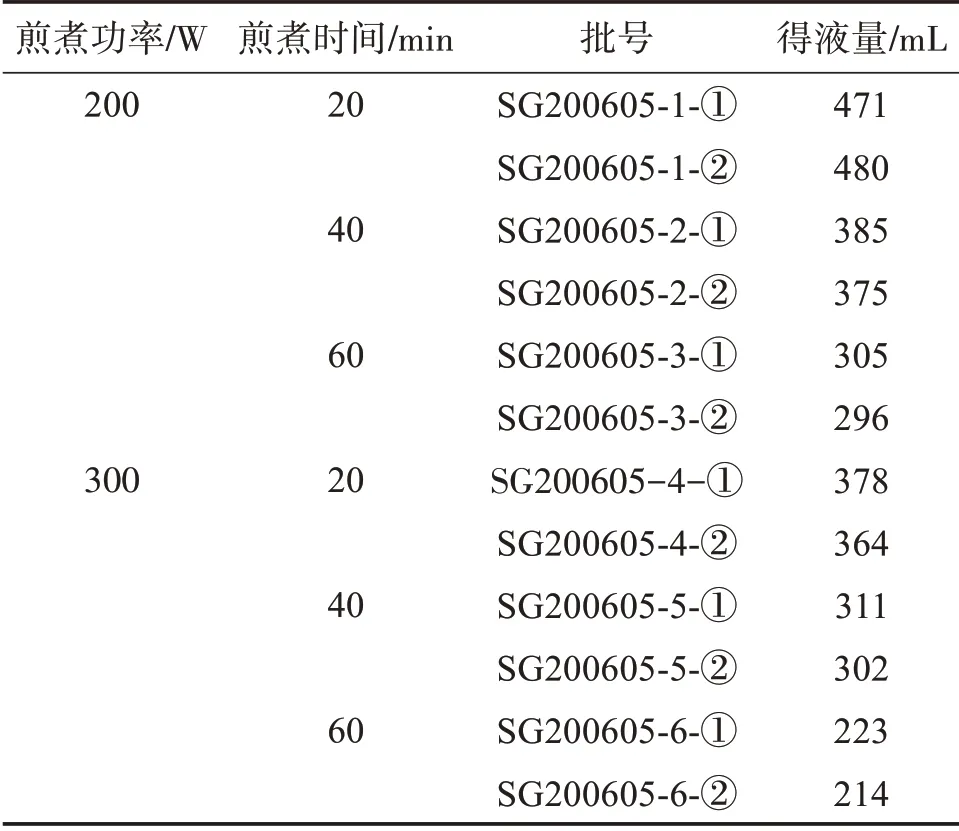
表1 得液量考察Table 1 Investigation of decoction volume
3.2 浸泡时间的考察
取同一批白芍、炒甘草饮片各12 g,平行6份,分别浸泡30 min和60 min,同法煎煮、过滤。按照“2.2”“2.3”“2.4”项下的方法测定出膏率、浸出物以及芍药苷、甘草苷、甘草酸含量,结果见表2。结果表明不同浸泡时间对出膏率、浸出物和芍药苷、甘草苷、甘草酸含量均无明显影响。为提高效率,选择浸泡30 min。
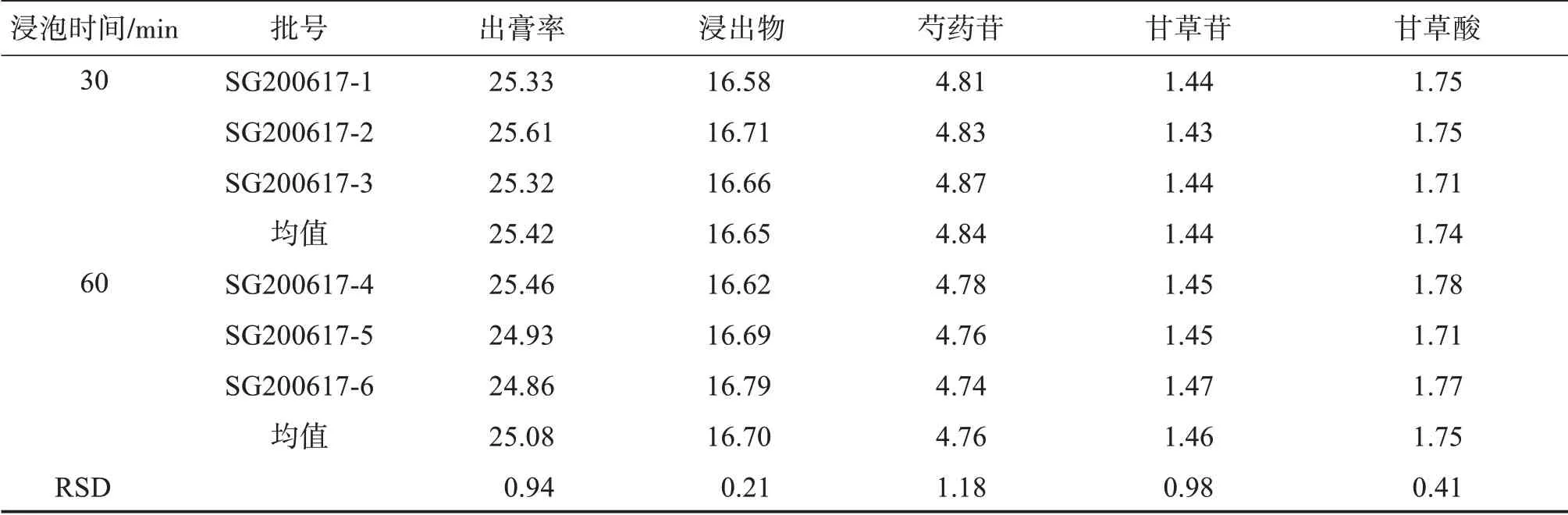
表2 浸泡时间考察Table 2 Investigation of soaking time w/%
3.3 煎煮器具的考察
取同一批白芍、炒甘草饮片各12 g,平行6份,分别置陶瓷锅和不锈钢锅,同法煎煮,所得煎液约300 mL,趁热过滤。按照“2.2”“2.3”“2.4”项下的方法测定出膏率、浸出物以及芍药苷、甘草苷、甘草酸含量,结果见表3。结果显示陶瓷锅基准样品出膏率和芍药苷、甘草苷、甘草酸含量优于不锈钢锅,故采用陶瓷锅作为煎煮容器。

表3 煎煮器具的考察Table 3 Investigation of decoction utensils w/%
3.4 煎煮时间的考察
取同一批白芍、炒甘草各12 g,平行6份,置陶瓷锅中,加水600 mL,浸泡30 min,武火煮沸后转文火煎煮,其中三份功率300 W煎煮40 min,另三份功率200 W煎煮60 min,趁热过滤。按照“2.2”“2.3”“2.4”项下的方法测定出膏率、浸出物以及芍药苷、甘草苷、甘草酸含量,结果见表4。结果显示不同煎煮时间的出膏率、浸出物和芍药苷、甘草苷、甘草酸含量均无明显差异。为提高煎煮效率,选择煎煮时间40 min。

表4 煎煮时间的考察Table 4 Investigation of decoction time w/%
3.5 过滤方式的考察
取同一批白芍、炒甘草饮片各24 g,置陶瓷锅中,加水1 200 mL,浸泡30 min,武火煮沸转文火煎煮40 min,所得煎液约600 mL,分成平行5份,分别采用不同的过滤方式:①趁热用纱布过滤;②趁热过200目筛网;③趁热过350目筛网;④趁热过680目筛网;⑤离心,取上清液。分别按照“2.2”“2.3”“2.4”项下的方法测定出膏率、浸出物以及芍药苷、甘草苷、甘草酸含量,结果见表5。结果表明五种过滤方式的出膏率、浸出物和芍药苷、甘草苷、甘草酸含量均无显著差异,而纱布和200目网筛过滤滤液浑浊,350目筛网易过滤且滤液澄清,故采用350目网筛。
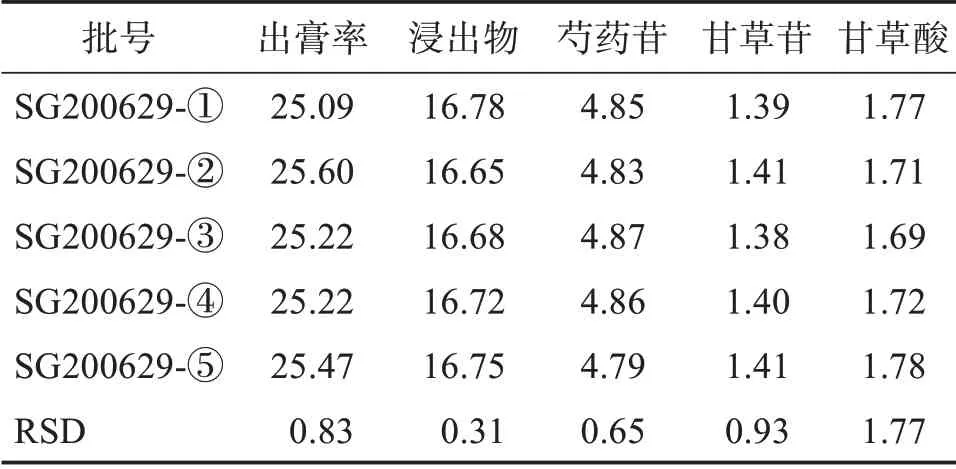
表5 过滤方式的考察Table 5 Investigation of filter method w/%
4 工艺验证
综上所述,芍药甘草汤基准样品的制备工艺为:取白芍、炒甘草饮片各12 g,置陶瓷锅中,加水600 mL,浸泡30 min,武火煮沸转文火煎煮40 min,所得煎液约300 mL,趁热过350目筛网,即得。
按上述方法,平行制备6批标准煎液,按照“2.2”“2.3”“2.4”项下的方法测定其出膏率、浸出物以及芍药苷、甘草苷、甘草酸含量,结果如表6所示,说明所建立的芍药甘草汤基准样品制备工艺稳定可行,重复性好。
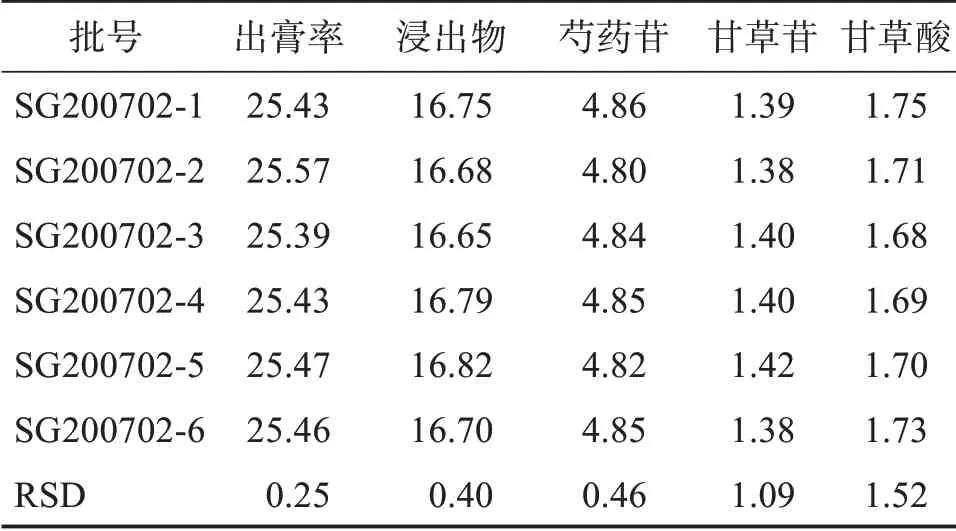
表6 工艺验证结果Table 6 Results of process validation w/%
5 讨论
经典名方是至今仍广泛应用、疗效确切、具有明显特色与优势的古代中医典籍所记载的方剂。2018年5月,国家药品监督管理局发布的《古代经典名方中药复方制剂简化注册审批管理规定》明确指出经典名方复方制剂开发必须首先进行物质基准(基准样品)研究,为其后的制剂开发提供依据。在两千多年的历史发展过程中,经典名方的药物基原、炮制、剂量、煎煮法、功能主治等历经变化,莫衷一是,因此关键信息考证是经典名方开发利用的关键性、源头性问题。《伤寒论》[1]记载的芍药甘草汤“白芍药甘草(炙,各四两),上二味,以水三升,煮取一升五合,去滓,分温再服”,据文献考证[8],原方芍药基原为芍药科多年生草本植物芍药Peaonia lactifloraPall.的根;甘草基原为乌拉尔甘草Glycyrrhiza uralensisFisch.。而对于原文所述“炙甘草”经过考证应该是炒甘草,同时原文所述“白芍药”即生用白芍药。计量方面,原方的一两合今3 g、一升合今200 mL[3-4]。
在“遵古”的基础上充分考虑当前临床和生产实际是经典名方开发的主要原则[8],本文在前人考证的基础之上,通过试验考察浸泡时间、煎煮容器材质、煎煮时间、过滤方式对出膏率、浸出物以及芍药苷、甘草苷、甘草酸含量的影响,从而确定基准样品最佳现代制备工艺。
根据《医疗机构中药煎药室管理规范》[12]要求,煎煮前饮片的浸泡时间应不少于30 min。本文考察了浸泡30 min和浸泡60 min对评价指标的影响,结果显示两者差异不大,为提高效率选择浸泡30 min。传统的煎药器皿主要以砂锅、陶瓷锅为主,现代煎药多采用金属不锈钢容器进行煎煮,研究显示陶瓷锅煎煮在指标性成分浓度及出膏率上优于砂锅[13],因此本文考察了陶瓷锅和不锈钢锅对芍药甘草汤煎煮的影响,结果显示陶瓷锅制得的基准样品出膏率和芍药苷、甘草苷、甘草酸含量均高于不锈钢锅,故采用陶瓷锅作为煎煮容器。由于古籍记载古代煎药多“常令文火小沸”[14],故考察了文火煎煮40 min和煎煮60 min对煎液的影响,结果无明显差异,为提高效率选择煎煮时间40 min。文中还考察了5种不同过滤方式对煎液的影响,结果提示彼此无明显差异,最终采用趁热过350目筛网。还通过工艺验证证明了制备工艺的稳定可行,为芍药甘草汤进一步开发为复方颗粒提供了科学依据。

