高水分活度中药制剂处方分析与微生物污染风险预测
李 辉, 马仕洪, 朱加武, 胡 科, 绳金房, 钱卫东, 田 斌*
(1.陕西科技大学 食品科学与工程学院, 陕西 西安 710021; 2.陕西盛德泰林生物安全技术检测有限公司, 陕西 西安 710065; 3.中国食品药品检定研究院, 北京 100050; 4.西安海欣制药有限公司, 陕西 西安 710075; 5.陕西省药品技术审评中心, 陕西 西安 710065)
0 引言
水分活度(aw)是影响微生物生长繁殖的关键因素[1],而高水分活度液体/半固体制剂因其微生物污染风险较高而引起普遍关注.近年来发生多起高水分活度的制剂的微生物污染事件[2-4],2021年7月美国FDA发布公告提醒药品生产者,洋葱伯克霍尔德菌复合体(BCC)可能会对水基非无菌药品造成污染风险[5].国内也报道了多起高水分活度液体/半固体制剂的微生物污染和生长繁殖问题[6-12].
为进一步提高药品质量,《中国药典》2020年版四部对高水分活度的非无菌药品微生物控制提出了更严格的要求,将1107非无菌产品微生物限度标准中的液体制剂和半固体的微生物限度标准要求合并,修订为“液体及半固体制剂”[13,14].受中药饮片的微生物污染等因素影响[15,16],非无菌中药制剂可能存在一定水平的生物负载,且中药成分复杂,常含有糖、蛋白质等多种营养物质,而所使用抑菌剂抗菌谱具有局限性,致使高水分活度的中药液体/半固体制剂更有利于微生物的生长繁殖,因此,高水分活度的中药液体/半固体制剂是非无菌制剂中微生物污染和增殖风险最高的剂型.
研究中药液体/半固体制剂的水分活度,评估微生物增殖风险,探讨利用aw、pH、抑菌剂等因素协同作用进行处方评价和优化的方法,对于提升制剂自身抵御微生物增殖风险的能力,进而提高中药制剂的质量安全具有现实意义.本文分析5种常见非无菌中药液体/半固体制剂的水分活度,探讨水分活度与处方之间的关系,并对其最可能的潜在微生物增殖风险进行预测,进而选择2种高水分活度的中药制剂采用人工模拟污染的方法对预测结果进行验证,以期利用aw进行非无菌中药制剂的抑菌剂筛选和微生物控制.
1 材料与方法
1.1 实验样品
测定水分活度所使用的5种剂型的中药制剂信息见表1所示.

表1 水分活度测定用中药制剂样品信息
微生物增殖预测的验证实验采用萸杞滋肾膏(A)和小儿生血糖浆(B)进行.
1.2 实验仪器
使用的仪器设备为水分活度测定仪(Aqualab Series 4TEV,METER Group,Inc.USA),使用前经过验证和校准,采用aw分别为0.500,0.760,0.920,1.000的标准液进行校准,均满足±0.003 aw的精度要求.
1.3 试验菌株
金黄色葡萄球菌、铜绿假单胞菌、大肠埃希菌、白色念珠菌、黑曲霉均购自中国医学细菌保藏管理中心(CMCC),试验菌株为第3代,洋葱伯克霍尔德菌购自中国工业微生物菌种保藏管理中心(CICC),试验菌株为第4代,均满足《中国药典》2020年版中试验菌株不超过5代的要求.
1.4 实验方法
依据《中国药典》2020年版制剂通则,选择5种不同剂型的常见中药液体/半固体制剂,每种剂型选择3个以上的品种,每个品种收集3个以上批次的样品.实际获得的实验样品与设计的理想状况略有不同.测定前,对所用设备进行验证和校准.测定时,在室温条件下,取均匀的样品3~5 mL,使样品铺满杯底部且不超过样品杯容量的1/2,将设备手柄置于OPEN位置,然后把样品杯放到样品仓,盖上盖子,并且拨动手柄至READ位置,等待2~5 min,读数稳定后,记录设备屏幕上显示的aw和温度.测试完毕后,取出样品并开始下一份样品的测试.每份样品平行测定3次.
选择未添加抑菌剂的2种中药制剂A煎膏剂和B糖浆剂,分别接种金黄色葡萄球菌、铜绿假单胞菌、大肠埃希菌、洋葱伯克霍尔德菌、白色念珠菌、黑曲霉等6种试验菌,接种后A和B中的含菌量分别为18、25、50、55、98、36 cfu/ml,至A和B中,同时做阴性对照和阳性对照,在21 d中分别于0 h、24 h、48 h、72 h、5 d、8 d、13 d、16 d和21 d分别按照《中国药典》2020年版四部1105中需氧菌总数与霉菌及酵母菌总数的检测方法在23 ℃培养,计数.
2 结果与讨论
2.1 5类中药液体/半固体制剂的aw分析
5类中药液体/半固体制剂的aw测定结果见表2所示,表明5种剂型aw从高到低依次是洗剂、口服液、露剂、糖浆剂、煎膏剂.相同剂型不同品种之间aw差异程度不同,例如煎膏剂蜜炼强力枇杷膏的aw与雪梨膏高0.170, 而洗剂青柏洁身洗液的aw比利夫康洗液高0.012.相同剂型相同品种不同厂家生产的中药液体制剂存在差异,甚至相同厂家同品种不同批次的中药液体制剂也存在差异.
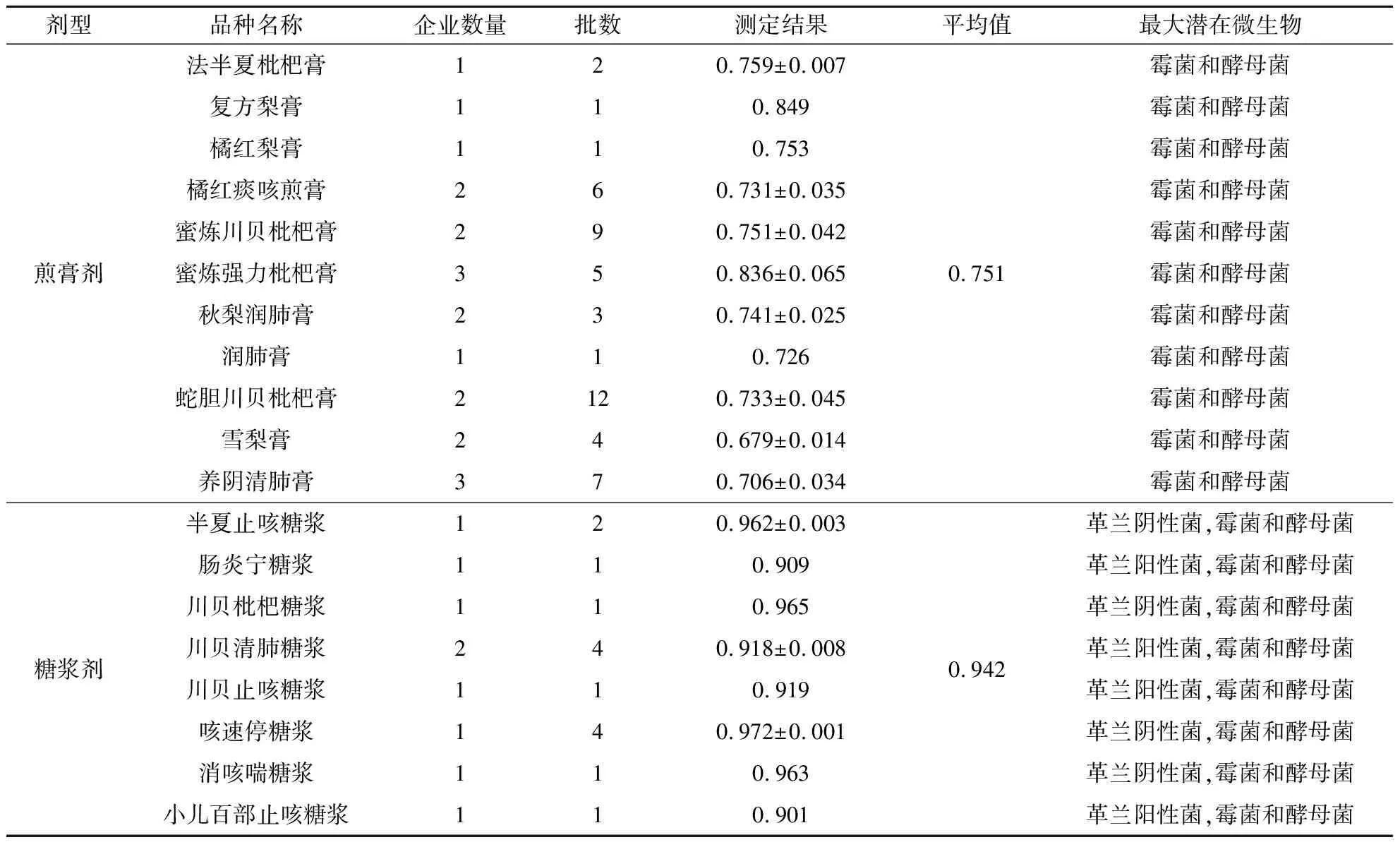
表2 中药液体/半固体制剂的水分活度测定结果及最大潜在微生物增殖风险预测
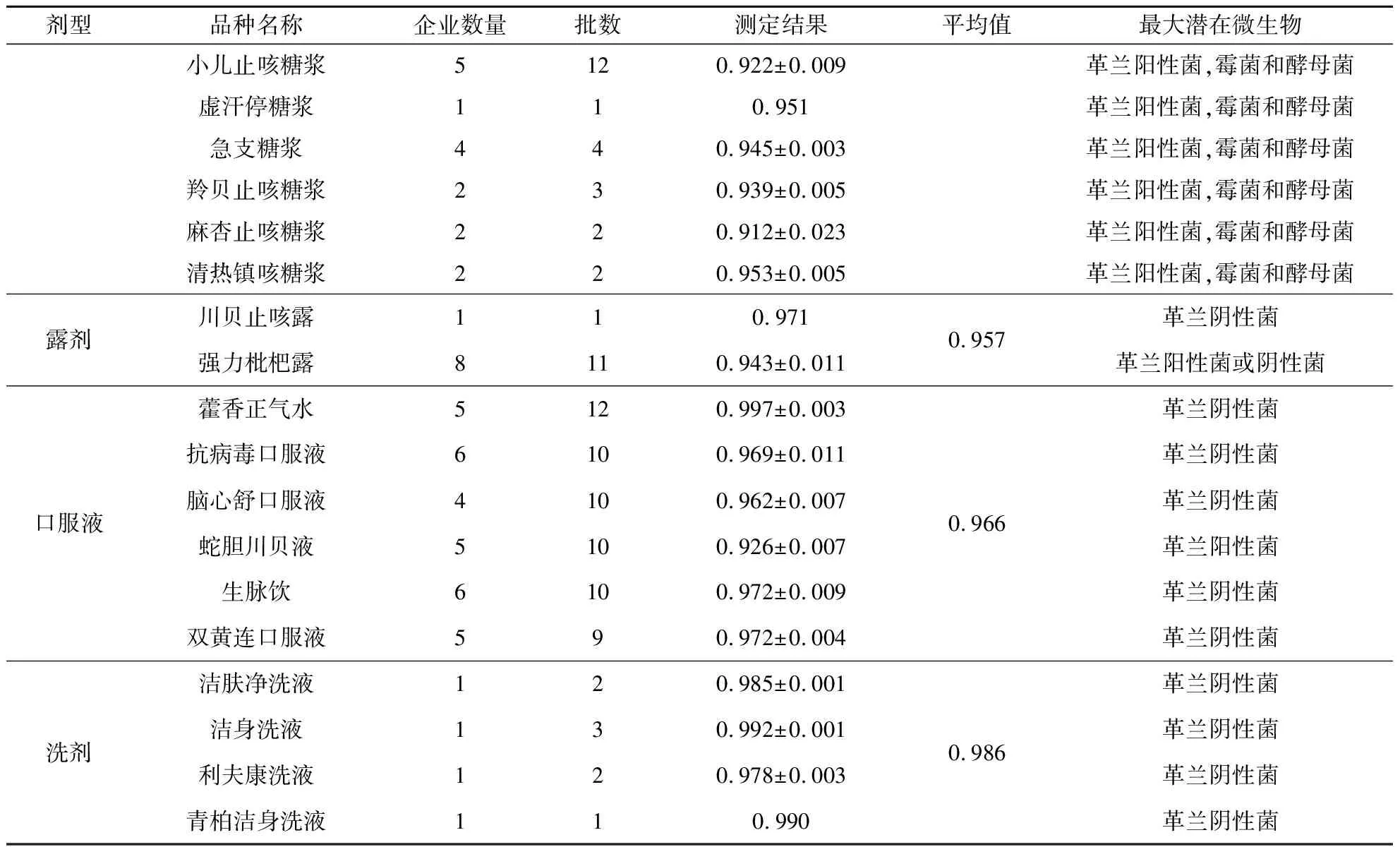
续表2
5种剂型的中药液体/半固体制剂的aw分析结果见图1所示.煎膏剂为半固体制剂,aw远低于洗剂等其他中药液体制剂.糖浆剂、露剂、口服液和洗剂的aw较高且分布更集中,对大多数微生物增殖有利.

图1 5种剂型的高水分活度中药制剂的aw分布图
2.2 5类高aw中药制剂潜在微生物增殖风险分析
中药制剂的aw越高,微生物污染和增殖的风险越高,微生物污染和增殖风险由高到低依次为:洗剂>口服液>露剂>糖浆剂>煎膏剂.中药制剂水分活度差异将会影响潜在污染微生物的种类.根据不同微生物生长所需aw的规律[17],即:当制剂aw>0.95,革兰阴性菌增殖风险较高,如大肠埃希菌、沙门菌、铜绿假单胞菌、洋葱伯克霍尔德菌复合体[18]等;制剂aw>0.86,革兰阳性菌增殖风险较高,如金黄色葡萄球菌[19]等;当制剂aw>0.75,且制剂含有较多的蔗糖或蜂蜜等糖类成分时,霉菌和酵母菌增殖风险高,如黑曲霉等;当制剂0.75>aw>0.60,只有耐受极端条件的霉菌和酵母菌才会生长,如鲁氏酵母等;当制剂aw<0.60,不支持微生物生长,结合高aw的中药制剂测定结果,形成了表2所示的高水分活度中药制剂的最大潜在增殖风险的微生物评估结果.
2.3 基于aw的3组药品不同剂型的处方分析
aw是中药制剂的重要属性,利用aw差异可评价相同品种的处方抑制微生物增殖的能力.3个品种不同剂型的中药制剂aw比较见图2所示,处方差异见表3所示.
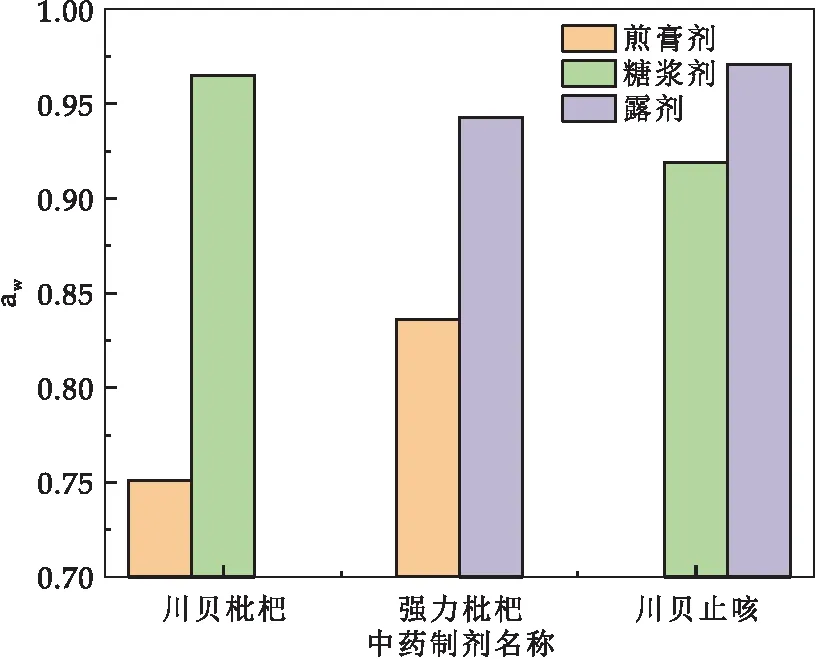
图2 不同剂型的3组6种中药制剂aw比较

表3 不同剂型的3组6种中药制剂处方分析
2.3.1 蜜炼川贝枇杷膏与川贝枇杷糖浆
蜜炼川贝枇杷膏与川贝枇杷糖浆的aw差异大,煎膏剂含有大量aw较低的炼蜜从而降低了制剂总体的aw,处方不利于大多数微生物的增殖,因处方含糖量高,仅耐受低aw胁迫的部分霉菌和酵母菌可生长.糖浆剂中加入的蔗糖也可降低aw,但本处方中糖浆剂aw降低的程度不如煎膏剂高,aw为0.965的糖浆剂可支持革兰阴性菌、革兰阳性菌、霉菌和酵母菌等微生物的生长.潜在微生物增殖风险可用来指导抑菌剂的合理应用,若蜜炼川贝枇杷膏使用抑菌剂,应选择对霉菌和酵母菌作用强的抑菌剂,若川贝枇杷糖浆使用抑菌剂,应选择对细菌、霉菌和酵母菌都有作用的广谱抑菌剂.
2.3.2 蜜炼强力枇杷膏与强力枇杷露
蜜炼强力枇杷膏与强力枇杷露的处方除所含炼蜜,饴糖及蔗糖不同外,主要处方相同(表3),蜜炼强力枇杷膏aw均值比强力枇杷露的膏aw均值低0.107(图2).根据aw的不同,蜜炼强力枇杷膏仅支持部分霉菌和酵母菌的增殖,微生物增殖风险低,而强力枇杷露可支持部分细菌,霉菌和酵母菌的生长繁殖,处方对微生物增殖的敏感性更高,抑菌剂应选择更为广谱的种类及更高的浓度.文献报道[20]从强力枇杷露中可分离出引起胀瓶的污染微生物拜耳接合酵母,而强力枇杷露中大肠埃希菌[21]及BCC[22]的生长与否与产品的aw密切相关.
2.3.3 川贝止咳糖浆与川贝止咳露
川贝止咳糖浆与川贝止咳露虽名称相似,然而其处方中的药味种类及用量差异较大,aw差异不大,若仅以aw因素考虑其微生物增殖风险,川贝止咳糖浆最大潜在污染微生物为革兰阳性菌,而川贝止咳露的最大潜在污染微生物为革兰阴性菌.抑菌剂选择时二者的侧重点有所不同.
2.4 微生物污染风险预测的结果验证
在21d中,阳性对照生长良好,阴性对照均未生长,根据A和B的aw,预测最大潜在微生物增殖风险及其21d的验证结果见表4所示.由于A和B的aw均较低,抑制了大多数细菌、酵母菌和霉菌的增殖,验证结果优于预测结果,风险预测具有较好的应用价值.

表4 中药煎膏剂和糖浆剂微生物污染预测验证结果
中药制剂aw的首要决定因素是剂型,其次是品种,再次是处方工艺.按照QbD理念,在新药处方设计阶段可利用aw作为制剂处方微生物易感性的评价工具,指导抑菌剂的合理使用[23,24];在生产加工阶段可利用aw作为工具确定关键工艺参数和关键质量属性,控制生产过程种微生物和水分的引入,保障药品安全有效及质量可控[25],aw为非无菌中药制剂的微生物过程控制提供了有力工具;在质量控制阶段,可利用aw判断最大潜在污染微生物,评估药品的微生物污染风险,制定更合理的标准.
高aw的非无菌中药制剂应考虑aw因素,制定更严格的微生物限度标准.例如,BCC在盐酸美沙酮口服溶液[8]、保济口服液[22]中的增殖,白色念珠菌和黑曲霉可在部分半夏糖浆/半夏止咳糖浆[12]中的增殖,拜耳接合酵母在强力枇杷露中的增殖[20]等高aw中药制剂微生物污染和增殖现象均符合本文的理论预测结果.高aw的中药液体制剂除了本文调查的5类制剂外,还有诸如中药代煎煮液[9,26,27]、凝胶剂、合剂、冲洗剂、搽剂等多种剂型,均为微生物污染和增殖风险较高的制剂,也是容易造成微生物生长繁殖的中药制剂,因此,在进行该类制剂的处方设计、工艺确定、质量控制时,可关注制剂的aw参数.
此外,研究所获高aw中药制剂的平均aw应理解为该类制剂的aw参考值,参考值的价值在于将剂型进行初步的分类,预测微生物的增殖风险.非无菌中药制剂处方中的药味组成和形态,辅料的种类和用量等因素影响制剂的aw,进而影响制剂对微生物的敏感性.
尽管A和B两种中药制剂验证结果与预测模型结果不一致,但微生物增殖风险的验证结果优于预测,说明除aw外,可能其他因素如中药成分也起到了抑制作用,使微生物控制的综合效果优于预测,这可能与中药制剂成分的复杂性有关.同一剂型甚至同一品种的aw差异较大,这与原辅料、处方[22]、工艺的关系密切,科学的微生物控制策略的建立依赖实际测定的针对具体品种的aw.
3 结论
高aw的中药制剂包括液体/半固体制剂,通常aw>0.60,微生物污染和增殖风险相对较高.研究非无菌中药制剂的aw的分布,在控制高aw中药制剂生物负载的前提下,可通过aw反映和评价制剂的微生物风险,将为非无菌中药制剂的处方优化,过程控制和标准制定提供参考.

