索马鲁肽治疗2型糖尿病疗效与安全性的系统评价Δ
胡锦华,韩菁婕,金 旻,曾 芳,胡 滨,娄月芬
(同济大学附属上海市第四人民医院药剂科,上海200434)
2021年,全世界约有5.37亿糖尿病患者,其中670万人死于糖尿病,世界卫生组织预测到2030年糖尿病将成为全球第七大死因[1-2]。我国糖尿病人群中,90%以上为2型糖尿病(type 2 diabetes mellitus,T2DM)患者[3]。T2DM始于胰岛素抵抗,最常见的诱因为超重和运动不足,糖尿病控制不佳可能导致严重并发症。口服降糖药种类很多,其中胰高血糖素样肽1受体激动剂(glucagon-like peptide-1 receptor agonist,GLP-1RA)在临床上被推荐为口服二甲双胍疗效不佳的T2DM患者的二线治疗药物,尤其适合于合并动脉粥样硬化性心血管病和慢性肾脏病的患者[3]。2017年,索马鲁肽注射制剂上市,在降糖、减重和心血管系统获益等方面表现出优势[4]。2019年,首个GLP-1RA口服制剂索马鲁肽也获批上市[5]。本研究旨在评价索马鲁肽治疗T2DM的疗效和不良反应,以期为临床用药提供循证依据。
1 资料与方法
1.1 纳入与排除标准
1.1.1 纳入标准:(1)年龄≥18岁并明确诊断为T2DM的患者,排除胰腺炎、心血管疾病患者。(2)干预措施为索马鲁肽皮下注射制剂或口服制剂,疗程≥26周,对照措施为安慰剂。(3)结局指标,①主要疗效指标,糖化血红蛋白(HbA1c)下降水平;②次要疗效指标,包括HbA1c<6.5%达标率、HbA1c<7.0%达标率、空腹血糖(FBG)下降水平、体重下降水平、收缩压(SBP)下降水平和舒张压(DBP)下降水平;③安全指标,包括不良事件发生率、低血糖发生率和胃肠道事件发生率。(4)研究类型为随机对照试验(RCT)。
1.1.2 排除标准:非RCT研究、动物实验、综述、简讯、会议文摘以及无可用结局指标数据的文献。
1.2 文献检索策略
检索中国知网(CNKI)、中国生物医学文献(CBM)、万方数据库(Wanfang Data)、维普数据库(VIP)、PubMed、Embase、the Cochrance Library、Web of science(WOS)和ClinicalTrials.gov数据库,时限为建库至2021年7月。中文检索词:疾病类型为“糖尿病”“2型”和“2型糖尿病”等;干预措施为“索马鲁肽”“司美格鲁肽”“诺和泰”和“口服索马鲁肽”等;研究方法为“随机对照试验”和“RCT”等。英文检索词:“Diabetes Mellitus”“Type 2”及其自由词;“semaglutide”“Ozempic”和“Rybelsus”;“randomized controlled trial”“RCT”“randomized”和“placebo”。
1.3 文献筛选、数据提取与质量评价
由2名评价员独立进行文献筛选、提取并交叉核对,意见不一致时,进行讨论或听取第三方意见。提取的信息包括作者、发表年份、年龄、性别、病程、随访时间、基线HbA1c水平、基线FBG水平、基线体重以及疗效和安全性指标。按照Cochrane系统评价手册5.1.0,由2名评价者独立进行文献质量评价,包括随机分配、分配隐藏、盲法、数据完整性、选择性报告和其他偏倚。
1.4 统计学方法
数据分析采用Stata 16和RevMan 5.3软件。把握度α=0.05,P<0.05为差异有统计学意义。结果以效应量及95%置信区间(CI)表示。连续性变量采用均数差(MD)作为效应量,分类变量采用相对危险度(RR)或率差(RD)作为效应量。研究异质性采用Q统计量和I2检验,I2<50%且P>0.1,说明异质性无统计学差异,选择固定效应模型;50%≤I2≤75%,提示存在中等异质性,采用随机效应模型;I2>75%,提示存在高异质性,寻找异质性来源进行亚组分析。发表偏倚评价采用漏斗图和Egger’s检验,当存在发表偏倚时采用剪补法进行迭代,估计缺失研究的数量。
2 结果
2.1 文献筛选结果与纳入文献的基本信息
按纳入与排除标准进行筛选,最终获得11篇文献[6-16],包括患者5 753例(索马鲁肽组4 023例,安慰剂组1 730例)。文献筛选流程见图1;纳入文献的基本信息见表1。
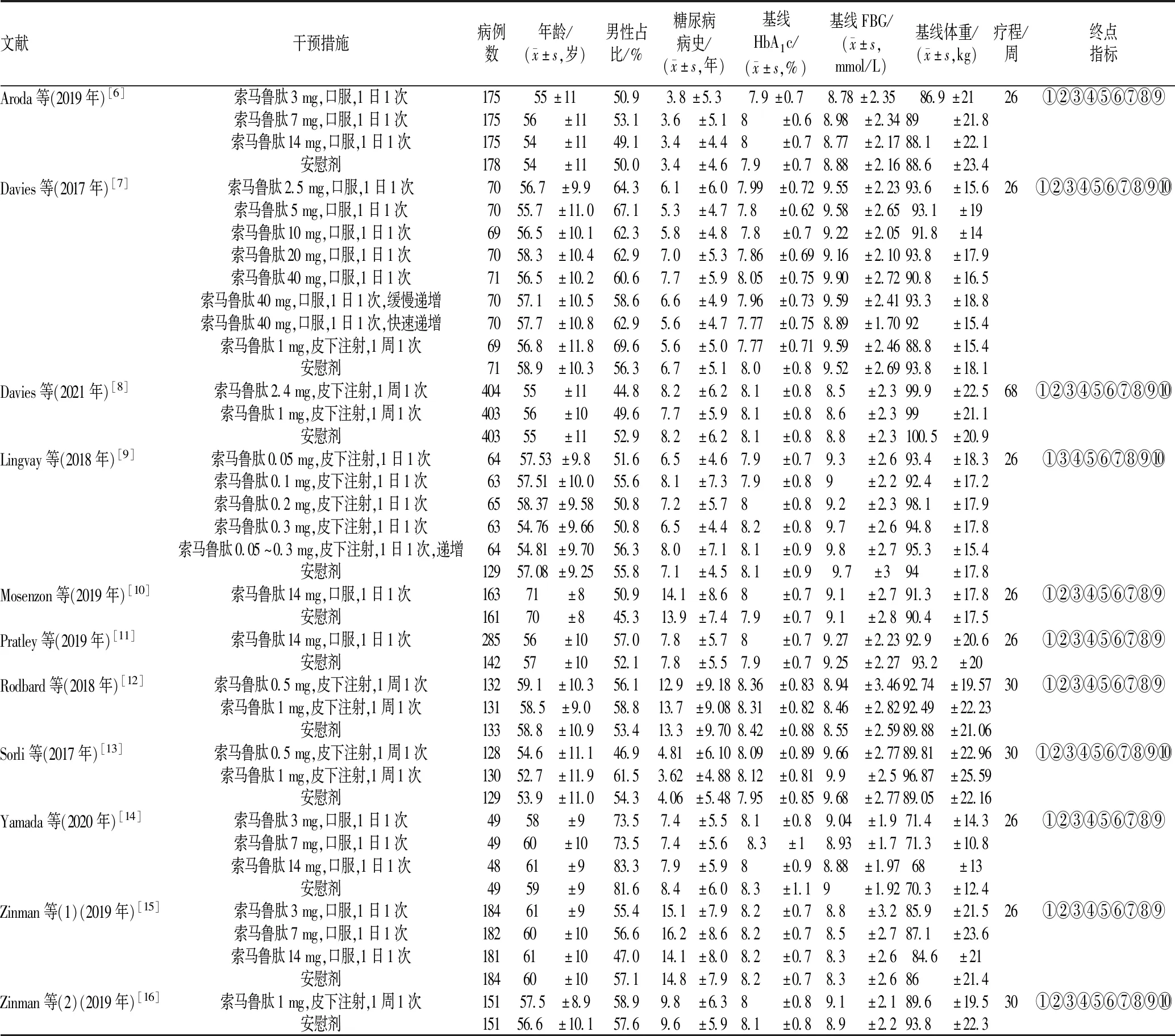
表1 纳入文献的基本信息Tab 1 Genral characteristics of included literature
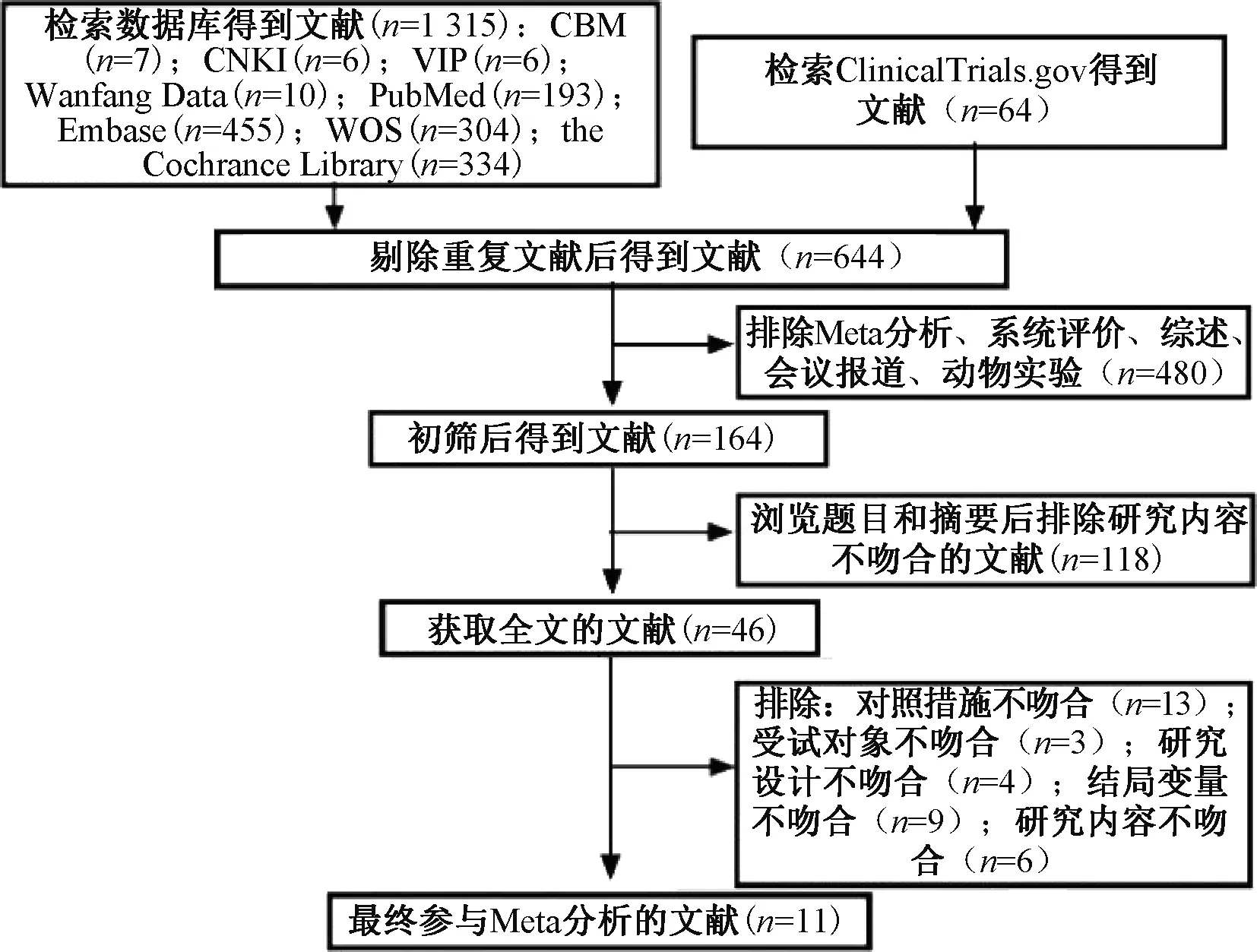
图1 文献筛选流程Fig 1 Literature screening process
2.2 纳入研究的质量评价
10项研究描述了随机分配和分配隐藏;11项研究均为双盲试验,报告了退出人数;无选择性报告数据;其他偏倚来源均不清楚。纳入研究的偏倚风险条形图见图2。
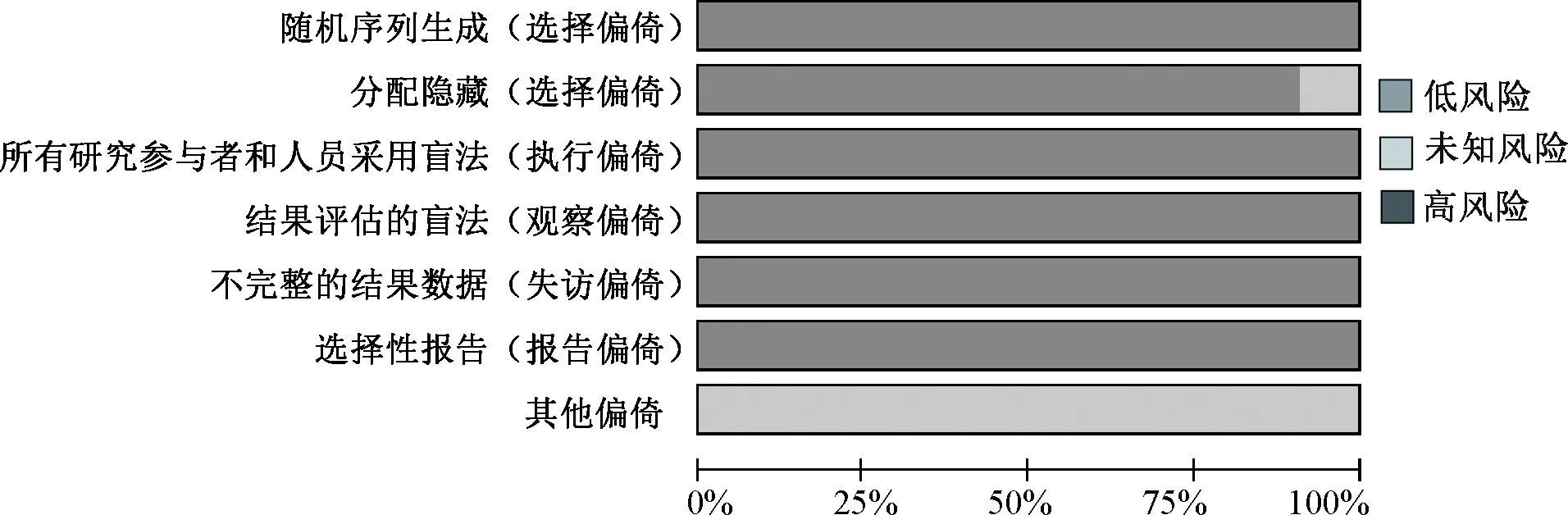
图2 纳入研究的偏倚风险条形图Fig 2 Bar plot of risk of bias
2.3 Meta分析结果
2.3.1 HbA1c水平降低值:11项研究[6-16]报告了HbA1c水平降低值,研究组与对照组患者基线HbA1c水平一致,各研究间的异质性极强(I2=85%,P<0.01),采用随机效应模型合并分析。最终得出,与安慰剂比较,索马鲁肽治疗可显著降低患者HbA1c水平,差异有统计学意义(MD=-1.18,95%CI=-1.35~-1.02,P<0.000 1),提示治疗有效。敏感性分析没有考察出异质性的来源,未发现任何一篇文献会对研究结果造成很强的影响。初步怀疑为用法用量造成的异质性,故按照给药方式和给药剂量分组,分别为皮下注射1周0.35~0.75 mg、皮下注射1周1 mg及以上、口服1日2.5~5 mg、口服1日7~10 mg和口服1日14 mg及以上5个亚组。以组别变量为协变量进行Meta回归,各项研究间的异质性能够解释回归方程I2=62.845%,该模型的拟合度Tau2=0.026 4,回归系数P<0.000 1,差异具有统计学意义,提示索马鲁肽的用法用量为异质性来源之一。考虑按照用法用量进行亚组Meta分析,结果见图3。(1)索马鲁肽皮下注射1周0.35~0.75 mg亚组中,各研究间仅有轻度异质性(I2=55%,P=0.11),选择随机效应模型合并效应量,研究组与对照组患者HbA1c水平降低值的差异有统计学意义(MD=-1.28,95%CI=-1.49~-1.06,P<0.000 01)。(2)索马鲁肽皮下注射1周1 mg及以上亚组中,各研究间具有中度异质性(I2=74%,P=0.002),选择随机效应模型合并效应量,研究组与对照组患者HbA1c水平降低值的差异有统计学意义(MD=-1.53,95%CI=-1.72~-1.34,P<0.000 01)。(3)索马鲁肽口服1日2.5~5 mg亚组中,各研究间异质性不具有统计学意义(I2=26%,P=0.25),选择固定效应模型合并效应量,研究组与对照组患者HbA1c水平降低值的差异有统计学意义(MD=-0.56,95%CI=-0.68~-0.44,P<0.000 01)。(4)索马鲁肽口服1日7~10 mg亚组中,各研究间异质性不具有统计学意义(I2=30%,P=0.23),选择固定效应模型合并效应量,研究组与对照组患者HbA1c水平降低值的差异有统计学意义(MD=-1.04,95%CI=-1.17~-0.92,P<0.000 01)。(5)索马鲁肽口服1日14 mg及以上亚组中,各研究间具有中度异质性(I2=70%,P=0.005),选择随机效应模型合并效应量,研究组与对照组患者HbA1c水平降低值的差异有统计学意义(MD=-1.18,95%CI=-1.37~-1.00,P<0.000 01)。各亚组内的研究间没有异质性或仅轻中度异质性,意味着用法用量是产生异质性的主要原因之一,按其进行分组是合适的。
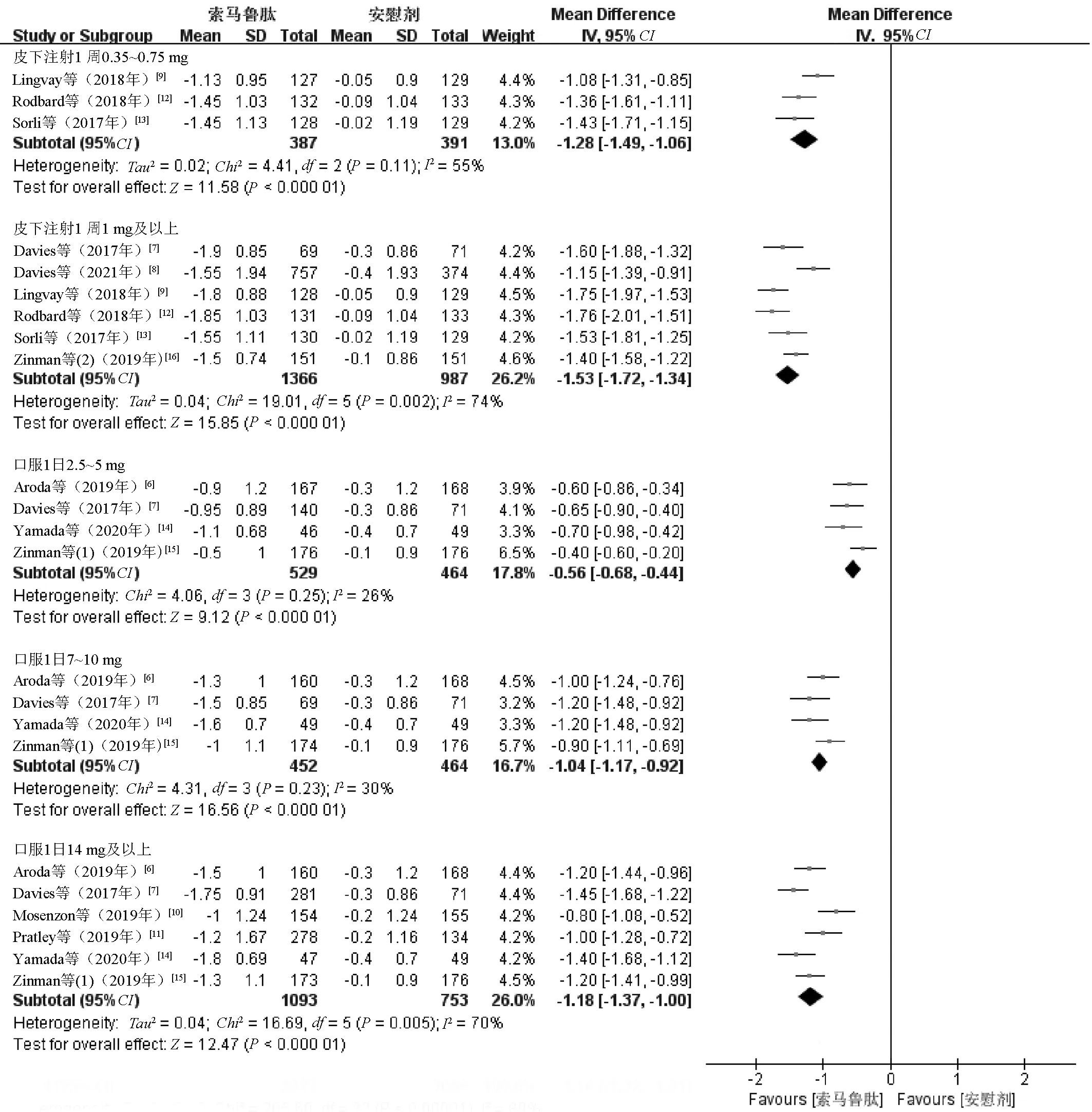
图3 HbA1c水平降低值亚组Meta分析森林图Fig 3 Subgroup Meta-analysis of HbA1c reduction
2.3.2 HbA1c达标率:10项研究[6-8,10-16]报告了HbA1c<6.5%达标率,各研究间的异质性具有统计学意义(I2=71%,P=0.000 3);11项研究[6-16]报告了HbA1c<7.0%达标率,各研究间的异质性具有统计学意义(I2=74%,P<0.000 1)。进一步考察拉贝图和星状图提示文献存在中度异质性,选择随机效应模型合并效应量。Meta分析结果提示,与安慰剂比较,索马鲁肽能够显著提高HbA1c达标率,差异具有统计学意义(HbA1c<6.5%达标率:RR=5.57,95%CI=4.06~7.63,P<0.000 01;HbA1c<7.0%达标率:RR=3.55,95%CI=2.88~4.36,P<0.000 01),见图4—5。

图4 HbA1c<6.5%达标率的Meta分析森林图Fig 4 Meta-analysis of control rate of HbA1c<6.5%

图5 HbA1c<7.0%达标率的Meta分析森林图Fig 5 Meta-analysis of control rate of HbA1c<7.0%
2.3.3 FBG水平降低值:11项研究[6-16]报告了FBG水平降低值,研究组与对照组患者基线FBG水平一致,各研究间具有很强异质性(I2=79%,P<0.01),采用随机效应模型合并效应量。最终得出,与安慰剂比较,索马鲁肽治疗可显著降低FBG水平,差异有统计学意义(MD=-1.65,95%CI=-1.95~-1.36,P<0.000 1),提示治疗有效。敏感性分析没有考察出异质性的来源,按照用法用量将研究分为5个亚组进行Meta回归分析,发现索马鲁肽用法用量为异质性来源之一(I2=69.54%,Tau2=0.194 6,P<0.000 1)。各亚组内研究间的异质性在可接受范围内,采用随机效应模型合并效应量。Meta分析结果显示,索马鲁肽皮下注射1周0.35~0.75 mg亚组(MD=-1.55,95%CI=-2.03~-1.07,P<0.000 01)、皮下注射1周1 mg及以上亚组(MD=-2.17,95%CI=-2.51~-1.83,P<0.000 01)、口服1日2.5~5 mg亚组(MD=-0.77,95%CI=-1.34~-0.21,P=0.007)、口服1日7~10 mg亚组(MD=-1.36,95%CI=-2.00~-0.73,P<0.000 1)和口服1日14 mg及以上亚组(MD=-1.69,95%CI=-2.17~-1.21,P<0.000 01)中,研究组患者FBG降低水平均优于对照组,差异均有统计学意义,见图6。
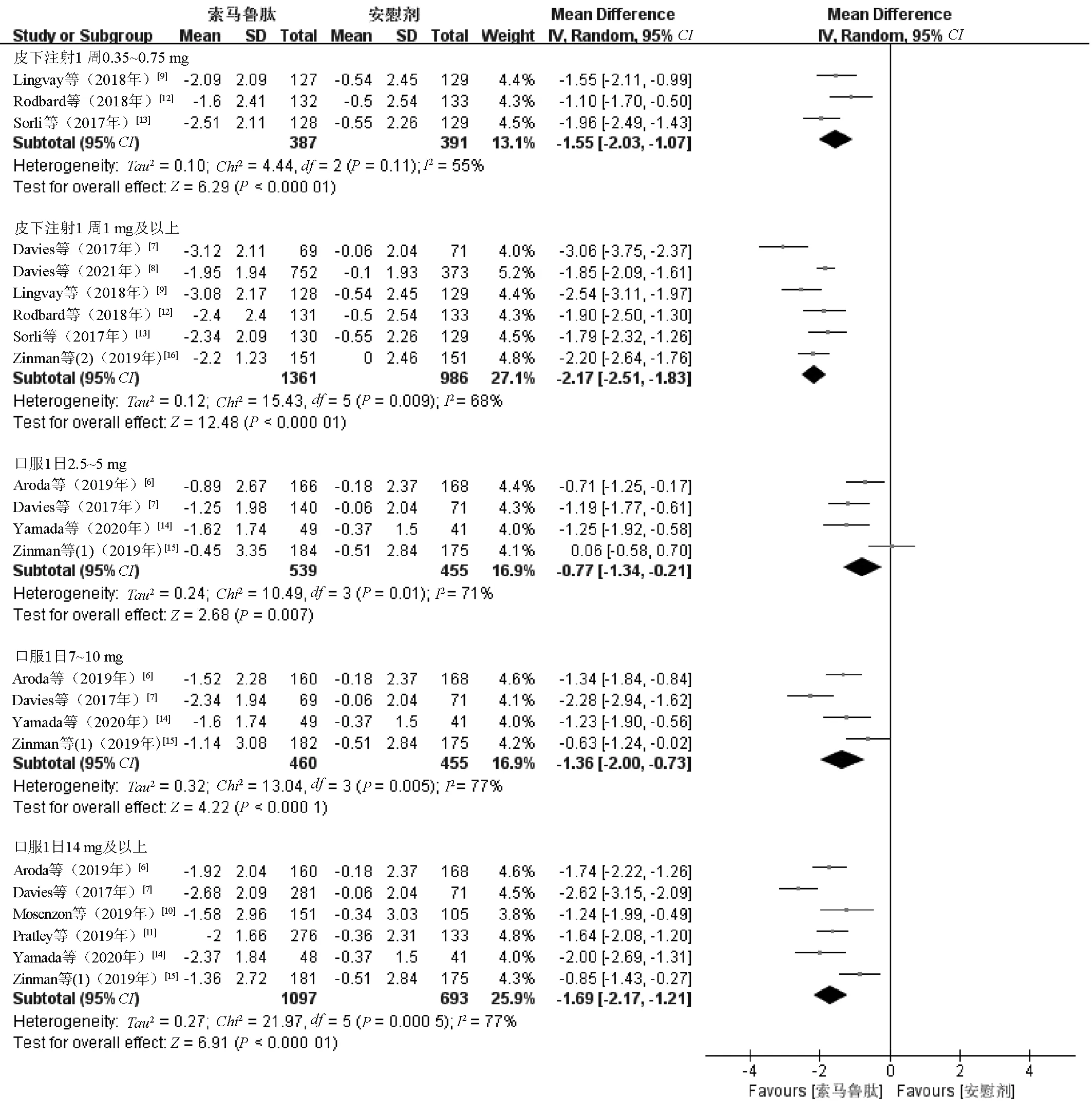
图6 FBG水平降低值亚组Meta分析森林图Fig 6 Subgroup Meta-analysis of FBG reduction
2.3.4 体重降低值:11项研究[6-16]报告了体重降低值,各研究间具有极强异质性(I2=93%,P<0.000 01),采用随机效应模型合并效应量。最终得出,与安慰剂比较,索马鲁肽治疗可显著降低患者体重,差异有统计学意义(MD=-3.06,95%CI=-3.94~-2.19,P<0.000 01)。敏感性分析没有考察出异质性的来源,Meta回归分析发现用法用量为异质性来源之一(I2=70.61%,Tau2=0.937 3,P<0.000 1)。亚组分析中,索马鲁肽皮下注射1周0.35~0.75 mg亚组采用固定效应模型,其余组采用随机效应模型合并效应量。Meta分析结果显示,索马鲁肽皮下注射1周0.35~0.75 mg(MD=-2.42,95%CI=-3.00~-1.85,P<0.000 01)、皮下注射1周1 mg及以上(MD=-4.76,95%CI=-5.56~-3.95,P<0.000 01)、口服1日7~10 mg(MD=-1.62,95%CI=-2.90~-0.34,P=0.01)和口服1日14 mg及以上(MD=-3.13,95%CI=-4.11~-2.16,P<0.000 01)的减重效果显著强于安慰剂,差异均有统计学意义;索马鲁肽口服1日2.5~5 mg的减重效果不显著,与安慰剂的差异无统计学意义(MD=-0.37,95%CI=-1.09~0.34,P=0.31),见图7。
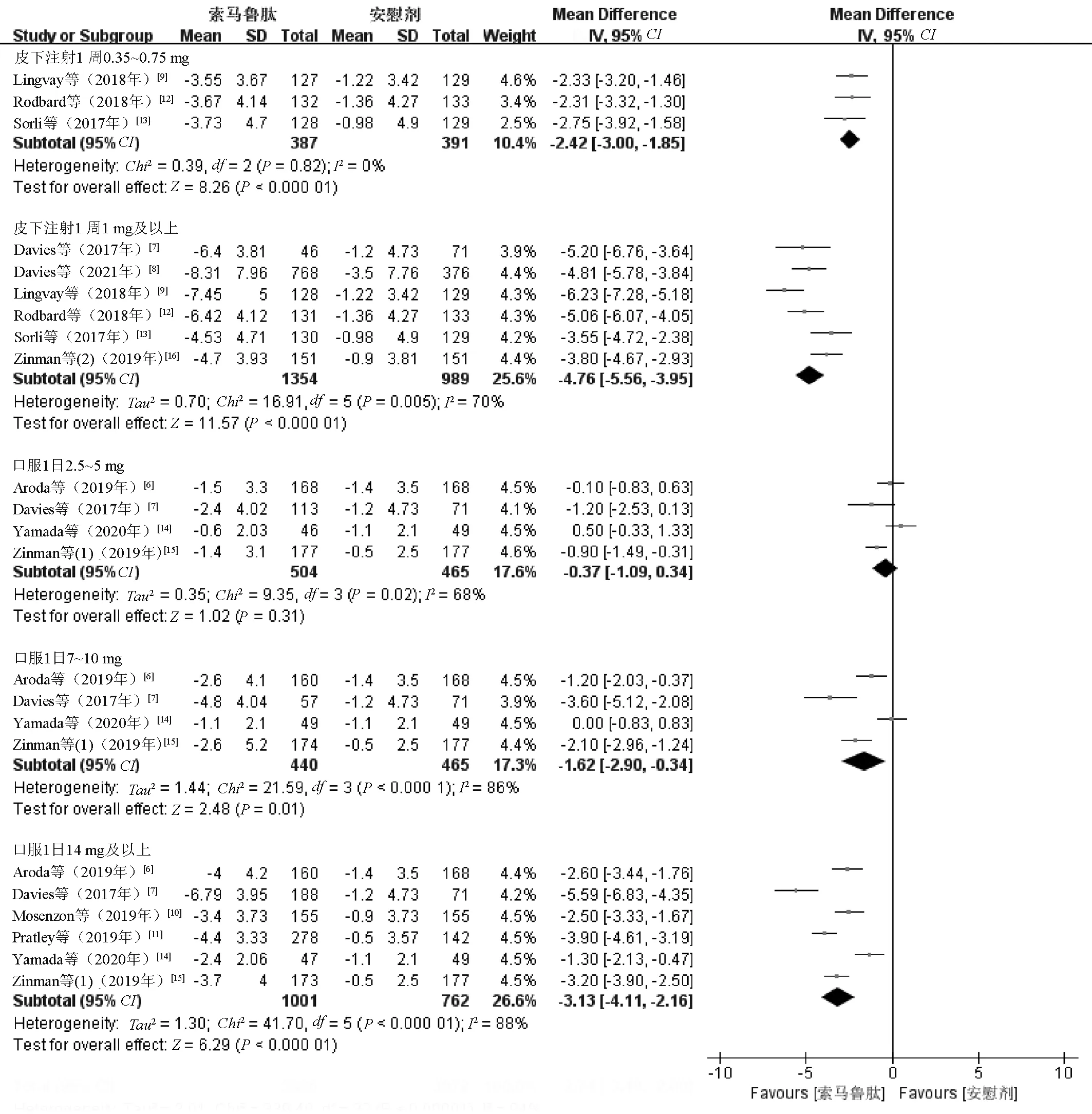
图7 体重降低值亚组Meta分析森林图Fig 7 Subgroup Meta-analysis of body weight loss
2.3.5 血压水平:11项研究[6-16]报告了血压水平变化。Meta分析结果显示,与安慰剂比较,索马鲁肽可降低患者SBP水平,差异有统计学意义(MD=-3.16,95%CI=-4.30~-2.02,P<0.000 01),见图8。在降低DBP水平方面,索马鲁肽与安慰剂的差异无统计学意义(MD=-1.40,95%CI=-3.06~0.26,P=0.06)。
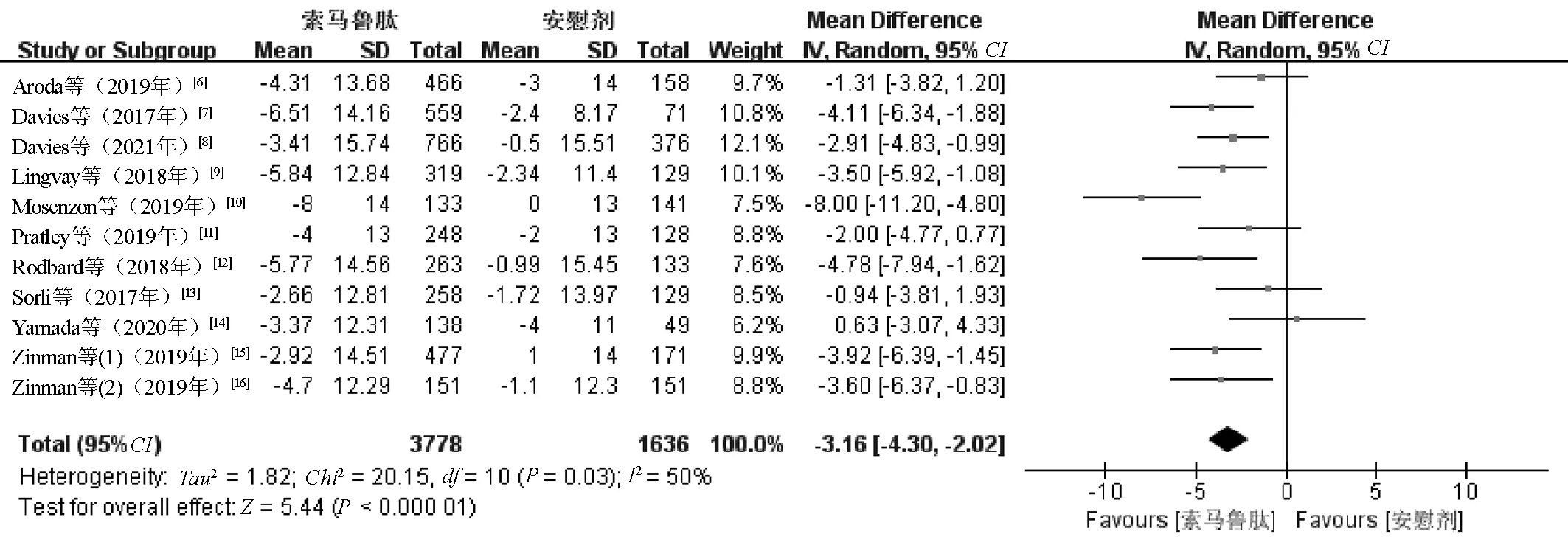
图8 SBP降低值的Meta分析森林图Fig 8 Meta-analysis of SBP reduction
2.3.6 安全性指标:索马鲁肽的不良事件发生率为安慰剂的1.09倍,胃肠道反应发生率为安慰剂的1.95倍,恶心、呕吐、腹泻、食欲减退、便秘和消化不良事件的发生率显著高于安慰剂,差异均有统计学意义(P<0.05);索马鲁肽与安慰剂的严重不良事件、低血糖和胰腺炎的发生率比较,差异均无统计学意义(P>0.05),见表2。

表2 安全性指标的Meta分析结果Tab 2 Meta-analysis of safety index
2.4 敏感性分析和发表偏倚评价
各项分析指标经敏感性分析,未发现删除单篇文献后效应量发生重大翻转,提示结果基本稳定。对疗效指标绘制漏斗图并进行Egger’s检验,结果显示,HbA1c水平降低值、FBG水平降低值、体重降低值和SBP降低值的漏斗图对称,不存在发表偏倚,见图9。HbA1c<6.5%达标率的漏斗图不对称,存在发表偏倚(P=0.011),见图9;采用减补法经过5次迭代后虚拟出5篇文献,减补后结果出现明显逆转(RR=47.51,95%CI=16.28~208.51),减补法校正后的漏斗图对称,见图10。HbA1c<7.0%达标率的漏斗图不对称,存在发表偏倚(P=0.011),见图9;经5次迭代后虚拟出3篇文献,减补后结果出现明显逆转(RR=21.15,95%CI=11.90~23.57),减补法校正后的漏斗图对称,见图10。现有的Meta分析结果并不稳定,未来有新的研究结果可能会导致Meta分析结果发生较大变化。
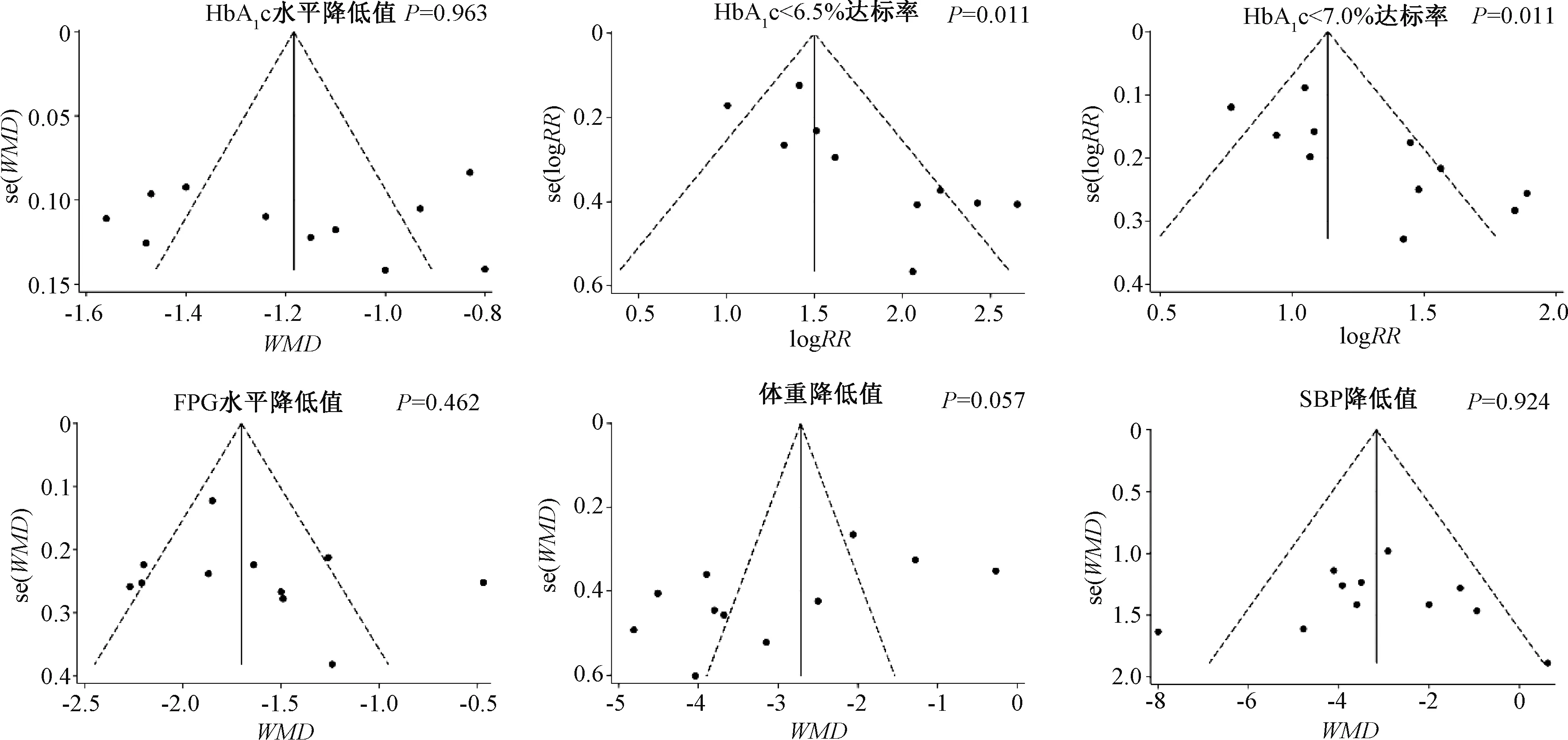
图9 疗效指标的漏斗图Fig 9 Funnel plot of efficacy index
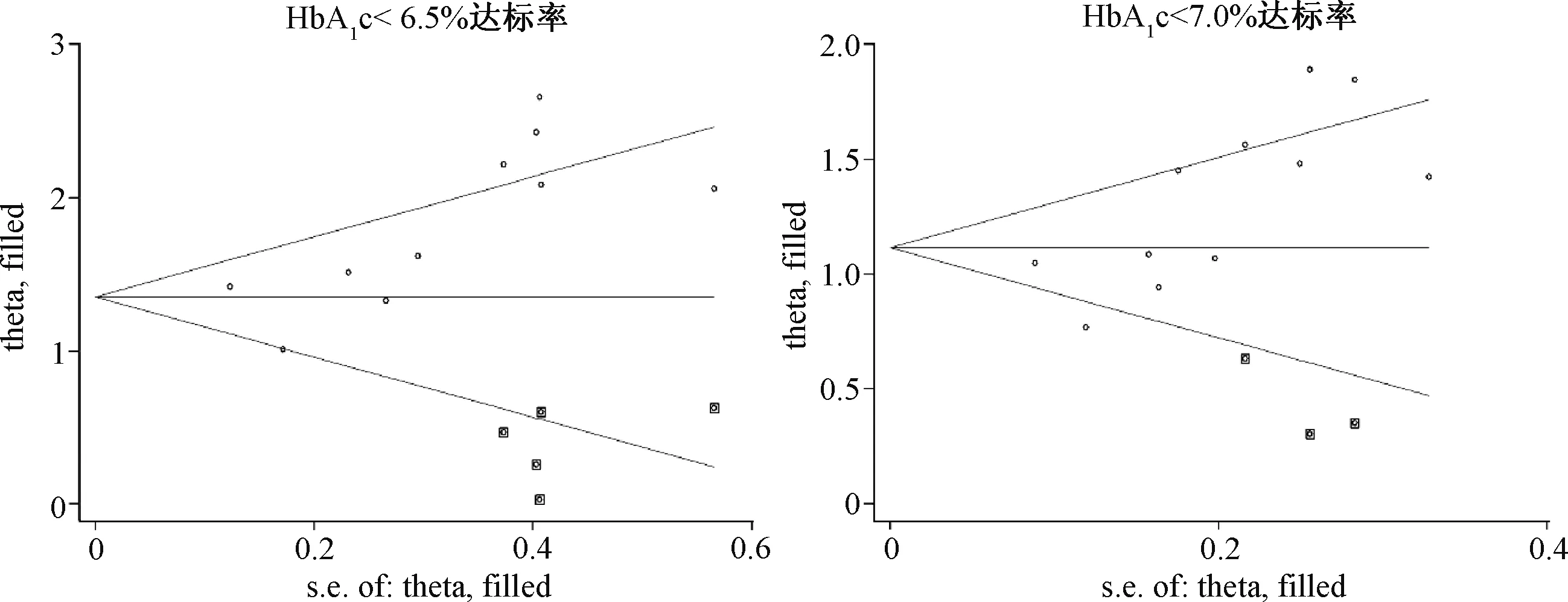
图10 HbA1c达标率经减补法校正后的漏斗图Fig 10 Filled funnel plot of control rate of HbA1c corrected by subtraction and supplement method
3 讨论
胰高血糖素样肽1受体在许多器官中表达,主要存在于胰腺、下丘脑和胃肠道,但也存在于心脏和肾脏中。GLP-1RA以葡萄糖依赖性方式刺激胰导β细胞分泌胰岛素并抑制胰高血糖素释放,同时通过复杂的内分泌机制减少胰岛α细胞的胰高血糖素分泌[17]。此外,GLP-1RA可降低食欲,这种影响不仅可归因于胃排空延迟,而且可归因于其作为神经递质对中枢神经系统的影响[18]。因而,GLP-1RA可通过多种机制有效控制T2DM患者的血糖和体重。内源性胰高血糖素样肽1的其他作用包括降低SBP、增加心肌收缩、改善内皮血管舒张、增加糖原储存、改善脂质分布、利尿和诱导尿钠排泄等作用。一些临床研究结果表明,GLP-1RA有额外的心血管益处,还可减少肾脏不良结局[19-20]。索马鲁肽已被批准用于非糖尿病患者的超重治疗。其中索马鲁肽皮下注射制剂具有出色的心血管特性,其口服制剂的心血管获益还有待进一步验证。关于微血管并发症,索马鲁肽具有减少糖尿病肾病的潜力,但同时也担心糖尿病视网膜病变可能恶化,因此需要进一步研究验证。本研究对索马鲁肽用于T2DM患者的疗效和安全性进行了系统评价,结果数据供临床治疗决策时参考。
本研究结果显示,与安慰剂比较,索马鲁肽可有效降低T2DM患者的HbA1c水平(MD=-1.18,95%CI=-1.35~-1.02,P<0.000 1)、FBG水平(MD=-1.65,95%CI=-1.95~-1.36,P<0.000 1)和体重(MD=-3.06,95%CI=-3.94~-2.19,P<0.000 01),同时可显著提高HbA1c达标率(HbA1c<6.5%达标率:RR=5.57,95%CI=4.06~7.63,P<0.000 01;HbA1c<7.0%达标率:RR=3.55,95%CI=2.88~4.36,P<0.000 01),差异均有统计学意义。亚组分析结果显示,索马鲁肽的降糖及减重效果与给药方式、使用剂量直接相关。与安慰剂相比,索马鲁肽皮下注射1周1 mg及以上使HbA1c水平、FBG水平和体重分别降低了约1.53%、2.17 mmol/L和4.76 kg,皮下注射1周0.35~0.75 mg使HbA1c水平、FBG水平和体重分别降低了约1.28%、1.55 mmol/L和2.42 kg,口服1日14 mg及以上使HbA1c水平、FBG水平和体重分别降低了约1.18%、1.69 mmol/L和3.13 kg,口服1日7~10 mg使HbA1c水平、FBG水平和体重分别降低了约1.04%、1.36 mmol/L和1.62 kg,口服1日2.5~5 mg使HbA1c水平、FBG水平和体重分别降低了约0.56%、0.77 mmol/L和0.37 kg;但索马鲁肽口服1日2.5~5 mg的减重效果与安慰剂的差异无统计学意义(P>0.05)。本研究结果显示,索马鲁肽皮下注射1周1 mg及以上的降糖、减重效果最佳,皮下注射1周0.35~0.75 mg和口服1日14 mg及以上的疗效次之,口服1日7~10 mg的疗效再次之,口服1日2.5~5 mg的疗效相对最差。一项关于索马鲁肽皮下注射制剂的Meta分析结果显示,与安慰剂相比,0.5和1 mg索马鲁肽分别使HbA1c水平降低了1.01%(95%CI=0.56~1.47)和1.38%(95%CI=1.05~1.70),分别使体重减轻2.32 kg(95%CI=1.46~3.19)和4.11 kg(95%CI=3.37~4.85)[21]。另一项关于索马鲁肽口服制剂的Meta分析结果显示,与安慰剂相比,口服索马鲁肽1日3~14 mg治疗使HbA1c水平降低了0.89%(95%CI=0.71~1.07 ),使体重减轻了2.99 kg(95%CI=2.30~3.69)[22]。本研究与之前的研究结果基本一致。此外,本研究中,与安慰剂相比,索马鲁肽显著降低了患者SBP水平约3.16 mm Hg(95%CI=2.02~4.30,1 mm Hg=0.133 kPa)。总体而言,合并肥胖和高血压的T2DM患者能从索马鲁肽治疗中获益更多。
索马鲁肽组患者总体不良事件发生率稍高于安慰剂,差异有统计学意义(P<0.05);少数索马鲁肽组患者出现低血糖、胰腺炎、流感和头痛等不良事件,但其发生率与安慰剂组的差异无统计学意义(P>0.05)。与其他GLP-1RA相似,索马鲁肽最常见的不良反应为消化道反应[23]。2018年,一项关于索马鲁肽皮下注射制剂的Meta分析纳入了6项RCT,共4 432例受试者,结果显示,与安慰剂相比,索马鲁肽皮下注射制剂的胃肠道反应风险更高,主要为恶心(OR=3.24,95%CI=2.66~3.94)、呕吐(OR=3.10,95%CI=2.42~3.98)和腹泻(OR=1.91,95%CI=1.58~2.30)[21]。2019年,一项关于索马鲁肽口服制剂的Meta分析纳入了6项RCT,共3 319例受试者,结果显示,与安慰剂相比,索马鲁肽口服制剂的胃肠道反应风险更高,主要为恶心(OR=3.71,95%CI=2.71~5.07)、呕吐(OR=3.60,95%CI=2.32~5.59)和腹泻(OR=2.35,95%CI=1.68~3.29)[22]。本次Meta分析研究结果显示,与安慰剂比较,索马鲁肽的胃肠道反应风险显著增加(RR=1.95,95%CI=1.73~2.20),主要包括恶心(RR=3.53,95%CI=2.90~2.49)、呕吐(RR=4.08,95%CI=3.00~5.57)和腹泻(RR=2.00,95%CI=1.65~2.43)等。索马鲁肽治疗中断的主要原因为胃肠道反应,为提高胃肠道耐受性,建议对索马鲁肽采用滴定方案[24]。索马鲁肽皮下注射制剂可以从0.25 mg、1周1次治疗4周开始,增加剂量至0.5 mg、1周1次治疗4周;在耐受的前提下,如需更高的剂量,则可以增至1.0 mg,1周1次。索马鲁肽口服制剂初始剂量为3 mg,1日1次治疗4周,然后增至7 mg,1日1次治疗4周,血糖控制不佳者可将剂量增至14 mg,1日1次。
本研究纳入的大部分RCT为多中心、随机、双盲对照试验,各项研究指标的基线均一致,敏感性分析和发表偏倚检验结果较为稳定,总体而言,结果可信度较高。在疗效结果的Meta分析中观察到高度异质性,为分析异质性来源,进行了敏感性分析,发现单篇RCT研究结果不能对效应量产生重大影响,对患者性别、年龄、病程、疗程、基础治疗、用法和用量等进行单因素Meta回归分析,并没有找到异质性来源;其后以用法用量为协变量进行Meta回归并分组后进行亚组分析,各亚组内研究间的同质性相对较好,说明用法用量是造成异质性的原因之一。本研究存在的局限性:是否还有其他未知原因造成异质性,尚无依据;HbA1c达标率研究指标存在发表偏倚,可能与治疗周期、患者的病程以及治疗背景不统一等因素相关;另外,纳入研究的方法学质量大多被认为是高的,但其都是行业资助的,因此容易出现赞助偏差。
综上所述,索马鲁肽皮下注射制剂和口服制剂均具有良好的降糖、减重效果,低血糖风险低,胃肠道反应为其常见不良反应但一般症状较轻,具有良好的临床应用前景。

