取环致宫腔化脓性感染引发腰椎间盘炎一例报道并文献复习
杨艳艳,王新玲,李娜,王蓓,段晓妍,张蕴霞
盆腔炎性疾病(pelvic inflammatory disease,PID)是妇科常见感染性疾病,包括子宫内膜炎、输卵管炎、输卵管卵巢脓肿和盆腔腹膜炎[1]。我国育龄期妇女中PID的发病率高达40%[2-3]。对PID进行及时诊断并规范化治疗是全科医生面对的重要问题之一。宫腔化脓性感染是由子宫内膜炎发展而来,是PID的一种特殊、严重的表现形式,治疗以抗菌药物为主,治疗原则要求经验性、广谱、及时并个体化。对于抗菌药物控制效果不佳的化脓性感染病灶,需要及时进行手术治疗。椎间盘炎是发生于椎间盘间隙和邻近椎体或软骨板的感染性病变[4],通常认为椎间盘炎是由细菌感染的血源性传播引起的[5],其症状及体征缺乏特异性,临床上容易延误诊断甚至出现椎体骨质破坏及下肢肌力减弱。门诊流产手术和取环手术可诱发盆腔感染,引起患者腰腹痛、月经失调等,甚至引发全身感染。研究发现流产手术后盆腔感染的发生率为5.88%~8.79%[6-7]。门诊取环手术可引起宫腔化脓性感染,临床表现为发热、腹痛、阴道分泌物增多等。而宫腔化脓性感染引发腰椎间盘炎目前国内外尚未见相关报道。本文报道了1例取环手术致宫腔化脓性感染引发腰椎间盘炎患者的诊疗过程,并结合详细的病例资料及复习相关文献,分析、探讨了该例患者的发病原因、感染途径、治疗经过、抗菌药物应用及手术时机,总结经验,以提升临床医生对PID及腰椎间盘炎的认识,为规范诊治方案和开展相关研究提供参考。
1 病例简介
患者,女,44岁,因“取环术后腰痛1月余,左下肢疼痛伴行走障碍5 d”于2021-09-08至河北省人民医院疼痛科就诊。患者因阴道出血伴重度贫血超过1个月,就诊于当地县医院,超声提示:子宫肌瘤,子宫内膜病变,宫内节育器。给予输血纠正贫血后行诊断性刮宫术+取环术,手术困难,操作时间约2 h,取环失败。术后2 d患者出现高热、寒战伴腰骶部疼痛,体温最高达41 ℃,考虑感染性休克转至当地医院重症监护监护病房(ICU)治疗,于ICU抗炎治疗9 d体温恢复正常,腰骶部疼痛较前稍减轻,下肢活动自如。诊断性刮宫病理回报:增殖期宫内膜。出院后腰痛仍持续存在,呈过电样锐痛,间断发作,夜间显著,与活动、体位改变及排便等无关,无法长时间保持平卧位,无双下肢乏力及感觉异常。于当地医院查腰椎CT示“腰3~4、腰4~5椎间盘膨出、腰4~5椎间盘钙化、腰椎骨质增生”,未予特殊治疗。随后由于患者出现左下肢抽搐样疼痛,自觉无力及行走困难,疼痛每次发作持续约数分钟,持续5 d后到河北省人民医院疼痛科就诊并住院治疗。
既往病史:确诊“子宫肌瘤”3个月,拟择期行手术治疗。无高血压病、冠心病、糖尿病等慢性病史,否认肝炎、结核病史。4年前因“甲状腺结节”行“甲状腺部分切除术”,20年前因“产后出血”输血治疗,1个月前因“重度贫血”输血治疗。
体格检查:体温36.3 ℃,脉搏98 次/min,呼吸20 次/min,血压122/69 mm Hg(1 mm Hg=0.133 kPa)。患者神清语利,查体合作,心肺腹查体未见明显异常,脊柱无畸形,无侧弯,各椎体无压痛及叩击痛,活动无障碍。双侧骶骨外侧及坐骨结节之间压痛,双侧骶髂关节处无压痛,双侧直腿抬高试验阴性,双侧4字征阴性,骨盆分离试验阴性,骨盆挤压试验阴性。双下肢无畸形,无水肿,活动自如,各关节无红肿,活动无障碍。肌肉无萎缩,肌力正常。
实验室检查:红细胞沉降率、C反应蛋白升高,白细胞计数及降钙素原正常。影像学检查:腰椎MRI平扫,腰5、骶1椎体及部分附件、椎体后方硬膜外异常信号(图1),考虑感染性病变可能。PET-CT检查:腰5骶1椎体上下缘代谢增高伴骨质破坏,腹盆腔多个轻度高代谢淋巴结,考虑椎间盘炎伴淋巴结炎症。子宫体积增大、壁增厚、内膜不均匀、代谢增高,考虑为刮宫术后改变伴感染可能,子宫壁内节育器影。
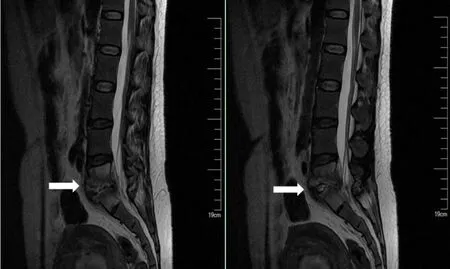
图1 患者腰椎MRI检查结果,可见腰5骶1椎体骨质破坏Figure 1 Lumbar spine MRI findings of the patient
诊断与治疗:入院后给予头孢哌酮钠舒巴坦钠联合奥硝唑静脉滴注抗感染,持续静脉泵入盐酸右美托咪啶及地佐辛镇痛、镇静。患者仍诉腰部及左小腿发作性疼痛,同时出现双侧臀部剧烈疼痛,坐位明显,侧卧位可稍缓解。因患者子宫肌瘤继发重度贫血,且宫内节育器嵌顿,遂转入妇科行腹腔镜下子宫切除术及椎间盘探查术。术中见子宫均匀增大如妊娠3个月,表面光滑,与周围组织无粘连。双侧输卵管充血并见炎性渗出小泡,双侧卵巢外观未见异常。子宫离体后剖视:宫腔内为化脓性感染,可见直径约7 cm黏膜下肌瘤,表面有脓苔附着,其中部分肌瘤组织坏死、感染化脓,局部见脓腔及灰白色脓液,有臭味,留取黏膜下肌瘤化脓感染组织送细菌培养。宫腔内见吉妮致美节育器1枚,嵌顿扎入子宫后壁肌层内。经阴道探查,阴道后壁与直肠之间有一脓腔,黏膜肿胀充血、糟脆,留取脓腔壁送细菌培养。骨科医生行腹腔镜下椎间盘探查术,粗针穿刺腰5骶1椎间盘,未见脓液流出,分离椎间盘间隙,见暗红色血水样渗液约20 ml自椎间隙流出,留取部分椎间盘组织送细菌培养。以大量稀释碘伏、0.9%氯化钠溶液冲洗盆腹腔后关腹。术后病理结果:(1)子宫黏膜下平滑肌瘤,局部梗死,表面溃疡坏死,伴化脓性炎症、子宫腺肌症;(2)增生期子宫内膜;(3)子宫颈轻度慢性炎症,腺体鳞化;(4)(双侧)输卵管充血,伴泡状附件。宫腔内及直肠前组织细菌鉴定:大肠埃希菌感染,椎间盘组织细菌培养为阴性。细菌培养结果显示大肠埃希菌对头孢哌酮钠舒巴坦钠敏感,故未再调整抗生素,术后继续给予头孢哌酮钠舒巴坦钠联合奥硝唑静脉滴注抗感染,总疗程14 d,配合局部理疗。术后第5天,患者所有症状均得到缓解,腰部疼痛消失,下肢活动自如,可以正常行走,出院前复查红细胞沉降率、白细胞计数、C-反应蛋白及降钙素原均在参考范围,准予出院。术后2个月患者返院复查,阴道残端愈合好,盆腔空虚,未触及肿物,无压痛。腰椎椎体无压痛及叩击痛,双侧骶髂关节处无压痛,双侧直腿抬高试验阴性,双侧4字征阴性,骨盆分离试验阴性,骨盆挤压试验阴性。复查腰椎MRI显示正常。
2 讨论
PID是女性上生殖道感染引起的一组疾病,包括子宫内膜炎、输卵管炎、输卵管卵巢脓肿和盆腔腹膜炎[3]。PID主要的病原体是淋病奈瑟菌和沙眼衣原体[3],生殖道支原体感染也是不可忽视的病因之一[8]。阴道菌群中的微生物包括链球菌、葡萄球菌、大肠杆菌和流感嗜血杆菌与PID的发生也有关[2,9],多为混合感染。有文献报道因盆腔炎引起脊髓硬膜外脓肿的病例[10],其病原体为阴道加德纳菌和羊膜普雷沃氏菌,显示了与PID相关的厌氧菌群的致病潜力。宫腔化脓性感染是由子宫内膜炎发展而来,是PID的一种特殊而严重的表现形式。此患者因宫内节育器嵌顿合并黏膜下肌瘤,使得取环困难,宫腔手术操作时间长,造成子宫内膜损伤后发生子宫内膜炎,又因同时合并子宫黏膜下肌瘤,炎性渗液引流不畅,造成宫腔内化脓性感染。正常女性生殖道有一定的自然防御能力,此患者阴道流血时间长使得生殖道的防御功能和自净能力降低,容易出现阴道菌群异常并发阴道炎,加之患者重度贫血、身体虚弱,均促进了宫腔化脓性感染的发生。取环术后患者出现高热、寒战,体温最高达41 ℃,已经出现感染性休克,此时细菌入血引发菌血症。由于县医院条件有限,未行血培养检查,患者病程迁延近2个月,期间多次接受抗菌药物治疗。前来本院就诊时体温已恢复正常,考虑留取血培养意义不大,未再留取血培养化验。PID治疗以抗菌药物治疗为主,正确、规范使用抗菌药物可使90%以上的PID患者治愈,抗菌药物治疗至少持续14 d,必要时需行手术治疗[1]。此患者因院外使用多种抗生素治疗且效果欠佳,入院后即给予头孢哌酮钠舒巴坦钠联合奥硝唑静脉滴注抗感染治疗并进行腹腔镜下子宫切除术及椎间盘探查术。术中见双侧输卵管充血及炎性渗出小泡,剖视宫腔内为化脓性感染,均符合PID特异性诊断标准[2,11]。术后细菌培养结果显示大肠埃希菌对头孢哌酮钠舒巴坦钠敏感,故未再调整抗生素,给予足疗程应用14 d,出院前患者复查各项炎症指标及血红细胞沉降率均已恢复正常。
椎间盘炎亦称化脓性椎间盘炎、椎间隙感染等,指椎间盘间隙和邻近椎体或软骨板的感染性病变[4]。其病因主要有以下3种学说[12],血源性细菌感染、无菌性炎症和人体自身免疫反应。多数学者认为椎间盘炎是由细菌感染的血源性传播引起的[13-15],金黄色葡萄球菌感染约占50%,革兰氏阴性杆菌如大肠杆菌感染(大多源自盆腔及泌尿系统)占7%~33%。细菌通常经动脉或静脉途径血行感染侵入椎间盘[16]。脊柱椎体-间盘在解剖结构上类似于关节,尤其是椎体前部动脉血管终末支分布丰富,因此血源性感染最先、最常累及椎体前部终板下骨质,炎症随后可突破皮质,向韧带下、椎间盘、邻近椎体、后柱及椎管侵犯。静脉途径为细菌通过无瓣膜的Batson静脉丛,是泌尿系统及盆腔器官感染脊柱的主要血源扩散途径。原发性椎间盘炎可发生于颈椎、胸椎、腰椎,因腰椎间盘承受的应力较大,又靠近盆腔,更易受细菌侵扰,故以腰椎更常见[17]。女性盆腔静脉密集,膀胱、生殖器官、直肠及其周围具有大量静脉丛且相互吻合,使得盆腔静脉感染易于蔓延[18]。女性盆腔淋巴结解剖结构复杂,淋巴结转移途径相互交织,当发生局部感染时细菌可沿淋巴管侵入,引起局部淋巴结肿大,进而病变可沿淋巴管的流注方向扩散和转移[19]。椎间盘炎症状及体征缺乏特异性,临床上容易诊断延迟,文献报道确诊时间从30~90 d不等[20]。椎间盘炎的诊断要点:大部分缓慢起病,腰骶部疼痛,休息平卧无法缓解。实验室检查中,红细胞沉降率和C反应蛋白被广泛应用于椎间盘炎的初步诊断[21],而白细胞计数的敏感性较低,仅在42.6%的患者中升高[22]。影像学检查中早期X线检查常无明显异常,CT扫描灵敏度为67%,特异度为50%,但其对软组织的评估有限[23]。MRI是诊断椎体骨髓炎的金标准成像方式,因其灵敏度、特异度和准确性高(96%、92%和94%)而被推荐[24],MRI可在X线、CT检查阴性或难以确定时早期诊断[25]。PET-CT依据不同细胞的葡萄糖代谢情况差异,炎性细胞葡萄糖代谢旺盛呈“热点”显像,诊断脊柱感染的灵敏度可达100%,特异度为87%[26],特别推荐在不能进行MRI时,PET-CT可作为替代诊断成像方式,在鉴别腰椎感染和退行性改变方面具有显著优势[27]。椎间盘穿刺取样微生物培养是抗生素选择的金标准[28],但其阳性检出率并不高。对于标本取样前接受过抗菌治疗的患者,微生物培养结果阴性并不能排除感染。本例患者取环术后出现高热、寒战及腰骶部疼痛,曾诊断为感染性休克,存在细菌血源性传播,住院后查红细胞沉降率沉及C反应蛋白均升高,但白细胞总数正常,仅中性粒细胞计数稍高,考虑与院外应用抗生素有关。PETCT提示腰5骶1椎体上下缘代谢增高伴骨质呈片状破坏,椎体形态仍然存在,周围伴发软组织密度影,考虑感染性病变。手术探查发现阴道后壁与直肠之间有一脓腔,宫腔内组织及直肠前组织细菌鉴定均为大肠埃希菌,但椎间盘组织细菌培养为阴性,考虑与术前应用抗生素有关,仍考虑为宫腔化脓性感染引发椎间盘炎。分析其感染途径有可能为细菌通过直肠周围淋巴管向后蔓延,沿子宫骶韧带到达骶前间隙;也可能为细菌通过损伤的子宫内膜及肌层入血,通过椎旁静脉丛感染椎体,透过终板发展到椎间隙出现椎体骨质破坏。
查阅国内外相关文献,目前尚无取环引发宫腔化脓性感染进而引发腰椎间盘炎的报道。国内有学者报道1名女性患者因异位妊娠行阴道后穹隆穿刺术后出现下腹及腰部疼痛,误诊为腰椎结核,病程迁延约3个月,最终确诊为腰椎椎间隙大肠埃希菌感染[29]。GENTILE等[5]报道1名女性患者因“子宫Ⅲ度脱垂”行腹腔镜下Y型网片子宫骶骨固定术,术后1个月患者出现持续性腰骶部僵硬伴腰痛及右下肢疼痛等症状,进而症状恶化不能站立及行走,最终诊断为腰椎化脓性椎间盘炎。结合本例患者,提示临床医生,患者接受盆腔有创操作后出现持续性腰背疼痛,同时伴有红细胞沉降率、C反应蛋白明显升高及腰椎MRI的异常改变,应考虑椎间隙感染的可能。
综上所述,取环手术为临床常见手术,但因取环致宫腔化脓性感染引发腰椎间盘炎及行走障碍的病例较罕见。此病例提示宫腔操作存在感染风险,除应严格无菌操作之外,还需动作轻柔,遇取环困难时,应由有经验的医生完成或改行宫腔镜下取环,不能粗暴实施手术造成损伤、感染、穿孔等不良后果。对于临床上遇到腰椎间盘炎的女性患者应详细询问病史,警惕盆腔炎症所致的可能,如做到早期诊断、早期治疗,根除原发病灶,能够缩短病程,减轻患者痛苦,减少由其导致的严重后果。
作者贡献:杨艳艳进行资料收集整理、撰写论文并对文章负责;王新玲、李娜、王蓓进行文章的修改;段晓妍负责英文修订;张蕴霞指导论文撰写与修改,负责文章的质量控制及审校,并对文章整体负责、监督管理。
本文无利益冲突。

