光敏ROS 响应型雷帕霉素脂质体的制备及表征
高习清,卢光照,鲁 莹,邹 豪
(海军军医大学药学系药剂学教研室, 上海 200433)
近红外光响应的肿瘤光热治疗因具有组织穿透性强、生物安全性好等优点,已引起广泛关注。作为新兴的光敏剂,八丁氧基酞菁钯具有成本低、易合成、毒性低等优点,在肿瘤光动力治疗(PDT)领域表现出巨大潜力。由于高渗透强滞留效应(EPR),脂质体作为药物载体可靶向集中于肿瘤组织,同时ROS 可氧化破坏脂质双层膜,促进包载药物在肿瘤组织的精准释放。本实验以雷帕霉素为模型药物,采用课题组合成的八丁氧基酞菁钯为光敏剂,制备近红外光触发的ROS 响应型雷帕霉素脂质体,并对其理化性质及体外释放特性进行考察。
1 材料与方法
1.1 仪器
R206D 旋转蒸发仪(上海申生科技有限公司);730 nm/1 500 mW 激光器(长春市亮丽光电有限公司);U3000 高效液相色谱仪(Thermo Fisher 公司);JY92.IIDN 超声波细胞粉碎机(宁波新芝生物科技股份有限公司);马尔文激光粒度仪(英国Malvern公司)。
1.2 试剂
二硬脂酰磷脂酰胆碱(DSPC,Avanti 公司);1,2-二亚油酰基-sn-甘油基-3-磷酸胆碱(DLPC,Avanti公司);二硬脂酰基磷脂酰乙醇胺-聚乙二醇2000(DSPE-mPEG2000,Lipoid 公司);胆固醇、雷帕霉素(MCE 公司)、八丁氧基酞菁钯[PdPC(OBu)8,实验室自制];磷酸盐缓冲液(PBS,HyClone 公司)。
1.3 脂质体的制备[1]
采用薄膜分散法制备脂质体。精密称取DSPC、DLPC、胆固醇、DSPE-mPEG2000、雷帕霉素、八丁氧基酞菁钯置于250 ml 圆底烧瓶中,加入适量氯仿溶解。65 ℃水浴,65 r/min 减压旋转蒸发形成均匀薄膜,取PBS 溶液4 ml 水化。吸出脂质体,用PBS 稀释至5 ml,200 W 探头超声5 min,即得近红外光触发ROS 响应型雷帕霉素脂质体。空白脂质体除不加雷帕霉素、八丁氧基酞菁钯外,制备方法相同。
1.4 脂质体处方筛选
以脂质体成膜及水化效果、药物包封率及载药量、包载药物光敏释放效率为指标,从DLPC、胆固醇、DSPE-mPEG2000处方量及PdPC(OBu)8投药量对光敏ROS 脂质体处方进行单因素考察。
1.5 粒径、PDI 及Zeta 电位
取少量脂质体溶液,用去离子水稀释,使用马尔文激光粒度仪测量脂质体粒径、PDI 及Zeta电位。
1.6 雷帕霉素含量测定[2]
1.6.1 色谱条件
色谱柱:Agilent TC-C18(2)(4.6 mm×250 mm,5 μm);流动相:甲醇-水(84∶16);流速1.0 ml/min;检测波长:278 nm;柱温:50 ℃;进样量:20 μl。
1.6.2 标准曲线绘制
精密称取雷帕霉素2.50 mg 置于10 ml 容量瓶中,用甲醇定容至刻度,得到浓度为250 μg/ml 储备液。精密吸取储备液800、400、200、100、40、20、10、4 μl,分别于5 ml 容量瓶中用甲醇定容。制成浓度为40、20、10、5、2、1、0.5、0.2 μg/ml 的对照品溶液。HPLC 仪检测并记录峰面积A,绘制出峰面积A与对照品质量浓度C的标准曲线并进行线性回归分析。
1.6.3 专属性考察
吸取雷帕霉素脂质体溶液500 μl 加入5 ml 容量瓶中,甲醇定容至刻度。超声20 min 破乳后,以10 000 r/min 进行超速离心10 min。取适量上清液过0.45 μm 有机膜,制得供试品溶液。吸取空白脂质体按同法制备阴性对照品溶液。分别取对照品、阴性对照品、供试品按照“1.6.1”项下方法进样,记录HPLC 图。
1.6.4 精密度
选取低、中、高3 个浓度的对照品溶液,1 d 内重复进样考察日内精密度,连续3 d 每天测定一次,考察日间精密度。
1.6.5 提取回收率
吸取用于制备选定的低、中、高3 个浓度对照品溶液的储备液于不同的5 ml 容量瓶中,同一浓度共制备3 个样品。向每个容量瓶中加入100 μl空白脂质体溶液,再用甲醇定容至刻度。超声20 min 破乳后,进行超速离心,10 000 r/min,10 min。取适量上清液过0.45 μm 有机膜,进行HPLC 检测。
1.7 包封率及载药量
包封率与载药量是评价脂质体的重要指标。包封率是脂质体中包封药物量与脂质体中药物总量的百分比。载药量是脂质体中药物量与脂质体总量的百分比。
精密吸取脂质体500 μl 置于5 ml 容量瓶中,甲醇稀释至刻度。超声20 min 破乳后,再进行超速离心,10 000 r/min,10 min。取适量上清液过0.45 μm 有机膜,进行HPLC 检测,计算得出脂质体中药物总量。
精密吸取适量脂质体溶液,先进行低速离心[3],3 000 r/min,15 min。取上层液体500 μl 置于5 ml容量瓶中用甲醇稀释至刻度。超声20 min 破乳后,再进行超速离心,10 000 r/min,10 min。取适量上清液过0.45 μm 有机膜,进行HPLC 检测,计算出脂质体中包封药物量。
1.8 体外释放实验[2]
采用反向透析法测定雷帕霉素脂质体光敏释放特性。以30 ml 20%乙醇为释放介质,加入50 ml离心管内;另吸取1 ml 释放介质并加入透析袋内,将透析袋两端扎紧后放入离心管中;取300 μl 雷帕霉素脂质体,用730 nm,1 W/cm2近红外光照射5 min 后,转移至释放介质;将离心管移至摇床内,设置摇床条件为37 ℃,180 r/min。分别在1、2、4、8、12 h 从透析袋内取样200 μl,用于样品测定和累积释放率的计算。取样后即补加新鲜释放介质200 μl,保持释放介质总量不变。以时间(t)为横坐标,以累积释放率(Q%)为纵坐标,绘制释放曲线。
2 结果
2.1 雷帕霉素的含量测定
2.1.1 标准曲线的绘制
回归方程为A= 0.624 0C-0.173 8 (r= 0.999 5)。雷帕霉素在0.2~40 μg/ml 浓度范围内线性关系良好。
2.1.2 专属性考察
按照“1.6.1”项下色谱条件测定,雷帕霉素出峰良好,保留时间为7.8 min。表明此方法专属性良好(图1)。
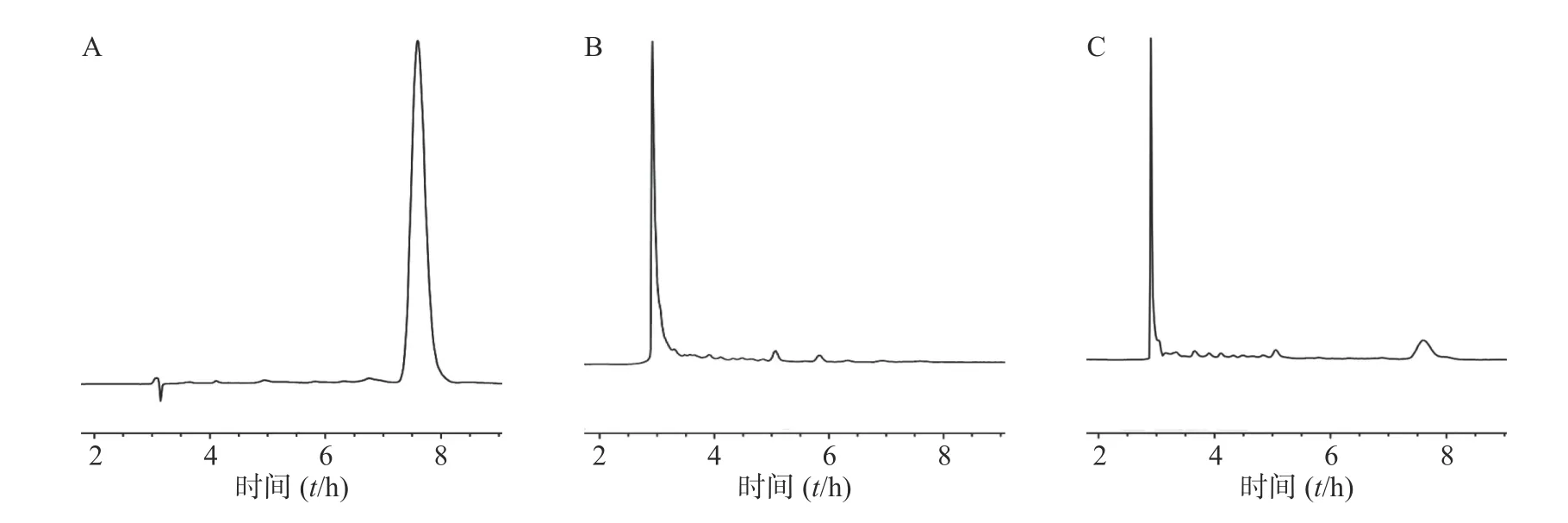
图1 雷帕霉素的专属性
2.1.3 精密度考察
由表1 可知,雷帕霉素在低、中、高3 个浓度都具有较好的准确度,日间精密度和日内精密度值均小于5%,表明该方法可用于雷帕霉素的含量测定。

表1 雷帕霉素 HPLC 分析的精密度( x±s ,n=3)
2.1.4 提取回收率
由表2 可知,雷帕霉素在低、中、高3 个浓度的回收率为97.64%~98.62%,符合95%~105%的范围,且RSD 值均小于1%,表明该提取方法稳定可靠。
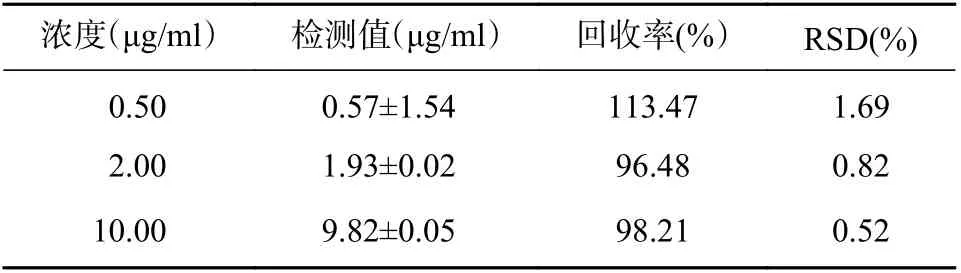
表2 雷帕霉素 HPLC 分析的提取回收率( x±s ,n=3)
2.2 脂质体处方单因素考察
2.2.1 DLPC 用量
由表3 可知,包含不同摩尔量DLPC 的处方制得的脂质体,成膜及水化效果较好,粒径<200 nm,PDI<0.2,雷帕霉素包封率>90%,载药量>1%;脂质体体外释放试验,光照12 h 后,测得雷帕霉素药物累积释放率>60%(图2A)。当DLPC 含量较低时(DSPC∶DLPC=69∶1),雷帕霉素释放速率明显低于其他处方。随着DLPC 含量的增加,雷帕霉素释放速率及12 h 内累积释放率并无明显增加。
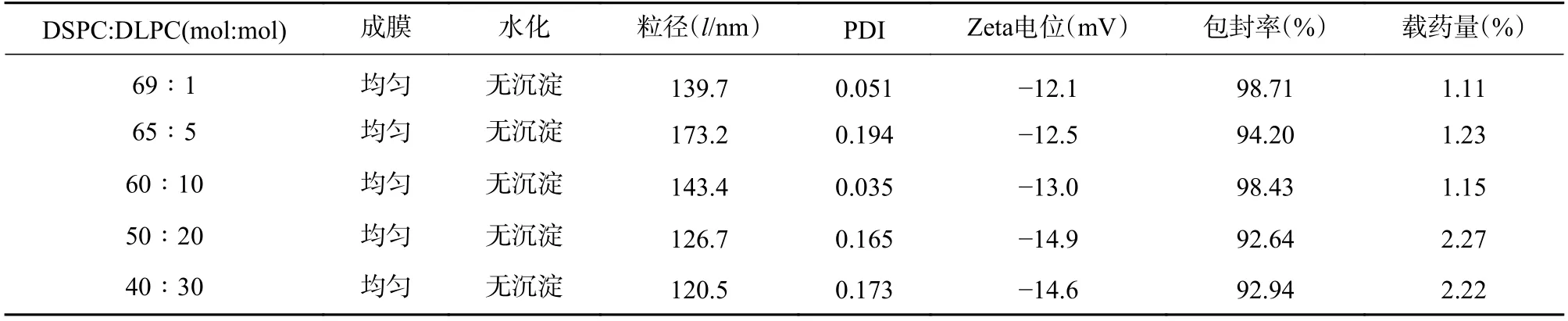
表3 不同摩尔量DLPC 脂质体的表征
2.2.2 胆固醇用量
由表4 可知,PC(DSPC+DLPC)与胆固醇之比过大(70∶10)或过小(70∶40),脂质体都不能成膜。当PC 与 胆 固 醇 之 比 为70∶20、70∶25、70∶30 时,所得脂质体成膜及水化效果较好,粒径<200 nm,PDI<0.2,雷帕霉素包封率>90%,载药量在1%左右。在进行脂质体体外释放实验中,测得12 h 后雷帕霉素药物累积释放率>60%(图2B)。
2.2.3 DSPE-mPEG2000的用量
由表5 可知,当DSPE-PEG2000用量较小时,脂质体不能成膜。当PC 与DSPE-PEG2000之比为70∶5、70∶10、70∶15 时,所得脂质体成膜及水化效果较好,粒径<200 nm,PDI<0.2,雷帕霉素包封率>90%,载药量>1%。在进行的12 h 脂质体体外释放实验中,摩尔比70∶5 组测得雷帕霉素药物累积释放率>60%,其余两组药物累积释放率在33%左右(图2C)。
2.2.4 PdPC(OBu)8的用量
由表6 可知,当PdPC(OBu)8用量较大(质量比1∶50),脂质体不能成膜。当PdPC(OBu)8与PC 质量之比为1∶100、1∶200、1∶300、1∶400,测 得 粒 径<200 nm,PDI<0.2,雷 帕 霉 素 包 封 率>90%,载药量>1%。在进行的12 h 脂质体体外释放实验中,质量比1∶100、1∶200 组释放效率高于其余两组,在60%左右(图2D)。
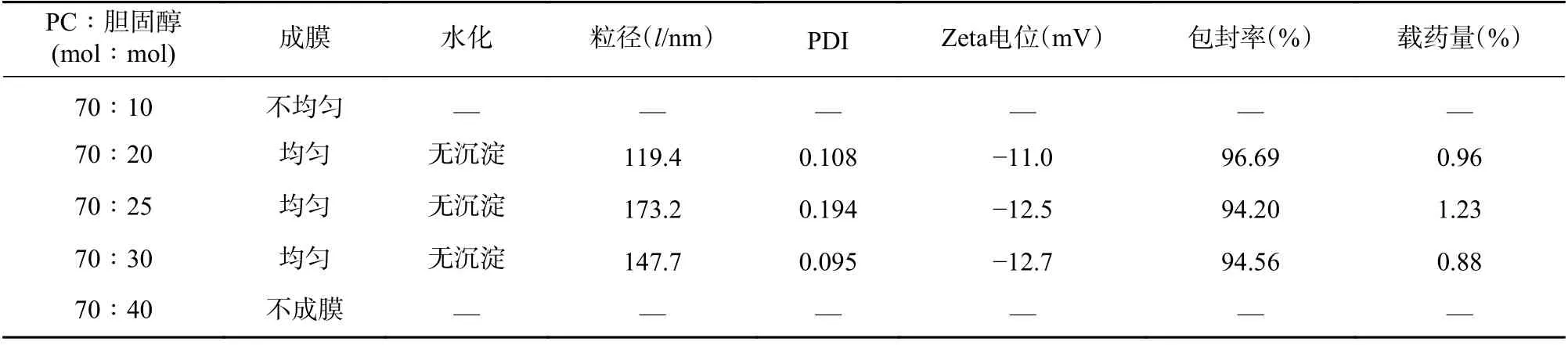
表4 不同摩尔量胆固醇脂质体的表征
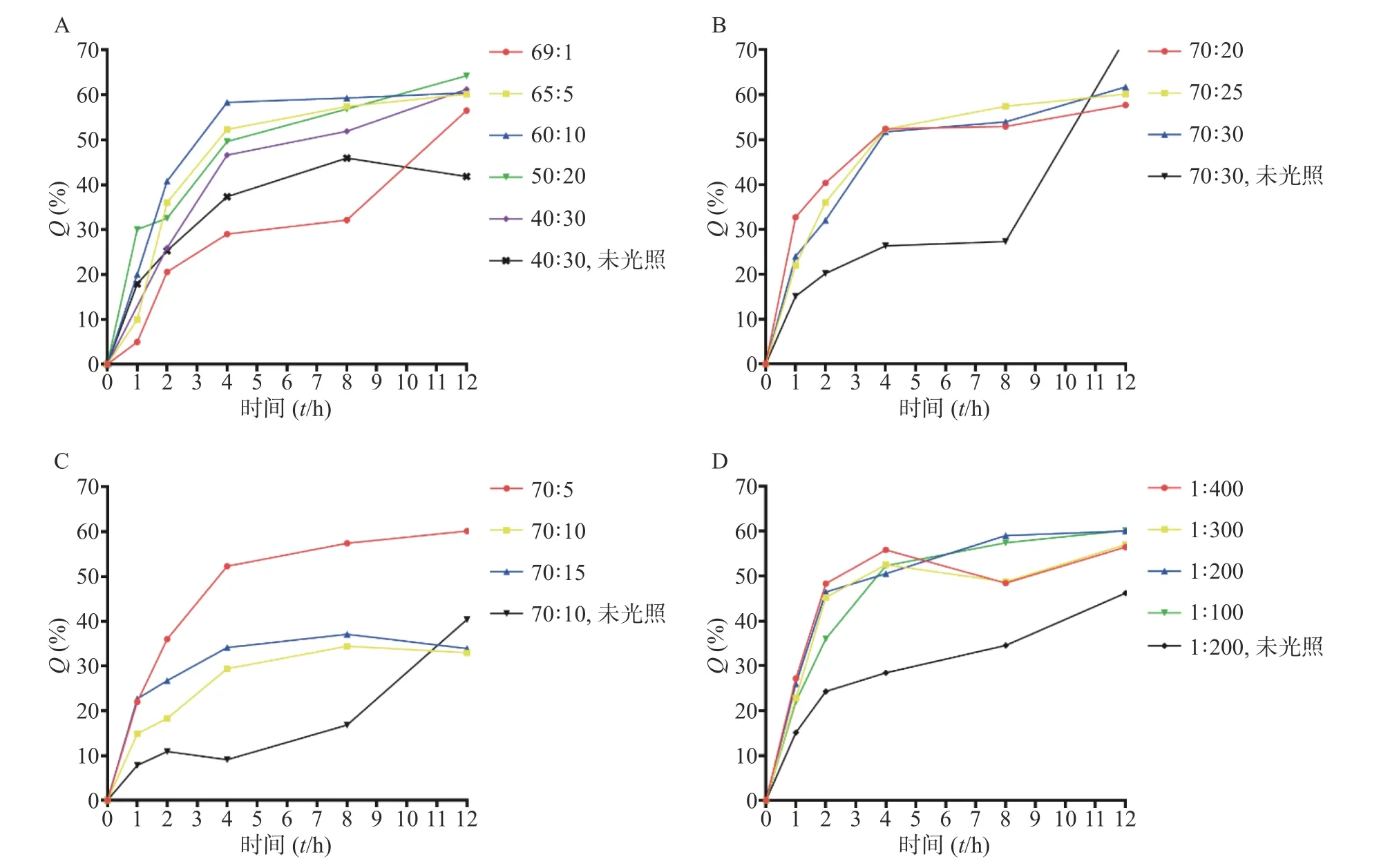
图2 雷帕霉素光敏释放特性考察
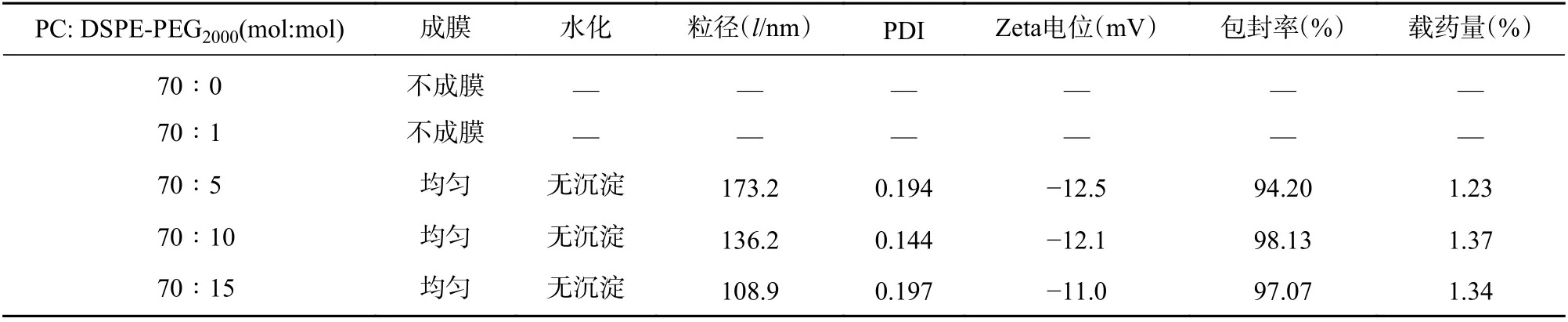
表5 不同摩尔量DSPE-PEG2000 脂质体的表征

表6 不同用量PdPC(OBu)8 脂质体的表征
3 讨论
DLPC 是一种人工合成的不饱和磷脂,在制成的脂质体中,DLPC 将均匀分散在脂质双分子层膜上。当有ROS 存在时,DLPC 结构中的不饱和碳碳双键可被氧化,使脂质膜结构遭到破坏,促进包载药物的释放。光敏剂可在特定波长光照射下产生ROS,在肿瘤疾病的光动力治疗中得到广泛应用。但光敏剂自身潜在的光毒性和溶解性差是其突出缺陷。本文将光敏剂包载在脂质体中可以减少潜在的细胞毒性,同时可增加其溶解度。在研究脂质体中雷帕霉素释放的释放介质确定上,文献[2,4-5]中提供了多种选择。预实验显示,20%乙醇溶液作为释放介质时,不仅克服了脂溶性药物雷帕霉素在水中溶解性差的缺点,同时也使得在进行HPLC 检测时干扰峰较少。综上所述,本研究成功制备了光敏ROS 响应型雷帕霉素脂质体,表征结果较好。在短时间特定波长照射后,可实现脂溶性药物的快速释放。
——雷帕霉素

