腐植酸对Se(Ⅳ)的吸附特征与机制①
邓华为,蒋代华,黄雪娇,黄金兰
腐植酸对Se(Ⅳ)的吸附特征与机制①
邓华为,蒋代华*,黄雪娇,黄金兰
(广西大学农学院,南宁 530004)
通过扫描电镜、元素分析和红外光谱研究了腐植酸的结构形态,通过分析腐植酸对Se(Ⅳ)的吸附动力学特征、吸附等温曲线、外界条件对腐植酸吸附Se(Ⅳ)的影响以及腐植酸对Se(Ⅳ)的解吸特性,探讨了腐植酸对Se(Ⅳ)的吸附特征及机制。结果表明:腐植酸腐殖化程度高,比表面积较大,可为Se(Ⅳ)提供更多的吸附位点。腐植酸对Se(Ⅳ)的吸附能力随pH降低以及Se(Ⅳ)初始浓度、腐植酸含量增加而增强。腐植酸对Se(Ⅳ)的吸附主要发生在前15 min,吸附过程符合准二级动力学方程;Freundlich等温吸附模型能较好地描述其等温吸附过程。腐植酸对Se(Ⅳ)的吸附与C=O、C–O、C=C、O–H、N–H等官能团相关,吸附机制为静电引力与配体交换。
腐植酸;Se(Ⅳ);吸附特征;机制
硒(Se)是人体所必需的微量元素,若摄取过量或不足,均会诱发人体疾病[1]。日常饮食是目前人体摄入硒的主要方式[2],而富硒农产品是日常饮食中硒的主要来源。为改善目前普遍存在的人体缺硒现象[3],发展富硒农产品变得至关重要,而生产富硒农产品的关键在于提高土壤有效硒的含量[4]。土壤中的硒主要以Se(0)、Se(–Ⅱ)、Se(Ⅳ)、Se(Ⅵ)及有机态硒存在,其中Se(Ⅳ)、Se(Ⅵ)以及极小部分有机态硒是土壤有效态硒,可供植物直接吸收利用[5]。Se(Ⅳ)是土壤中硒的主要存在形态,然而Se(Ⅳ)在土壤中容易被有机质、黏土矿物等吸附固定,导致其有效性很低[6-7]。可见,研究有机质与Se(Ⅳ)的作用对提高土壤硒有效性具有重要意义[8]。
腐植酸是土壤有机质的主要成分,是一类复杂的大分子有机混合物,由于来源与提取方式不同,其元素组成和含量、分子质量、结构等均有差异。一般腐植酸由碳、氧、氮、氢、硫等元素组成,平均分子质量在3 000 ~ 1 000 000 Da范围,含有羧基、羟基、羰基、甲氧基等多种活性官能团[9],这些活性基团使腐植酸具有了吸附、络合等能力。目前有关腐植酸的报道多与镉、砷、铅等离子的络合情况及机制相关,与硒作用的报道较少。Yang和Hodson[10]研究表明,高羧基含量的合成类腐植酸可以提高络合铜、镍、铅等金属的能力,有效地将它们从农业土壤中去除。Aldmour等[11]研究发现,腐植酸在去除Cr(Ⅵ)时,先是其酚羟基与Cr(Ⅵ)反应生成中间体铬酸盐酯,再由铬酸盐酯分解发生氧化还原反应,将Cr(Ⅵ)还原为Cr(Ⅲ),从而降低Cr(Ⅵ) 有效性。王锐等[12]主要针对针铁矿与胡敏酸复合体吸附Se(Ⅳ)的影响与机制进行了研究,然而,腐植酸本身也具有与Se(Ⅳ)作用的特性,但相关研究鲜少。
本文以腐植酸为研究对象,通过扫描电镜、元素分析和红外光谱研究腐植酸的结构形态,分析腐植酸对Se(Ⅳ)的吸附动力学特征、吸附等温曲线、外界条件对腐植酸吸附Se(Ⅳ)的影响以及腐植酸对Se(Ⅳ)的解吸特性,探讨了腐植酸对Se(Ⅳ)的吸附性能及其机制,为进一步了解有机质与硒生物有效性的关系、调节硒生物有效性、开发富硒农产品生产技术提供理论参考。
1 试验材料与方法
1.1 试验材料
主要试剂:腐植酸、亚硒酸钠(均购买自Sigma- Aldrich品牌)。
主要仪器:元素分析仪(Elemantar:Vario EL cube,德国元素分析系统公司)、新型高分辨场发射扫描电镜(SU8020,日立高新技术国际贸易有限公司)、傅里叶变换红外光谱仪(Frontier,美国PE公司)、恒温培养振荡器(ZWF-211,上海智城分析仪器制造有限公司)、台式高速离心机(H3-18K,湖南可成仪器设备有限公司)、原子荧光形态分析仪AFS(SA-20,北京吉天仪器有限公司)。
1.2 试验方法
1.2.1 腐植酸表征 利用元素分析仪测定腐植酸中碳、氧、氮、氢、硫元素的含量;采用新型高分辨场发射扫描电镜观测腐植酸的表面形态;使用傅里叶变换红外光谱仪表征腐植酸吸附Se(Ⅳ)前后化学官能团的变化。
1.2.2 腐植酸对Se(Ⅳ)的吸附试验 1)动力学吸附试验:称量0.05 g 腐植酸放入50 ml离心管中,添加10 ml pH为5、浓度为1 mg/L的硒溶液,置于振荡箱中振荡0、15、30、60、120、180、240 min,振荡结束后,离心过滤上清液,测定其Se(Ⅳ)的浓度。
2)等温吸附试验:称量0.05 g腐植酸放入50 ml离心管中,分别添加pH为5、浓度为0.01 mol/L 的NaCl溶液与1 mg/L的硒溶液共10 ml,使离心管中硒溶液浓度分别为0.05、0.10、0.25、0.50、0.75、1.00 mg/L,置于振荡箱中振荡至吸附平衡,振荡结束后,离心过滤上清液,测定其Se(Ⅳ)的浓度。
3)腐植酸添加量的影响:分别称量0.01、0.02、0.04、0.06、0.08、0.10 g 腐植酸放入50 ml离心管中,再加10 ml pH为5、浓度为0.05 mg/L的硒溶液,置于振荡箱中振荡至平衡,振荡结束后,离心过滤上清液,测定其Se(Ⅳ)的浓度。
4)反应体系pH的影响:称量0.05 g 腐植酸放入50 ml离心管中,添加9 ml浓度为0.01 mol/L 的NaCl溶液,将pH分别调为3、4、5、6、7、8、9、10,放于振荡箱中振荡2 h,取出离心管再次调节pH后,加入0.01 ml pH为7、浓度为100 mg/L的硒溶液,以NaCl溶液定容至10 ml,置于振荡箱振荡至吸附平衡,振荡结束后,离心过滤上清液,测定其Se(Ⅳ)的浓度。
以上吸附试验的条件均为:用亚硒酸钠以0.01 mol/L NaCl溶液为电解质配制硒溶液,并提前用HCl溶液或NaOH溶液调节其pH;离心管置于25 ℃、220 r/min的振荡条件下振荡,以4 000 r/min的速度离心10 min,离心后吸取上清液过0.45 μm滤膜,最后使用原子荧光形态分析仪AFS测定。每个处理3个重复,设置空白试验。
1.2.3 Se(Ⅳ)解吸试验 本研究采用磷酸盐浸提法对吸附反应后的样品进行解吸[13]。将上述腐植酸添加量试验完成后的样品进行自然风干,风干后向样品中加入10 ml 0.7 mol/L的KH2PO4溶液,放于点阵机上振荡至悬浮液充分分散,再置于振荡条件为25℃、220 r/min的振荡箱中避光振荡4 h。振荡结束后,以4 000 r/min离心10 min,吸取上清液过0.45 μm滤膜,并稀释至适当浓度,使用原子荧光形态分析仪测定Se(Ⅳ)浓度,该解吸量为配体可交换态硒(EX-Se)。
1.3 数据处理
使用Office Excel 2019记录、整理试验数据并制表,用SPSS 26分析数据,通过Origin 2021软件拟合吸附动力学曲线和等温吸附曲线并作图。相关计算公式与吸附结果拟合模型如下所示:
硒的吸附量:=(0–e)/(1)
吸附率:= 100(0–e)/0(2)
EX-Se含量:E=/(3)
EX-Se占比:E= 100E/(4)
式中:为腐植酸对硒的吸附量,mg/kg;0为硒的初始浓度,mg/L;e为平衡溶液中硒的浓度,mg/L;为溶液体积,L;为腐植酸添加量,kg;E为可交换态硒含量,mg/kg;为解吸平衡溶液中硒的浓度,mg/L;为吸附率,%;E为可交换态硒占吸附硒的比例,%。
本研究的吸附动力学数据利用准一级动力学方程、准二级动力学方程、Elovich方程、抛物线方程与双常数方程进行线性拟合。
准一级动力学方程:ln(1–Q)=ln1–1(5)
准二级动力学方程:/Q=1/(222) + (1/2)(6)
Elovich方程:Q= a + bln(7)
抛物线方程:Q= a + b1/2(8)
双常数方程:ln(Q)=a + bln(9)
式中:Q为时腐植酸对硒的吸附量,mg/kg;为振荡时间,min;1为准一级动力学方程拟合达到平衡时腐植酸对硒的吸附量,mg/kg;2为准二级动力学方程拟合达到平衡时腐植酸对硒的吸附量,mg/kg;1为准一级动力学方程吸附速率常数,min–1;2为准二级动力学方程拟合吸附速率常数,kg/(mg·min);a为通过方程拟合得到的参数,mg/kg;b为通过方程拟合得到的参数,mg/(kg·min)。当趋近于0时,=222为反应初始速率,mg/(kg·min)。
本研究运用Langmuir方程与Freundlich方程拟合腐植酸吸附Se(Ⅳ)的等温吸附曲线。
Langmuir方程:e/= 1/(L·m) +e/m(10)
Freundlich方程:=F·e1/n(11)
式中:e为吸附平衡溶液中硒浓度,mg/L;为腐植酸对Se(Ⅳ)的吸附量,mg/kg;L为表征吸附键能的常数,L/mg;m为最大吸附量,mg/kg;F为表示吸附能力的常数,L/kg;1/为表征吸附强度的常数。
2 结果与讨论
2.1 腐植酸的表征
2.1.1 元素分析 利用元素分析仪测定供试腐植酸碳(C)、氢(H)、氧(O)、氮(N)与硫(S)的含量,结果如表1所示。不同来源的腐植酸,其主要元素含量不同,但一般情况下C、O含量最高,其范围分别为42% ~ 67% 与25% ~ 45%[14]。本研究供试腐植酸的C、H、O、N与S的含量分别为50.03%、2.50%、36.25%、1.16% 和0.85%。O/C原子个数比为0.54,H/C原子个数比为0.60,N/C原子个数比为0.02。与Barnie等[15]的研究相比,本研究中的腐植酸O/C比较高,H/C、N/C比较低,表明供试腐植酸腐植化程度高,具有较多的含氧官能团。

表1 腐植酸的元素组成和相应原子摩尔比
2.1.2 扫描电镜图像 供试腐植酸的扫描电镜图像如图1所示。从图1中可看出,腐植酸表面呈现层状以及零碎的片状与颗粒状,形状大小各异,这样的结构可能比较利于Se(Ⅳ)进入腐植酸内部,并与其形成稳定的络合物。此外,腐植酸表面还具有较多的孔隙,说明腐植酸表面积较大,可以为Se(Ⅳ)提供更多的吸附位点。

图1 腐植酸的扫描电镜图
2.1.3 腐植酸与Se(Ⅳ)作用前后的红外图谱 腐植酸与Se(Ⅳ)作用前后的红外图谱如图2所示。从图2中可见,腐植酸含有羟基化合物、羰基化合物等特征基团的吸收带,与元素分析结果一致。根据文献将该红外图谱吸收带的归属整理如下:3 500 ~ 2 400 cm–1为羧基、酚羟基与醇羟基的O–H键伸缩振动吸收带、酰胺的N–H键伸缩振动吸收带以及芳香结构的C–H键伸缩振动带[16-17];1 715 cm–1为缔合态羧酸C=O键的伸缩振动吸收带[18];1 663 cm–1为烯烃C=C键伸缩振动吸收带[16];1 620 cm–1为羧酸根COO–反对称伸缩振动吸收带或酰胺N–H面内弯曲振动[16,18];1 401 cm–1为羧酸根COO–对称伸缩振动吸收带或脂肪族C-H键面内弯曲振动吸收带[16-18];1 165 cm–1为酚的C–O键伸缩振动吸收带[18];1 034 cm–1为醇的C–O键伸缩振动吸收带[18]。

图2 腐植酸吸附Se(Ⅳ)前后的红外光谱图
腐植酸吸附Se(Ⅳ)前后结构基本没有改变,但吸收峰的强度与所在波数均发生了变化。腐植酸吸附Se(Ⅳ)后,位于3 500 ~ 3 000 cm–1的宽峰明显上移并且峰强明显变弱,3 132 cm–1处的吸收峰位移至3 143 cm–1,1 715 cm–1处的吸收峰向低波数移动了7 cm–1,1 663 cm–1处的C=C键吸收峰消失,1 620 cm–1处吸收峰移动至1 622 cm–1,1 401 cm–1处的吸收峰峰强变弱,1 034 cm–1处的吸收峰峰形明显上移,以上说明C=O、C–O、C=C、O–H、N–H等官能团发生变化,腐植酸中的羧酸、醇、酰胺等均参与了Se(Ⅳ)的吸附。由于腐植酸中也可能存在铁、铝等元素,因此Se(Ⅳ)可能与腐植酸直接络合,也可能通过铁铝等氢氧化物间接与其络合[19-20]。
2.2 腐植酸吸附Se(Ⅳ)的影响试验
2.2.1 吸附动力学特征 腐植酸对Se(Ⅳ)的吸附动力学曲线如图3A所示。反应前15 min,Se(Ⅳ)吸附量急剧增加,且其增量在整个吸附过程中最大;15 min后,Se(Ⅳ)吸附量开始缓慢增加;120 min后,趋于稳定状态;240 min时,吸附量达到最大值31.56 mg/kg。该试验结果说明,随着反应时间的增加,腐植酸吸附Se(Ⅳ)的过程可分为3个阶段:快速反应、慢速反应与接近饱和趋于稳定。反应前15 min,腐植酸表面有大量的吸附位点,吸附很快,吸附量快速增加;而15 min后,因吸附了大量Se(Ⅳ),吸附位点减少,吸附过程变缓,吸附量缓慢增加;120 min后,吸附趋近饱和状态,吸附量趋于稳定。
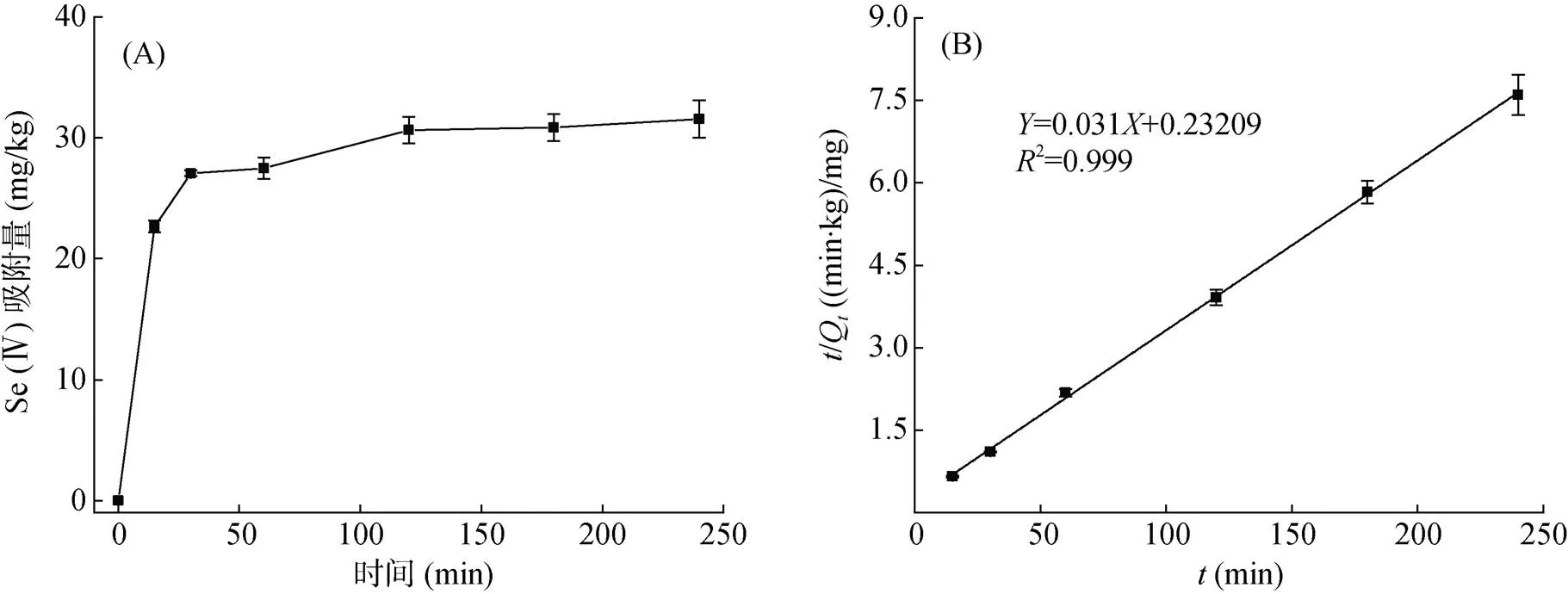
图3 腐植酸吸附Se(Ⅳ)的动力学过程(A)与准二级动力学方程拟合结果(B)
本研究的吸附动力学数据利用准一级动力学方程、准二级动力学方程、Elovich方程、抛物线方程与双常数方程进行线性拟合。其中准一级动力学方程、准二级动力学方程、Elovich方程、双常数方程拟合效果较好,各方程拟合参数如表2所示。由表2可知,准一级动力学方程、准二级动力学方程、Elovich方程、双常数方程的2分别为0.924、0.999、0.934、0.916,可见准二级动力学方程的拟合度最高,如图3B所示;并且该方程拟合所得的Se(Ⅳ)平衡吸附量理论值为32.36 mg/kg,与240 min时实际的平衡吸附量接近,说明准二级动力学方程符合腐植酸对Se(Ⅳ)的吸附动力学描述。腐植酸对Se(Ⅳ)的吸附过程不是单一过程,而是以化学吸附为主,与Kamei-Ishikawa等[21]的研究结果一致。该过程的吸附速率2=0.004 kg/(mg·min),吸附初始速率=4.31 mg/(kg·min)。

表2 腐植酸吸附Se(Ⅳ)的动力学模型相关参数
2.2.2 等温吸附特征 Se(Ⅳ)初始浓度对腐植酸吸附Se(Ⅳ)的影响如图4A所示。Se(Ⅳ)吸附量随初始浓度的增大而增大,初始浓度为0.05 mg/L时,吸附量为2.63 mg/kg;初始浓度为1.00 mg/L时,吸附量为22.57 mg/kg。然而,其吸附率随初始浓度的增大而减小,该结果说明初始浓度为0.05 mg/L时腐植酸对Se(Ⅳ)的吸附效果最强,随着初始浓度的增加,吸附效果减弱。造成这一结果的原因是,Se(Ⅳ)初始浓度的增量大于腐植酸的吸附量,导致有更多的Se(Ⅳ)留在土壤溶液中。

图4 Se(Ⅳ)初始浓度对腐植酸吸附Se(Ⅳ)的影响(A)与Langmuir方程和Freundlich方程拟合结果(B)
本研究运用Langmuir方程与Freundlich方程拟合腐植酸吸附Se(Ⅳ)的等温吸附曲线,拟合结果如图4B所示,拟合参数如表3所示。由表3可知,Langmuir方程与Freundlich方程的拟合参数2分别为0.971 3、0.985 6,Freundlich模型的拟合效果最佳,可以更好地描述腐植酸对Se(Ⅳ)的等温吸附行为,与Kamei-Ishikawa等[22]的研究结果一致。由前人研究可知,Freundlich模型的平衡参数1/能够反映腐植酸对Se(Ⅳ)的吸附强度。一般情况下,当1/在0 ~ 1范围内时,数值越小,表示吸附能力越强;当1/>2时,则表示吸附行为难以发生[23]。本研究中该模型的平衡参数1/为0.754 7,说明腐植酸对Se(Ⅳ)的吸附行为容易发生。

表3 腐植酸吸附Se(Ⅳ)的 Langmuir 和 Freundlich等温模型拟合参数
2.2.3 腐植酸添加量的影响 腐植酸添加量对吸附Se(Ⅳ)的影响如图5所示。随着腐植酸添加量的增加,Se(Ⅳ)吸附量持续增加,当腐植酸添加量为0.01 g时,Se(Ⅳ) 吸附量为0.65 mg/kg;当腐植酸添加量为0.10 g时,Se(Ⅳ) 吸附量为3.07 mg/kg,是腐植酸0.01 g添加量下的5倍。该结果表明,腐植酸含量的增加,使其表面积增大,活性官能团增多,能为Se(Ⅳ)提供更多的吸附位点,从而增强对Se(Ⅳ)的吸附。
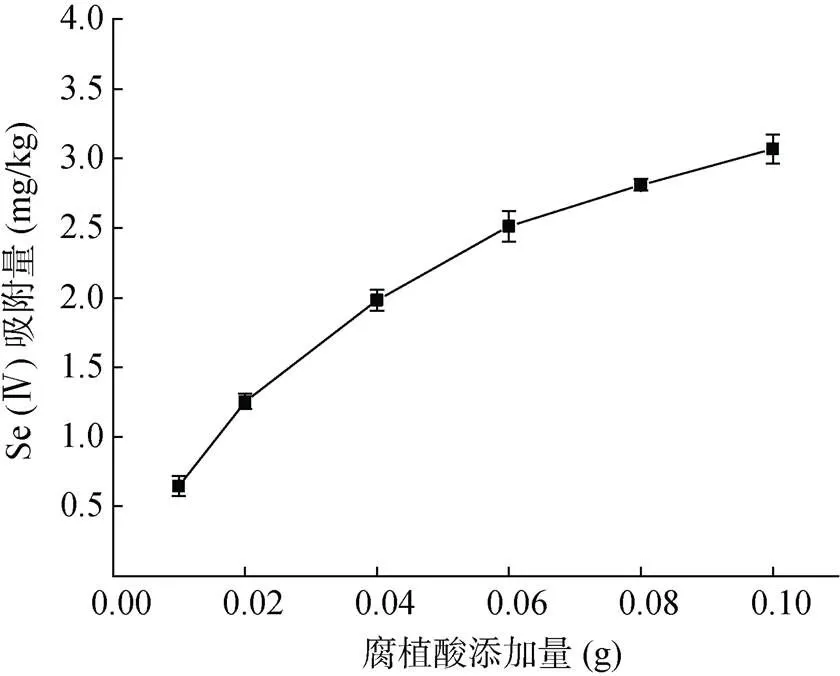
图5 腐植酸添加量对吸附Se(Ⅳ)的影响
2.2.4 体系pH的影响 体系pH对腐植酸吸附Se(Ⅳ)的影响如图6所示。在pH 3 ~ 6范围内,Se(Ⅳ)吸附量随着pH的增加不断减小;在pH 6 ~ 7范围内,Se(Ⅳ)吸附量为上升的趋势;在pH>7时,Se(Ⅳ)吸附量急剧下降,直到pH 9时仍呈下降趋势。该试验结果表明,pH是影响腐植酸吸附Se(Ⅳ)的重要因素,Se(Ⅳ)的吸附量总体趋势是随着溶液pH的增加而降低,在试验的最低pH下,Se(Ⅳ)的吸附量最大。邹光中和任海清[24]的研究表明,在pH 1 ~ 5范围内,pH增高,腐植酸对硒的吸附量增加;当pH>5时,硒的吸附量减小,本试验结果与之不一致,可能原因是采用的腐植酸与硒的来源不同。然而,本试验结果与Lee等[25]对土壤吸附Se(Ⅳ)的研究结果一致,即土壤对Se(Ⅳ)的吸附取决于pH,并且在pH 5 ~ 9范围内,最低pH时Se(Ⅳ)的吸附量最大,随着pH升高,吸附量降低。
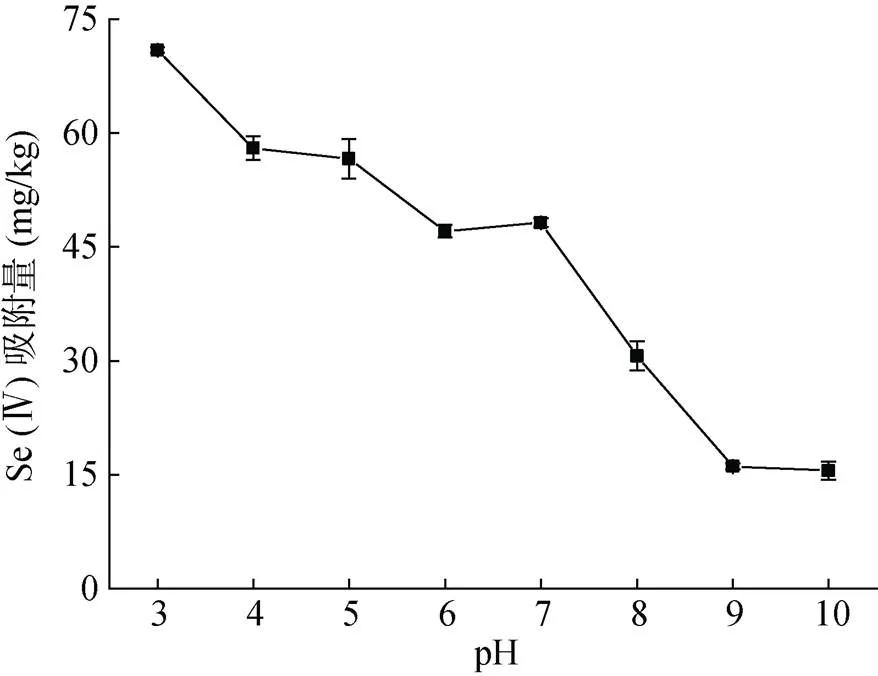
图6 pH对吸附Se(Ⅳ)的影响
在本试验的pH范围内,Se(Ⅳ)是以硒氧阴离子的形态存在,始终带负电荷,而腐植酸含有丰富的活性基团,当溶液H+浓度改变,腐植酸发生质子化或去质子化,其表面电荷随之改变[26-27]。酸性条件下,腐植酸质子化程度大,质子化提高腐植酸表面的正电荷,增强腐植酸表面与硒氧阴离子的静电引力,从而有较强的吸附能力吸附更多的Se(Ⅳ),但随着pH的升高,去质子化程度增加,正电荷减少,其吸附能力减弱。因此,在最低pH时腐植酸吸附Se(Ⅳ)的吸附量最大,随着pH的增大而吸附量减小。中性条件下,Saada等[28]研究指出,pH为7时,腐植酸胺基质子化带正电荷,在有机物吸附As(Ⅴ)中有显著影响,而硒与砷的行为相似。因此,pH为7时,可能是腐植酸的胺基被质子化,从而增强了对Se(Ⅳ)的吸附。碱性条件下,溶液中的OH–增多,与硒氧阴离子形成竞争关系,共同竞争腐植酸表面的活性位点,并且腐植酸会溶于碱溶液,因此吸附量不断减小[27,29]。
2.3 Se(Ⅳ)解吸试验
据前人研究可知,目前对土壤有效硒含量的测定还没有统一的方法,但磷酸盐溶液是使用最为普遍的浸提剂。磷酸盐提取的硒含量与植物中的硒含量高度相关,由磷酸盐浸提出的配体可交换态硒(EX-Se)是植物可直接吸收利用的硒[30-32],因此本试验使用磷酸盐浸提剂对吸附后的样品进行解吸,进而探究腐植酸对Se(Ⅳ)的吸附方式及对硒生物有效性的影响。
如图7所示,随着腐植酸添加量的增加,EX-Se含量增加,EX-Se占比也增加;当腐植酸添加量为0.01 g时,EX-Se占比为42.99%,当腐植酸添加量为0.10 g时,EX-Se占比为81.23%。腐植酸含量增加,有效硒含量增多,说明与腐植酸结合较弱的表面形态硒增多。然而Wang等[33]的盆栽试验表明,与腐植酸结合的硒结构稳定,难以分解供给植物利用。因此推断在短时间内腐植酸对See(Ⅳ)的吸附能力较弱,可以促进硒生物有效性的提高。

图7 腐植酸添加量与EX-Se的关系
3 结论
1)腐植酸对Se(Ⅳ)的吸附主要发生在反应前15 min;随着Se(Ⅳ)初始浓度和腐植酸添加量的增加,腐植酸对Se(Ⅳ)的吸附能力增强;随着体系pH增加,腐植酸吸附Se(Ⅳ)的能力减弱。腐植酸对Se(Ⅳ)的吸附过程符合准二级动力学方程;Freundlich等温吸附模型能较好地描述其等温吸附过程。
2)腐植酸对Se(Ⅳ)的吸附与C=O、C–O、C=C、O–H、N–H等官能团相关。吸附反应的机制是酸性条件下,腐植酸表面发生质子化,表面正电荷增加,增强了腐植酸与硒氧阴离子之间的静电引力,腐植酸表面的活性官能团与Se(Ⅳ)发生配位体交换反应。
[1] Wang S F, Lei L, Zhang D N, et al. Stabilization and transformation of selenium during the Fe(II)-induced transformation of Se(IV)-adsorbed ferrihydrite under anaerobic conditions[J]. Journal of Hazardous Materials, 2020, 384: 121365.
[2] 张丽, 张乃明, 张玉娟, 等. 云南耕地土壤硒含量空间分布及其影响因素研究[J]. 土壤, 2021, 53(3): 578–584.
[3] 覃建勋, 付伟, 郑国东, 等. 广西岩溶区表层土壤硒元素分布特征与影响因素探究——以武鸣县为例[J]. 土壤学报, 2020, 57(5): 1299–1310.
[4] 王张民, 袁林喜, 朱元元, 等. 我国富硒农产品与土壤标准研究[J]. 土壤, 2018, 50(6): 1080–1086.
[5] Etteieb S, Magdouli S, Zolfaghari M, et al. Monitoring and analysis of selenium as an emerging contaminant in mining industry: A critical review[J]. Science of the Total Environment, 2020, 698: 134339.
[6] Zafeiriou I, Gasparatos D, Massas I. Adsorption/desorption patterns of selenium for acid and alkaline soils of xerothermic environments[J]. Environments, 2020, 7(10): 72.
[7] Supriatin S, Weng L P, Comans R N J. Selenium speciation and extractability in Dutch agricultural soils[J]. Science of the Total Environment, 2015, 532: 368–382.
[8] Li Z, Liang D L, Peng Q, et al. Interaction between selenium and soil organic matter and its impact on soil selenium bioavailability: A review[J]. Geoderma, 2017, 295: 69–79.
[9] 江韬. 胡敏酸氧化还原特性及其对汞非生物还原过程的影响研究[D]. 重庆: 西南大学, 2012.
[10] Yang T, Hodson M E. Investigating the use of synthetic humic-like acid as a soil washing treatment for metal contaminated soil[J]. Science of the Total Environment, 2019, 647: 290–300.
[11] Aldmour S T, Burke I T, Bray A W, et al. Abiotic reduction of Cr(VI) by humic acids derived from peat and lignite: Kinetics and removal mechanism[J]. Environmental Science and Pollution Research International, 2019, 26(5): 4717–4729.
[12] 王锐, 许海娟, 魏世勇, 等. 针铁矿和针铁矿–胡敏酸复合体对Se(Ⅳ)吸附机制[J]. 土壤学报, 2018, 55(2): 399–410.
[13] Fang D, Wei S Y, Xu Y, et al. Impact of low-molecular weight organic acids on selenite immobilization by goethite: Understanding a competitive-synergistic coupling effect and speciation transformation[J]. Science of the Total Environment, 2019, 684: 694–704.
[14] 李伟. 超滤分级腐植酸结构特征及其对磷有效性的调控[D]. 北京: 中国农业科学院, 2021.
[15] Barnie S, Zhang J, Wang H, et al. The influence of pH, co-existing ions, ionic strength, and temperature on the adsorption and reduction of hexavalent chromium by undissolved humic acid[J]. Chemosphere, 2018, 212: 209–218.
[16] 王鹏, 冯金生, 金韶华, 等. 有机波谱[M].北京:国防工业出版社, 2012.
[17] Tatzber M, Stemmer M, Spiegel H, et al. FTIR-spectroscopic characterization of humic acids and humin fractions obtained by advanced NaOH, Na4P2O7, and Na2CO3extraction procedures[J]. Journal of Plant Nutrition and Soil Science, 2007, 170(4): 522–529.
[18] 王锐, 朱朝菊, 向文军, 等. 针铁矿与胡敏酸的交互作用及其复合物的稳定性[J]. 环境科学, 2017, 38(11): 4860–4867.
[19] Coppin F, Chabroullet C, Martin-Garin A. Selenite interactions with some particulate organic and mineral fractions isolated from a natural grassland soil[J]. European Journal of Soil Science, 2009, 60(3): 369–376.
[20] Qin H B, Zhu J M, Su H. Selenium fractions in organic matter from Se-rich soils and weathered stone coal in selenosis areas of China[J]. Chemosphere, 2012, 86(6): 626–633.
[21] Kamei-Ishikawa N, Tagami K, Uchida S. Sorption kinetics of selenium on humic acid[J]. Journal of Radioanalytical and Nuclear Chemistry, 2007, 274(3): 555–561.
[22] Kamei-Ishikawa N, Nakamaru Y, Tagami K, et al. Sorption behavior of selenium on humic acid under increasing selenium concentration or increasing solid/liquid ratio[J]. Journal of Environmental Radioactivity, 2008, 99(6): 993–1002.
[23] 王华伟, 李晓月, 李卫华, 等. pH和络合剂对五价锑在水钠锰矿和水铁矿表面吸附行为的影响[J]. 环境科学, 2017, 38(1): 180–187.
[24] 邹光中, 任海清. 腐植酸与硒的吸附模型研究[J]. 稀有金属, 2003, 27(3): 413–415.
[25] Lee S H, Doolittle J J, Woodard H J. Selenite adsorption and desorption in selected south Dakota soils as a function of pH and other oxyanions[J]. Soil Science, 2011, 176(2): 73–79.
[26] Dinh Q T, Li Z, Tran T A T, et al. Role of organic acids on the bioavailability of selenium in soil: A review[J]. Chemosphere, 2017, 184: 618–635.
[27] 陆欣, 谢英荷. 土壤肥料学[M]. 2版. 北京: 中国农业大学出版社, 2011.
[28] Saada A, Breeze D, Crouzet C, et al. Adsorption of arsenic (V) on kaolinite and on kaolinite-humic acid complexes. Role of humic acid nitrogen groups[J]. Chemosphere, 2003, 51(8): 757–763.
[29] Gabos M B, Goldberg S, Alleoni L R F. Modeling selenium (IV and VI) adsorption envelopes in selected tropical soils using the constant capacitance model[J]. Environmental Toxicology and Chemistry, 2014, 33(10): 2197–2207.
[30] 谢薇, 杨耀栋, 菅桂芹, 等. 四种浸提剂对果园与菜地土壤有效硒浸提效果的对比研究[J]. 岩矿测试, 2020, 39(3): 434–441.
[31] 宋晓珂, 王金贵, 李宗仁, 等. 富硒土壤中有效硒浸提剂和浸提条件研究[J]. 中国农学通报, 2018, 34(3): 152–157.
[32] Wang S S, Liang D L, Wang D, et al. Selenium fractionation and speciation in agriculture soils and accumulation in corn (L.) under field conditions in Shaanxi Province, China[J]. Science of the Total Environment, 2012, 427/428: 159–164.
[33] Wang D, Dinh Q T, Anh Thu T T, et al. Effect of selenium-enriched organic material amendment on selenium fraction transformation and bioavailability in soil[J]. Chemosphere, 2018, 199: 417–426.
Adsorption Characteristics and Mechanisms of Se (Ⅳ) on Humic Acid
DENG Huawei, JIANG Daihua*, HUANG Xuejiao, HUANG Jinlan
(College of Agriculture, Guangxi University, Nanning 530004, China)
The surface properties and structural characteristics of humic acid, as an adsorbent, were characterized by elemental analysis, scanning electron microscope (SEM), and Fourier-transform infrared spectroscopy (FTIR), the adsorption characteristics and mechanisms of humic acid on Se(Ⅳ) was explored through the analysis of adsorption kinetics, adsorption isotherm, external conditions on the adsorption of humic acid on Se(Ⅳ) and desorption characteristics. The results show that high degree of humification and large surface area of humic acid could offer more binding sites. The adsorption capacity of humic acid on Se(Ⅳ) is increased with the decrease of pH, and the increase of Se(Ⅳ) initial concentration and humic acid content. Furthermore, the adsorption of Se(Ⅳ) by humic acid is mainly occurred in the first 15 minutes, and the adsorption process could be described by the quasi second-order kinetic equation; adsorption isotherm data is fitted the Freundlich model. FTIR spectra reveal that C=O, C–O, C=C, O–H and N–H are possibly involved in the binding process as the main functional groups, and the major mechanism of humic acid adsorption for Se(Ⅳ) is electrostatic attraction and ligand exchange.
Humic acid; Se(Ⅳ); Adsorption characteristics; Mechanism
S153.6
A
10.13758/j.cnki.tr.2022.04.022
邓华为, 蒋代华, 黄雪娇, 等. 腐植酸对Se(Ⅳ)的吸附特征与机制. 土壤, 2022, 54(4): 827–833.
国家自然科学基金地区基金项目(41967006)和广西自然科学基金重点项目(2018GXNSFDA281035)资助。
(dhjiang2008@gxu.edu.cn)
邓华为(1997—),女,云南昆明人,硕士研究生,主要从事土壤生态学研究。E-mail:1051713644@qq.com

