生物法脱除含硫气体中硫化氢试验研究
包 飞
(中石化南京化工研究院有限公司,江苏南京210048)
生物脱硫是近年来新兴的研究课题,因其特有的节能环保的特点而倍受关注。生物脱硫技术是将硫化氢等含硫气体与吸收液反应生成硫化物,由培育的微生物吃进硫化物,利用硫杆菌的生物催化作用,吐出硫黄并再生出吸收液,实现脱硫的过程。典型的生物脱硫工艺有荷兰的Shell-Paques工艺和日本的Bio-SR工艺等。Shell-Paques工艺是从气相物流中脱除硫化氢并以元素硫的形式进行硫黄回收的生物反应过程,该工艺适合脱硫化氢后硫黄产量在0.05~50 t/d的气体处理过程,适用于高压天然气、合成气、燃料气和来自胺吸收再生过程酸性气的脱除[1]。Shell-Paques工艺将气体净化及硫黄回收在同一工艺流程中实现完美结合,硫化氢脱除率高达99.8%,而净化气中的φ(H2S)也不超过0.000 4%。目前,该技术在世界范围内得到广泛应用,已拥有数十套生物脱硫商业化装置。Bio-SR工艺使用的细菌与Shell-Paques工艺不同,该工艺在吸收塔内就通过硫酸铁溶液将元素硫氧化为硫黄,然后将溶液中的硫黄进行分离,分离硫黄后的溶液送入生物反应器中再生。细菌在生物反应器中将二价铁氧化成三价铁,由于该细菌为嗜酸菌,因此操作的pH值在2.0~2.5的较强酸性条件下进行[2]。国内生物脱硫研发起步较晚,尚未有成套的成熟工艺,仅局限于小试规模及少量中试研究,设计能力还不够完善,且装置、工艺及填料的不同也使工艺参数的设计参差不齐。生物脱硫技术受微生物基础和工艺设备研究的限制在国内仍处于起步阶段。
很多企业都存在着石化含硫气体的回收利用问题。中低潜硫量的含硫气体,采用传统技术脱硫后,再生酸性尾气燃烧后排放气达不到排放标准;常规湿式氧化工艺处理再生酸性尾气存在设备多、流程长、投资较高的问题。而生物脱硫技术在一定程度上可简化流程、操作过程简单、能耗低、投资少、不易造成二次污染[3],将含硫气体中的硫元素进行回收,净化后的气体可达到环保标准要求。
该试验以含硫化氢的原料气为研究对象,使用生物法对其进行净化处理,评价脱硫效果及生物硫黄的生成情况。
1 试验部分
1.1 试验原料
试验原料气为原料气混合罐内配制的φ(H2S)为0.2%的气体;脱硫液(包含菌种)为pH值为8.0~9.5的钠碱液。
1.2 仪器
电导率测定仪:DDS-307型,上海雷磁仪器有限公司;pH测定仪:PHS-3C型,上海雷磁仪器有限公司;氧化还原电位测定仪:DZB-715型,上海雷磁仪器有限公司;激光粒度分析仪:LS-609型,欧美克仪器公司。
1.3 主要设备
试验在生物脱硫中试装置上进行,该装置处理气体流量约30 m3/h,主要设备见表1。

表1 生物脱硫中试装置主要设备
1.4 工艺流程
生物脱硫工艺分为脱硫吸收、富液生物再生和单质硫分离三个单元,工艺流程见图1。
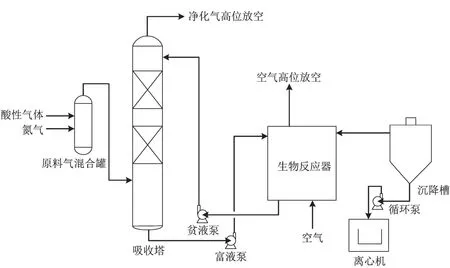
图1 生物脱硫工艺流程
原料气从底部进入吸收塔,在塔内自下而上与由塔顶部喷淋下来的弱碱性溶液逆流接触,气体中的H2S被吸收,净化气由塔顶引出,经气液分离后放空;吸收了H2S的碱液(富液)从吸收塔底部出来,进入生物反应器。在生物反应器中,控制温度在30~40 ℃,吸收硫化氢形成的可溶性硫化钠等物质在空气曝气和微生物脱硫菌种的生物催化作用下,与氧反应生成单质硫,空气由塔顶排出,同时碱液得到再生,返回吸收塔循环使用。从生物反应器出来的再生碱液进入沉降槽,单质硫从沉降槽中以颗粒沉淀的方式输送入离心机,分离后的滤液回流去生物反应器。硫黄料浆在离心机中浓缩成w(S)60%的硫黄饼,可进一步干燥成硫黄粉末。
1.5 试验方法
1.5.1 溶液的配制
向脱盐水中加入碳酸钠和碳酸氢钠,搅拌溶解后加入生物反应器,保持CO32-与HCO3-的总摩尔浓度为0.5~0.8 mol/L,建立系统循环,控制pH值在8.5~9.5。按接种量5%~20%向系统溶液中加入菌液。对溶液进行分析,pH值为8.86,电导率值为43.4 mS/cm。
1.5.2 原料气的配制
将含H2S的气体与来自管网的氮气通过流量控制系统精确计量,按恒定比例连续不断地进入原料气混合罐混合,不间断地配制并供给φ(H2S)为0.2%的原料气。
1.5.3 生物脱硫试验
先在生物脱硫中试装置上建立吸收再生循环,然后在常温下向吸收塔中通入含H2S的原料气,考察气液比(体积比)对净化气中H2S含量的影响,气液比的取值分别为20∶1、15∶1和10∶1。
2 结果与讨论
以30 m3/h的流量将φ(H2S)为0.2%的原料气通入生物脱硫中试装置,改变气液比测定净化气中H2S的含量,试验结果见表3。

表3 生物脱硫试验结果
由表3可见,在不改变其他工艺参数的情况下,随着气液比的变化,净化气中的H2S含量也相应变化。当φ(H2S)为0.2%,气液比在20∶1时,净化气中的ρ(H2S)>20 mg/m3。随着贫液量的增加,气液比调整至15∶1,净化气ρ(H2S)<20 mg/m3。随着气液比继续降低,净化气中的H2S含量也继续降低。
运行一段时间待系统形成稳定的乳浊液后,用激光粒度分析仪对沉降槽中的溶液进行粒度分析,结果见图2。
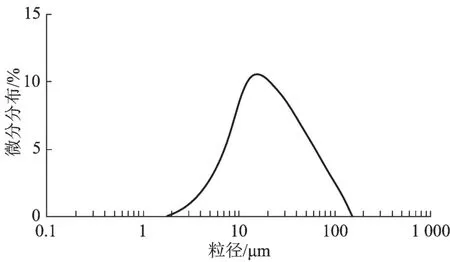
图2 激光粒度仪分析结果
由图2可见,硫黄颗粒的粒度大部分集中在10~30 μm的区域。
试验过程中还发现,在净化气ρ(H2S)<20 mg/m3长期稳定的情况下,氧化还原电位(ORP)对脱硫液的性状有明显影响。ORP变化时,脱硫液性状会相应变化。ORP与脱硫液性状的关系见表4。

表4 ORP与脱硫液性状的关系
曝气适当时,一般氧硫比控制在1.5,此时脱硫液的ORP在-390~-300 mV,为最佳操作状态,形成乳浊液;当ORP大于-300 mV时,脱硫液的颜色为淡黄色透明液体,未形成乳浊液;当ORP小于-390 mV时,脱硫液颜色转化成墨绿色甚至黑色,判断为硫含量超过了细菌的处理能力。
溶液的pH值控制在8.5~9.5,pH值下降时,脱硫效果会下降。长时间运行后,溶液中会有一部分硫化物转化为硫酸盐。运转初期硫酸盐(ρ)为1 g/L,运转3个月后硫酸盐(ρ)升高至10 g/L。
3 结论
通过生物法脱除原料气中硫化氢试验研究得出以下结论:
1)在原料气流量30 m3/h条件下,当φ(H2S)约0.2%时,气液比调整至15∶1以下可满足净化气ρ(H2S)<20 mg/m3的要求。
2)当氧硫比控制在1.5,溶液的ORP在-390~-300 mV,为最佳操作状态,系统产生生物硫黄,脱硫液形成乳浊液。
运行一段时间后硫酸盐在系统中会有累积,但硫酸盐的产生在该中试研究中未对脱硫系统产生明显的影响。后续要针对生物硫黄的沉降和长时间运转中硫酸盐对生物菌的影响做进一步的研究,对脱硫液性状变化的机理进行探讨。

