纳米钯铜改性毛竹炭三维电催化还原水中硝酸盐氮的机理研究
吴雨晴,朱宗强,2,3*,张立浩,2*,董 翼,刘霜霜,朱义年,2,3,李艳红,2,3
1. 桂林理工大学环境科学与工程学院,广西 桂林 541006
2. 广西环境污染控制理论与技术重点实验室,广西 桂林 541006
3. 岩溶地区水污染控制与用水安全保障协同创新中心,广西 桂林 541006
硝酸盐氮(NO3-N)是地表水和地下水中常见的污染物,会随着水循环进入人类生活环境或者动植物体内,进而给人体健康、动植物生长代谢甚至整个自然环境带来安全隐患[1-4]. 因此,对水中NO3-N 污染的控制意义重大. 当前水中NO3-N 的去除方法主要包括生物处理[5]和物理化学处理[6]两大类. 电催化还原脱氮法因其具有快速、高效、材料易回收等优势而受到众多学者的青睐[7]. 通过电化学反应装置和电极的特定设计,可以提高电催化还原水中NO3-N 的脱氮效率[8-9]. 其中,电极的设计和使用方法,直接影响电催化还原的高效性和经济性[10]. 三维粒子电极可以较好地提升电催化还原效率[11-12],其作用核心在于电极表面的元素修饰. 钯(Pd)、铂(Pt)、钌(Ru)、铑(Rh)和铱(Ir)等贵金属均可作为还原催化剂的主要表面修饰元素,其中Pd 被认为是最适用于催化还原NO3-N的贵金属[13-17]. 另外,通常辅以过渡金属〔铜(Cu)、镍(Ni)、铁(Fe)、锡(Sn)、铟(In)等〕开展联合表面修饰[18],提升金属粒子在载体上的稳定性和催化还原高效性[19-21]. 生物炭因具比表面积大、孔隙度发达和结构稳定等特点,被认为是吸附应用和催化剂制备的良好载体. 经过高温改性的生物炭具导电、高比表面积和分级多孔等特性,可作为金属负载分散的高效载体,利于促进三维粒子电极的催化还原脱氮界面过程[22].
因此,该研究以毛竹生物炭为材料制备载体,采用浸渍焙烧-氢还原法制备获取纳米钯铜改性毛竹炭(Nano-Pd/Cu-BC),搭建三维电催化还原脱氮体系,研究三维粒子电极对电催化还原脱氮的影响与机理,研究结果可为地下水NO3-N 污染防治工作提供技术指导与参考.
1 材料与方法
1.1 主要试剂和仪器
1.1.1 主要试剂
氯钯酸钠(Na2PdCl4)、二水合氯化铜(CuCl2·2H2O)、硝酸钠(NaNO3)、硫酸钠(Na2SO4)氯化铁(FeCl3)、氯化铜(CuCl2)、亚硝酸钠(NaNO2)、氯化铵(NH4Cl)、氨基磺酸、磺胺、酒石酸钾钠、碘化钾(KI)、碘化汞(HgI2)、盐酸,均购自西陇科学股份有限公司,以上试剂均为分析纯级. 硝酸钠、亚硝酸钠和氯化铵在使用之前均在80 ℃条件下烘干2 h. 试验用水均为超纯水(电导率为18.20 MΩ).
1.1.2 试验装置与方法
紫外分光光度计(UV-6100A,上海元析仪器有限公司);可见光分光光度计(V-5800PC,上海元析仪器有限公司);场发射扫描电镜(JSM-7900F,日本电子公司);X 射线衍射仪(X'Pert3 Powder,英国马尔文 &荷兰帕纳科公司);电感耦合等离子体光谱发生仪(Optima 7000DV PerkinElmer,美国PerkinElmer 公司);电化学工作站(CHI660E,上海辰华仪器有限公司).试验装置(见图1)主要由反应室(10 cm×5 cm×6 cm)、阴阳电极(钛钌网,4.5 cm×3.5 cm)和直流稳压电源(北京大华电子集团)组成,其中反应室被质子膜分为阳极室和阴极室. 试验过程中,阴阳两极板间距控制为3 cm,通过转速为800 r/min 的磁力搅拌操作保证反应体系溶液的充分混合;NO3-N 初始浓度为100 mg/L(以N 计),电解质Na2SO4溶液的浓度为0.20 g/L,电催化反应时间为4 h,每隔30 min 从阴极室取出水样,测定NO3-N、NO2-N 和NH3-N 的浓度.
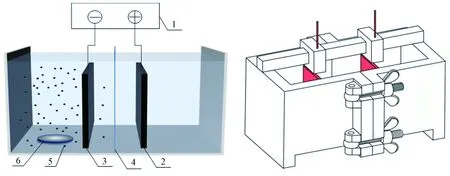
图1 三维电催化还原NO3-N 的试验装置示意Fig.1 Schematic diagram of an experimental device for 3D electrocatalytic reduction of nitrate
1.2 试验方法
1.2.1 材料制备
催化剂制备步骤主要如下:首先将洗净烘干后的毛竹杆材(<0.25 mm)以1 L∶100 g 的比例分别放入0.50 mol/L 的FeCl3溶液和0.5 mol/L 的CuCl2溶液中,超声1 h,以保证金属前驱液浸入毛竹内;然后在50 ℃下干燥24 h;干燥后的样品置于管式炉中,N2气氛下600 ℃加热碳化4 h,冷却后分别制得铁改性毛竹炭(Fe-BC)和铜改性毛竹炭(Cu-BC).
采用湿化学法及氢气还原等手段对Fe-BC 和Cu-BC 进行Pd 金属负载改性[23]:在50 mL 的烧瓶中,将Fe-BC 或Cu-BC 放 入1.00 g/L 的Na2PdCl4溶 液中,超声1 min 使Fe-BC 或Cu-BC 样品分散在溶液体系中,900 r/min 下磁力搅拌5 min,使体系达到吸附平衡状态;用两根16 号不锈钢针经橡胶塞插入,一根针伸入距液面0.50 mm 位置作为H2进气口,另一根针作为气体出口,向悬浮液中通入H2,喷注5 min 完成金属Pd 的还原,分别制得纳米钯铁改性毛竹炭(Nano-Pd/Fe-BC)和纳米钯铜改性毛竹炭(Nano-Pd/Cu-BC). 同样条件下,以商业活性炭(AC)为负载载体制备纳米钯铜改性活性炭(Nano-Pd/Cu-AC).
1.2.2 产物的测定及相关参数的计算NO3-N 的浓度采用HJ/T 346-2007《水质 硝酸盐氮的测定 紫外分光光度法(试行)》测定;NO2-N 的浓度采用GB 7493-1987《水质 亚硝酸盐氮的测定分光光度法》测定;NH3-N 的浓度采用HJ 535-2009《水质 氨氮的测定 纳氏试剂分光光度法》测定.Mca和 G RN2的计算方法如下:

2 结果与讨论
2.1 材料表征
2.1.1 SEM-EDS 表征
采用SEM-EDS 对催化剂材料的微观形态(见图2)进行表征分析,由图2 可以看出,毛竹炭(BC)材料为蜂窝状结构,具有丰富的孔隙结构,其表面较为光滑. Nano-Pd-BC 的表征结果显示,BC 表面负载了Pd 纳米粒子,但由于纳米粒子具有较高的表面能,粒子在载体表面易团聚,形成纳米簇,粒径平均为87.52 nm. 图2(b)为Nano-Pd/Cu-BC 粒子催化材料的微观结构表征图,EDS 表征结果表明,在进行Pd 负载前加入助金属Cu 进行浸渍改性,使得Pd 纳米粒子在毛竹炭表面分布均匀,其金属粒子粒径相对较小,分布较其他材料更均匀,分散程度较高.
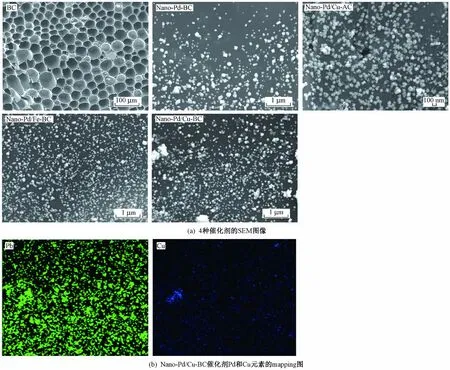
图2 不同催化剂的SEM-EDS 图Fig.2 SEM-EDS diagram of different catalytic materials
运用Nano Measurer 软件,以SEM 图为对象对催化剂中的纳米颗粒进行粒径大小统计分析,结果如图3 所示. 在4 种纳米金属改性催化剂中,仅负载Pd的生物炭上纳米颗粒平均粒径为87.52 nm、负载双金属Pd 和Cu 的生物炭上的纳米颗粒平均粒径为68.93 nm,加入助金属Fe 或者以AC 为负载基材均存在较大程度的粒子团聚. 统计结果表明,在以BC 为负载基材的基础上,加入适量的助金属Cu 在一定程度上可以有效抑制Pd 金属颗粒在生物炭表面的团聚,使得金属颗粒在生物炭表面分布较为均匀.
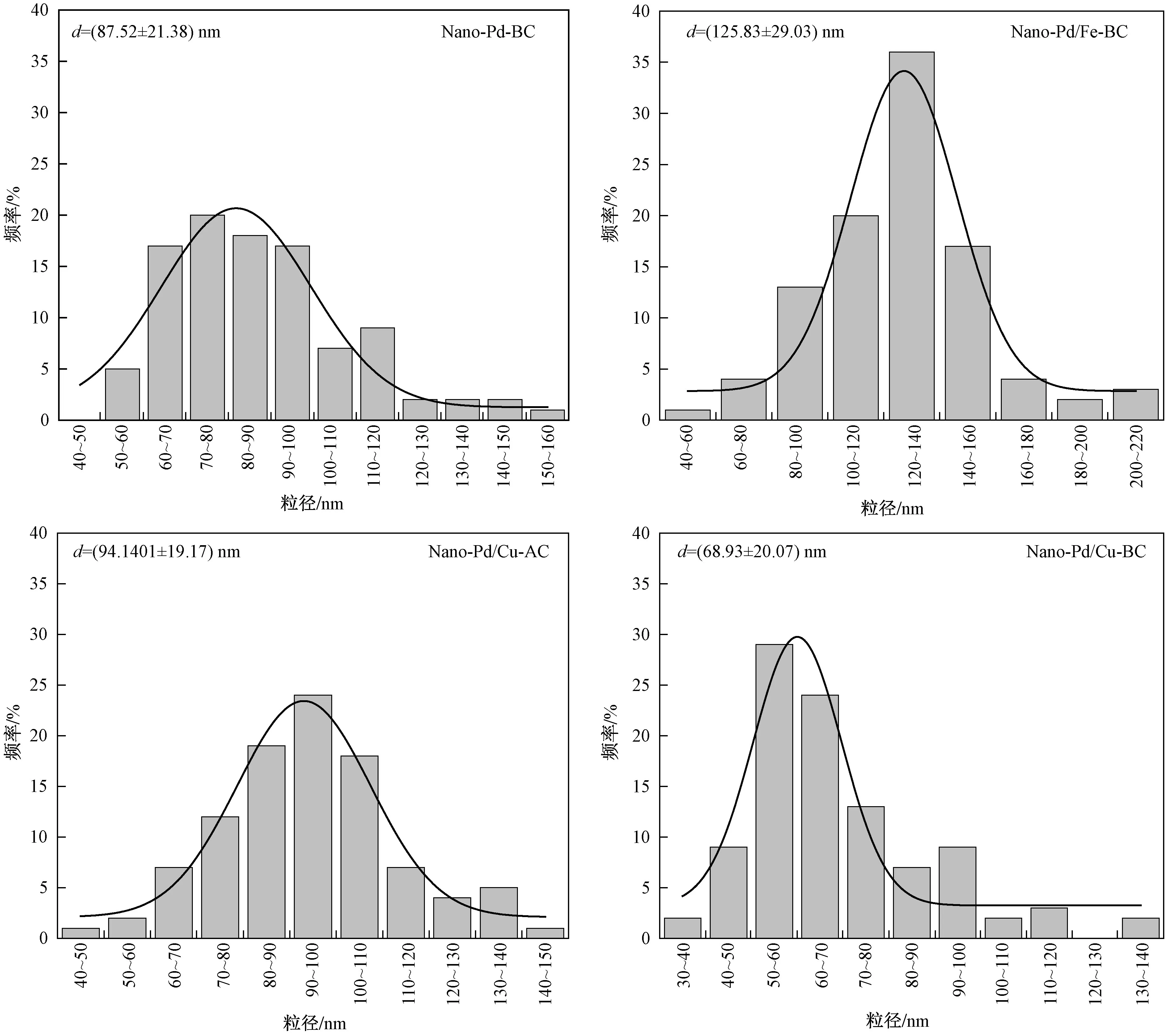
图3 不同纳米金属改性催化剂的粒径分布Fig.3 The particle size distribution of different nano-metal modified particle catalyst
2.1.2 XRD 表征
不同催化剂XRD 表征图谱如图4 所示. 通过X' pert Highscore plus 软件对比标准PDF 卡片,结果显示,催化剂的XRD 衍射图谱在2θ为41.5°处存在较强的归属于单质Pd0的(111)的晶面衍射,通过分析可知,该衍射峰与Pd-Cu 合金的标准衍射图谱(PDF#48-1551)中的衍射峰(111)晶面相吻合,揭示了该研究方法制备的Nano-Pd/Cu-BC 的构成主要为合金结构类型,除此之外,图谱无明显的衍射峰存在,可以说明Pd/Cu 合金在生长过程中晶胞表面主要以(111)晶面为主[24-25]. 和单金属Pd-BC 催化剂相比,在2θ为40°、46.67°、68.31°和82.22°处分别存在归属于Pd (111)、Pd (200)、Pd (220)和Pd (222)的晶面衍射峰,但衍射强度较弱,说明在合成的催化剂中Pd 主要以单质形式存在. 在2θ为40°处出现Pd0的(111)晶面衍射峰,表明制备的材料原子结构中,Pd 晶体颗粒中没有Cu 原子的掺杂,形成的双金属催化剂结构以异质结形式的结构存在. 与标准PDF 卡片对比可知,Nano-Pd/Cu-AC 和Nano-Pd/Cu-BC 催 化 剂 颗 粒XRD 图谱检测到在2θ为43.3°处存在Cu(111)的晶面 衍 射 峰,Nano-Pd/Fe-BC 在2θ为36°处 检 测 到 了Fe 的晶面衍射,并且衍射强度较强,揭示笔者的研究方法可以成功地在毛竹炭表面进行金属Pd、Cu、Fe的负载改性,并且金属负载量相对较高,合成的晶体结构以合金结构和异质结结构为主.
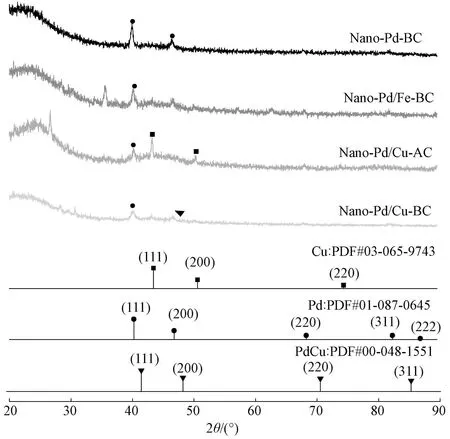
图4 不同纳米金属改性催化剂的XRD 图Fig.4 XRD patterns of different nano-metal modified catalysts
2.1.3 电化学交流阻抗EIS
催化剂在铁氰化钾混合溶液中的电化学交流阻抗图谱如图5 所示. 由图5 可见:BC 的电荷转移阻抗(Rct)值最大,为61.11 Ω;Nano-Pd-BC、Nano-Pd/Fe-BC和Nano-Pd/Cu-AC 的Rct值次之,依次分别为42.83、41.75 和43.37 Ω; Nano-Pd/Cu-BC 的Rct值最 小,为38.46 Ω. 这 表 明 BC、 Pd-BC、 Nano-Pd/Fe-BC 和Nano-Pd/Cu-AC 催化剂材料界面转移电阻较大,导电性能较差. Nano-Pd/Cu-BC 的Rct最小,表明其表面电荷传输速率最快,且电荷传输速率越快,越有利于NO3-N 的催化还原反应发生.

图5 不同纳米金属改性催化剂电化学阻抗测试EIS 图Fig.5 EIS diagram of electrochemical impedance test of different nano-metal modified catalysts
2.2 NO3-N 的去除性能影响分析
2.2.1 不同电催化体系对NO3-N 去除效果的影响
在电流大小为100 mA 的条件下,对比传统电催化还原体系和三维电催化还原体系对NO3-N 的去除效果,结果如图6 所示. 由图6 可见,传统电催化还原体系在240 min 内,仅可去除15 mg/L 的NO3-N. 少量的硝酸根离子在传统电催化还原体系中,吸附到了阴极的电极表面上,在电子参与下被还原成NO2-N 或NH3-N. 该反应过程较慢,且对NO3-N 的还原能力较弱. 而投加了BC,在相同条件下,对NO3-N 的质量催化活性为0.019 mg/mg,较传统电催化还原体系提升了1.51 倍;其中间产物NO2--N 和副产物NH3-N 的产量没有增加,而N2生成率增加了2.55 倍. 这表明BC的投加有助于增加阴极电极面积,提高反应速率,促进了NO3-N 的电催化还原过程. 因此,较传统电催化还原体系,投加粒子电极的三维电催化还原体系更有助于对NO3-N 的还原.
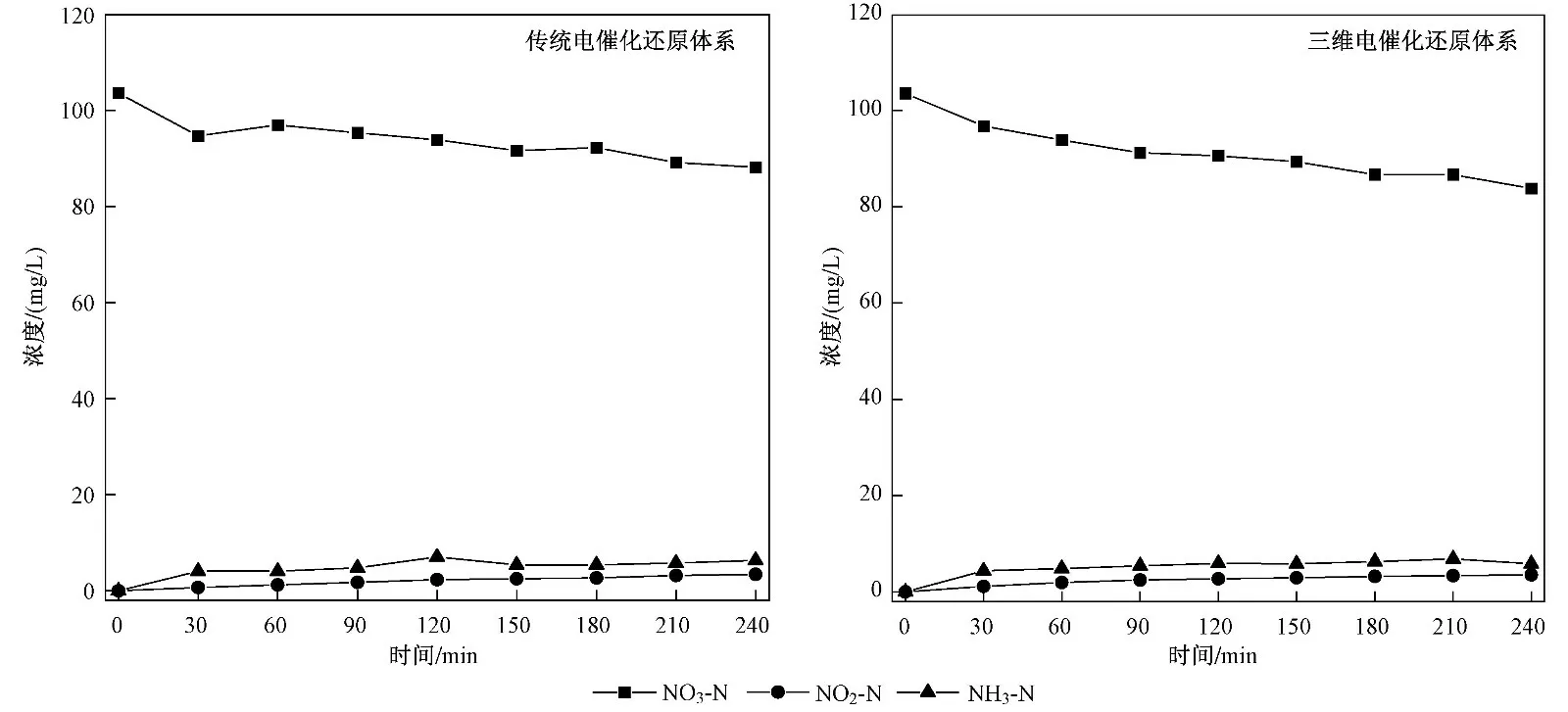
图6 不同电催化体系对NO3-N 的去除效果Fig.6 Removal effects of different electrocatalytic systems on NO3-N
2.2.2 不同催化剂对NO3-N 去除效果的影响
在催化剂投加量为100 mg,电流大小为100 mA的条件下,对比投加不同催化剂(BC、Pd-BC、Nano-Pd/Fe-BC、Nano-Pd/Cu-AC 和Nano-Pd/Cu-BC)电催化还原去除NO3-N 的效果,结果如图7 所示. 由图7 可见,在催化反应时间240 min 时,BC 对NO3-N的质量催化活性仅为0.019 mg/mg,Pd-BC 对NO3-N的质量催化活性也仅为0.023 mg/mg. 而采用双金属负载的Pd/Fe 和Pd/Cu 的催化剂对NO3-N 的质量催化活性较BC 和Pd-BC 均有所提高,且在催化还原反应进行240 min 后,Pd/Cu 双金属体系的催化剂对NO3-N 的去除效果更为显著,其中Nano-Pd/Cu-AC和Nano-Pd/Cu-BC 对NO3-N 的质量催化活性分别可达到0.050 和0.069 mg/mg,分别为BC 的2.63、2.17倍和Pd-BC 的3.63、3.00 倍.
不同催化剂催化还原NO3-N 的反应过程中生成中间产物NO2-N 和副产物NH3-N 的情况如图7 所示. 随着催化反应的进行,NO2-N 的积累量和NH3-N的生成量均有所增加. 其中双金属Pd/Cu 负载的催化剂在一定程度上能有效地将NO3-N 还原成NO2-N和NH3-N,且对N2的生成率有所提高,N2生成率最高为13.40%. 基于电流效率和能耗的计算方法[26-28],该试验中Nano-Pd/Cu-BC 在催化还原NO3-N 240 min后的电流效率为23.91%,能耗(EC)为0.31 kW·h/g.
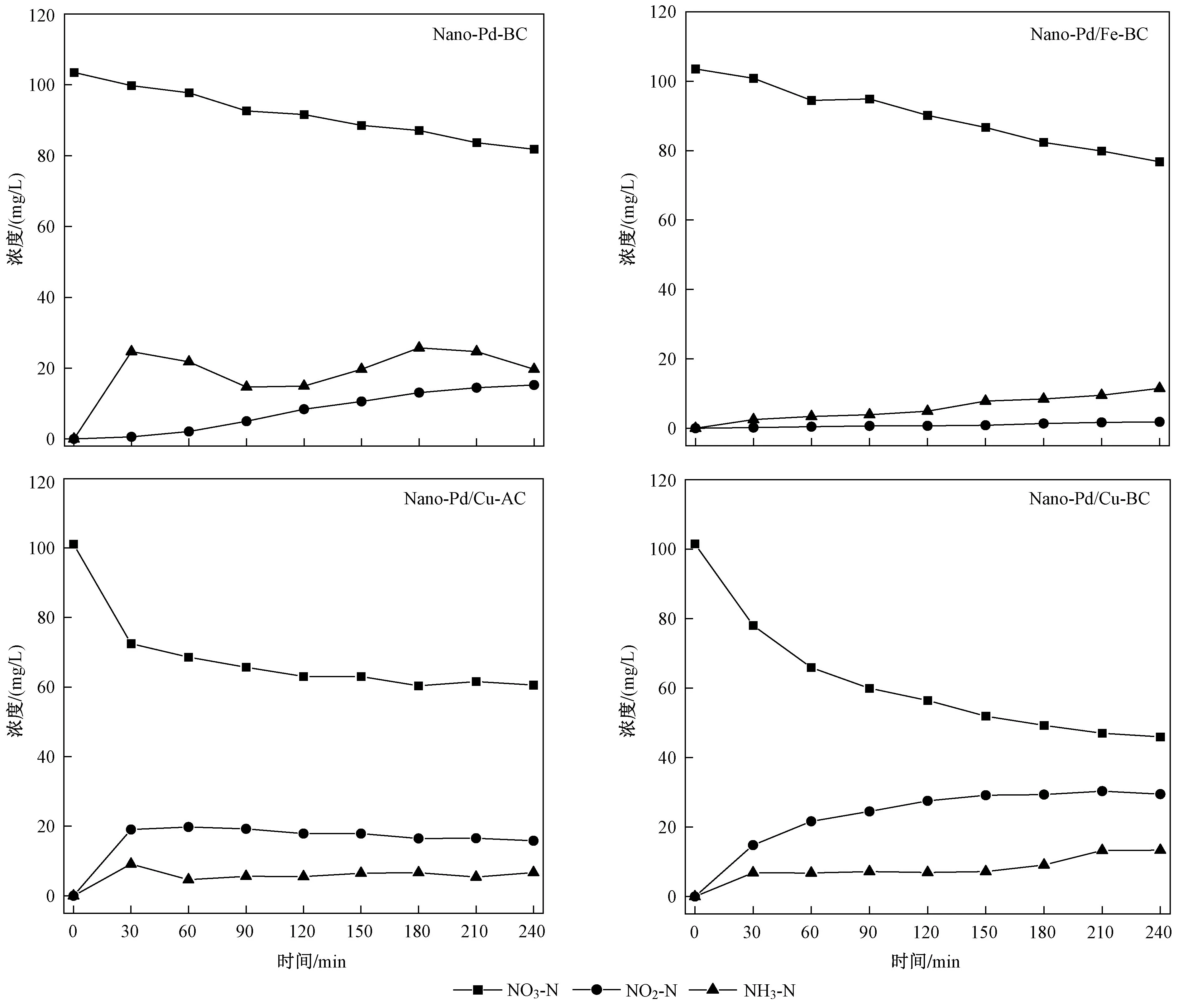
图7 不同催化剂对NO3-N 的去除效果Fig.7 Removal effects of different catalysts on NO3-N
2.2.3 Nano-Pd/Cu-BC 投加量对NO3-N 去除效果的影响
Nano-Pd/Cu-BC 投加量对NO3-N 的去除效果如图8 所示. 由图8 可见,随着Nano-Pd/Cu-BC 投加量的增加,反应体系中NO3-N 的去除效果逐渐提高. 当Nano-Pd/Cu-BC 投加量为0.100 g 时,体系对NO3-N达到最佳的去除效果,而当Nano-Pd/Cu-BC 投加量超过0.100 g 后,整个体系对NO3-N 的去除效果反而呈现下降的趋势. 结果表明,在三维粒子电极反应体系中,当Nano-Pd/Cu-BC 投加量超过0.100 g 时,因装置体积有限及粒子表面电荷等作用的限制,导致Nano-Pd/Cu-BC 在反应体系中相互碰撞而聚结,出现失稳现象,降低了体系对NO3-N 的去除效果.
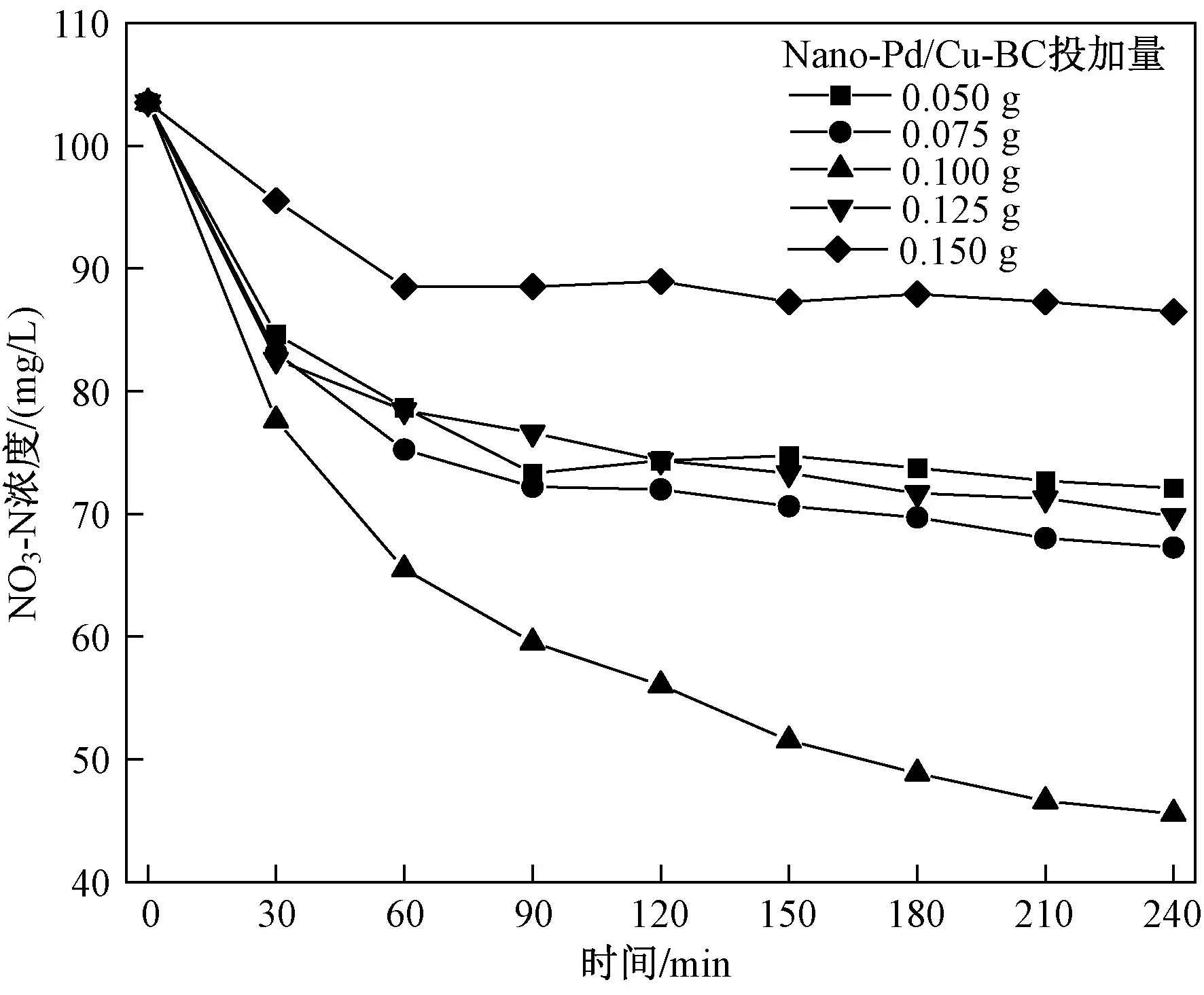
图8 不同Nano-Pd/Cu-BC 投加量对NO3-N 的去除效果Fig.8 Removal effects of Nano-Pd/Cu-BC on NO3-N at different dosages
2.3 电催化还原NO3-N 机理
催化NO3-N 还原为NO2-N 和N2,反应过程中还原速率及产物选择性会受到催化剂载体以及活性金属成分的影响. NO3-N 的催化还原需要在双金属体系中完成,助金属Cu 的介入提升了双金属催化剂在催化活性和选择性[29-33]. 该研究结果显示,在电催化间接还原NO3-N 过程中,分隔电极室的质子交换膜只允许H+通过,电极室首先发生水的电解反应,体系中产生的H 在阴极室聚集,助金属(以掺入助金属Cu为例)将吸附的H2活化分解为原子H*[16],并将原子H*传递到Pd-BC 表面,与NO3-N 发生反应,将其还原为NO2-N. 因此,Pd 金属有助于将NO2-N 选择性还原为NH3-N 和N2(见图9). 还原过程的主要反应方程式如下:
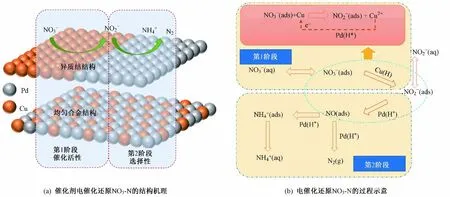
图9 电催化还原NO3-N 的机理和过程示意Fig.9 Mechanism and process of electrocatalytic reduction of NO3-N
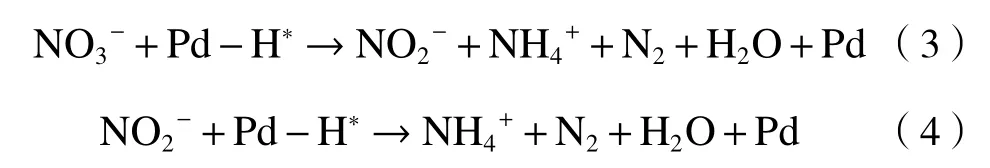
有研究[16,18,34-35]报道,NO3-N 的催化还原存在直接还原和间接还原2 个过程. 一般而言,在催化还原的第1 阶段,助金属Cu 提供NO3-N 的结合位点,将NO3-N 吸附在晶体表面,并将其还原为NO2-N,该步骤被认为是整个反硝化过程中的限速步骤. 助金属Cu 在NO3-N 还原过程中被氧化为最高价态. 在第2阶段,处于高价态的助金属在贵金属Pd 催化剂的作用下,被阴极产生的原子H*重新还原为零价态助金属,生产的中间产物NO2-N 在Pd 贵金属的作用下选择性地还原为N2和NH3-N,进而完成双金属催化剂的循环利用及再生[36],然而双金属结构的催化剂催化还原NO3-N 受主助金属比例的影响显著,2 种晶体结构对NO3-N 的还原效率和产物选择性上存在较大的差异.
当催化剂结构以合金结构形式存在时,Cu 原子掺杂在Pd 金属原子中,被Pd 原子锚固,从而阻碍了助金属Cu 与NO3-离子发生氧化还原反应,影响催化反应第1 阶段的反应速率. 由于Cu 原子无法有效吸附N 原子,导致吸附在Pd 原子表面的N 原子距离较大,生成N2过程需要克服的能垒较高,导致副产物NH3-N 生成[37]. Zhang 等[25,38]研究显示,均匀的合金结构催化剂在第1 阶段的催化活性和第2 阶段的N2生成性均较低. 当催化剂结构以异质结形式为主要形式时,其具有比合金结构更优的催化活性和N2生成率,但其作用机理目前尚未明确,有待进一步研究.
3 结论
a) 采用浸渍焙烧及氢气还原等方法制备4 种纳米金属改性毛竹炭催化剂. 表征结果显示,Nano-Pd/Cu-BC 相较于其他3 种纳米Pd 金属改性的催化剂,其颗粒粒径更小,在生物炭表面分布更为均匀.
b) 电化学性能结果显示,制备的Nano-Pd/Cu-BC电阻小,表面电荷传输速率较快,有利于催化还原反应的发生,对NO3-N 的去除效果良好.
c) 在电流大小为100 mA、电解液(Na2SO4)浓度为0.20 g/L、NO3-N 初始浓度为100 mg/L、三维粒子电极投加量为100 mg 的条件下,Nano-Pd/Cu-BC 对NO3-N 的去除效果最佳,在240 min 内,对NO3-N 的质量催化活性达0.069 mg/mg,N2生成率为13.50%,此时反应体系的能耗为0.31 kW·h/g.
d) 与传统电催化还原体系相比,三维电催化还原体系的N2生成率提升了2.84 倍,其中Nano-Pd/Cu-BC的质量催化活性较BC 提升了5.35 倍.

