美洛昔康磷脂复合物过饱和自纳米乳的制备及体外质量评价
王艳艳,赵文轩,贾皓月,宁婧歧,杨星钢*(.江苏联合职业技术学院连云港中医药分院,江苏 连云港 006;.沈阳药科大学药学院,沈阳 006)
美洛昔康(meloxicam,MLX)是非甾体抗炎药(NSAIDs)之一,常用于风湿性关节炎或骨关节炎等炎症性疾病,是环氧合酶-2(COX-2)的选择性抑制剂,具有抗炎、镇痛和解热的作用。由于MLX属于BCS Ⅱ类药物,水溶性差,溶出速率限制了吸收而导致生物利用度过低。
自纳米乳给药系统(self-nano emulsifying drug delivery systems,SNEDDS)是由油相、表面活性剂和助表面活性剂组成的各向同性且热力学稳定的混合体系,在胃肠道的蠕动下自发形成粒径小于100 nm的O/W
型微乳。SNEDDS可以有效改善难溶性药生物利用度差的问题,但是口服SNEDDS存在药物沉淀和吸收减少的风险。过饱和自纳米乳(supersaturated self-nanoemulsifying drug delivery system,S-SNEDDS)通过使用沉淀抑制剂可避免药物沉淀,促进其吸收。磷脂复合物(phospholipid complex,PC)可提高药物的亲脂性,提高了药物在SNEDDS的油相中的溶解度,从而增加其载药量,同时SNEDDS在介质的自发乳化分散性能也能解决PC因黏稠的质地而不易均匀分散的问题。目前利用沉淀抑制剂使自纳米乳形成过饱和或者将PC与自纳米乳体系相结合的研究均有不少报道,但将三者相结合的研究鲜有报道,因此本文考虑将三者相结合制备成美洛昔康磷脂复合物过饱和自纳米乳(MLX-PC-S-SNEDDS),以期提高MLX的载药量、溶解度和生物利用度。
1 材料
1.1 试药
美洛昔康(MLX,纯度:98%,天津希恩思奥普德科技有限公司);油酸聚乙二醇甘油酯(Labrafil M 1944 CS)、二乙二醇单乙基醚(Transcutol HP)[嘉法狮(上海)贸易有限公司];聚氧乙烯氢化蓖麻油(Cremophor RH40)、聚乙烯吡络烷酮-K30(PVP K30)、聚丙烯酸树脂L100(Eudragit L100)、共聚维酮S-630(PS-630)[巴斯夫(中国)有限公司];大豆卵磷脂(Lecithin High Potency)(山东优索化工科技有限公司);聚乙烯已内酰胺-聚醋酸乙烯酯-聚乙二醇接枝共聚物(Soluplus)、聚氧乙烯35蓖麻油(Kolliphor ELP)、聚氧乙烯蓖麻油(Cremophor EL)、脂肪醇聚氧乙烯醚(AEO-9)(德国BASF公司);棕榈酸异丙酯(IPP)(临沂绿森化工有限公司);油酸(Oleic acid,天津市恒兴化学试剂有限公司);辛酸/癸酸甘油三酯(GTCC,KLK吉隆坡甲洞集团公司);吐温80(Tween 80,天津市恒兴化学试剂有限公司);肉豆蔻异丙酯(IPM,广州享安精细化工有限公司);羟丙甲纤维素E15LV(HPMC E15LV)、羟丙甲纤维素 K4M(HPMC K4M)(上海卡乐康辅料有限公司);聚乙二醇400(PEG400,天津市光复精细化工研究所);β
-环糊精(β
-CD,淄博千汇生物科技有限公司);异丙醇(分析纯)、甲醇(色谱级)(山东禹王化学试剂有限公司)。1.2 仪器
ZRS-7G型药物溶出度仪(天津天大天发科技有限公司);XW-80A旋涡混合器(上海青浦泸西仪器厂);XS105型电子分析天平(梅特勒-托利多仪器有限公司);UV-8000 紫外可见分光光度计(上海元析仪器有限公司);TS-100恒温摇床(捷呈实验仪器);TG16MW台式高速离心机(湖南赫西仪器装备有限公司);SMD200-2 电子分析天平(奥豪斯国际贸易有限公司);PB-10 pH计(美国Sartorius公司);Nano ZS90粒度测定仪(英国马尔文公司);KQ-250DE型数控超声波清洗器(昆山市超声仪器有限公司);JEM-2100透射电子显微镜(日本电子株式会社);DF-101S集热式恒温磁力搅拌器(巩义市予华仪器有限责任公司)。
2 方法
2.1 MLX在不同辅料中的饱和溶解度测定
称取过量的MLX置于EP管中,分别加入2 mL各辅料,涡旋混匀,(37±0.5)℃、100 r·min恒温振荡72 h。达到平衡后,12 000 r·min离心10 min取上清液,用甲醇稀释到合适倍数,过滤,用UV法在361 nm处测定MLX在不同辅料中的吸光度,计算其溶解度,平行操作3次。其中,由于Cremophor RH40在室温下为固体,需要先将其在40℃下水浴加热熔化后再进行试验。
2.2 三元相图绘制
将表面活性剂和助表面活性剂按照一定的质量比(K
)分别为4∶1、3∶1、2∶1、1∶1、1∶2、1∶3进行混合,再与油相按照比例分别为1∶9、2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1进行混匀,固定体系质量为1 g,缓慢滴入37℃水浴磁力搅拌下100 mL蒸馏水中,观察其乳化状态。以油相、表面活性剂、助表面活性剂分别为三元相图的三个顶点,用Origin 8.0软件绘制三元相图。以能够形成的微乳区域面积大小为指标,利用Image J软件对三元相图内乳化面积大小进行相对计算,进而确定适合的三相以及各组分比例。2.3 星点设计联合归一化法综合评定进行多指标处方优化
以Labrafil M 1944 CS 用量百分比(X
)与表面活性剂与助表面活性剂的比例K
(X
)作为考察因素。效应指标分别为粒径(Y
)、粒径分散系数(PDI,Y
)与载药量(Y
)。采用Design Expert 10.0.7软件进行二因素、五水平星点设计。用归一化法对数据进行标准化处理,利用熵值法方法计算得到标准化数据和权重系数,并以综合评分Y
表达最终效应,并建立数学模型进行优化与预测分析,对MLX-SNEDDS处方进行优化。2.4 沉淀抑制剂筛选
2.4.1 沉淀抑制剂种类的筛选精密称MLXSNEDDS处方中各组分,分别加入2%的各类沉淀抑制剂,超声搅拌使其混合均匀,形成MLXS-SNEDDS。将油状浓缩物分别加入装有100 mL 0.1 mol·LHCl溶液的锥形瓶中,(37±0.5)℃、100 r·min恒温振荡,并于5、15、30、45、60、90、120、180、240 min分别取样1 mL,不补液,用甲醇稀释并过滤,在361 nm处测定吸光度,计算其药物浓度,比较加入不同的沉淀抑制剂后提高和维持药物浓度的能力,筛选出合适的沉淀抑制剂。
2.4.2 沉淀抑制剂用量的确定 基于“2.4.1”项下试验结果,固定其他条件不变,分别加入0.5%、1%、2%、3%的Soluplus,筛选出Soluplus的用量。
2.5 MLX-S-SNEDDS的制备及载药量的测定
按优化后的处方比例称取油相、表面活性剂和助表面活性剂,磁力搅拌使其混匀置于西林瓶中,得到澄明均一的空白SNEDDS。按比例精密称取Soluplus加入到空白SNEDDS中,超声搅拌至均匀分散,使其溶解,得到澄清透明的S-SNEDDS。将过量MLX加入S-SNEDDS,涡旋充分混匀,得MLX-S-SNEDDS。于(37±0.5)℃、100 r·min恒温振荡72 h后,12 000 r·min离心10 min,取上清液,用甲醇稀释至合适倍数,过滤,361 nm处测定吸光度,计算MLX-SSNEDDS的载药量。
2.6 MLX-PC和MLX-PC-S-SNEDDS的制备工艺研究
经测定,“2.5”项下MLX-S-SNEDDS的载药量较低,因此考虑将其制成MLX-PC,以期提高载药量。磷脂是体内生物膜的主要成分,将其与药物复合形成药物-PC,可改善药物的溶解性和稳定性,提高生物利用度。采用溶剂蒸发法制备MLX-PC,精密称取MLX与适量的大豆卵磷脂于四氢呋喃中,水浴磁力搅拌一定时间,采用旋转蒸发法仪回收溶剂,真空干燥即得MLX-PC。以载药量为评价指标,对可能影响结果的药脂比、反应时间、反应温度、药物质量浓度等反应条件进行单因素考察,确定MLX-PC制备工艺。
MLX-PC-S-SNEDDS的制备及载药量的测定同“2.6”项下方法,将制得的过量MLX-PC加入至空白S-SNEDDS中,计算MLX-PC-S-SNEDDS的载药量。
MLX-PC油/水分配系数的测定采用经典摇瓶法,取适量MLX-PC,加入2 mL水相饱和的正辛醇,再分别加入18 mL正辛醇饱和的pH 7.4 PBS、pH 6.8 PBS、蒸馏水、pH 4.5醋酸盐缓冲液、pH 1.2 HCl,(37±0.5)℃、100 r·min恒温振荡72 h,平衡后将水层和正辛醇层分离开,测定正辛醇层和水层中的MLX吸光度,计算其浓度,并与MLX的logP
进行比较。2.7 三种美洛昔康自纳米乳递药系统的质量评价
2.7.1 形态与分布 分别取MLX-SNEDDS、MLX-S-SNEDDS、MLX-PC-S-SNEDDS各1 g,将其缓慢滴入(37±0.5)℃水浴的100 mL蒸馏水中,缓慢搅拌使其完全乳化。分别取少量乳液喷洒到铜网上,自然晾干,再滴加2%浓度的磷钨酸负染载药铜网,用滤纸吸去多余负染色液,风干后使用JEM-2100透射电镜观察三种制剂的形态。
2.7.2 粒径与Zeta电位的测定 同“2.8.1”项下方法操作,缓慢搅拌使其完全乳化。经微孔滤膜过滤(0.45 μm),马尔文粒度分析仪测定其粒径及Zeta电位。
2.7.3 自乳化效率 通过目测法观察自乳化体系在不同稀释倍数(50、100、200 mL蒸馏水)和不同种类分散介质(100 mL蒸馏水、pH 1.2 HCl、pH 7.4 PBS)中完全乳化所需的时间,测定乳化后乳液的粒径及PDI,以作为评价制剂自乳化效率的指标。具体操作方法如下:取MLX-SNEDDS、MLX-S-SNEDDS、MLX-PC-SSNEDDS各1 g,分别将其缓慢滴入(37±0.5)℃水浴的分散介质中,观察成乳时间,测定并记录其粒径及PDI。
2.7.4 稳定性考察
① 物理稳定性试验:分别取适量MLXSNEDDS、MLX-S-SNEDDS、MLX-PC-SSNEDDS于5 mL离心管中,12 000 r·min离心15 min,观察制剂外观是否变化,是否出现分层现象。
②冷热循环试验:分别取适量MLXSNEDDS、MLX-S-SNEDDS、MLX-PC-SSNEDDS于西林瓶中,密封避光贮存,每12 h将西林瓶交替放置于37℃和4℃的条件下,分别在0、1、5、10 d时取适量制剂,观察制剂外观是否变化,并测量其粒径和药物含量的变化情况。
③留样观察试验:分别取适量MLXSNEDDS、MLX-S-SNEDDS、MLX-PC-SSNEDDS于西林瓶中,常温避光储存,分别于0、1、3、5个月取样观察外观是否变化,测量其粒径和药物含量的变化情况。
④ 形成自纳米乳后的稳定性:同“2.7.2”项下方法操作,缓慢搅拌使其完全乳化。室温下放置48 h,观察24 h 及48 h 时自纳米乳的状态,是否出现油水分离,是否出现药物析出等现象。
2.7.5 体外溶出度的考察 取一定量的MLXSNEDDS、MLX-S-SNEDDS、MLX-PC-S-SNEDDS灌入胶囊中(相当于MLX 7.5 mg),同时取等剂量的原料药于胶囊中用作对照,按照2020年版《中国药典》桨法规定测定溶出度,以900 mL的pH 1.2 HCl、pH 7.4 PBS作为溶出介质,设定温度为(37±0.5)℃,转速为100 r·min,分别于5、15、30、45、60、90、120、180、240 min取 样5 mL,同时用等温同体积的相应介质进行补液,过滤(0.45 μm),取续滤液稀释至合适浓度测定吸光度值,并计算其累积溶出百分率。
3 结果
3.1 美洛昔康在不同辅料中的溶解度
测定MLX在不同辅料中的溶解度,结果见表 1。MLX在油相油酸和Labrafil M 1944 CS中的溶解度较其他油相中高,在表面活性剂中溶解度均较好,特别是在Tween 80、Cremophor RH40、AEO-9中,助表面活性剂中,MLX在Transcutol HP、PEG400中溶解度较大。选择对药物溶解度较好的辅料进一步利用三元相图来进行油相、表面活性剂、助表面活性剂的筛选。
表1 MLX在不同辅料中的溶解度
Tab 1 Solubility of MLX in different excipients
类别 辅料 溶解度/(mg·mL-1)油相 油酸 2.435±0.03 IPM 0.151±0.09 IPP 0.172±0.10 GTCC 0.244±0.12 Labrafil M 1944 CS 1.072±0.05表面活性剂 Tween 80 11.902±0.06 Cremophor EL35 4.423±0.15 Kolliphor ELP 1.274±0.06 AEO-9 7.194±0.12 Cremophor RH40 7.188±0.20助表面活性剂 PEG400 1.765±0.18 Transcutol HP 3.351±0.04 Ethanol 0.278±0.15 Isopropanol 0.215±0.12
3.2 三元相图绘制
3.2.1 油相的筛选 选择对药物溶解度比较好的油酸、Labrafil M 1944 CS作为油相,固定Tween 80为表面活性剂,Transcutol HP为助表面活性剂,绘制三元相图。由图1可知,当油相为Labrafil M 1944 CS时,三元相图的自乳化面积最大。

图1 油相为油酸(A)和Labrafil M 1944CS(B)的三元相图Fig 1 Tertiary phase diagrams of oleic acid(A)and Labrafil M 1944CS(B)
3.2.2 表面活性剂的筛选 选择对药物溶解度前3位的Tween 80、AEO-9、Cremophor RH40作为表面活性剂,油酸和Labrafil M 1944 CS为油相、Transcutol HP 为助表面活性剂,绘制三元相图。由图2可知,当表面活性剂为Cremophor RH40时,不论油相为油酸或Labrafil M 1944 CS,相较于其他表面活性剂,三元相图的自乳化面积最大。

图2 不同表面活性剂的三元相图Fig 2 Ternary phase diagrams of different surfactants
3.2.3 助表面活性剂的筛选 固定Cremophor RH40为表面活性剂,油酸和Labrafil M 1944 CS为油相,以Transcutol HP、PEG400为助表面活性剂,绘制三元相图并观察乳化情况。由图3可知,当油相为Labrafil M 1944 CS,表面活性剂为Cremophor RH40,助表面活性剂为Transcutol HP时,三元相图的自乳化面积最大。因此确定最终处方为Labrafil M 1944 CS、Cremophor RH40、Transcutol HP。

图3 不同助表面活性剂的三元相图Fig 3 Ternary phase diagrams of different co-surfactants
3.3 星点设计联合总评“归一值”进行多指标处方优化
3.3.1 星点设计及结果 运用星点设计进行处方优化,考察指标的水平见表 2,根据星点设计得到的处方进行试验,结果见表 3。
表2 星点设计的自变量水平
Tab 2 Level of independent variable in the central composite design
因素 水平-1.414 -1 0 +1 +1.414 X1 9.64 20 45 70 80.36 X2 0.38 1 2.5 4 4.62
表3 星点设计的试验结果
Tab 3 Central composition design
No.X1 X2 Y1/nm Y2 Y3/(mg·mL-1)1 80.36 2.50 74.64 0.51 0.77 2 9.64 2.50 17.83 0.11 4.58 3 70.00 4.00 95.28 0.23 1.41 4 45.00 0.38 196.17 0.18 2.77 5 45.00 4.62 35.03 0.06 2.98 6 45.00 2.50 35.80 0.10 2.99 7 20.00 4.00 21.31 0.05 4.83 8 45.00 2.50 35.36 0.10 2.90 9 20.00 1.00 22.02 0.06 4.09 10 70.00 1.00 99.51 0.23 1.20 11 45.00 2.50 35.53 0.08 3.97 12 45.00 2.50 35.75 0.09 4.06 13 45.00 2.50 36.85 0.10 3.31
3.3.2 归一化法综合评定 利用归一化法对数据进行标准化处理,使得每个指标均标准化为0~1之间的“归一值”,对取值越小越好的因素(粒径)和取值越大越好的因素(载药量)采用Hassan方法分别进行数学转换求“归一值”d
和d
,公式如下:d
=(Y
-Y
)/(Y
-Y
)d
=(Y
-Y
)/(Y
-Y
)选用熵值法对标准化后的效应指标进行权重计算。熵值是不确定性的一种度量,信息量越大,不确定性就越小,熵也就越小;信息量越小,不确定性越大,熵也越大。因而利用熵值携带的信息进行权重计算,结合各项指标的变异程度,利用信息熵这个工具,计算出各项指标的权重,为多指标综合评价提供依据。
使用SPSS AU进行计算。使用熵值法对Y
、Y
、Y
等3项进行权重计算,权重值分别是0.251、0.238、0.511。并且各项间的权重相对较为均匀,均在0.333附近,其中Y
权重最大。根据上述方法计算得到的标准化数据和权重系数,星点设计各响应值最后得到综合评分,综合评分(Y
)=Y
×权重系数(Y
)+Y
×权重系数(Y
)+Y
×权重系数(Y
)。结果如表4所示。表4 处方的综合评分
Tab 4 Comprehensive scores of formulations
No.X1 X2 Y1/nm Y2 Y3/(mg·mL-1) Y 1 80.36 2.50 74.64 0.51 0.77 0.17 2 9.64 2.50 17.83 0.11 4.58 0.94 3 70.00 4.00 95.28 0.23 1.41 0.37 4 45.00 0.38 196.17 0.18 2.77 0.17 5 45.00 4.62 35.03 0.06 2.98 0.74 6 45.00 2.50 35.80 0.10 2.99 0.72 7 20.00 4.00 21.31 0.05 4.83 1.00 8 45.00 2.50 35.36 0.10 2.90 0.71 9 20.00 1.00 22.02 0.06 4.09 0.90 10 70.00 1.00 99.51 0.23 1.20 0.33 11 45.00 2.50 35.53 0.08 3.97 0.85 12 45.00 2.50 35.75 0.09 4.06 0.87 13 45.00 2.50 36.85 0.10 3.31 0.75
3.3.3 数据模型拟合分析及处方优化 使用Design Expert 10.0.7软件对试验结果与考察因素进行分析,对综合评分(Y
)进行二项式拟合。经拟合回归,得到模型方程:Y
=0.78-0.29X
+0.12X
-0.015X
X
-0.076X
-0.13X
。对模型进行ANOVA分析,模型的P
值小于0.05,这说明模型参数的显著性检验通过,失拟值大于0.05,说明该方程拟合度良好。因此可表明该模型能够准确预测自纳米乳的处方最佳组成。3.3.4 处方验证 以载药量最大、粒径和PDI最小为优化目标,预测的最佳处方为:Labrafil M 1944 CS 20%,Cremophor RH40 40%,Transcutol HP 40%。预测综合评分Y
=0.997。按照优化后的处方制备MLX-SNEDDS,对预测处方进行验证,综合评分Y
=0.952,偏差值为-4.73%,表明所建拟合的模型具有较好的预测结果。3.4 沉淀抑制剂筛选
3.4.1 沉淀抑制剂种类 在MLX-SNEDDS中分别加入2%不同的沉淀抑制剂,将所制得的不同MLX-S-SNEDDS加入介质中,经稀释后形成了澄清透明,略带微蓝乳光的纳米乳液体。由图 5可知,MLX-SNEDDS中药物的质量浓度在15 min时就迅速降到了23.41 μg·mL,加入PVP K30、β
-CD、Eudragit L100、HPMC E15LV的制剂中MLX的浓度在15 min时都迅速沉降到20.00 μg·mL左右,因此可看出这些沉淀抑制剂对药物没有抑制沉淀的作用。而加入HPMC K4M、PS-630以及Soluplus的SNEDDS中MLX在60 min时的质量浓度分别为36.07、33.72、43.48 μg·mL,说明HPMC K4M、PS-630、Soluplus对MLX有不同程度的抑制沉淀作用,其中以Soluplus的效果最好。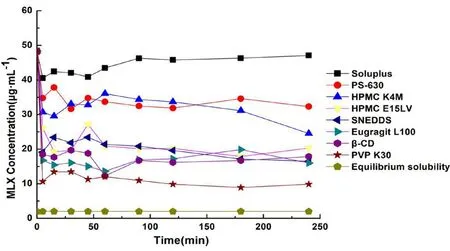
图5 不同沉淀抑制剂沉淀的效果Fig 5 Effect of different precipitation inhibitors on inhibition of preparation
3.4.2 沉淀抑制剂用量的确定 为了考察沉淀抑制剂的用量对抑制沉淀的作用的影响,对处方中的Soluplus用量进行进一步试验,结果如图6所示,Soluplus用量的变化对促过饱和作用没有明显差异,由于Soluplus在制剂中完全溶解所需时间较长,因此选择0.5%的用量。

图6 沉淀抑制剂的用量对于抑制沉淀的作用的影响Fig 6 Effect of different amounts of Soluplus on the inhibition of preparation
3.5 MLX-S-SNEDDS载药量的测定
平均载药量为4.82 mg·mL,与MLXSNEDDS一致,沉淀抑制剂能对纳米乳中的MLX有沉淀抑制作用,但并不能增加药物载药量。
由于MLX每日服用量为7.5 mg,若制成胶囊,以现在的载药量计算,则需服用约3粒500 μL的胶囊,因此应考虑提高载药量以减少服用体积,增加顺应性。考虑将MLX先制成MLX-PC,提高其脂溶性,从而提高MLX在S-SNEDDS给药系统中的载药量。
3.6 MLX-PC的制备工艺研究
3.6.1 单因素考察
① 药脂比的选择:设定药脂比(MLX和PC的质量比)为1∶3、1∶2、1∶1、2∶1,药物的质量浓度为4 mg·mL,在40℃条件下反应1 h,载药量分别为7.80、7.40、6.06、5.46 mg·mL,以载药量为评价指标,其他条件不变,药脂比为1∶3时,载药量最大。
② 反应时间的选择:设定反应时间为0.5、1、1.5、2 h,药物的质量浓度为4 mg·mL,药脂比为1∶3,在40℃条件下反应至试验设计的时间,载药量分别为6.84、6.97、7.43、5.06 mg·mL,以载药量为评价指标,其他条件不变,反应时间为1.5 h时,载药量最大。
③ 反应温度的选择:设定反应温度为25、40、50、60℃,药物的质量浓度为4 mg·mL,药脂比为1∶3,在各温度条件条件下反应1.5 h,载药量分别为7.93、8.00、8.18、7.61 mg·mL,以载药量为评价指标,其他条件不变,反应温度为50℃时,载药量最大。
④ 药物质量浓度的选择:设定药物质量浓度分别为4、6、8、10 mg·mL,药脂比为1∶3,在50℃下反应1.5 h,载药量分别为8.20、8.71、8.42、7.72 mg·mL,以载药量为评价指标,其他条件不变,当药物质量浓度为6 mg·mL时,载药量最大。
3.6.2 MLX-PC-S-SNEDDS载药量的测定MLX-PC按自纳米乳的制备方法制成MLX-PC-SSNEDDS,和MLX-S-SNEDDS相比,平均载药量从4.82 mg·mL变成了8.73 mg·mL,约提高了一倍,可以减少服用体积。
3.6.3 油/水分配系数的测定 与MLX进行对比,MLX-PC在正辛醇饱和的pH 7.4 PBS、pH 6.8 PBS、蒸馏水、pH 4.5醋酸盐缓冲液、pH 1.2 HCl中logP
分别由0.67、0.84、1.26、2.22、2.31增 大 到1.62、2.20、2.56、2.73、2.81,说 明 将MLX制备成MLX-PC后药物在油相中的溶解度变大,脂溶性增加,可预期药物在体内的吸收增加,从而提高生物利用度。3.7 制剂质量评价
3.7.1 外观与形态MLX-SNEDDS、MLX-SSNEDDS、MLX-PC-S-SNEDDS 三种制剂均为黄色透明且均一的油状液体,其中MLX-PC-SSNEDDS颜色会更深,可能是加入了磷脂的缘故。乳化后的纳米乳,乳液微粒呈类球形。
3.7.2 粒径与Zeta电位的测定 MLX-SNEDDS、MLX-S-SNEDDS、MLX-PC-S-SNEDDS的粒径分别为(18.71±1.04)、(18.30±0.48)、(23.07±0.28)nm,Zeta电位分别为(-1.44±0.11)、(-5.56±0.61)、(-7.07±0.88)mV,PDI分 别为(0.086±0.03)、(0.11±0.03)、(0.132±0.03)。MLX-SNEDDS和MLX-S-SNEDDS乳化后的微粒粒径相似,MLX-PC-S-SNEDDS粒径则有所增大。三种制剂的Zeta电位皆为负值,绝对值依次增大。
3.7.3 稳定性考察 观察MLX-SNEDDS、MLX-SSNEDDS、MLX-PC-S-SNEDDS乳化后形成的纳米乳在24 h及48 h的状态,可看出MLX-S-SNEDDS、MLX-PC-S-SNEDDS到48 h时仍然是均一、澄清透明的状态,无沉淀析出。而MLX-SNEDDS在24 h时虽然未出现油水分离现象,但已经出现略微浑浊,48 h时在烧杯底部能发现明显沉淀物。
3.7.4 自乳化效率 稀释倍数的影响:结果如表 5所示,不同稀释倍数对制剂的自乳化时间以及PDI没有显著影响,自乳化时间均小于30 s,MLXSNEDDS与MLX-S-SNEDDS自乳化后的粒径相差不大,而MLX-PC-S-SNEDDS的粒径则明显增大。
表5 不同稀释倍数对自乳化效率的影响(=3)
Tab 5 Effect of dilution multiple on self-emulsification efficiency(=3)
稀释倍数 制剂 自乳化时间/s 粒径/nm PDI 50 MLX-SNEDDS 25.99±2.8117.44±0.360.177±0.11 MLX-S-SNEDDS 26.28±3.2317.93±0.230.086±0.01 MLX-PC-S-SNEDDS26.63±0.7427.36±0.600.151±0.02 100 MLX-SNEDDS 25.54±3.1220.33±0.450.062±0.05 MLX-S-SNEDDS 26.80±2.8117.19±0.480.112±0.03 MLX-PC-S-SNEDDS27.39±1.4629.23±0.620.159±0.03 200 MLX-SNEDDS 25.29±2.4819.93±0.090.081±0.06 MLX-S-SNEDDS 24.21±3.9319.91±0.610.108±0.07 MLX-PC-S-SNEDDS26.88±2.4427.90±0.480.132±0.07
稀释介质的影响:不同稀释介质下,三种制剂的自乳化时间以及粒径分布相差不大,且自乳化时间均小于30 s,MLX-PC-S-SNEDDS乳化后的粒径大于MLX-SNEDDS与MLX-S-SNEDDS,可能是由于药物与磷脂形成了复合物的缘故。
3.7.5 物理稳定性试验 MLX-SNEDDS、MLXS-SNEDDS、MLX-PC-S-SNEDDS经过高速离心后,未观察到制剂有分层或者析出的现象,外观依然是黄色透明且均一的油状液体。
3.7.6 冷热循环试验 MLX-SNEDDS、MLX-SSNEDDS、MLX-PC-S-SNEDDS经过冷热循环后仍然为黄色透明的均一油状液。乳化后进行粒径以及药物含量的测定,结果显示,经过冷热循环后制剂的粒径、PDI以及药物含量没有明显变化,说明所制备的制剂有较好的稳定性,温度变化对制剂的影响较小。
3.7.7 留样观察试验 经过长期放置以后,制剂的外观、粒径以及PDI均无明显变化,说明制剂经过长期放置以后,稳定性良好。
3.7.8 体外溶出度的考察 结果如图7所示,在pH 1.2 HCl、pH 7.4 PBS介质中,三种制剂相比于MLX原药,均明显提高了药物的溶出速率和溶出程度。在体外溶出结果中,三种制剂的溶出行为并没有显著区别,但在pH 7.4 PBS中三种制剂的累积溶出百分率大于在pH 1.2 HCl中的。这是由于MLX本身的理化性质决定的,在pH 7.4 PBS中溶解度大于pH 1.2 HCl。

图7 三种制剂在pH 1.2 HCl(A)和pH 7.4 PBS(B)中的体外溶出曲线Fig 7 In vitro dissolution curve of the three preparations in pH 1.2 HCl(A)and pH 7.4 PBS(B)
4 讨论
促过饱和物质的筛选试验证明,对MLX起抑制沉淀作用的沉淀抑制剂有HPMC K4M、PS-630、Soluplus,HPMC可以与MLX上的羟基形成氢键作用,但由试验结果可知HPMC E15LV对MLX没有明显的沉淀抑制作用,说明氢键并不是HPMC K4M抑制药物的晶核长大的主要原因。据有关文献报道,分子量及黏度大小对沉淀抑制剂抑制药物沉淀的作用有关,对HPMC来说,分子量越高,黏度越大,这可能对药物晶体的成核以及长大形成了更多的空间位阻,从而起到抑制药物沉淀的作用,而HPMC K4M的分子量及黏度均远大于HPMC E15LV,这可能是HPMC K4M能对MLX起到沉淀抑制作用的主要原因。
PS-630是乙烯吡咯烷酮和乙烯醋酸酯的共聚物,相比于PVP,由于加入了醋酸乙烯酯基团,PS-630增加了疏水性,而疏水性可以使PS-630能够对药物的晶体表面的吸附作用更强,从而达到抑制药物沉淀的作用。这可能是PS-630相比于PVP K30具有更好的抑制沉淀作用的原因。
Soluplus是聚乙烯醇己内酰胺-聚乙烯醇-聚乙二醇接枝共聚物,其结构中既具有作为其主链的亲水性的PEG 6000,又具有侧链中疏水的乙酸乙烯醋与乙烯基己内酞,因此Soluplus具有两亲性,属于一种非离子表面活性剂,可能与MLX-SSNEDDS中的起乳化作用的表面活性剂Cremophor RH40形成了混合胶束,从而抑制药物晶体的聚集及晶核的长大,达到抑制药物沉淀的效果。
自乳化后所形成的纳米乳粒径以及Zeta电位是影响自纳米乳化体系稳定性的重要因素,且粒径大小同时也对溶出速率有影响。可以看出三种制剂的粒径较小,均小于30 nm,纳米乳微粒分散均匀,PDI均小于0.200。粒径越小,所形成的纳米乳油水界面面积越大,乳滴粒子的表面自由能越大,这时就有降低界面自由能的趋势,驱使小乳滴聚集形成大乳滴,通过降低比表面积来减少总油水界面面积。纳米乳微粒带电荷后,由于带有同种电荷,乳滴间会产生静电斥力,Zeta电位绝对值越大,则静电斥力越强,可以阻止乳滴间的聚集引起沉降,对增强体系稳定性有很大意义。同时,根据Stokes方程,粒径越小,沉降速度越小,越有利于自纳米乳乳化后体系的稳定。此三种因素使纳米乳成为动力学稳定系统。MLXSNEDDS、MLX-S-SNEDDS、MLX-PC-S-SNEDDS乳化后的Zeta电位均为负值,绝对值依次增大。虽数值均较小,但对制剂形成自纳米乳后的稳定性进行考察,发现只有MLX-SNEDDS在乳化后24 h时出现略微浑浊,48 h时在烧杯底部能发现明显沉淀物。可能是由于其Zeta电位绝对值较低,乳滴间斥力不足以与降低表面自由能的趋势相平衡,因此MLX-SNEDDS制剂稳定性不够好。
体外溶出试验证明在不同pH值的介质中,MLX-SNEDDS、MLX-S-SNEDDS、MLX-PC-SSNEDDS均能显著提高MLX的溶出度。在pH 7.4 PBS溶出曲线中,MLX-SNEDDS在40 min时累积溶出百分率开始下降,这可能是由于制剂在pH 7.4 PBS迅速乳化几乎完全溶出后,乳滴粒子附近药物浓度迅速升高,导致部分药物结晶析出,表现为溶出度降低。MLX-SNEDDS乳化后Zeta电位绝对值仅为1.44,体系稳定性不够,微粒容易聚集沉降,且MLX在水中几乎不溶,可以预见在胃肠道内被大量稀释后,表面活性剂与助表面活性剂对药物的增溶能力大大下降,容易形成沉淀。而MLX-S-SNEDDS、MLX-PC-SSNEDDS 中加入了沉淀抑制剂,同时Soluplus的两亲性质可能对MLX有一定增溶作用,能在一定程度下维持过饱和状态,提高了稳定性。
此外,载药量方面相较MLX-S-SNEDDS的4.82 mg·mL,MLX-PC-S-SNEDDS载药量为8.73 mg·mL,结合磷脂本身的性质使得药物制成PC后容易穿过细胞膜,MLX-PC-S-SNEDDS在提高生物利用度上更有潜力。

