Mn含量对Al-Zn-Sn-Ga-Mn铝合金阳极电化学性能的影响*
高思睿,杨炳林,贾志明,王月莹,何立子
(1. 东北大学 材料电磁加工重点实验室,沈阳 110819;2. 东北大学 材料科学与工程学院,沈阳 110819)
0 引 言
随着人类社会发展和经济水平的提高,人类对能源的需求量也日益增加,但传统化石能源的形成往往需要经历漫长的过程,面对愈加增长的能源需求,日渐枯竭的传统能源及其所引发的环境污染难以满足人类长期持续发展[1]。而铝空气电池作为新兴的新能源,由其于比能量高、资源丰富、绿色环保等优点受到人们广泛的关注,具有良好的发展前景[2-4]。铝空气电池的理论比能量可达8.1 Wh/g,在常见金属中仅次于锂的13.3 Wh/g[5-7],同时与氢气,甲醇等其他用于燃料电池的燃料相比,金属具有较高的体积能量密度,更适用于体积能量密度备受重视的电动车领域[8-9]。
铝空气电池中的铝阳极在碱性电解液中主要存在下列两个问题:(1)阳极表面钝化膜的形成会降低表面电化学活性,使得铝阳极的腐蚀电位低于理论的腐蚀电位值[10-11];(2)铝阳极材料中的铜、铁、硅等微量元素会加重铝的自腐蚀,发生严重的析氢腐蚀,使得阳极利用率降低[12-15]。为了缓解以上两个问题所带来的不利影响,对铝阳极材料合金化是最常用、最有效的方法之一。近几年,研究者们研究了多种元素对铝阳极性能的影响[16-17]。在铝阳极材料中添加Mn元素,可以与其中的杂质Fe元素形成FeMnAl6相,降低铝阳极中Fe元素对其耐腐蚀性带来的不利影响,同时弥散细小的FeMnAl6相起到钉扎晶界的作用,阻碍晶粒长大从而细化晶粒[19-20]。且在大多数状况下,晶粒细化可以得到细小的枝晶,进而促进阳极表面均匀溶解,改善腐蚀均匀性[21-22]。但以往的研究多以高纯铝为基体金属,且对于不同的合金体系,Mn的含量也有所差别。本文以99.7%的工业铝为基体金属,以Al-Zn-Sn-Ga为基础合金,分别加入不同含量的Mn元素,制备不同种类的新型合金,分析Mn对铝阳极材料电化学性能的影响,并进一步研究不同摩尔浓度的电解液对铝合金阳极性能的影响。
1 实 验
1.1 实验材料
本实验设计了5种合金,具体成分如表1所示。实验合金原料为99.7%的工业铝锭,锌粒,Al-Mn中间合金、Ga粒和Sn粒。除铝锭外,纯度均在99.99%以上,99.7%的工业铝中主要杂质如表2所示。熔炼过程:按照合金配比,利用电子天平称量好备用,待将熔炼所需工具烘干后,将铝块放入中频炉中,铝块熔化后,加入合金元素,在720 ℃保温5 min后,将合金液搅拌均匀、扒渣,浇注在水冷铜模中冷却至室温。再将熔炼所得合金进行固溶处理,其中固溶温度和时间分别为540 ℃和4 h,冷却方式为水淬。将固溶处理后得到的铝合金去除表面氧化层后,轧制成5 mm板材。
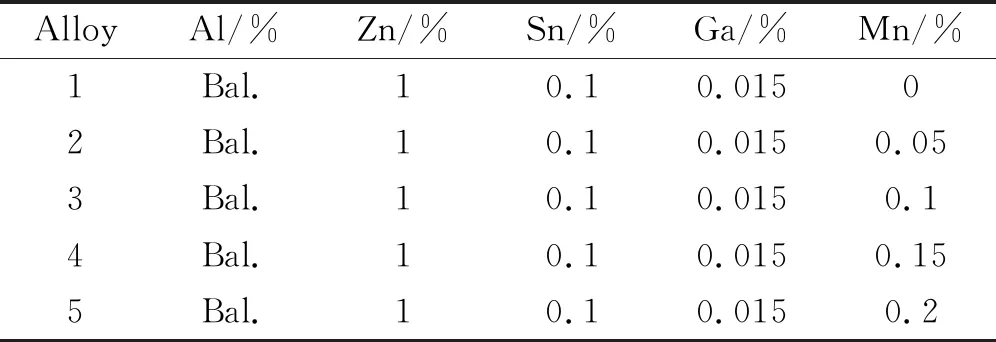
表1 Al-Zn-Sn-Ga-xMn 合金的成分(质量分数%)
1.2 实验方法
铝阳极合金的析氢速率测试是在恒温水浴的条件下进行的,水浴温度为25 ℃,利用排水集气法计算析氢量。电解液为4/6 mol/L KOH溶液,反应时间为1 h。自腐蚀速率测试是在室温(25 ℃)下进行的,利用失重法得到反应时间前后合金质量的差值后,算得出自腐蚀速率。电解液为4/6 mol/L KOH溶液,反应时间为4 h。使用上海辰华公司的 CHI660E 型电化学工作站对铝阳极合金进行开路电位、极化曲线的测试,测试所用电解液为 25 ℃ 恒温水浴下的 4/6 mol /L KOH 溶液,试样大小为 10 mm×10 mm×5 mm,一端引出铜导线,用义齿基托树脂密封,留出工作面1 cm2。实验为三电极测试系统,Pt片为辅助电极,汞/氧化汞(Hg /HgO) 电极为参比电极; 其中开路电位测试时间为 3600 s; 极化曲线电位为-1.7~-1.3 V,扫描速度为1 mV/s。铝阳极合金的恒流放电和I-V曲线采用 CT3001H 型蓝电电池测试系统进行测试,其中恒流放电的电流密度为 100 mA·cm-2,测试时间为3600 s。
2 结果分析
2.1 析氢速率及自腐蚀速率
图1与为不同Mn含量的Al-1Zn-0.1Sn-0.015Ga-xMn合金在4 mol/L KOH溶液中的析氢速率及自腐蚀速率曲线。由合金析氢速率曲线可知,未添加Mn时,合金的析氢速率和自腐蚀速率分别为0.40 mL·cm-2·min-1与0.29 mg·cm-2·min-1,添加Mn元素后,铝阳极合金的析氢速率与自腐蚀均呈增大而后又下降的趋势。究其原因是当Mn添加较少时,会优先与铝、锡等元素形成第二相,第二相与附近的铝基体形成腐蚀微电池,增加了析氢活性点,导致合金的析氢速率增大。此外,晶粒细化使得晶界总面积增加,也会导致析氢速率增大。而当Mn的添加量达到一定数目后,Mn会和工业铝中的杂质Fe形成FeMnAl6相,它与基体铝性质相近,减小了合金局部的微电偶腐蚀,降低了合金的析氢速率。在含Mn的四种合金中,Mn含量为0.2%(质量分数)的合金析氢速率与自腐蚀速率最小,为0.35 mL·cm-2·min-1与0.23 mg·cm-2·min-1。
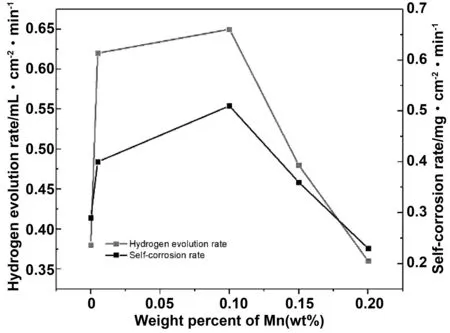
图1 Al-1Zn-0.1Sn-0.015Ga-xMn合金在4M KOH溶液中析氢速率及自腐蚀曲线
图2为不同Mn含量的Al-1Zn-0.1Sn-0.015Ga-xMn合金在6mol/L KOH溶液中的析氢速率与自腐蚀曲线。由析氢速率曲线与自腐蚀曲线可知,未添加Mn时,合金的析氢速率与自腐蚀速率分别为0.70 mL·cm-2·min-1与0.43 mg·cm-2·min-1。与4 mol/L相比,析氢速率大幅增加,其原因在于KOH浓度增加后,单位体积内离子的个数也随之增加,使得反应速率增加,导致析氢更加严重。在含Mn的四种合金中,Mn含量为0.2%(质量分数)的合金析氢速率及自腐蚀速率均为最小,分别为0.64 mL·cm-2·min-1及0.37mg·cm-2·min-1。
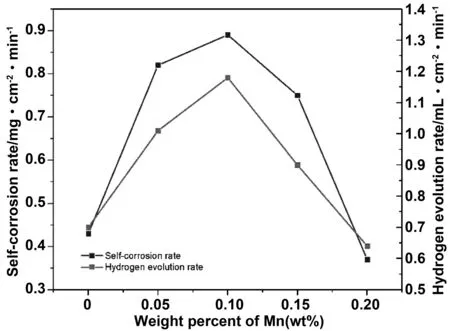
图2 Al-1Zn-0.1Sn-0.015Ga-xMn合金在 6mol/L KOH 溶液中析氢速率与自腐蚀速率曲线
2.2 开路电位
如图3为不同Mn含量的Al-1Zn-0.1Sn-0.015Ga-xMn合金在4 mol/L KOH溶液中的开路电位—时间曲线。由图3可知,添加Mn元素之后,铝阳极合金的开路电位均发生不同程度的负移,其中添加了0.1%(质量分数) Mn的铝阳极合金负移最大,负移了40 mV(Al-1Zn-0.1Sn-0.015Ga合金开路电位-1.45 V; Al-1Zn-0.1Sn-0.015Ga-0.1Mn合金开路电位-1.49 V) 。其原因在于,添加Mn元素后,合金的析出相增多,铝阳极合金的活化能力增强,开路电位负移。这与析氢及自腐蚀速率测试相对应。
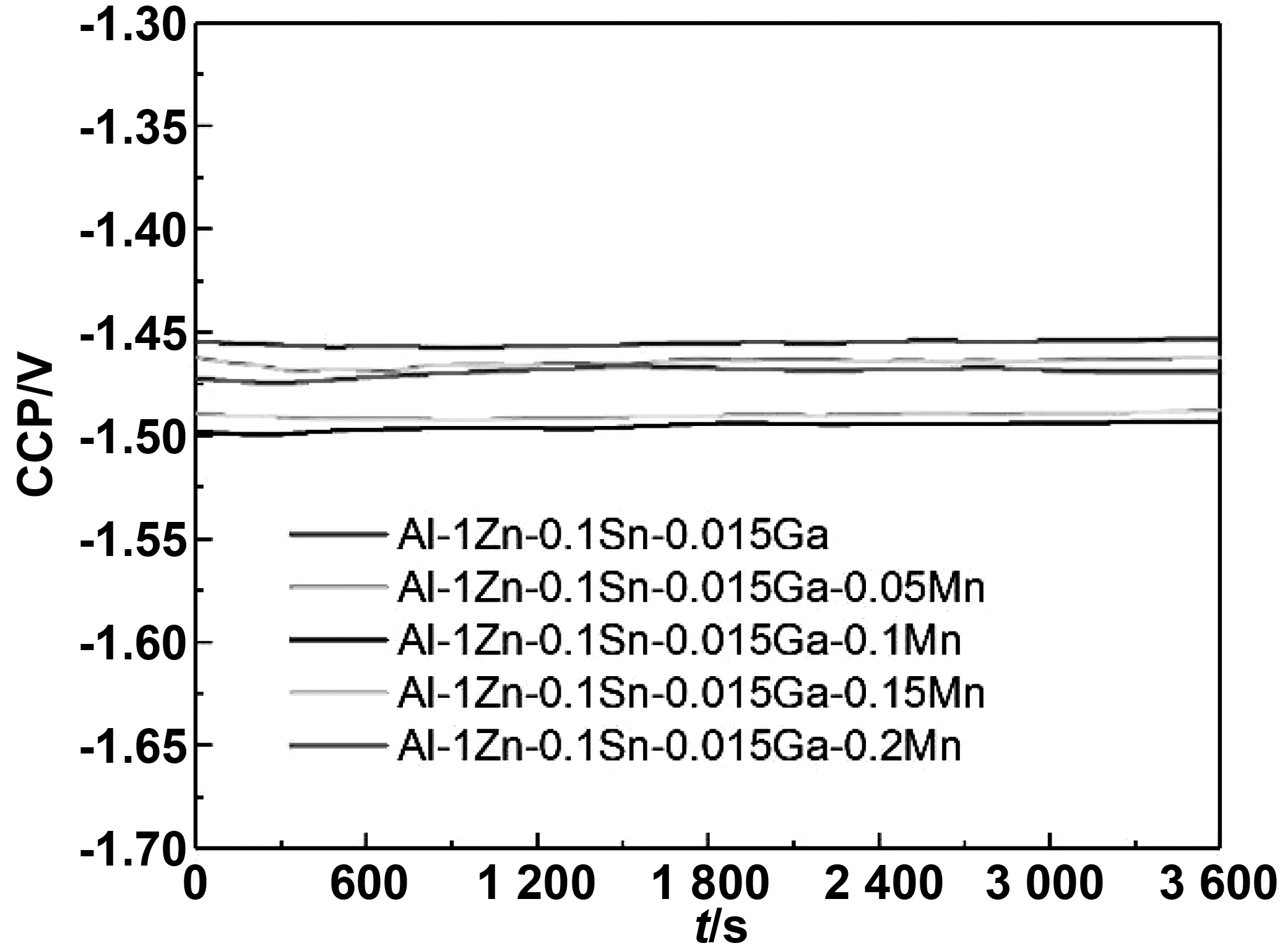
图3 Al-1Zn-0.1Sn-0.015Ga-xMn合金在 4 mol/L KOH 溶液中的开路电位-时间曲线
如图4为不同Mn含量的Al-1Zn-0.1Sn-0.015Ga-xMn合金在6 mol/L KOH溶液中的开路电位-时间曲线。开路电位的变化趋势与图3相同,其中添加了0.1%(质量分数) Mn的铝阳极合金负移最大,负移了50 mV(Al-1Zn-0.1Sn-0.015Ga合金开路电位-1.46 V; Al-1Zn-0.1Sn-0.015Ga-0.1Mn合金开路电位-1.51 V) 。同时,与图3相比,铝阳极合金的开路电位整体负移了约20 mV。
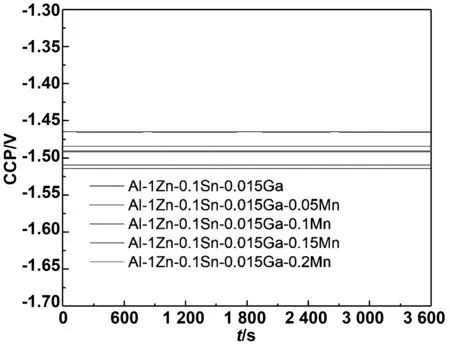
图4 Al-1Zn-0.1Sn-0.015Ga-xMn合金在 6 mol/L KOH 溶液中的开路电位-时间曲线
2.3 极化曲线
图5为不同Mn含量的Al-1Zn-0.1Sn-0.015Ga-xMn合金在4 mol/L KOH溶液中的极化曲线。表3为根据过 Tafel 外推法[23-24]计算得出的合金腐蚀参数: 自腐蚀电位(Ecorr) 、自腐蚀电流密度(Icorr) 和极化电阻(Rp)。通过图表可知,添加Mn元素后,合金的自腐蚀电位(Ecorr)均发生了负移,阳极合金的电极反应阻力有所减小。且当Mn的添加量达到0.1%(质量分数)时合金的腐蚀电位(Ecorr)达到最负为-1.498 V,说明该合金活性很高,但同时,自腐蚀电流密度(Icorr)明显增大,达到25.81 mA·cm-2,同时极化电阻(Rp)显著减小,为2.1 Ω·cm-2,合金的耐蚀性变差。不过随着Mn含量的增加,自腐蚀电流密度(Icorr)有所下降,极化电阻(Rp)也有了明显的提高,合金耐蚀性得到了相应的提升。与图1中的析氢速率与自腐蚀速率测试结果相一致。

图5 Al-1Zn-0.1Sn-0.015Ga-xMn合金在 4 mol/L KOH 溶液中的极化曲线

表3 Al-1Zn-0.1Sn-0.015Ga-xMn合金在 4 mol/L KOH 溶液中的电化学参数
图6为不同Mn含量的Al-1Zn-0.1Sn-0.015Ga-xMn合金在6 mol/L KOH溶液中的极化曲线。表4为根据过 Tafel 外推法计算得出的合金腐蚀参数。通过对比表3与表4可知,增加电解液的摩尔浓度后,5种铝阳极合金的自腐蚀电位(Ecorr)均发生了一定程度上的负移,表明铝阳极合金得到进一步活化,同时阳极合金的电极反应阻力减小,自腐蚀速率有所增大,耐蚀性能变差,与析氢和自腐蚀测试相对应。当Mn的添加量为0.1%(质量分数)时,铝阳极合金自腐蚀电位(Ecorr)达到最负为-1.513 V。

表4 Al-1Zn-0.1Sn-0.015Ga-xMn合金在 6 mol/L KOH 溶液中的电化学参数

图6 Al-1Zn-0.1Sn-0.015Ga-xMn合金在 6 mol/L KOH 溶液中的极化曲线
2.4 电池放电性能测试
图7是电流密度为100 mA·cm-2时,Al-1Zn-0.1Sn-0.015Ga-xMn合金在4 mol/L KOH溶液中的恒流放电曲线,图8为各合金的I-V曲线。可以看出,不添加Mn时,Al-1Zn-0.1Sn-0.015Ga合金稳定放电电压约为0.505V(vs Hg/HgO);添加Mn后,铝阳极合金的放电电压有所提高。Mn含量为0.15%和0.2%(质量分数)时,合金的工作电压分别达到0.575和0.553 V(vs Hg/HgO),Mn含量为0.1%(质量分数)时,放电电压最高,达到了0.618 V(vs Hg/HgO)。

图7 Al-1Zn-0.1Sn-0.015Ga-xMn合金在 4 mol/L KOH 溶液中的恒流放电曲线
通过图8铝阳极合金的I-V曲线可知加0.1%(质量分数) Mn时,铝阳极合金最大功率密度可达83.1 mW· cm-2,高于不添加Mn的75.7 mW·cm-2。使其在供电过程中能够提供更大的功率,以达到实际应用的目的。
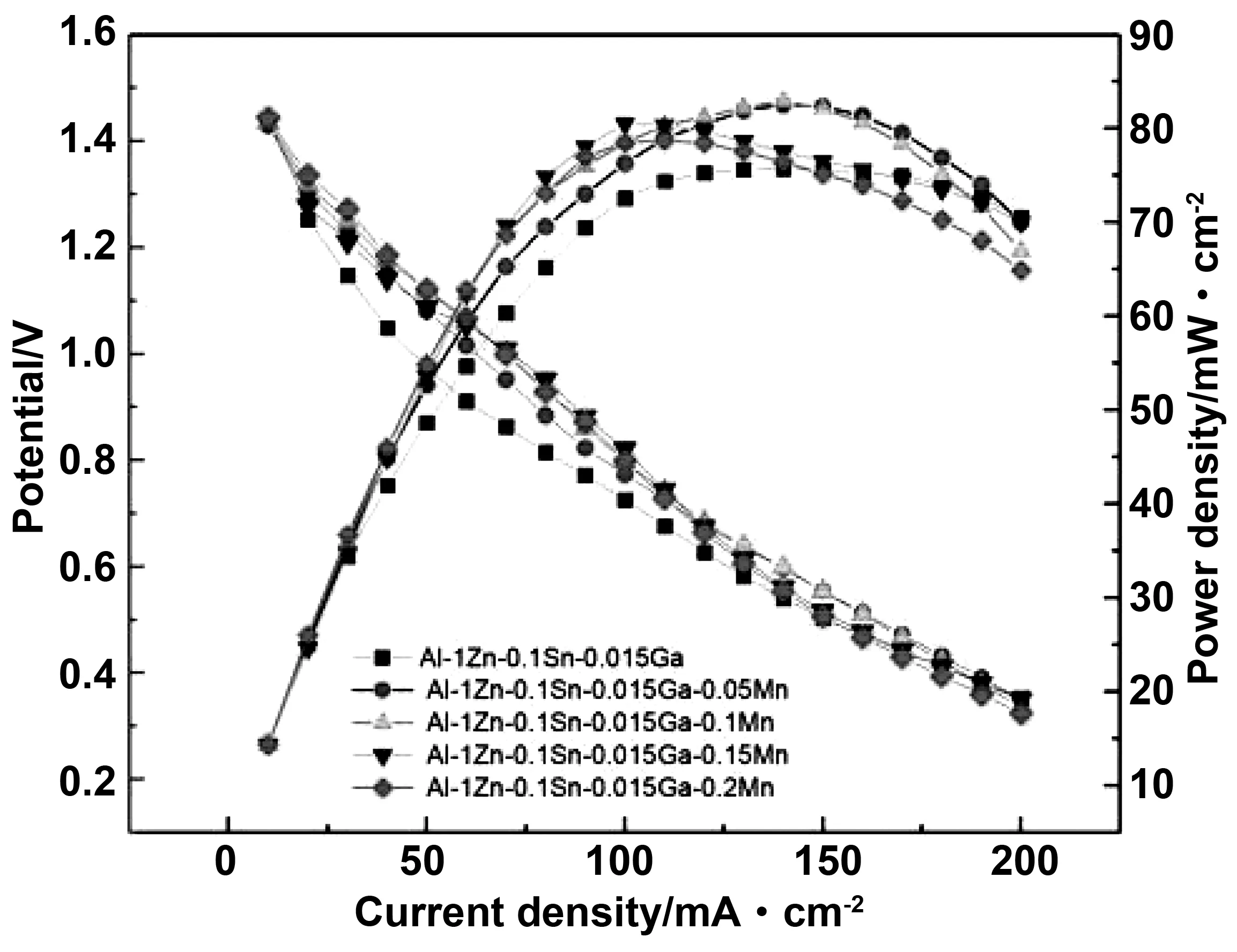
图8 Al-1Zn-0.1Sn-0.015Ga-xMn合金在 4 mol/L KOH 溶液中的I-V曲线
图9是电流密度为图100 mA·cm-2时,Al-1Zn-0.1Sn-0.015Ga-xMn合金在6 mol/L KOH溶液中的恒流放电曲线,图10为各合金的I-V曲线。可以看出,未添加Mn时,Al-1Zn-0.1Sn-0.015Ga合金稳定放电电压约为0.858V(vs Hg/HgO);添加Mn后,铝阳极合金的放电性能有所提高,放电电压均有所提高。当Mn的添加量为0.15%和0.2%(质量分数)时,铝阳极合金的工作电压分别达到了0.896和0.887 V(vs Hg/HgO)。当Mn的含量为0.1%(质量分数)时,放压最高最负,达到0.931 V(vs Hg/HgO)。相对应的,放电电压相对其他铝阳极合金放电曲线,其曲线波动较大,放电曲线变的不稳定。通过合金的I-V曲线可知,加0.1%(质量分数)Mn的合金最大功率密度可达104.6 mW·cm-2,高于不添加Mn的83.2 mW·cm-2。

图9 Al-1Zn-0.1Sn-0.015Ga-xMn合金在 6 mol/L KOH 溶液中的恒流放电曲线

图10 Al-1Zn-0.1Sn-0.015Ga-xMn合金在 6 mol/L KOH 溶液中的I-V曲线
表 5 为根据I-V曲线所得到的最大功率密度及阳极合金在 100 mA·cm-2恒流下放电的阳极利用率。由表可知当电解液浓度6 mol/L 时,此时铝阳极材料的最大功率密度普遍最高,且阳极利用率下降幅度较小。添加0.1%(质量分数)的Mn时,最大功率密度为104.6 mW·cm-2。但此时的阳极利用率较低,仅为71.9%。考虑到铝阳极材料的综合性能,Mn的添加量选择为0.2%(质量分数),电解液浓度选择为6 mol/L。
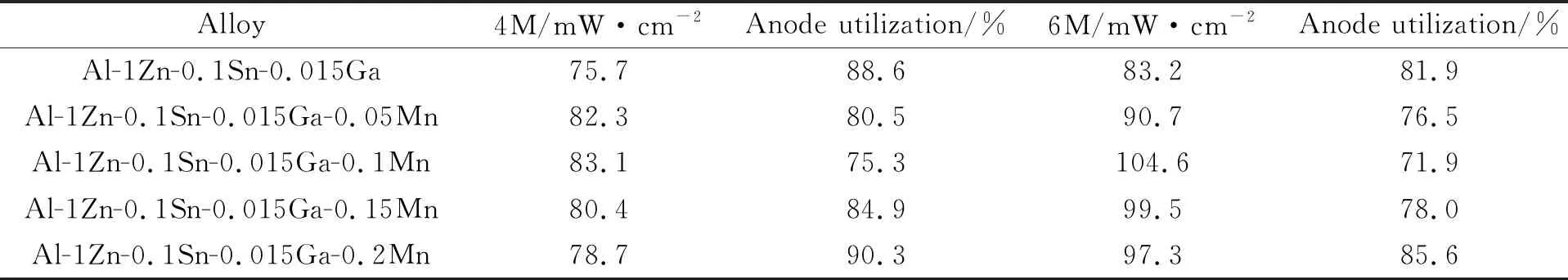
表5 Al-1Zn-0.1Sn-0.015Ga-xMn合金最大功率密度及阳极利用率
3 结 论
(1) 添加Mn元素后,Al-Zn-Sn-Ga系合金的析氢速率、自腐蚀电位以及工作电位都得到了极大的改善,在抑制析氢反应的同时,使得铝阳极的电化学性能大幅度提升。
(2) 当电解液浓度为6 mol/L时,最大工作电位(0.931 V)明显优于电解液浓度为4 mol/L(0.618 V),且此时阳极利用率仅下降5%左右,因此,Al-Zn-Sn-Ga系合金适宜的电解液浓度为6 mol/L。
(3) 当Mn的添加量为0.2 %(质量分数)时,Al-Mg-Ga-Sn-Mn合金具有良好的综合性能; 其开路电位和工作电位分别为-1.491 V(vs.Hg /HgO)和0.88 V,析氢速率最小,仅有0.64 mL·cm-2·min-1。

