Cu@Co 双核MOFs 衍生碳材料用于黄芩素的电化学传感分析
鲁猷栾,穆新伟,刘耀鹏,石 震,郑 寅†,黄文胜
1. 湖北民族大学超轻弹性体材料绿色制造民委重点实验室,湖北 恩施445000;2. 湖北民族大学化学与环境工程学院,湖北恩施445000
0 引 言
黄芩素(baicalein,BA)是一种常见的黄酮类物质,已在临床试验中表现出抗菌、抗炎、改善脑血循环及抗血小板凝集的作用,但摄入量过多时也会损伤机体[1~3]。已报道的用于BA 定量分析的方法有毛细管电泳法[4]、薄层色谱法[5]、紫外分光光度法[6]和高效液相色谱法[7]等,这些方法或需要复杂的预处理过程,或需要昂贵的仪器,或需要较长的检出时间,因而在实际使用中屡屡受限。相比之下,电化学传感具有操作简单、耗费少、响应快及可实时检测等优点,更适用于BA 的定量分析。
金属有机框架(metal organic frameworks,MOFs)材料因孔隙率高、结构和功能性多样等优点在吸附、储能、传感等领域得到广泛研究[8~11]。在电化学传感过程中,MOFs 的金属中心离子可通过提供丰富的活性位点来增加电极与待测物间的亲和力,因此可赋予电化学传感器较高的灵敏度[12,13]。但是,由于MOFs 的导电性不太理想,不适合直接用于构筑电化学传感器。为提高其导电效果,一般会将MOFs 用作前驱体来制备多孔碳材料[14]或金属氧化物材料[15]。MOFs 的金属氧化物可同时保留前驱体的形貌和金属中心离子,而相比于单核MOFs,双核MOFs 的金属氧化物中双金属离子间可在电化学传感过程产生协同作用,形成的局部“电容器”效应能够进一步增强材料的电导率,因而更 适 用 于 电 化 学 传 感 领 域[16,17]。目 前,将 双 核MOFs 的金属氧化物应用于电化学传感器的研究较为少见,而基于双核MOFs 金属氧化物测定BA 的电化学传感器未见报道。
纳米CoO 对有机物分子具有良好的亲和力[18],而纳米Cu 具有良好的导电效果[19],因此将两者联合运用可有效增敏电化学传感器。本文以Cu 盐和Co 盐为金属源,通过水热法合成了Cu@Co 双核MOFs,并以此为前驱体经热解法制备了一类Cu@C@CoO 材料,然后分别将其修饰到玻碳电极表面,通过电化学交流阻抗技术(EIS)、循环伏安法(CV)、微分脉冲伏安法(DPV)等方法比较了它们的电化学性能,通过优化BA 的检测条件,实现了实际样品中BA 的检测。
1 实验部分
1.1 仪器与试剂
仪器:CHI 660E 型电化学分析仪(三电极体系中的工作电极为玻碳电极(GCE,直径3 mm),对电极为铂片电极,参比电极为饱和Hg/Hg2Cl2电极(SCE),上海辰华公司);GWL-1600 型管式炉(南京南大仪器厂);Quanta FEG250 型扫描电子显微镜(SEM,FEI 公司);XRD-7000 型X 射线衍射仪(XRD,Shimadzu 公司);ESCALAB 250Xi 型X 射线光电子能谱分析仪(XPS,赛默飞世尔科技有限公司);LabRAM HR800 型激光共聚焦拉曼光谱仪(Raman,HORIBA Jobin Yvon 公司);热重分析仪(TGA,SII 公司);Autosorb iQ 型全自动比表面和孔径分析仪(Quantachrome 公司)。
试剂:Co(NO3)2·6H2O、Cu(NO3)2·3H2O、1,3,5-均苯三甲酸(TMA)、乙二醇(EG)、N,N-二甲基甲酰胺(DMF)、聚乙烯吡咯烷酮(PTA,平均分子质量44 000~54 000)为化学纯,黄芩素(BA)为分析纯,均购自上海阿拉丁生化科技股份有限公司;磷酸盐缓冲液(PBS)由0.1 mol/L 的Na2HPO4和KH2PO4混合配制;铁氰化钾溶液(PFS)由Fe[(CN)6]3-/4-和KCl 混合配制,其浓度分别为0.005 mol/L 和0.100 mol/L;所有溶液均由去离子水配制。
1.2 材料制备
在DMF 与EG 体积比为1∶1 的50 mL 混合溶液中 加 入2.5 g Co(NO3)2·6H2O、2.5 g Cu(NO3)2·3H2O、1.5 g TMA、1.0 g PTA,搅 拌 均 匀 后 在150 ℃条件下水热反应10 h,得到的固体物用乙醇和去离子水分别洗涤3 次,然后在60 ℃下干燥,获得前驱体双核MOFs。将双核MOFs 置于管式炉中,分别在N2氛围下以2 ℃/min 的速率升至400、500、600 ℃并维持1 h,然后自然冷却至室温。将得到的MOFs 衍生碳材料分别命名为Cu@C@CoO-400、Cu@C@CoO-500 和Cu@C@CoO-600。
1.3 修饰电极的制备
用0.05 μm 的Al2O3匀浆抛光GCE 后,再 分 别将其浸入乙醇和去离子水超声30 s,晾干。取10 mg 不同热解温度制备的MOFs 衍生碳材料于10 mL DMF 溶液中,超声3 h 制成分散液,然后取5 μL分散液滴涂在电极表面,于红外灯下干燥,根据热解温度的不同分别记为Cu@C@CoO-400/GCE、Cu@C@CoO-500/GCE与Cu@C@CoO-600/GCE。图1 为修饰电极的制备流程与BA 的反应机理图。
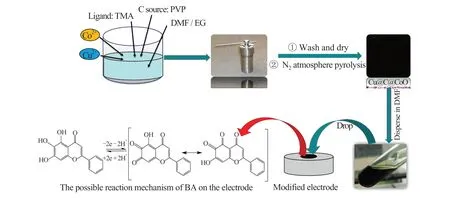
图1 修饰电极的制备流程及其与BA 的反应机理图Fig.1 Flow chart of preparation and reaction mechanism with BA of the modified electrode
1.4 电化学测试
采用电化学阻抗(EIS)研究电极的电化学性能时,支撑电解质为PFS 溶液,脉冲频率范围为0.01 Hz~100 kHz,脉冲振幅为5 mV;采用循环伏安法(CV)研究电极的电化学性能时,支撑电解质为pH 7.0 的PBS 溶液,扫描速率为100 mV/s,扫描范围为-0.2~0.6 V。
采用CV 法和差分脉冲伏安法(DPV)研究BA的电化学行为时,支撑电解质均为含1×10-6mol/L BA 的PBS 溶液(pH 2.0),CV 的 扫 描 速 率 为100 mV/s,扫描范围为0.2~0.8 V;DPV 的富集电位为0 V,富集时间为150 s,脉冲振幅为50 mV,脉冲宽度为50 ms,扫描速率为50 mV/s,扫描范围为0.2~0.6 V。
所有电化学测试都是在三电极体系的CHI 660E 电化学工作站进行的。
2 结果与分析
2.1 材料表征
图2(a)、(b)和(c)分别 为Cu@C@CoO-400、Cu@C@CoO-500 和Cu@C@CoO-600 的 扫 描 电 镜(SEM)图。可以看出,金属的纳米颗粒被三维互连的碳壳材料紧密包围,且随着热解温度的增加,碳壳材料明显减少。
本文根据光伏逆变器的特点,利用关键器件TMS320F240、SG3525、ICL8038,进行逆变器的研究和设计.该系统的基本功能比较完善,成本较低,开发周期较短,适合于市场推广.
图2(d)(e)(f)分别为不同热解材料的透射电镜(TEM)图。可以看出,较高温度下制备的热解材料内部纳米Cu 和纳米CoO 颗粒的间距明显较大(图2(f)),同时粒径变大且分布更加均一。这主要归因于高温条件下PTA 和配体等成分的进一步碳化分解,同时由于双核MOFs 的热解程度加剧,生成的还原Cu 与CoO 也越来越多,并随着碳层逐渐减少而变得均匀。

图2 各碳材料的SEM 图(a)~(c)及对应的TEM 图(d)~(f)Fig.2 SEM images (a)-(c)and TEM images (d)-(f)of the carbon materials
图3 为前驱体Cu@C@CoO 的TGA 曲线。可以看出,在350 ℃之前该材料比较稳定,失重率为12.06%,失重部分主要为材料内部残存的部分溶剂;从350 ℃到600 ℃,材料失重比例急剧增加,失重率达到58.45%,这是由于PTA 和有机配体等的热解[17],在600 ℃以后,材料中的PTA 和有机配体等基本碳化完全,形成了稳定的碳层结构,而纳米金属的形态稳定,因此残余质量基本不变。
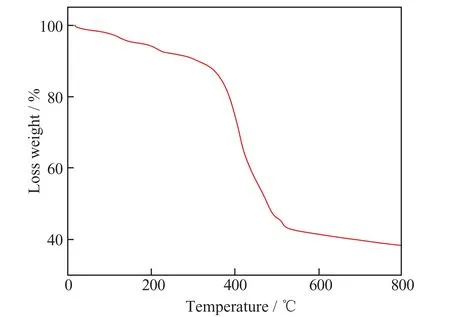
图3 Cu@C@CoO 的TGA 曲 线Fig.3 The TGA curves of Cu@C@CoO
图4 为各碳材料的Raman 光谱。Raman 光谱中D 峰(273.10 cm-1)强度ID与G 峰(661.20 cm-1)强度IG的比值可反映材料的石墨化程度,该值越低则材料的石墨化程度越高[20]。经计算,Cu@C@CoO-400、Cu@C@CoO-500 和Cu@C@CoO-600 的ID/IG分别为1.55、1.19 和1.07,说明在较高热解温度下制备的Cu@C@CoO-600 石墨化程度最高。

图4 各碳材料的Raman 光谱Fig.4 Raman spectra of the carbon materials
各碳材料的XRD 图谱如图5 所示。其中,22°左右出现的特征峰对应为无定形碳的(002)晶面;42.8°、50.2°和73.2°处衍射峰分别对应于Cu 的(111)、(200)和(220)晶面,表明该材料中的纳米Cu为典型的面心立方结构;36.5°、43.2°、62.5°和76.5°出现的衍射分别对应于CoO 的(111)、(200)、(220)和(222)晶面,表明该材料中的CoO 同样为典型的面心立方结构[21]。

图5 各碳材料的XRD 图Fig.5 XRD spectra of the carbon materials
以Cu@C@CoO-600 为例研究了碳材料的XPS谱图,分析材料中各元素的化学环境。图6(a)为XPS 总谱图,结合能在285、532、780 eV 和932 eV处的分峰分别归属于C 1s、O 1s、Co 2p 和Cu 2p;图6(b)为C 1s 的拟合峰,其在284.3 eV 和288.3 eV处的分峰分别对应于C=C 和C=O 键,285.5 eV处分峰对应于碳的石墨形态(HOPG);图6(c)为O 1s 的拟合峰,显示了该材料中O 的3 种形态,其在529.0、530.5 和531.6 eV 处的分峰分别归属于O—Co、O—H 和O—C 键;图6(d)为Co 2p 的拟合峰,Co 元素呈现3种价态,780.0 eV 处对应Co 2p3/2,785.5 eV 处 对 应CoO,795.8 eV 处 对 应Co 2p1/2,802.0 eV 处的分峰为Co 的卫星峰(Sat);图6(e)为Cu 2p 的拟合峰,表明该材料中的Cu 以游离态存在,在931.6、933.5、951.5 eV 和953.6 eV 处的分峰分 别 归 属 于CuCl(Co(NO3)2·6H2O 和Cu(NO3)2·3H2O 杂质成分中的Cl)、Cu 2p3/2、Cu 2p1和Cu 2p1/2,939.9 和942.9 eV 处的结合能分峰归属于Cu 2p3/2的卫星峰(Sat)。以上结果说明,Cu 和Co 在碳材料中是以纳米Cu 及纳米CoO 的形态存在。
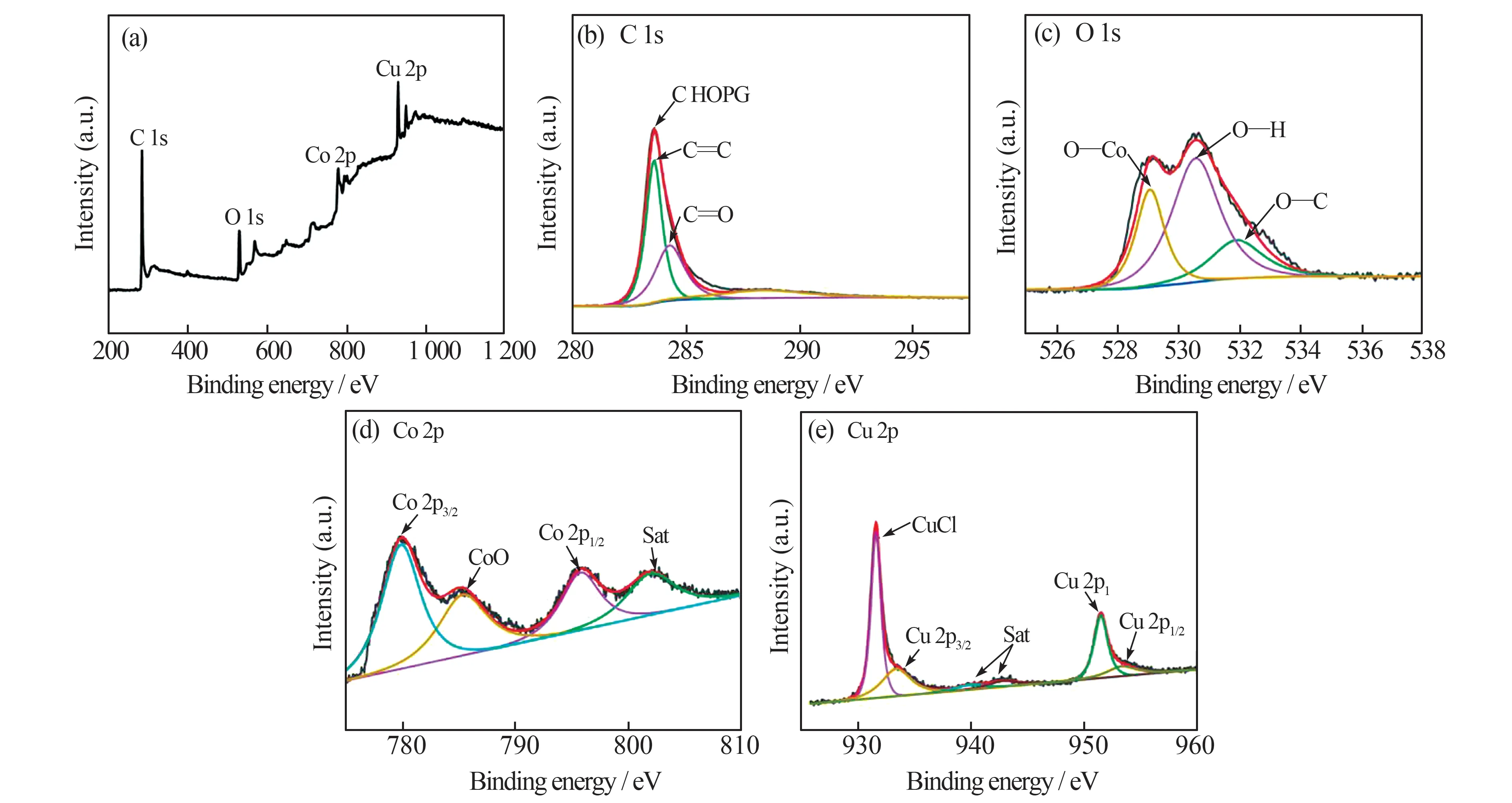
图6 Cu@C@CoO-600 的XPS 总谱(a)和C 1s(b)、O 1s(c)、Co 2p(d)、Cu 2p(e)的XPS 曲线图Fig.6 XPS spectrum (a)and XPS plots of C 1s (b), O 1s (c), Co 2p (d), Cu 2p (e)of Cu@C@CoO-600
2.2 材料的电化学性能
图7(a)为不同电极在PFS 溶液中的EIS 谱图,图中曲线不同的高频区圆弧半径反映了电子在该电极表面转移电阻的大小。其中,Cu@C@CoO-600/GCE 的圆弧半径最小,说明其电阻最小,材料表面电子传递速率最快。这可能是由于材料中三维互连的碳壳有效促进了电子的快速迁移,且随着热解温度升高,碳层变薄,电子的迁移速率加快。图7(b)为不同电极在pH 7.0 的空白PBS 溶液中的CV 曲线。其中,Cu@C@CoO-600/GCE 的界面电容和氧化电流明显大于GCE,但小于Cu@C@CoO-400/GCE 和Cu@C@CoO-500/GCE。这可能是由于在较低热解温度(400、500 ℃)下,Co 被氧化的程度较低,因此在CV 测试中被继续氧化而表现出较高的氧化电流。Cu@C@CoO-400 和Cu@C@CoO-500 较高的电容则可能源于较低温度热解导致较多的碳层残余量。尽管界面电容较大有利于电子传输,但氧化电流过大会干扰传感器对待测物的检测效果,因此,结合前文表征结果,选择Cu@C@CoO-600/GCE 作为BA 的电化学传感器。
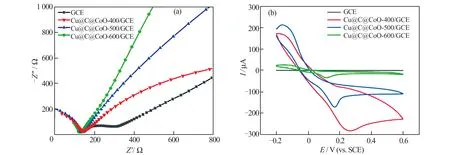
图7 不同电极在PFS 溶液中的EIS 曲线(a)和在PBS 溶液中的CV 曲线(b)Fig.7 EIS curves (a)in PFS and CV curves (b)in PBS of the different electrodes
2.3 BA 在不同修饰电极上的电化学行为
2.3.1 CV 与DPV 曲 线
图8 为PBS 溶液(pH 2.0)中不同电极对10.0 μmol/L BA 的CV 曲线(a)和DPV 曲线(b)。图8(a)中,BA 对GCE 响应电流的氧化还原峰电位差ΔE为0.121 V,而Cu@C@CoO-400/GCE、Cu@C@CoO-500/GCE 和Cu@C@CoO-600/GCE 的ΔE分 别 为0.073、0.066 和0.056 V,表明3 个碳材料都提高了GCE 表面 的电子 转移速率。 此外,BA 在Cu@C@CoO-600/GCE 表面的氧化还原反应为准可逆反应,根据Laviron 公式[13]计算其反应中的电子交换数n=1,大于其他电极。这归因于较高热解温度下形成的较薄碳层可更好地充当电子传导的桥梁,而基于两种金属纳米颗粒间可能形成的局部“电容器”效应,增加了该类材料在电化学测试过程中的电子交换数量[16,17]。
图8(b)比较了DPV 测试中不同电极对BA 的检测效果,峰电流Ip的大小代表Cu@C@CoO-600/GCE 对BA 的检测效果。其中,在热解温度较低(400、500 ℃)时,由于Cu@C@CoO 中的PTA 及部分配体未完全碳化,影响了纳米金属对BA 的亲和力,因此,Cu@C@CoO-400/GCE 和Cu@C@CoO-500/GCE 对BA 的检测效果较差;而在热解温度较高(600 ℃)时,得益于Cu@C@CoO-600 中碳层更薄且纳米金属颗粒尺寸和分布更均匀,Cu@C@CoO-600/GCE 对BA 表现出最好的检测效果。
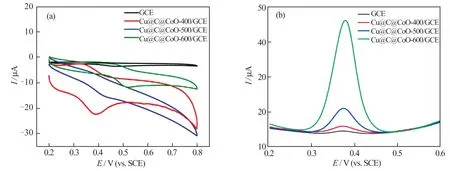
图8 不同电极对BA 检测的CV 曲线(a)和DPV 曲线(b)Fig.8 CV curves (a)and DPV curves (b)of BA detected by different electrodes
为探究最佳检测效果,研究了不同pH 环境(pH=2.0、2.5、3.0、3.5、4.0)对Cu@C@CoO-600/GCE 检测10.0 μmol/L BA 效果的影响。图9(a)为不同pH 值的PBS 溶液中Cu@C@CoO-600/GCE 对BA 检测的DPV 曲线,图9(b)中反映了电流与pH 值的关系。可以看出,BA 对Cu@C@CoO-600/GCE 的响应电流值在pH 2.0 的环境中最大,说明在此pH 环境中待测物的活性更强,更易被检出。此 外,图9(b)还 反 映 了BA 对Cu@C@CoO-600/GCE 的响应电流所对应峰电势E与pH 值的关系,其拟合方程为E(V)= 0.57 +0.08 pH,说明有等量的电子和质子参与了电极表面的电化学反应[22]。综上,选用pH 2.0 的PBS 溶液作为底液。

图9 不同pH 值的PBS 溶液中Cu@C@CoO-600/GCE 对BA 检测的DPV 曲线(a),响应电流及峰电势与pH 值的关系(b)Fig.9 DPV curves of Cu@C@ COO-600 /GCE for BA detection in PBS solutions with different pH values (a),relationship between potential, current and pH (b)
2.3.3 扫描速率对检测BA 的影响
图10(a)和(b)分别为在含10.0 μmol/L BA 的PBS(pH 2.0)中、不同扫描速率下,Cu@C@CoO-600/GCE 的CV 曲线及其线性关系曲线。图10(a)显示,在扫描速率为从20 mV/s 增加至500 mV/s时,BA 的氧化峰电流(Ipa)/还原峰电流(Ipc)随扫描速率的增大而不断增加,说明此时电化学反应主要受吸附过程影响[22]。 图10(b)反映出BA 对Cu@C@CoO-600/GCE 的响应电流值与扫描速率呈良好的线性关系。

图10 不同扫描速率时BA 对Cu@C@CoO-600/GCE 响应的CV 曲线(a)及其关系曲线(b)Fig.10 CV curves of BA response to Cu@C@ COO-600 /GCE at different scanning rates (a)and the linear relation curve (b)1-10:20,40,60,80,100,150,200,300,400,500 mV/s
2.4 方法的标准曲线与检出限
在最优实验条件下,将Cu@C@CoO-600/GCE应用于定量分析BA。图11(a)显示,BA 的氧化峰电流值随其含量的增加而不断增加;对其进行拟合分析(图11(b)),发现BA 的氧化峰电流值与其浓度在0.005~10 μmol/L 范围内呈良好的线性关系。根据计算:在0.005~0.5 μmol/L 浓度范围内,其线性拟合方程为Ip(μA)=41.89c(μmol/L)-0.39(R12=0.99),灵敏度为590 A·(mol/L)-1·cm-2,检出限为1.32×10-10mol/L;在0.5~10 μmol/L范围内,其线 性 拟合方程 为Ip(μA)=14.21c(μmol/L)-21.60(R22=0.99),灵敏度为200 A·(mol/L)-1·cm-2,检出限为0.390 nmol/L。相对于已报道的方法[23~30](表1),本文所构建的BA 电化学传感器Cu@C@CoO-600/GCE 具有灵敏度高、检出限低的优点。

表1 BA 检测方法对比Table 1 Comparison of different methods for BA determination mol/L
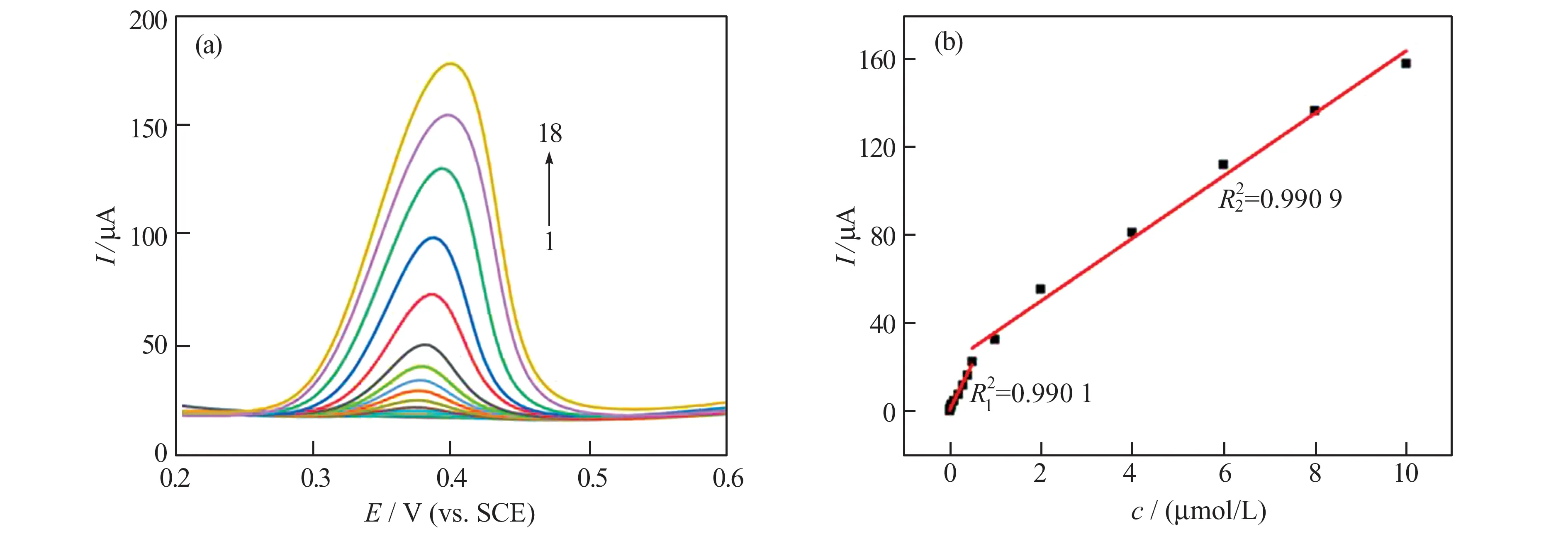
图11 Cu@C@CoO-600/GCE 检测BA 的DPV 曲线(a)和对应的标准曲线(b)Fig.11 DPV curves (a)and corresponding standard curve (b)for BA detection by Cu@C@CoO-600/GCE 1-18:0,0.005,0.01,0.02,0.03,0.04,0.05,0.1,0.2,0.3,0.4,0.5,1.0,2.0,4.0,6.0,8.0,10.0 μmol/L BA
2.5 方法的稳定性、重现性和抗干扰能力
研 究 了 Cu@C@CoO-600/GCE 检 测 10.0 μmol/L BA 的稳定性和重现性。将使用过的Cu@C@CoO-600/GCE 在室温下放置一周,再次用于检测BA,响应电流峰值的变化为3.70%;使用一支Cu@C@CoO-600/GCE 重复测定20 次,响应电流峰值的变化为3.20%。这些结果表明该传感器具有良好的稳定性和重现性。
向10.0 μmol/L BA 溶液中分别加入1 000 倍的K2SO4、NaCl、FeCl3,发现 对BA 的响 应电流峰 值的影响均小于5%;向10.0 μmol/L BA 溶液中分别加入50 倍的葡萄糖,20 倍的丙氨酸、赖氨酸和甘氨酸,对BA 的响应电流峰值的影响均小于5%。上述结果显示该传感器具有较好的抗干扰能力。
2.6 实际样品检测
考察了Cu@C@CoO-600/GCE 电化学传感器用于检测实际样品的可行性。取2 μL 双黄连口服液于10 mL 容量瓶中,用PBS 溶液(pH 2.0)定容。由表2 知,向实际样品溶液中加入标准的BA 溶液后,其回收率为99.23%~101.80%,RSD 均小于5%。

表2 实际样品中BA 的检测结果(n=3)Table 2 Determination results of BA in real samples (n=3)
3 结 语
本文采用水热法合成Cu@Co 双核MOFs,再将其热解后修饰到GCE 表面,构建了用于检测BA 的电化学传感器。Cu@C@CoO-600 中Cu 和CoO 纳米颗粒的尺寸及分布更均匀,碳层能更好地发挥促进电子传导的作用;纳米CoO 对BA 表现出较好的亲和力,纳米Cu 增强了材料的导电性能。该传感器在用于BA 的定量分析时,线性范围较宽且检出限优于已报道方法,同时具有较好的稳定性、重现性和抗干扰能力,在用于实际样品检测时也表现良好。

