基于特征图谱和一测多评法的黄柏质量控制研究
袁汉文,吕梦颖,罗江溢,邱伊星,刘 杨, 2,彭彩云*,王 炜*
基于特征图谱和一测多评法的黄柏质量控制研究
袁汉文1,吕梦颖1,罗江溢1,邱伊星1,刘 杨1, 2,彭彩云1*,王 炜1*
1. 湖南中医药大学药学院 中医药民族医药国际联合实验室,中巴中医药民族医药研究国际合作基地,创新药物研究所,湖南 长沙 410208 2. 湖南省食品药品检验研究院,湖南 长沙 410001
建立能有效区分黄柏与其易混淆品种关黄柏的特征图谱及一测多评方法,促进黄柏临床用药的安全性与有效性。利用HPLC对黄柏中化学成分进行分析,对色谱条件进行优化,确定最佳色谱条件,建立特征图谱,利用主成分分析(principal component analysis,PCA)和正交偏最小二乘判别分析(orthogonal partial least squares discriminant analysis,OPLS-DA)对特征图谱数据进行分析,筛选和确认差异性化合物,以盐酸小檗碱为参照物,建立一测多评方法测定黄柏主要有效成分含量。所建立的特征图谱及一测多评方法能鉴别黄柏与关黄柏,以木兰花碱、盐酸巴马汀、盐酸小檗碱以及一未知化合物(7号峰)为差异性化合物,黄柏中盐酸小檗碱含量明显高于关黄柏,黄柏中盐酸巴马汀峰面积极低而关黄柏中其峰面积较高。黄柏中木兰花碱的含量较低而未知化合物(7号峰)峰面积较高。所建立的特征图谱和一测多评方法简便,可作为《中国药典》修改标准的参考,用于黄柏的质量控制。
黄柏;关黄柏;特征图谱;一测多评;质量控制;木兰花碱;盐酸巴马汀;盐酸小檗碱
黄柏为芸香科黄柏属植物黄皮树Schneid.的干燥树皮,其广泛分布于中国西南地区,又习称“川黄柏”[1-2]。关黄柏为芸香科植物黄檗Rupr.的干燥树皮[1]。两者均为常用中药,其具有清热燥湿、泻火除蒸、解毒疗疮等作用,常用于湿热泻痢、黄疸尿赤、带下阴痒、热淋涩痛、脚气痿壁、骨蒸劳热等症[3]。《中国药典》2000年版及之前各版本《中国药典》中“川黄柏”和“关黄柏”均收载于黄柏项下[4],而自从《中国药典》2005年版开始,“川黄柏”和“关黄柏”被分列为2种药材[5]。
尽管被《中国药典》分列开来,黄柏与关黄柏的性味与归经及功能与主治相同。两者中的主要化学成分均为生物碱,如小檗碱、木兰花碱、药根碱等[6-9]。此外,其具有相似的生物活性或药理作用如抗菌、利尿、调血压、降血糖、抗氧化等[10]。因此临床应用上并未特别强调二者的差别,药材市场及成方制剂中也存在混用现象[11]。由于地理和历史的原因,中药药材品种混乱,基原复杂,加之中药的同名异物或同物异名现象普遍存在,甄别药材优劣、鉴别真伪变得异常困难[12]。然而,《中国药典》目前还没有强调对同源近属品种进行区分。而国际主流药典,如《美国药典》和《欧洲药典》均注重利用薄层色谱、指纹图谱或特征图谱等分析手段,从化学成分的角度鉴别同源近属品种,从而达到甄别真伪优劣的目的[13]。
为推动黄柏现代化及国际化进程,建立有效的、能被国际社会认可的质量控制标准,促进黄柏临床用药的安全性和有效性,本研究利用高效液相色谱(HPLC)建立了黄柏的特征图谱,并在特征图谱的基础上建立了一测多评的方法,用于测定黄柏中黄柏碱、木兰花碱和小檗碱的含量,阐明黄柏和关黄柏主要化学成分差异性。此外,为进一步验证和筛选差异性化合物,本研究结合化学计量学方法如主成分分析(principal component analysis,PCA)和正交偏最小二乘判别分析(orthogonal partial least squares discriminant analysis,OPLS-DA)对黄柏和关黄柏的特征图谱数据进行了比较分析。本研究系统阐明了易混淆品种黄柏和关黄柏的化学成分的差异性,所建立的特征图谱和一测多评含量测定方法能准确区分两者,可作为中国药典修改标准的参考,用于黄柏的质量控制。
1 材料与仪器
1.1 材料
27批黄柏药材采集于四川(HB-1~HB-15)、湖南(HB-16~HB-22)、广西(HB-23~HB-27),经湖南中医药大学龚力民副教授鉴定为芸香科植物黄皮树Schneid.的干燥树皮;6批关黄柏药材分别采集于吉林(GHB-1~GHB-2)、辽宁(GHB-3~GHB-4)和黑龙江(GHB-5~GHB-6),经湖南中医药大学龚力民副教授鉴定为芸香科植物黄檗Rupr.的干燥树皮;对照品盐酸小檗碱(批号ST03070120)、盐酸巴马汀(批号ST03040120)、盐酸黄柏碱(批号ST08670120)、盐酸药根碱(批号ST03080120)、木兰花碱(批号ST15050120)均购于上海诗丹德标准技术服务有限公司,所有对照品质量分数均大于98%;色谱级甲醇和乙腈购于美国Sigma-Aldrich公司;水为纯净水(华润怡宝饮料有限公司)。
1.2 仪器
Mettler-Toledo AE100S型电子天平(梅特勒-托利多公司);KQ2200DB型数控超声波清洗器(昆山市超声仪器有限公司);Agilent 1260高效液相色谱仪(安捷伦科技有限公司,配备二极管阵列检测器);Waters e2695高效液相色谱仪(沃特世公司,配备2489 UV/Vis检测器);Waters Atlantis® T3色谱柱(250 mm×4.6 mm,5 μm,Waters公司);Agilent 5 TC-C18色谱柱(250 mm×4.6 mm,5 μm,安捷伦科技有限公司);Agilent Poroshell EC-C18色谱柱(250 mm×4.6 mm,4 μm,安捷伦科技有限公司)。
2 方法与结果
2.1 供试品溶液的制备
黄柏和关黄柏药材粉碎后过四号筛,取样品粉末0.25 g,精密称定,置于25 mL锥形瓶中,加10 mL盐酸甲醇溶液(1∶100),超声提取30 min,取上清液离心后用0.45 μm微孔滤膜滤过,即得。
2.2 对照品溶液的制备
分别取盐酸小檗碱、盐酸巴马汀、盐酸药根碱、木兰花碱、盐酸黄柏碱适量,精密称定,置于10 mL量瓶中,用盐酸甲醇溶液(1∶100)溶解并定容,即得对照品储备液,将其置于4 ℃冰箱中保存,备用。用移液管吸取不同体积的各对照品溶液,于10 mL量瓶中混合后定容,得到不同质量浓度的混合对照品溶液,备用。
2.3 色谱条件
色谱柱:Waters Atlantis®T3(沃特世公司, 250 mm×4.6 mm,5 μm);流动相为乙腈(A)和0.3%磷酸-0.3%三乙胺溶液(B);梯度洗脱:0~25 min,10%~25% A;25~40 min;25%~40% A;40~55 min,40%~95% A;55~65 min,95% A;柱温20 ℃;体积流量0.8 mL/min;波长230 nm;进样量2 μL;黄柏和关黄柏的高效液相色谱图如图1所示。
2.4 特征图谱建立
2.4.1 精密度考察 按“2.1”项下供试品溶液制备方法,制备同一份样品(HB-1)溶液,吸取2 μL,按“2.3”项下的色谱条件连续进样6次分析,记录其色谱图。以9号峰(盐酸小檗碱)为参照,计算各色谱峰相对保留时间和相对峰面积,各共有峰相对保留时间的RSD小于1.35%,各色谱峰相对峰面积的RSD中,只有3号峰略大于3.00%,为3.04%,其余均小于3.0%,说明该方法精密度良好。
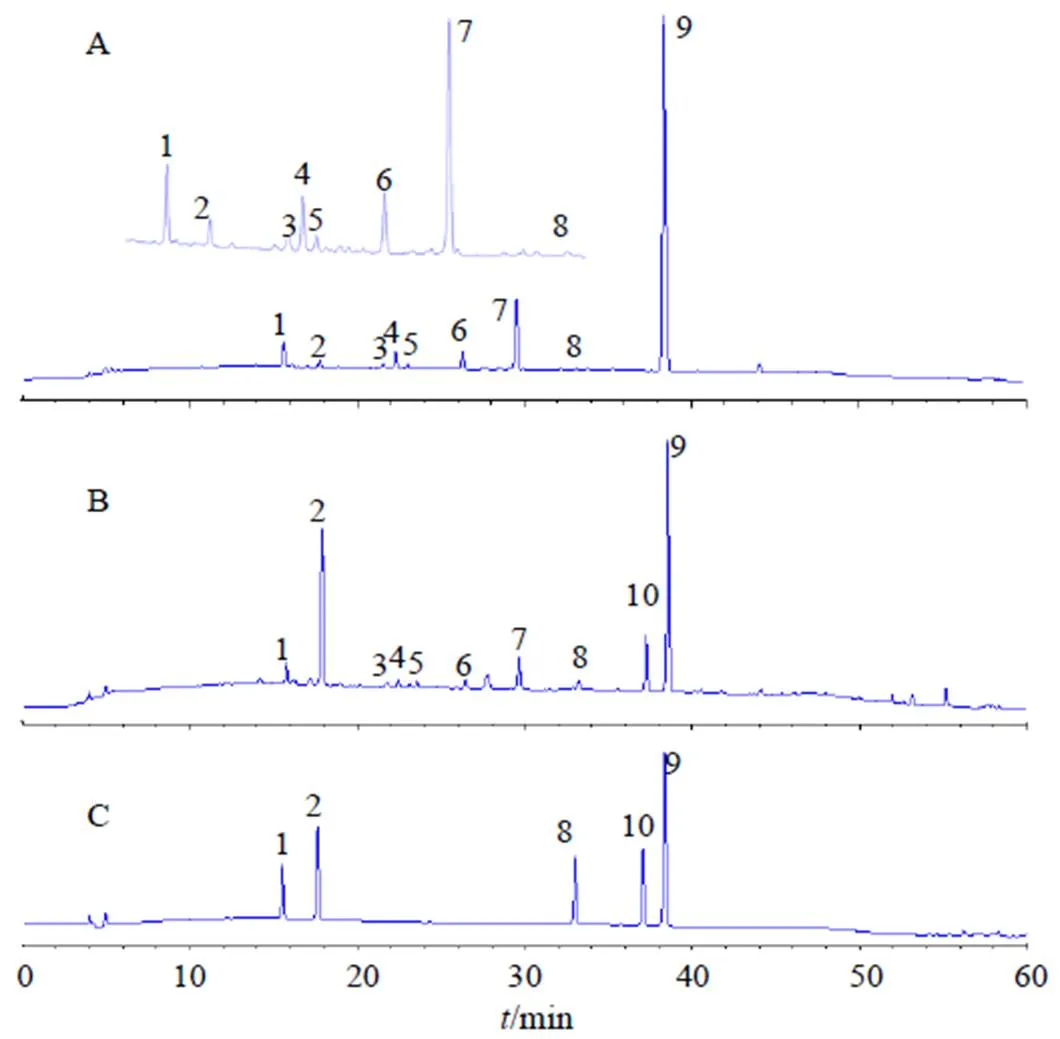
1-盐酸黄柏碱 2-木兰花碱 8-盐酸药根碱 9-盐酸小檗碱 10-盐酸巴马汀
2.4.2 稳定性考察 取同一供试品(HB-1)溶液,吸取2 μL,分别于0、2、4、8、12、24 h,按“2.3”项下的色谱条件进样分析,记录其色谱图。以9号峰(盐酸小檗碱)为参照,计算各色谱峰相对保留时间和相对峰面积,各共有峰相对保留时间的RSD小于1.05%,各共有峰相对峰面积的RSD小于2.88%,该方法稳定性良好。
2.4.3 重复性考察 取同一样品(HB-1),按“2.1”项下样品溶液制备方法,平行制备样品溶液6份,吸取2 μL,按“2.3”项下的色谱条件连续进样6次分析,记录其色谱图。以9号峰(盐酸小檗碱)为参照,计算各色谱峰相对保留时间和相对峰面积,各共有峰相对保留时间的RSD小于0.17%,各共有峰相对峰面积的RSD小于2.11%,该方法稳定性良好。
2.4.4 耐用性考察 取同一供试品溶液,分别利用3根不同柱子,在2台不同仪器按“2.3”项下的色谱条件进行进样分析并记录其色谱图。以9号峰(盐酸小檗碱)为参照,2号峰和3号峰相对保留时的RSD分别为8.60%和8.34%,其余各色谱峰相对保留时间RSD均小于4.97%,尽管1、2号峰受色谱系统影响较大,但是各色谱峰出峰顺序不变。
2.4.5 特征图谱的建立 按“2.1”项下方法制备供试品溶液,并按“2.3”项下色谱条件进行进样分析,记录各色谱图。将色谱图导入国家药典委员会颁布的“中药色谱指纹图谱相似度评价系统2004 A版”进行匹配,并生成黄柏及关黄柏的对照图谱(图2)。从特征图谱可看出,关黄柏中盐酸小檗碱(9号峰)的峰面积要明显低于黄柏。黄柏样品中盐酸巴马汀吸收峰强度十分低,并且部分样品中无法检出盐酸巴马汀。此外,可以看出,黄柏中7号峰的吸收强度大于关黄柏,而2号峰的吸收强度相对较小。即这些成分为鉴别黄柏与关黄柏的关键成分,将未知样品的色谱图与对照图谱进行比较,可定性鉴别黄柏和关黄柏。
2.5 PCA与OPLS-DA
2.5.1 PCA 将上述特征图谱峰面积导入Simia-P 14.1进行PCA,从其得分图(图3)可以看出,黄柏与关黄柏之间区分明显,从而验证了黄柏与关黄柏之间化学成分差异较大。其载荷图中,2、7、9、10号峰离原点较远,表明这些成分对各样品在得分图上的分布影响较大,即黄柏和关黄柏中这些成分含量的差异性较大,这些成分可作为鉴别黄柏与关黄柏的标志物。

图2 对照图谱对比图(A) 及黄柏(B) 与关黄柏(C) 特征指纹图谱
2.5.2 OPLS-DA 将各样品特征图谱数据导入到Simca-P 14.1中进行OPLS-DA,得到其得分图与变量贡献度图(Variable important in projection)。其得分图中(图4),黄柏与关黄柏分布区分明显,进一步验证了黄柏与关黄柏化学成分的差异性,同时,2、7、9、10号峰VIP值较大,其中2号和9号峰VIP值大于1,进一步确认了该4个成分可作为鉴别黄柏与关黄柏的标志物。
2.6 多指标成分的测定
上述已经建立区分黄柏与关黄柏的方法,但其无法区分黄柏样品质量的优劣,为了对黄柏更好地进行质量控制,在特征图谱的基础上,建立了一测多评的方法测定盐酸黄柏碱、木兰花碱、盐酸小檗碱3个主要成分含量。其供试品制备、对照品溶液制备、色谱条件分别如“2.1”“2.2”“2.3”项下所示。
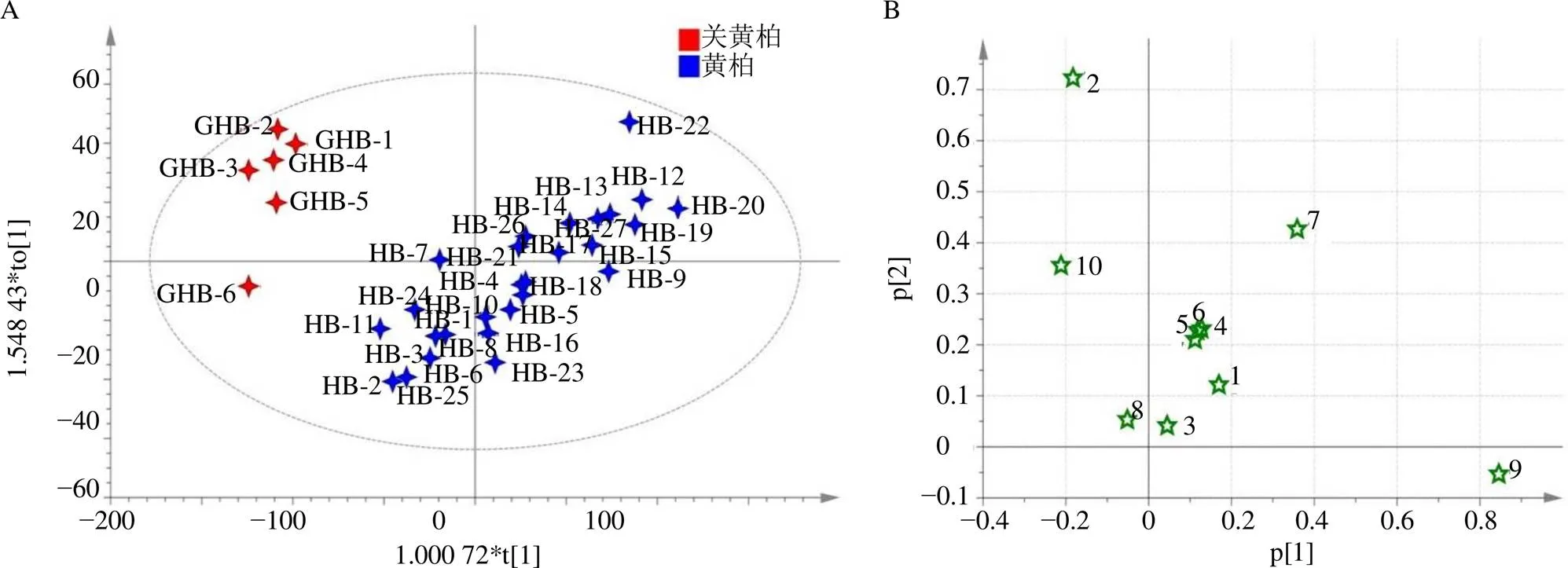
图3 PCA得分图(A) 与载荷图(B)
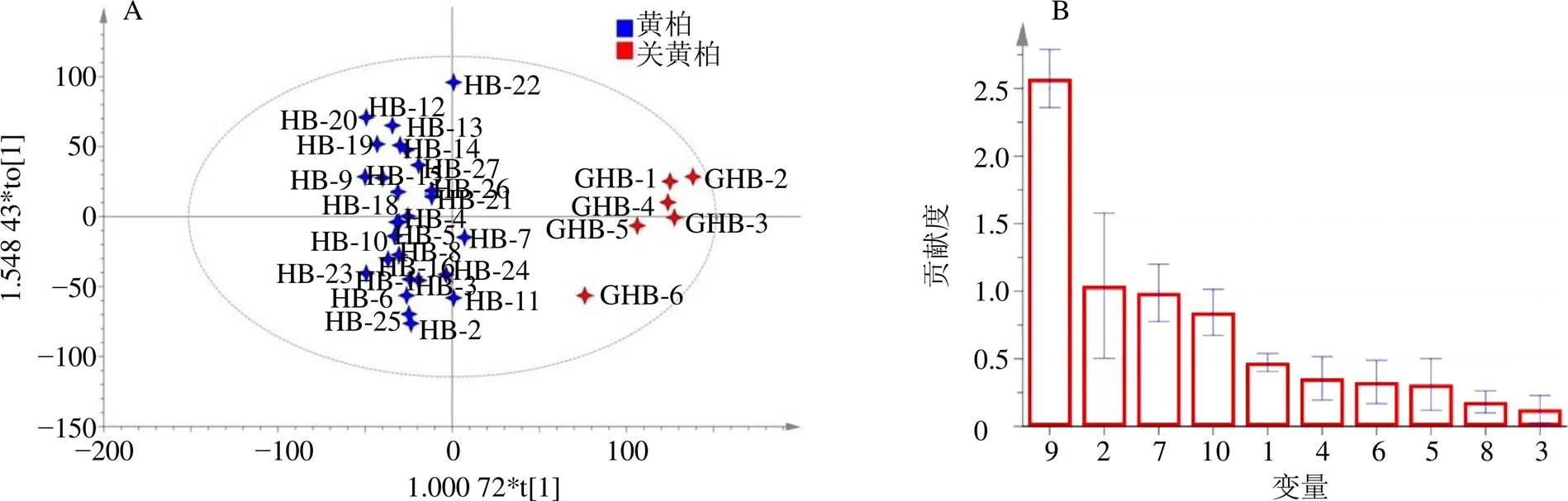
图4 OPLS-DA得分图(A)与变量贡献度图(B)
2.6.1 精密度、稳定性及重复性试验 精密度、稳定性及重复性测定方法同“2.4”项,记录盐酸黄柏碱、木兰花碱、盐酸小檗碱3个主要成分的峰面积,并计算其质量分数的RSD值。结果表明,各成分精密度的RSD均小于2.53%、稳定性的RSD值均小于1.68%、重复性的RSD值分别小于1.92%,说明该方法稳定、可靠。
2.6.2 线性方程、定量限与检测限 将对照品储备液进行稀释,制备6份不同质量浓度的混合对照品溶液,按“2.3”项下色谱条件进行分析,以峰面积为纵坐标(),质量浓度为横坐标(),绘制标准曲线。将对照品溶液进行逐级稀释,分别以性噪比的3倍和10倍计算检测限与定量限,结果见表1。
2.6.3 加样回收率试验 精密称取同一样品(HB1)9份,分别加入盐酸黄柏碱、木兰花碱、盐酸小檗碱高、中、低各3份,按“2.1”项下方法制备样品溶液,并按“2.3”项进行进样分析,盐酸黄柏碱、木兰花碱、盐酸小檗碱加样回收率在95.0%~106%,RSD小于0.5%,说明该方法准确度良好。
表1 线性方程、检测限及定量限结果
Table 1 Results of linearity, LOD and LOQ
化合物标准曲线R2线性范围/(mg·mL−1)检测限/(mg·mL−1)定量限/(mg·mL−1) 盐酸黄柏碱Y=4 733 X+0.108 80.998 60.005 376~0.336 0000.001 3440.002 688 木兰花碱Y=11 966 X-26.3090.998 60.006 368~0.398 0000.001 5920.003 184 盐酸小檗碱Y=9 841.2 X+7.961 70.998 60.005 696~1.78 0000.001 1390.002 848
2.6.4 一测多评方法建立
(1)相对校正因子计算:利用上述线性关系研究中6个不同质量浓度的对照品溶液的分析结果,以盐酸小檗碱为参照物,按下列公式计算盐酸黄柏碱和木兰花碱的相对校正因子(RCF),其中s和x分别表示参照化合物和待测化合物的单位响应值,s、x分别为参照化合物与待测化合物的峰面积,s和x分别为参照化合物和待测化合物的质量浓度。计算得到盐酸黄柏碱和木兰花碱的RCF平均值分别为2.071 6、0.822 1,其RSD分别为2.29%、3.00%。
RCF=s/x=(s/s)/(x/x)
(2)耐用性考察:分别利用3根不同色谱柱,在2台不同仪器按“2.3”项下的色谱条件进行进样分析并记录同一混合对照品溶液色谱图。以盐酸小檗碱(9号峰)为参照,盐酸黄柏碱和木兰花碱的RCF平均值分别为2.106 8、0.844 6,其RSD分别为2.43%、0.73%。
2.6.5 样品含量测定 所有样品按“2.1”制备供试品溶液,并按“2.3”项色谱条件重复进样3次分析,按一测多评法计算含量,取平均值,各批次样品含量测定结果如表2所示,各批次黄柏中盐酸小檗碱的含量差异较大,为2.34%~6.89%,其质量分数明显高于关黄柏(0.77%~1.74%)。除了样品HB-11为异常样品外,其余各批次黄柏中总生物碱量(以盐酸黄柏碱、木兰花碱、盐酸小檗碱计)为3.21%~7.70%,明显高于关黄柏(1.09%~2.83%)。利用这些特征也可以鉴别黄柏与关黄柏,该实验结果也说明黄柏和关黄柏中主要化学成分均为生物碱,其中盐酸小檗碱含量最高,但是各批次黄柏样品中盐酸小檗碱含量差异大,为保证黄柏临床用药的有效性,有必要对黄柏中盐酸小檗碱的含量进行限定。
表2 各成分含量测定结果
Table 2 Content results of each constituent
编号质量分数/% 盐酸黄柏碱木兰花碱盐酸小檗碱合计 HB-10.290.103.563.96 HB-20.260.062.953.27 HB-30.290.113.503.90 HB-40.430.204.805.43 HB-50.470.185.015.66 HB-60.270.073.503.83 HB-70.360.153.113.62 HB-80.360.074.104.54 HB-90.580.176.156.90 HB-100.390.094.575.05 HB-110.240.072.342.66 HB-120.610.206.267.07 HB-130.570.185.756.50 HB-140.560.205.636.39 HB-150.580.085.436.10 HB-160.440.064.334.83 HB-170.500.115.045.65 HB-180.370.054.584.99 HB-190.590.136.186.90 HB-200.690.126.897.70 HB-210.480.194.495.15 HB-220.620.295.786.69 HB-230.430.064.675.16 HB-240.300.042.873.21 HB-250.190.033.203.42 HB-260.490.234.605.31 HB-270.560.295.336.18 GHB-10.270.821.742.83 GHB-20.240.851.452.54 GHB-30.180.650.811.64 GHB-40.230.651.182.06 GHB-50.200.471.362.03 GHB-60.130.190.771.09
3 讨论
针对市场和临床应用中黄柏与关黄柏存在混用的情况,本实验建立了能区分鉴别黄柏与关黄柏的特征图谱,并结合PCA和OPLS-DA,确认了黄柏和关黄柏的差异性化合物为木兰花碱(2号峰)、盐酸小檗碱(9号峰)、盐酸巴马汀(10号峰)以及一未知化合物(7号峰),通过分析特征图谱中这些化合物的色谱吸收强度可准确鉴别黄柏和关黄柏。
此外,本实验建立的一测多评方法可有效测定黄柏和关黄柏中主要有效成分盐酸小檗碱、盐酸黄柏碱和木兰花碱的含量。27批次黄柏样品中三者的质量分数分别为2.34%~6.89%、0.19%~0.69%和0.03%~0.29%。黄柏中盐酸小檗碱的含量明显高于关黄柏,其3个生物碱的总含量也相对较高。鉴于黄柏和关黄黄柏中主要有效成分生物碱存在较大差异,两者的临床疗效应该也有所不同,因此,在临床用药中,黄柏和关黄柏应区别使用。
目前对单一成分的含量测定已经难以满足质量控制的需求,在中药或植物药的质量控制中,国际上主流药典标准均强调对其中的多指标成分进行含量测定,此外,中药基原复杂,中药要想被国际主流药典认可并走进国际市场,就必须建立合适的方法对齐其同源近属品种进行区分。本实验建立的黄柏特征图谱及一测多评法能够在有效的区分其易混淆品种关黄柏的同时,对其多指标活性生物碱进行含量测定,本研究可为黄柏的现代化和国际化提供参考依据。
利益冲突 所有作者均声明不存在利益冲突
[1] 中国药典[S]. 四部. 2020: 26.
[2] Liu Y, Chen J, Li X H,. Simultaneous determination of seven alkaloids inSchneid. by high-performance liquid chromatography [J]., 2010, 93(5): 1416-1421.
[3] 张凡, 孟莉, 刘蓬蓬, 等. 黄柏生品与盐炙品中生物碱类成分在大鼠肾组织脏器中的吸收差异 [J]. 中成药, 2020, 42(11): 2954-2959.
[4] 中国药典[S]. 二部. 2000: 236.
[5] 中国药典[S]. 三部. 2005: 126.
[6] Li Y B, Zhang T J, Zhang X L,. Chemical fingerprint analysis ofby ultra performance LC/Q-TOF-MS methods combined with chemometrics [J]., 2010, 33(21): 3347-3353.
[7] 田浩. 黄柏和黄茶化学成分研究 [D]. 兰州: 兰州理工大学, 2020.
[8] 廉莲, 咸晓燕, 楚冬海, 等. 川黄柏的化学成分研究 [J]. 中国实验方剂学杂志, 2013, 19(19): 149-152.
[9] Tomita M, Nakano T. Studies on the alkaloids of rutaceous plants. I. alkaloids ofRupr. (1) [J]., 1957, 5(1): 10-12.
[10] 金敏. 调剂中易混淆品种黄柏与关黄柏的探讨 [J]. 首都食品与医药, 2018, 25(1): 89-90.
[11] 李先宽, 冯杉, 郑艳超, 等. 黄柏与关黄柏的化学成分及生物活性研究进展 [J]. 药物评价研究, 2019, 42(5): 1033-1037.
[12] 崔光红, 黄璐琦. 中药材真伪鉴别新方法 [N]. 中国中医药报, 2007-02-05(007).
[13] 赵中振, 梁之桃, 郭平. 海外植物药的质量标准: 对中药标准化的一些启示 [J]. 中国中药杂志, 2009, 34(16): 2119-2125.
Quality control ofbased on HPLC characteristic fingerprint and single standard to determine multi-components method
YUAN Han-wen1, LYU Meng-ying1, LUO Jiang-yi1, QIU Yi-xing1, LIU Yang1, 2, PENG Cai-yun1, WANG Wei1
1. TCM and Ethnomedicine Innovation & Development International Laboratory, Innovative Material Medical Research Institute, School of Pharmacy, Hunan University of Chinese Medicine, Changsha 410208, China 2. Hunan Institute for Food and Drug Control, Changsha 410001, China
To establish HPLC characteristic fingerprint and single standard to determine multi-components methods to effectively distinguish Huangbai () from its confusing species,, so as to promote the efficacy and safety of.HPLC was used to analyze the chemical components from. The chromatographic conditions were optimized, the best chromatographic conditions were determined, and then the characteristic chromatogram was established. The differential compounds were screened and confirmed through PCA and OPLS-DA based on characteristic chromatogram data. Berberine hydrochloride was used as the reference compound to establish a single standard to determine multi-components method for the determination of the main effective components in.The established characteristic profile and the multiple evaluation methods were able to identifyand. Magnoflorine, palmatine hydrochloride, berberine hydrochloride and one unknown compound were identified to be the differential compounds. The level of berberine hydrochloridee was significantly higher inthan in. Berberine hydrochloride was not detected in, but its peak area was high in. The level of magnoflorine inis lower than that in, contrary to the peak area of the unknown compound (peak 7).The methods developed herein were simple and crudible for the discrimination ofand. They therefore can be the references for improving the quality control standard of Chinese Pharmacopoeia when revising the Chinese Pharmacopoeia.
;; characteristic fingerprint; quantitative analysis of multi-components by single marker; quality control; magnoflorine; palmatine hydrochloride; berberine hydrochloride
R286.2
A
0253 - 2670(2022)17 - 5491 - 06
10.7501/j.issn.0253-2670.2022.17.026
2022-02-16
国家重点研发计划中医药现代化研究重点专项-中药国际标准示范研究(2018YFC1707900);长沙市自然科学基金资助项目(kq2014086);湖南省科学技术厅重点研发计划项目(2018SK2119);湖南省自然科学基金资助项目(2020JJ4064)
袁汉文(1994—),男,助教,研究方向为中药化学与分析。Tel: 18711103975 E-mail: hanwyuan@hnucm.edu.cn
彭彩云(1972—),女,教授,硕士生导师,主要从事天然产物化学成分与活性研究。E-mail: caiyunpeng-hucm@qq.com
王 炜(1972—),男,教授,博士生导师,研究方向为中药化学与资源。E-mail: wangwei402@hotmail.com
[责任编辑 时圣明]

