灵芝酸A多克隆抗体制备及酶联免疫吸附测定法的建立
袁耀武,田益玲,李升云,杨心怡,马晓飞
(河北农业大学食品科技学院,河北 保定 071001)
灵芝通常是指多孔菌科真菌赤芝或紫芝的子实体,在中国传统医学中,灵芝是一种名贵的中药材。由于含有多种功效因子,灵芝往往被加工成干片、粉剂及胶囊等多种保健品,或经过提取制成口服液及医用注射液等制剂。然而由于生长环境及品种差异,不同来源的灵芝中各种功效因子含量存在较大差异,再考虑加工条件及人为掺假等因素,使得灵芝保健品市场中各类产品鱼龙混杂,质量良莠不齐。因此,提供一种能够衡量灵芝产品质量的快速检测方法,是本领域技术人员亟需解决的问题。在灵芝的多种功效因子中,灵芝三萜是其中之一,属于高度氧化的羊毛甾烷衍生物,化学性质稳定,不易在加工过程中降解。灵芝酸A在灵芝三萜中所占比例最大,是灵芝三萜类标志物之一,而且灵芝酸A具有抗氧化、抗肿瘤、抗辐射、缓解哮喘及抗疲劳等多种生物学活性,这些活性基本上能够体现灵芝在传统中药方剂里的功效。基于上述原因,可以将灵芝酸A作为衡量灵芝产品质量的重要指标之一进行精准测定,从而对灵芝产品质量作出快速评估。目前,灵芝酸A的检测方法有可见光比色法、紫外分光光度法、高效液相色谱法以及色谱-质谱联用技术。可见光比色法和紫外分光光度法测定灵芝酸A的缺点是特异性及灵敏度均较低,高效液相色谱法和色谱-质谱联用技术的缺点是仪器专业化程度高,检测时间和运行成本都比较高。与上述方法相比,酶联免疫吸附测定法反应条件温和又具有较高的灵敏度,对仪器专业化要求也不高,在小分子物质定量测定中得到了广泛的应用。Sakamoto等利用抗灵芝酸A的单克隆抗体,构建了灵芝酸A的酶联免疫吸附测定法,该方法用于灵芝酸A测定得到了较高的灵敏度。Yusakul等还尝试制备抗灵芝酸A的单链可变区片段,用于构建灵芝酸A的酶联免疫吸附测定法。酶联免疫吸附测定法是基于抗原-抗体反应的测定方法,特异性抗体是测定的关键因素,单克隆抗体与单链可变区片段具备较高的特异性,但是制备过程较为复杂,与上述抗体制备技术相比较,多克隆抗体的制备则相对简单,然而由于多抗中含有多种独特型抗体,靶向分散缺乏特异性,如果包被原选择不当,靶向其他区域的抗体会影响到小分子目标物的检测。本研究尝试制备低成本的抗灵芝酸A多克隆抗体,经过靶向分析后,选择合适的包被原,构建基于多克隆抗体的灵芝酸A酶联免疫吸附测定法并通过对市场中灵芝样品的测定验证其准确性。
1 材料与方法
1.1 材料、试剂与动物
灵芝粉、灵芝孢子粉,来自中国各省市市场。
鸡卵清白蛋白、牛血清白蛋白 美国Sigma-Aldrich公司;灵芝酸A 上海源叶生物科技有限公司;酶标板广州洁特生物过滤股份有限公司;羊抗兔IgG-HRP、3,3’,5,5’-四甲基联苯胺(tetramethylbenzidine,TMB)北京索莱宝科技有限公司;四氢呋喃(tetrahydrofuran,THF) 上海麦克林生化科技有限公司;1-羟基苯并三唑、,-二异丙基碳二亚胺 上海迈瑞尔化学技术有限公司。
新西兰大白兔购自河北实验动物中心,实验符合动物伦理要求。
1.2 仪器与设备
DNM-9602型酶标仪 北京普朗新公司;WZ80-2微孔板恒温振荡器 杭州佑宁仪器有限公司;1100高效液相色谱仪 美国Agilent公司;0.45 µm有机微孔滤膜上海安谱科学仪器有限公司。
1.3 方法
1.3.1 偶联蛋白的合成
灵芝酸A与牛血清白蛋白偶联物(bovine serum albumin-active ester method-ganoderic acid A,BSAAEM-GAA)的合成:采用活化酯法。取牛血清白蛋白500 mg,用8 mL溶解液(2%碳酸氢钠溶液∶四氢呋喃=1∶1)溶解。取灵芝酸A 100 mg、1-羟基苯并三唑140 mg、,-二异丙基碳二亚胺140 mg、四氢呋喃1 mL,以上试剂0~5 ℃搅拌1 h,形成活化酯。取上述活化酯溶液总质量的20%至牛血清白蛋白溶液中,室温反应2~4 h。将溶液冷冻干燥48 h得粉末。将粉末用50 mL纯化水溶解,0.45 μm滤膜过滤,除去不溶物,收集滤液。将滤液用3 kDa分子质量截留的渗透膜渗透10 h,每2 h换纯化水1 次。将渗透处理后的溶液再次冷冻干燥72 h,得固体粉末,即为BSA-AEM-GAA。
灵芝酸A与鸡卵清白蛋白偶联物(ovalbumin-active ester method-ganoderic acid A,OVA-AEM-GAA)的合成:采用活化酯法,与BSA-AEM-GAA的合成方法相同,将鸡卵清白蛋白替换牛血清白蛋白即可。
偶联物前体BSA-AEM-及OVA-AEM-的合成:与BSAAEM-GAA的合成方法相同,过程中不添加灵芝酸A。
1.3.2 抗BSA-AEM-GAA多克隆抗体的制备
选取健康雄性日本大耳白试验兔两只,以BSAAEM-GAA作为免疫原,进行4 轮免疫接种,每轮接种质量浓度为2 mg/mL,每次注射0.5 mL。第1轮接种与弗氏不完全佐剂混合使用,采用皮下多点注射,间隔14 d后进行第2、3、4轮免疫接种,采用耳静脉注射,每轮间隔7 d。第4轮接种7 d后,心脏采血,得到抗灵芝酸A免疫血清,通过A蛋白亲和层析柱纯化至IgG并浓缩至原始体积,4 ℃保存备用。
1.3.3 抗BSA-AEM-GAA多克隆抗体总效价的测定
采用间接酶联免疫吸附方法对BSA-AEM-GAA多克隆抗体总效价进行测定。BSA-AEM-GAA作为包被原,包被质量浓度为20 μg/mL。抗BSA-AEM-GAA多克隆抗体样本的递进稀释梯度为1∶5,各稀释度做3 个重复孔,1∶100稀释的阴性样本作对照。反应于微孔板恒温振荡器中进行,一抗与酶标二抗的反应条件均为800 r/min、37 ℃、20 min。显色底物为TMB工作液,显色时间10 min。终止显色后,用酶标仪在450/630 nm双波长处测定各实验孔吸光度。读值大于或等于0.2,且与阴性孔读值的比值大于等于2.1的结果判断为阳性孔,阳性孔最大稀释倍数即为血清效价。
1.3.4 抗BSA-AEM-GAA多克隆抗体的靶向分析
分别以BSA、OVA-AEM-GAA、OVA-AEM-、BSAAEM- 4 种物质包被酶标板,包被质量浓度均为20 μg/mL。总效价为1∶78 125的抗BSA-AEM-GAA多克隆抗体用样品稀释液1∶100稀释,分为3 个组:BSA吸收处理组(多抗溶液中加入等量的质量浓度为2 mg/mL的BSA溶液,振荡反应1 min)、GAA处理组(多抗溶液中加入等量的质量浓度为20 μg/mL的GAA溶液,振荡反应1 min)及未处理组(多抗溶液中加入等量的PBST溶液,振荡反应1 min)。采用间接酶联免疫吸附法对多克隆抗体进行测定,分析其中抗体的靶向区域,每组做3 个重复孔,1∶100稀释的阴性样本作对照,其他反应条件同于1.3.3节。
1.3.5 抗BSA-AEM-GAA多克隆抗体中灵芝酸A特异性抗体效价的测定
OVA-AEM-GAA作为包被原,包被质量浓度为20 μg/mL,其他操作与1.3.3节相同。
1.3.6 方法的建立、剂量反应关系曲线的拟合及标准曲线制备
合成抗原OVA-AEM-GAA经pH 9.6的碳酸盐缓冲液稀释至质量浓度20 μg/mL,100 μL/孔包被酶标版,37 ℃反应4 h,反应结束后PBST溶液洗板3 遍。灵芝酸A标准品用样品稀释液3 倍递进稀释,分为0、0.1、0.3、0.9、2.7、8.1、24、72、220、660 μg/L及2 000 μg/L 11 个标准剂量组。分别取50 μL各质量浓度的灵芝酸A标准品溶液,加入酶标版对应的标准孔中,每个质量浓度标准品及待测样品均做3 个孔。抗BSA-AEM-GAA多抗用样品稀释液稀释为灵芝酸A特异性抗体效价为1∶25,向上述各孔中加入多抗溶液50 μL。酶标板置于微孔板恒温振荡器中,800 r/min、37 ℃反应20 min,反应结束后PBST溶液洗板3 遍。于上述各孔中加入100 μL 1∶1 000(酶标记物体积∶样品稀释液体积)稀释的羊抗兔IgG-HRP(工作效价为1∶500~1∶2 000),置于微孔板恒温振荡器中,800 r/min、37 ℃反应20 min,反应结束后PBST溶液洗板3 遍。于上述各孔中加入100 μL TMB底物工作液,37 ℃反应10 min。反应结束后上述各孔中加入50 μL终止液,用酶标仪在450/630 nm双波长测定各实验孔吸光度。计算组内重复孔吸光度的变异系数(coefficient of variation,CV)计算每一剂量组相对吸光度,相对吸光度/%=/×100,其中,为某一质量浓度灵芝酸A反应孔的平均吸光度,为0 μg/L灵芝酸A反应孔的平均吸光度。通过Excel工具栏中的数据分析选项,进行单因素方差分析,确定吸光度与0 μg/L及2 000 μg/L剂量组差异显著的剂量组,利用与上述两个剂量组均差异显著的剂量组数据绘制相对吸光度与灵芝酸A质量浓度的关系曲线,得到回归方程并计算灵芝酸A的IC、IC、IC及IC。以IC~IC之间质量浓度作为该测定方法的线性范围,以IC对应的质量浓度为检出限。然后将IC与IC之间的质量浓度分5 个剂量组,制备灵芝酸A测定的工作曲线。
1.3.7 可重复性验证与回收率的测定
称取0.25 g灵芝孢子粉,置于10 mL样品管中,加入无水乙醇5 mL,浸泡24 h,离心后收集上清液,用样品稀释液5 倍递进稀释,取适当稀释度的试样液作为待测液,用1.3.6节建立的间接竞争酶联免疫吸附法进行测定,同时测定灵芝酸A标准品,绘制回归曲线。根据试样孔的相对吸光度,在标准曲线上查得试样液对应的灵芝酸A质量浓度再乘以样品稀释倍数则为样品中灵芝酸A的含量。得到孢子粉中灵芝酸A的含量后,以其含量大约1 倍剂量(70 mg/kg)的灵芝酸A标准品加入到灵芝样品中,同法处理后进行5 个批次的测定,得出样品加标回收率。
1.3.8 样品中灵芝酸A的测定
从市场中收集22 份灵芝粉剂产品:11 种破壁灵芝孢子粉(BGSP1~BGSP11)、6 种灵芝粉(GP1~GP6)及5 种灵芝孢子粉(GSP1~GSP5)。采用1.3.6节及1.3.7节样品处理及测定方法进行测定,计算灵芝酸A的含量,并进行方差分析。将上述22 种产品采用高效液相色谱法进行灵芝酸A测定,对2 种方法的测定结果进行比较。
2 结果与分析
2.1 抗BSA-AEM-GAA多克隆抗体总效价的测定结果
如表1所示,出现阳性反应的最高稀释度为1∶78 125,效价以出现阳性反应的样本最高稀释度表示,因此抗BSA-AEM-GAA多克隆抗体总效价为1∶78 125,结果说明免疫原的免疫接种取得了成功。总效价是衡量动物对免疫原整体应答效果的指标,并不能反映出针对半抗原的应答效果,针对半抗原的应答效果需要测定半抗原特异性抗体的效价。

表1 抗BSA-AEM-GAA多克隆抗体总效价的测定结果Table 1 Result of determination of total titer of polyclonal antibody against BSA-AEM-GAA
2.2 抗BSA-AEM-GAA多克隆抗体的靶向分析
由表2可知,抗BSA-AEM-GAA多克隆抗体能够与包被原BSA-AEM-出现阳性反应,而与包被原OVA-AEM-反应阴性,说明其中不存在靶向图1中3号位的抗体,但是可能存在靶向图1中1号位及2号位的抗体,与包被原BSA的阳性反应证实了靶向图1中1号位抗体的存在。经过BSA吸收处理的多抗与包被原BSA的反应阴性,但是与包被原BSA-AEM-的反应依然阳性,也证实了靶向图1中2号位抗体的存在。抗BSA-AEM-GAA多抗与包被原OVA-AEM-GAA出现阳性反应,但是与OVA-AEM-呈现阴性反应,因此可以推断多克隆抗体中存在靶向图1中4号位或5号位的抗体。经过GAA吸收处理的多抗与包被原OVA-AEM-GAA的反应阴性,证实了靶向图1中5号位抗体的存在,也否定了靶向4号位抗体的存在。因此,在经过靶向分析后,明确了抗BSA-AEM-GAA多克隆抗体中含有靶向BSA、GAA以及BSA与联接部结合点等区域的抗体。

表2 抗BSA-AEM-GAA多克隆抗体的靶向分析结果Table 2 Target analysis of polyclonal antibody against BSA-AEM-GAA
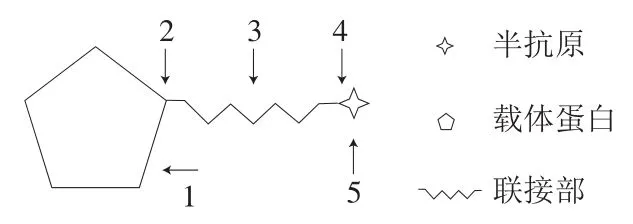
图1 抗偶联抗原的多克隆抗体中各独特型抗体靶向位置示意图Fig. 1 Target location of each idiotypic antibody in polyclonal antibody against conjugated antigen
2.3 抗BSA-AEM-GAA多克隆抗体中灵芝酸A特异性抗体效价的测定结果
如表3所示,多抗样本出现阳性反应的最高稀释度为1∶3 125。由表3可知,以OVA-AEM-GAA作为包被原,抗BSA-AEM-GAA多抗样品中只有抗灵芝酸A抗体能够参与反应,因此抗BSA-AEM-GAA多抗中灵芝酸A特异性抗体效价为1∶3 125。灵芝酸A特异性抗体效价与总效价相比明显降低,但其含量足以用于灵芝酸A的酶联免疫吸附测定,说明本实验对灵芝酸A免疫原的合成获得成功,其能够激发动物免疫系统对灵芝酸A足够的应答强度。
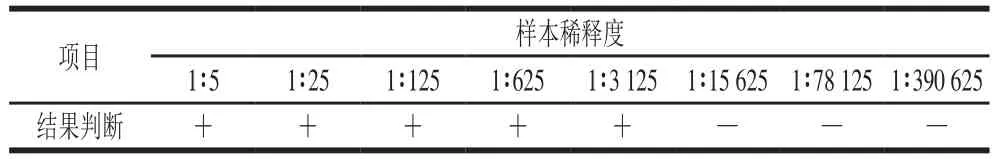
表3 灵芝酸A特异性抗体效价的测定结果Table 3 Results of determination of titer of specific antibody against ganoderma acid A
2.4 剂量反应关系曲线的拟合及线性分析
按照1.3.6节方法采用间接竞争酶联免疫吸附测定法,灵芝酸A每一剂量组的相对吸光度、组间差异显著性及CV结果见表4。选取与0 μg/L及2 000 μg/L剂量组吸光度均表现为显著差异的剂量组(0.3、0.9、2.7、8.1、24、72 μg/L)数据进行曲线拟合,表示相对吸光度,表示灵芝酸A质量浓度,在对数函数模型下,取得较好的拟合效果,回归方程:=-15.45ln+71.424,=0.988 7。如果轴以灵芝酸A质量浓度的自然对数表示,可以得到线性回归方程:=-15.454+178.17,值相同。计算出灵芝酸A的IC为4.0 μg/L,IC为0.6 μg/L,IC为27.3 μg/L,IC为0.3 μg/L。确定该测定方法的线性范围(IC~IC)为0.6~27.3 μg/L,检出限(IC)为0.3 μg/L。经过比较,该法用于灵芝酸A的测定比高效液相色谱法、液相色谱-串联质谱法及免疫层析法具有更低的检出限,与Sakamoto等构建的酶联免疫吸附测定法相比,检出限低1 个数量级,且反应用时更短。
根据线性范围,将灵芝酸A分为0.6、1.5、4.0、10.5、27 μg/L剂量组,通过间接竞争酶联免疫吸附测定法,制备出灵芝酸A测定的工作曲线,得到线性回归方程:=-16.177+184.84,表示相对吸光度,表示灵芝酸A质量浓度的自然对数值,值可达0.996 4,表明该工作曲线具有较高的拟合度。

表4 不同质量浓度灵芝酸A的间接竞争酶联免疫吸附测定结果Table 4 Results of ic-ELISA for ganoderma acid A at different concentrations
2.5 可重复性实验验证与回收率实验结果
样品加标前后5 批次实验测定结果见表5,加标样品与不加标样品5 个批次测定结果的批间CV均小于10%,样品加标回收率在82.9%~118.6%之间,不同批次的测定结果说明该方法对样品中灵芝酸A测定具有较好的重复性,加标回收率结果说明该方法对样品中灵芝酸A测定具有较高的准确度。

表5 不同批次实验测定灵芝酸A含量Table 5 Recoveries and intra-batch coefficients of variation of ganoderic acid A from spiked samples
2.6 实际产品中灵芝酸A的测定结果
通过间接竞争酶联免疫吸附法对22 份灵芝粉剂产品的测定结果见表6。不同品牌灵芝粉剂产品中灵芝酸A含量存在较大的差异,相差可以达到100 倍以上。进一步进行数据分析发现,不同类别的灵芝粉剂产品之间,灵芝酸A含量的差异显著性有所不同,其中破壁灵芝孢子粉与灵芝孢子粉的组间差异不显著(≥0.05),而灵芝粉与破壁灵芝孢子粉及灵芝孢子粉的组间差异极显著(≤0.01),即便是同一类别的产品,不同品牌间的组间差异性也是极显著(≤0.01),这种结果在灵芝粉、破壁灵芝孢子粉及灵芝孢子粉3 类产品中都存在。
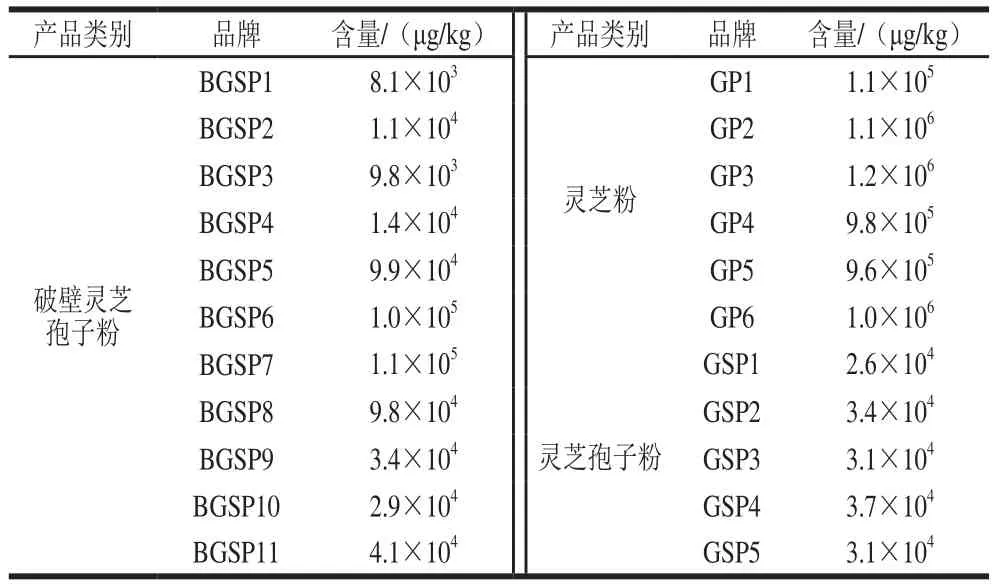
表6 不同品牌灵芝粉剂产品中灵芝酸A含量的测定结果Table 6 Results of determination of ganoderic acid A in different brands of G. lucidum powder
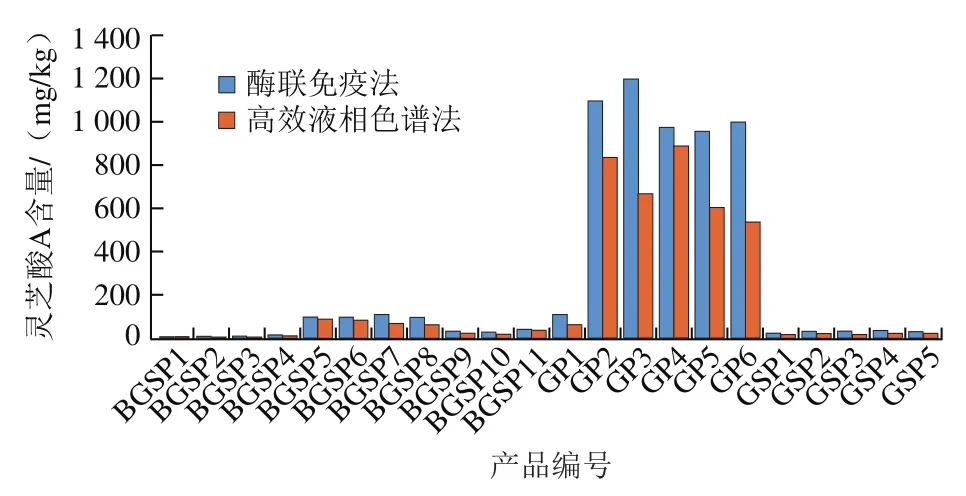
图2 酶联免疫吸附测定法与高效液相色谱法测定比较Fig. 2 Comparison of results of ELISA and HPLC for ganoderic acid A
将上述22 种产品采用高效液相色谱法进行灵芝酸A的测定,两种方法的测定结果对比图见图2。经数据分析,酶联免疫吸附测定法与高效液相色谱法的测定结果相比,相关系数=0.972,由此可见,本实验所建立的间接竞争酶联免疫吸附测定法对样品中灵芝酸A的测定结果具有较高的可信度。
3 讨 论
灵芝保健品市场中,同一类别和相同质量的产品,价格可以相差10 倍以上,价格与质量相关性,以及性价比,会让消费者难以抉择。本研究选用灵芝酸A作为评估灵芝产品质量的检测指标,是考虑到灵芝酸A在不同品种的灵芝中普遍存在,在灵芝三萜中占有比例最大、稳定性好,而且其经过验证的抗氧化、抗肿瘤、抗辐射、缓解哮喘及抗疲劳等多种生物学活性基本上可以代表灵芝的功效。然而,灵芝的功效因子不止一种,某种药效的作用或许是多种因子共同作用的结果,所以单独用灵芝酸A作为评估灵芝产品质量的指标有不完善之处。当前灵芝酸A测定还主要是依赖高效液相色谱等专业化的分析仪器,运行成本及技术要求都比较高,酶联免疫吸附测定法是基于抗原-抗体反应的测定方法,反应条件温和又具有较高的灵敏度,对仪器专业化要求也不高,而且能够开发出商业化试剂盒,便于基层的应用,所以利用酶联免疫吸附法测定灵芝酸A是一个可以考虑的选项。在酶联免疫吸附法中特异性抗体是测定的关键因素,如果需要测定的物质为半抗原,由于本身没有免疫原性,半抗原需要与载体联接才能合成免疫原获得抗体,因而在针对小分子半抗原的多克隆抗体中,往往含有多种独特型抗体,这些抗体的靶向位置理论上可以分布于免疫原的载体蛋白、载体蛋白与联接部的结合点、联接部、半抗原与联接部的结合点及半抗原5 个区域。在酶联免疫吸附测定法中,只有靶向半抗原的抗体才是测定目标物所必需抗体,如果包被原选择不当,多抗中靶向其他区域的抗体与包被原反应会影响到测定的灵敏度或者使测定不能开展。在做小分子目标物酶联免疫吸附测定时,通常是将包被原与免疫原采用不同的载体,往往就能够得到理想的效果,然而如果多抗中存在靶向与联接部有关的抗体,只更换载体则无法保证实验的正常进行,这也是本实验中遭遇失败的经验总结,所以多克隆抗体的靶向分析有一定的必要性。在抗体制备技术中,单克隆抗体与基因工程抗体具有更高的技术含量,但是在酶联免疫吸附测定法中,只要包被原选择合理或者多抗经过适当处理,利用多克隆抗体构建的测定方法在灵敏度与特异性方面并不低于单抗与基因工程抗体,而且具有更低的成本。
4 结 论
利用活化酯法合成BSA-AEM-GAA作为免疫原,接种实验兔获得了兔抗BSA-AEM-GAA的多克隆抗体,经过对多克隆抗体总效价及灵芝酸A特异性抗体效价的测定,证明免疫原的合成及动物免疫接种都获得了成功。本研究还利用多克隆抗体构建了灵芝酸A测定的间接竞争法酶联免疫吸附法,对所构建测定方法的可重复性、样品回收率进行测定,结果证明该方法对样品中灵芝酸A测定具有较好的可重复性和较高的准确度。本研究利用构建的间接竞争酶联免疫吸附法对市场上22 份灵芝粉剂产品进行测定,测定结果与高效液相色谱法结果具有较强的相关性,证明该方法用于灵芝酸A的测定具有较高可信度。上述结果表明本研究构建的方法用于灵芝酸A测定具有可行性,该方法能够为灵芝保健品市场中相关产品的质量监控提供一种辅助手段。

