改性多壁碳纳米管的制备及吸附甲基橙的性能研究
杨家萍,王艺洁
(兰州交通大学博文学院,甘肃 兰州 730000)
有机染料被广泛应用于造纸、印刷、皮革和纺织[1]等工业领域。甲基橙(MO)是一种常见的单偶氮化合物酸性阴离子染料,也属于已知致癌物的偶氮染料[2]。由于这种危险染料的急性暴露[3-4],使含甲基橙染料的废水会毒害水生生物,导致人类出现心率增快、呕吐、黄疸、休克、发绀、四肢瘫痪和组织坏死等症状。这些染料具有水溶性,且化学性质稳定,因而难以有效去除,因此,从相关行业产生的废水中彻底、有效地去除这种染料至关重要。目前,诸如通过金属氧化物的光催化降解[5]、组合电化学工艺[6]降解、超声降解[7]、膜过滤、混凝絮凝、生物处理和吸附等各种技术已被应用于工业废水的净化。吸附已被用于去除水和工业废水中的偶氮染料,因为它能够去除高浓度和低浓度的染料,同时易于设计、环保且成本相对较低[8]。碳纳米管是一种被广泛用于各种研究的碳的同素异形体,在科学领域显示出无限的应用潜力。本研究以多壁碳纳米管(MWCNTs)为原材料,对其进行KMnO4氧化改性并表征,从而研究改性制备的吸附剂KMnO4-MWCNTs对甲基橙染料的去除效果。
1 实验部分
1.1 试剂与仪器
试剂:多壁碳纳米管(MWCNTs),KMnO4(AR),甲基橙(AR),H2SO4(AR);溶液均采用去离子水配置。
仪器:pH计(PHS-3C),集热式恒温加热磁力搅拌器(DF-101S),电子天平(ME104E/02),电热鼓风干燥箱(101型),台式高速离心机(H/T18MM),落地恒温振荡器(HZQ-211C),扫描电子显微镜(SEM,dual-beam FIB-SEM),化学吸附仪(BET,Micromeritics Chemisorb 2750r),X-ray粉末衍射仪(XRD,x'pert pro),傅里叶变换红外光谱仪(FTIR,Ni-colet NEXUS 670)。
1.2 改性多壁碳纳米管的制备
将2.0 g的MWCNTs加入200 mL、1 mol/L的KMnO4溶液中,将以上混悬液在80 ℃下加热4 h,再用H2SO4处理,以去除MnO2;用蒸馏水洗涤直到洗涤水的pH值接近中性,然后离心(3 500 rmp,30 min)使其固液分离,固体产品在空气中50 ℃的条件下进行干燥,记为KMnO4-MWCNTs。
1.3 吸附实验
将改性制备好的0.02 g的KMnO4-MWCNTs纳米复合材料添加到盛有50 mL、10 mg/L的甲基橙溶液(MO)的锥形瓶中。将以上溶液置于180 rpm的落地恒温振荡器中,以恒定温度(20 ℃)振荡约10 h后取出,用0.45 μm的滤膜快速过滤,并测定溶液中MO的含量,计算出吸附容量。
1.4 KMnO4-MWCNTs的表征
用扫描电子显微镜(SEM)观察KMnO4-MWCNTs的表面形貌;比表面积用化学吸附仪(BET)来表征;傅里叶变换红外光谱仪(FT-IR)来表征KMnO4-MWCNTs的官能团;X-ray粉末衍射仪(XRD)来分析KMnO4-MWCNTs的晶体结构。
1.5 分析及计算方法
溶液中残留的MO浓度通过CAM UV300分光光度计测定,吸附平衡时的吸附容量Qe(mg/g)的计算公式为:

式中C0(mg/L)为初始时刻溶液中MO的质量浓度,Ce为吸附平衡时溶液中MO的质量浓度,V为溶液体积,m为KMnO4-MWCNTs的投加量。
2 结果与讨论
2.1 KMnO4-MWCNTs的表征
从图1可以看出原始多壁碳纳米管MWCNTs可以保持均匀的管状结构,排列相对杂乱无序,改性后的KMnO4-MWCNTs(b)改变了原始多壁碳纳米管的管状结构,出现聚团形貌,团状相对管状较厚且更规则。这可能是因为KMnO4对多壁碳纳米管氧化改性的结果。氧化剂的改性使多壁碳纳米管被氧化,可能出现羧基和内酯基团等,使其表面具有亲水性,增加了离子交换的能力[9]。

图1 MWCNTs(a)和KMnO4-MWCNTs(b)的SEM图
用FT-IR来表征KMnO4改性前后的官能团变化。图2(b)显示了KMnO4改性后的MWCNTs在579 cm-1处有较强的吸收峰来自于羧酸基团(–COOH);578 cm-1处的宽峰强度相比MWCNTs在1 580 cm-1处的峰强更强,该峰代表OH的伸缩振动峰的出现,原因是羟基或羧基等出现在改性样本中。在1 390 cm-1处发现了弱而宽的峰,可能是由于酚类的C-O延伸。这些结果清楚地表明,多壁碳纳米管被氧化而且可能氧化获得羧基、酚基官能团[10]。但在3 500 cm-1处振动吸收峰几乎消失,这表明KMnO4改性后的MWCNTs杂质明显减少。

图2 MWCNTs(a)和KMnO4-MWCNTs(b)的FT-IR图
X射线衍射分析(XRD)是重要的分析方法之一。从图3的XRD图可以看出,改性后KMnO4-MWCNTs(b)的衍射峰和改性前MWCNTs(a)的衍射峰位置基本一致,出现在2θ=26°和43°处,可以被索引为石墨碳的(002)和(101)晶面,但改性后KMnO4-MWCNTs(b)的峰强更强[9-11]。改性前后图谱一致,表征结果确定改性并不会影响多壁碳纳米管的性质。

图3 MWCNTs(a)和KMnO4-MWCNTs(b)的XRD图
2.2 各因素对吸附性能的影响
2.2.1 吸附时间对吸附性能的影响及吸附动力学
为了研究吸附机理和吸附特性常数,分别使用拟一级动力学模型和拟二级动力学模型来对动力学数据进行拟合。

式中,qe是达到吸附平衡时的吸附容量(mg/g);qt是t时刻的吸附容量(mg/g);k1、k2分别是拟一级和拟二级动力学速率常数;t为吸附时间(min)。
时间对吸附性能的影响见图4,在前20 min吸附量随着时间的增加而增加,在20 min时吸附达到平衡。前20 min吸附容量增加是因为反应开始主要是表层吸附,且有足够的吸附位点,同时扩散速度较快,随着反应的进行,MO分子占据碳纳米管表面的空隙且吸附位点逐渐饱和,使扩撒速度减慢,吸附达到平衡的同时达到最大值9.786 mg/g。
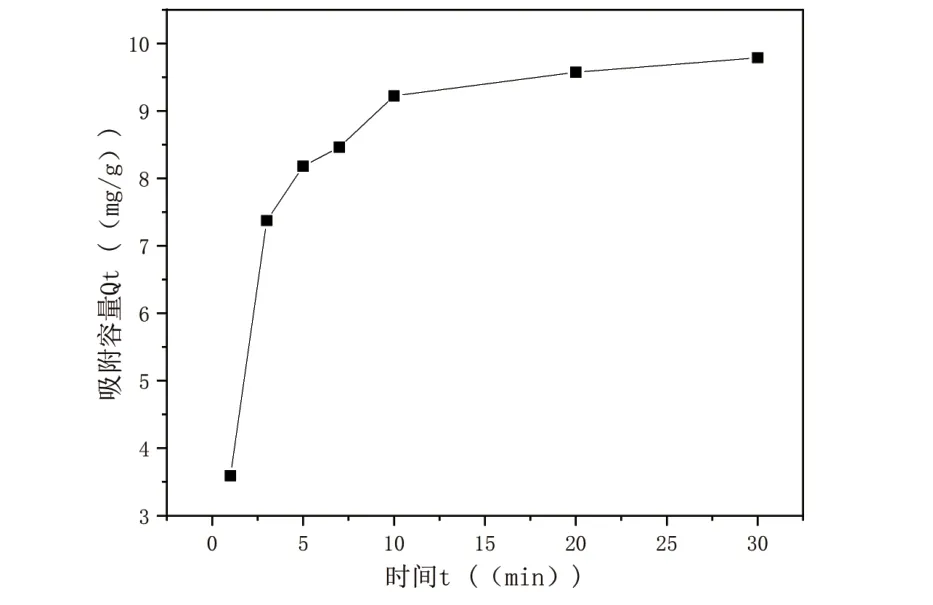
图4 吸附量随时间的变化关系
由表1可知,拟一级的相关系数明显比拟二级要高,因此得出结论,MO在KMnO4-MWCNTs上的吸附动力学模型拟合为拟一级动力学模型(见图5)。伪一级动力学模式假设吸附速度的快慢是由吸附过程的扩散步骤决定的,且吸附速率与反应平衡时的吸附量及某个时间点的吸附量差值成正相关,吸附质从溶液到达吸附剂表面是受扩散步骤的控制,吸附剂表面只有一种结合点位。
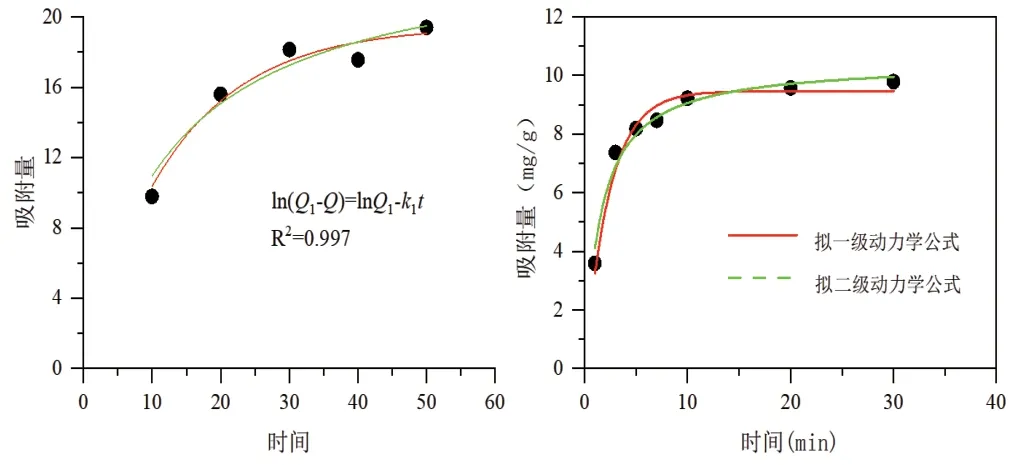
图5 两种非线性动力学方程对吸附试验数据的拟合曲线
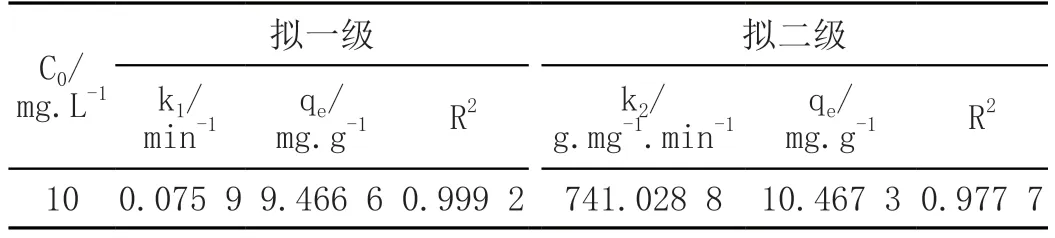
表1 MO在KMnO4-MWCNTs上的吸附动力学模型参数
2.2.2 MO初始浓度的影响及吸附等温线
图6是吸附容量随MO初始浓度的变化关系。当初始浓度从10 mg/L逐渐增大到50 mg/L时,吸附容量也逐渐增大到19.4 mg/g。随着MO浓度的增高,所需克服水、固相阻力的驱动力变高,因此吸附反应具有吸附容量高的MO浓度就高。

图6 吸附容量随初始浓度的变化关系
吸附等温线的分析可以为热力学研究提供基础数据,以推断吸附机理。在温度为293 K以及MO溶液初始浓度为10 mg/L~50 mg/L下吸附10 min,根据目前最常用的吸附等温线模型Freundlich和Langmuir等温线对吸附实验结果进行拟合分析。
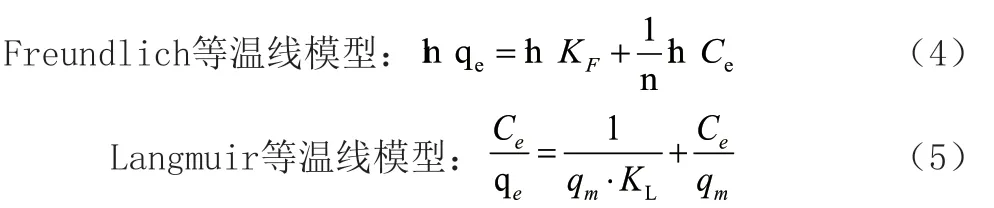
式中,qe为达到吸附平衡时的吸附容量(mg/g);KF、n、KL为Freundlich的吸附等温线常数;Ce为平衡时溶液中MG的浓度(mg/L);qm是吸附过程中的最大吸附量(mg/g)。
分析结果见图7、表2,从图表中可以看出Langmuir的相关系数大于0.98,因此Langmuir等温线模型更符合拟合结果,从Langmuir模型看出改性多壁碳纳米管的表面活性位点是均匀的,吸附质溶液与材料表面结合位点之间是单层吸附。
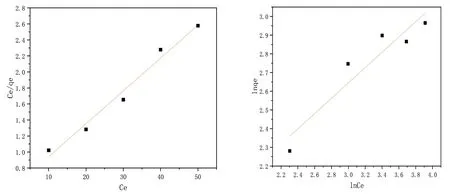
图7 Langmuir(a)和Freundlich(b)等温线拟合

表2 MO在KMnO4-MWCNTs上的吸附等温线模型参数
2.2.3 离子强度对吸附性能的影响
0.05g的KMnO4-MWCNTs在MO初始浓度为10 mg/L、20 ℃的条件下,加入不同浓度的NaCl吸附30 min,结果见图8。随着NaCl浓度的上升,吸附容量明显未发生变化,从9.923 mg/g到9.797 mg/g,少量下降的原因是随着NaCl浓度的增加,Na+的增加会和MO发生竞争吸附,削弱了吸附剂与MO之间的静电力,因此吸附容量减少。

图8 离子强度对KMnO4-MWCNTs吸附MO的影响
3 结论
(1)本文利用KMnO4-MWCNTs进行氧化改性,通过SEM、FTIR、XRD和BET对其进行表征,结果表明,KMnO4-MWCNTs的SEM图中摈弃原始多壁碳纳米管的管状结构,出现聚团形貌,团状相对管状较厚且更规则;FT-IR图出现的羧酸基团(–COOH)和变强的OH伸缩振动峰,均说明多壁碳纳米管被氧化获得羧基、酚基等官能团。
(2)拟一级动力学可以很好地描述KMnO4-MWCNTs对MO的吸附过程。吸附容量最初增加是因为反应开始主要是表层吸附,且有足够的吸附位点,同时扩散速度较快;随着反应的进行,MO分子占据碳纳米管表面的空隙且吸附位点逐渐饱和,扩撒速度减慢,吸附在20 min达到平衡;Langmuir等温线模型更符合拟合结果,故KMnO4-MWCNTs表面活性位点是均匀的且吸附过程是单层吸附;随着NaCl浓度的增加,吸附容量基本不变,离子强度对吸附性能没有太大影响。
(3)KMnO4-MWCNTs改性制备是在多壁碳纳米管的基础上,对其进行氧化改性,出现聚团形貌,增加了表面官能团的数量,且杂质减少。未来纳米吸附剂可以直接在氧化多壁碳纳米管的基础上改性制备,以探究更广泛的吸附性能和应用。

