苹果SRS基因家族的鉴定与功能分析
王锦锋
(陇东学院 农林科技学院,甘肃庆阳 745000)
SHI-relatedsequence(SRS)作为植物激素反应的重要调节因子,亦称短节间(SHI)基因家族[1],可通过控制GA和生长素的反应或信号转导来调节植株的生长或发育,编码一类具有2个不同保守区域的植物特异性转录因子[2],分别为RING结构域和IGGH结构域[3]。RING结构域编码C-X2-C-X7-C-X-H-X2-C-X2-C-X7-C-X2-H[4],锌指结构域(C3H2C3或C3HC4)是一大类与RNA、蛋白质和脂质底物结合后可发挥作用的环状结构域,参与细胞许多生理生化过程[5]。另一个区域称为IGGH结构域,是SRS基因家族的特异结构域[6],其功能目前未知,需要进一步研究。
研究发现,许多SRS家族成员通过调节激素合成、信号转导或反应来影响植物器官的发育。例如,STY1蛋白上调生长素生物合成,而SHI则通过转录控制作为GA反应的抑制因子[2]。此外,SHI通过GA调控大麦糊粉细胞中a-淀粉酶的表达,表明SHI可以负调控异源物种中的GA反应。另外,当SRS7基因过表达时,茉莉酸(JA)信号中断,花药开裂延迟[7]。对SRS家族基因突变植物进行广泛研究表明,SRS转录因子可控制植物多种发育过程,如根的形成[8]、叶的发育[9]、花的诱导、花的发育[10]和光形态[11],突变会影响雌蕊发育、花的雌性生殖结构以及花轮的叶片发育和器官特性。最近的一项研究表明,SRS5通过直接结合光形态建成促进基因的启动子来促进光形态建成[11]。SRS基因参与植物器官发育的研究在其他植物中也有报道。例如,已经发现SRS转录因子通过玉米生长素信号调节大麦(HordeumvulgareL.)的激素、花序模式[12]和根系发育[13]。SRS转录因子控制生长素的生物合成,进而影响植物生长[14],并塑造水稻(OryzasativaL.)的植物结构[15]。
AtSRS基因家族表达模式及系统发育,已进行了全基因组鉴定和功能分析,相比之下,对苹果(MalusdomesticaBorkh.)SRS基因家族(MdSRS)的研究少之又少。苹果是世界性果品,其产量和品质易受环境影响,特别是干旱、盐和激素等非生物胁迫已成为影响苹果生长发育的最主要问题之一[16]。本研究鉴定了苹果的SRS基因,明确各个基因的系统发育进化关系、理化性质、Motif预测、亚细胞定位及在不同胁迫后的表达水平,并研究了其在苹果对各种刺激反应中的潜在功能,这些研究结果将为苹果育种提供参考。
1 材料和方法
1.1 试验材料
选取生长状态良好、长势基本一致的3周龄‘长富’苹果组培苗作为试验材料,用10% PEG6000、1 mmol·L-1ABA和150 mmol·L-1NaCl分别模拟干旱胁迫、激素胁迫和盐胁迫,收集处理(0、12、24、48和72 h)后的叶片。每个处理3个重复,锡箔纸包裹标记,液氮速冻后保存于-80 ℃保存备用,用于后续的定量反转录PCR (quantitative reverse transcription PCR,qRT-PCR)分析。
1.2 方 法
1.2.1MdSRS家族成员鉴定与理化性质分析苹果SRS家族基因的蛋白质序列通过苹果基因组数据(https://iris:angers.inra.fr/gddh13/)获得,拟南芥SRS蛋白数据从TAIR(https://www.arabidopsis.org)获得。从Pfam(http://pfam.xfam.org/)网站下载隐马尔可夫模型,通过在线软件SMART(https://smart.embl-heide-lberg.de/)对初步筛选得到的候选基因家族进行结构域验证,最终筛选得到11个苹果MdSRS家族成员。采用ExPASy Proteomics Server(http://web.expasy.org /protparam)分析苹果MdSRS氨基酸序列的分子量、长度、等电点及不稳定系数等。利用在线网站(http://www.genscript.com/psort/wolf-psort.html)进行亚细胞定位预测。
1.2.2 苹果MdSRS家族基因结构分析利用在线软件MEME(http://meme-suite.org/tools/meme)预测苹果MdSRS基因家族的保守基序,最大保守序列鉴定数目设置为10。利用TBtools绘制苹果MdSRS基因家族基因结构和保守基序图。
1.2.3 苹果MdSRS基因家族染色体定位及SRS系统发育和进化分析利用MapChart2.2软件和TBtools对苹果MdSRS家族基因进行染色体定位。为了分析多物种SRS基因间的进化关系,从PlantTFDBv5.0(http://planttfdb.gao-lab.org/)数据库中下载拟南芥(Arabidopsisthaliana)、水稻(Oryzasativa)和杨树(Populustrichocarpa)等SRS基因蛋白序列构建进化树(参数设置默认),利用AI软件对SRS进化树进行修饰。
1.2.4 苹果MdSRS基因家族顺式作用元件分析通过PlantCARE对MdSRS家族成员启动子上游2 000 bp的顺式作用元件进行分析,然后对激素诱导、环境适应及逆境诱导表达元件的数量进行分析。
1.2.5 苹果MdSRS基因家族定量表达分析用于qRT-PCR分析的苹果材料如1.1所述。RNA提取试剂盒和cDNA第一条链合成所采用的反转录试剂盒购自宝生物工程有限公司(TaKaRa)。MdSRS荧光定量引物如表1所示,选用MdActin作为内参基因。反应体系为:TB GreenⅡ10 μL,上、下游混合引物各2 μL,6 μL ddH2O,cDNA 2 μL,总体积20 μL。反应条件为:95 ℃预变性3 min;95 ℃变性5 s,58 ℃退火30 s,72 ℃延伸30 s,40个循环。样品均为3次重复。并采用2-ΔΔCT计算基因的相对表达量。采用SPSS软件的单因素分析法进行差异显著性分析。
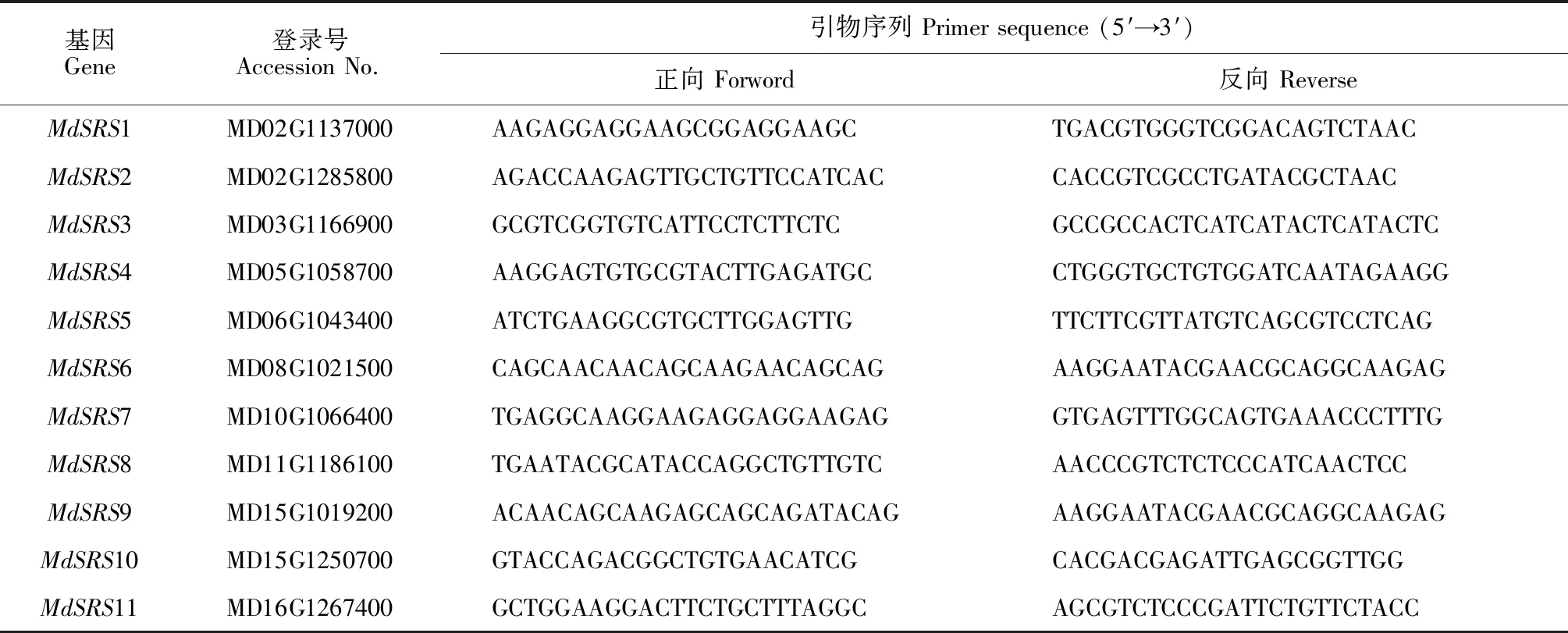
表1 qRT-PCR引物序列Table 1 qRT-PCR primer sequences
2 结果与分析
2.1 苹果MdSRS家族成员理化性质分析
利用苹果基因组数据库,经过Blast同源比对及SMART分析共得到11个苹果MdSRS基因。MdSRS基因家族蛋白的理化性质如表2所示,包括等电点、分子质量、不稳定系数和亲和指数等指标。苹果MdSRS基因家族氨基酸残基为229~414 aa,MdSRS3最长,MdSRS7最短;等电点范围在6.38~9.36之间;蛋白分子量介于25.40~43.04 kD之间;均为不稳定蛋白;亚细胞定位显示,11个家族成员在细胞膜上都有分布,个别分布于叶绿体上,MdSRS3和MdSRS8分布最广。

表2 苹果MdSRS基因家族理化性质分析Table 2 Analysis of physicochemical properties of apple MdSRS gene family
2.2 苹果MdSRS基因家族成员系统进化及基因结构分析
MdSRS基因家族成员的基因结构分析结果显示(图1),7个基因均含外显子和内含子。保守基序分析发现,11个MdSRS基因的保守基序数量在3~8之间不等,其中保守基序数量最少的MdSRS2只有3个保守基序,且Motif 1为该家族所共有,同一类群中的大多数成员具有相似的motif,说明同一类群中的基因存在着功能上的相似性。根据Motif数量和种类的不同,可将进化树大致划分为3组,进化树中同一亚家族内成员间基因结构较相似,但并不完全相同,可能是由于SRS基因功能的多样性且在进化过程中发生了变异。
2.3 苹果SRS染色体定位分析
MdSRS染色体定位结果显示(图2),苹果的11个SRS家族成员不均匀地分布在其中9条染色体中,2号和15号染色体(Chr 02,Chr15)分布2个SRS成员,其他染色体上各分布1个。
2.4 苹果MdSRS基因家族系统发育和进化分析
为揭示SRS蛋白在植物中的系统发育关系,以苹果(Malusdomestica)、拟南芥(Arabidopsisthaliana)和水稻(Oryzasativa)等的SRS基因家族成员的蛋白序列通过NJ法构建系统进化树。结果(图3)表明,所有SRS蛋白被分为5个亚家族(A1
-A5),每个亚家族所包含的SRS成员不等。MdSRSs在5个亚家族中均有分布,其中在A4中分布最多(3),其他亚家族分布数目一样,均为2个。
2.5 苹果MdSRS基因家族启动子顺式作用元件分析
通过PlantCARE对MdSRS家族翻译起始位点上游2 000 bp顺式作用元件进行分析,结果(图4)显示,苹果SRS基因家族成员启动子上游2 000 bp序列存在着逆境胁迫响应[低温响应元件(LTR)]、激素响应[生长素反应元件(TGA-element)、水杨酸反应元件(TCA-element)、脱落酸反应元件(ABRE)]、防御和应激反应顺式作用元件(TC-rich repeats)等。启动子区域顺式作用元件分析表明,苹果SRS基因家族的11个基因大多含有防御和应激反应顺式作用元件(TC-rich repeats)和脱落酸响应元件(ABRE),这表明MdSRS能够参与调控一系列非生物逆境胁迫。
2.6 苹果MdSRS基因家族在盐胁迫、干旱胁迫及ABA胁迫下的表达特点
为了进一步研究MdSRS基因家族的功能,本研究对苹果分别进行了非生物胁迫和激素处理,结果如图5所示。在盐胁迫下经过不同处理时间(0、12、24、48、72 h)后,MdSRS家族11个成员均有表达且主要为下调表达。在同一胁迫时间下,大部分基因的表达大致为降-升-降趋势且差异显著,其中MdSRS1、MdSRS5、MdSRS5、MdSRS7及MdSRS10表达量在各时期表达量相对最高,均介于0.6~1.2之间。而同一基因随胁迫时间的延长呈多样性变化,以MdSRS1为典型的先降后升型(MdSRS4、MdSRS7、MdSRS8、MdSRS9、MdSRS11),以MdSRS6为代表的持续降低型(MdSRS2、MdSRS3、MdSRS5、MdSRS6、MdSRS10),说明SRS基因在苹果生长发育过程中对盐胁迫有明显响应,其中MdSRS6随盐胁迫变化最明显且在72 h后降至最低值。
为了揭示MdSRS家族基因在干旱胁迫下的表达模式,利用10%渗透压PE6000溶液模拟干旱胁迫,本研究对11个MdSRS基因在PEG胁迫下的基因表达进行qRT-PCR验证。结果表明(图5),随胁迫时间的延长,PEG模拟干旱胁迫促进大多数MdSRS基因发生差异表达。MdSRS1、MdSRS3、MdSRS6和MdSRS10随胁迫时间的延长呈先升后降的趋势且大多在12 h达到最高,表达量介于1.2~1.6之间;MdSRS7在24 h数值最高,为1.538;MdSRS2、MdSRS5、MdSRS8和MdSRS9随胁迫时间的延长呈下降趋势;MdSRS4呈先降后升趋势,24 h降至最低值后在72 h上升,但还是低于0 h的表达量;MdSRS11随胁迫时间的延长呈逐渐上升趋势,72 h的表达量是0 h的1.54倍。而在同一胁迫时间下,大多数基因呈降-升趋势,除12 h的MdSRS1-MdSRS11,48和72 h的MdSRS1-MdSRS6(呈降-升-降-升),表达量最高时可达1.6,以MdSRS1、MdSRS6及MdSRS7为代表。
MdSRS基因在ABA处理下不同时间的表达量变化结果显示,各基因的表达模式均有不同,有以MdSRS2为代表的先升后降型,但表达量达到最高的时间点不同(24、48 h)且在72 h的表达量要高于0 h;以MdSRS3为代表的持续升高型;以MdSRS1为代表的升-降-升-降型等;以MdSRS5为代表的升-降-升型等,在24 h上升后开始下降,72 h达到最大值。不同基因在同一胁迫时间下的结果表明,ABA胁迫显著提高了MdSRSs的表达量,11个基因在同一时间下呈降-升-降-升的趋势,其中MdSRS3在72h表达量为2.99,显著高于同一时间下其他基因的表达量,表示这11个苹果MdSRS基因能积极响应ABA胁迫相关生物学过程。
3 讨 论
作为传统大众果品,苹果销量突出,前景广阔,其优质高产一直是果树栽培生产追求的最终目标[17],但种植过程中多种环境胁迫通过影响植株体内的激素含量及比例分布而严重影响产量和品质[18]。有研究认为SRS基因家族参与维持生长素体内平衡,例如在器官形成时期生长素合成增加,下调KNOX基因的表达,而KNOX基因的表达量增加或减少到一定阙值,都会抑制GA20ox基因表达,从而抑制赤霉素生物合成,另外,SRS可通过调节激素的生物合成、信号转导或反应来影响植物器官的发育[19]。因此如何提高苹果的抗性,缓解严重环境胁迫对苹果产量质量的影响,是目前栽培过程中亟需解决的问题。缓解产量损失的一种方法是发现抗胁迫基因,培育出非生物胁迫下的强健品种。在本研究中,我们对苹果SRS家族进行了全基因组分析,并探讨了苹果对各种刺激反应的潜在功能。我们鉴定了MdSRS在干旱、盐和ABA响应中的作用,这些结果将为我们对苹果SRS家族提供新的认识,并为苹果育种提供候选抗性基因。
转录因子在植物的生长发育中起着重要的作用,许多转录因子已被确定参与了一系列响应生物和非生物胁迫[20]。自2017年公布了高质量苹果基因组序列以来[21],越来越多的苹果基因家族被鉴定出来,SRS家族作为一类古老的转录因子,已在拟南芥、玉米、大麦和水稻等物种中得以验证,但对苹果SRS基因家族的鉴定和分析还未见报道。在本研究中,鉴定出了11个苹果SRS家族成员,数量少于模式植物拟南芥的16个,但多于单子叶植物玉米的6个,说明SRS基因家族在长期的进化过程中出现了扩增或缩减。通过对MdSRS基因进行理化性质分析,发现MdSRSs氨基酸个数为229~414 aa且大多属于不稳定蛋白;蛋白分子量范围在25.40~43.04 kD之间,且11个家族成员在细胞膜上都有分布,个别在叶绿体上也有分布。通过理化性质预测发现不同的MdSRS编码蛋白理化性质均存在一定差异,推测其在植物体内的功能可能也不相同。内含子是影响转录速率、核输出和转录稳定性、提高mRNA翻译效率的重要结构,虽然内含子不能作为转录因子的结合位点,但它们可以增加基因的表达。我们对MdSRSs基因结构进行了分析,发现位于同一亚家族的成员具有相似的基因结构,证明了同一群体的成员具有相似的进化关系或功能。然后对苹果、番茄、水稻、杨树、拟南芥中的63个SRS蛋白构建系统发育进化树,结果发现亚家族A1~A5中都含有MdSRS基因家族的成员,说明这些成员在进化上同源,功能上也相似,而MdSRSs位于不同的分支中,可能是在进化过程中引起的这种差异,表明该家族在植物进化过程中其功能较保守。植物在响应生物以及非生物胁迫过程中常涉及复杂的调控机制,正如在对SRS基因启动子中的顺式作用元件的分析中所述,它们包含了许多与胁迫相关的元件,如ABRE、LTR、TGA、TCA。ABRE结合蛋白(AREBs/ABFs)可以结合ABRE元件,参与ABA、脱水和高盐胁迫等反应。在水稻中,ABRE结合因子OSBZ8可能调控水稻的耐盐性。AtHSFA7b通过与E-BOXmoti结合,正向调控拟南芥的耐盐性。SRS基因在苹果中的表达模式存在差异,提示这些基因可能参与不同的生物学过程或执行不同的生物学功能[22]。本试验在模拟干旱、盐胁迫和ABA胁迫的基础上,通过实时荧光定量检测可得,MdSRS的11个基因在盐胁迫和干旱胁迫下总体呈下调趋势,但表达模式不同,其中以盐胁迫下MdSRS6为典型的持续降低型和以MdSRS7为代表的先升后降型,表达量最高维持在1.4~1.8之间,说明SRS转录因子家族能够参与植物生长发育过程,并响应生物及非生物胁迫,其中可以有效调节干旱、盐等非生物胁迫对植物造成的伤害;相对于盐胁迫和干旱胁迫,ABA胁迫后,MdSRSs表达各异但总体呈上调表达,部分呈不规则变动,由此说明ABA对叶中MdSRS基因的表达有不同的影响,这意味着MdSRS基因可以以特异性的方式调节苹果发育过程中的植物激素调控,可能是SRS与ABA信号通路中的核心转录因子ABI5存在互相作用,通过正向调控ABA的生物合成来增强植株对非生物胁迫的耐受性[23-24]。鉴于SRS在干旱胁迫和ABA胁迫中均有不可替代的作用,我们可想象MdSRS基因可能在依赖于ABA调控的干旱胁迫响应信号通路上发挥作用,具体结论还有待试验进一步验证。
综上所述,本研究的结果丰富了苹果SRS家族转录因子的基本信息,对其蛋白理化特征、保守基序和基因结构等进行了分析。在苹果基因组中鉴定出了11个SRS基因。系统发育分析表明,系统进化树将63个SRSs划分为5个亚类,同一亚组在基因结构方面具有相似性,且同一或不同亚类MdSRSs基因在胁迫处理后的表达模式彼此不同,说明这些基因可能参与了不同的生物学过程或执行不同的生物学功能,也为苹果进一步抗性研究提供良好资源。

