基于特征图谱结合色彩图像技术的白芍与炒白芍差异研究△
纪玉华,洪婉敏,干丽,姚晓璇,钟文峰,黄贵发,魏梅*
1.广东一方制药有限公司,广东 佛山 528244;
2.广东省中药配方颗粒企业重点实验室,广东 佛山 528244
白芍为毛茛科芍药Paeonia lactifloraPall.的干燥根[1],全国各地种植广泛,产自浙江、安徽、四川、河南、湖南等地,以四川中江、安徽亳州、浙江磐安所产白芍为道地药材[2]。白芍味苦、酸,性微寒,归肝、脾经,具有养血调经、敛阴止汗、柔肝止痛、平抑肝阳的功效,可用于治疗血虚萎黄、月经不调、自汗、盗汗、胁痛、腹痛、四肢挛痛、头痛眩晕等症[1]。白芍药材中含有单萜及其苷类、黄酮及其苷类、三萜类等化学成分[3]。药理研究表明,白芍具有保护心血管、保肝、镇痛、抗炎、抗氧化等作用[4]。炒白芍为《中华人民共和国药典》(以下简称《中国药典》)2020 年版收载的白芍炮制品,白芍经炒制后外观性状和功效均发生了显著变化。古人对白芍炒制前后的功效变化描述为“生则伐肝,炒则入脾肺”“伐肝生用,止痛炒用”[5]。相关文献表明,白芍炒制前后功能主治发生的变化可能是多种成分共同作用的结果,炒制后不同类别化学成分呈现出不同的变化规律[5-6]。
《中国药典》2020 年版(一部)仅以芍药苷含量作为白芍药材、炒白芍饮片的质量控制指标,不能全面反映白芍的质量,具有一定局限性。为了体现中药多成分的特点,确保其内在质量均一、稳定,可以采用中药特征图谱技术对中药质量进行整体控制[7]。近年来,基于色彩图像分析技术实现中药颜色客观量化的研究越来越多,色度分析已被应用于栀子、陈皮、山楂等中药炮制程度的判别[8-11],但对于白芍炮制程度的量化判别未见报道。笔者参考相关文献,以白芍药材和炒白芍为研究对象,建立超高效液相色谱法(UPLC)特征图谱分析方法,结合Lab 模式色度值读取,建立更加全面合理的白芍药材、炒白芍鉴别和质量评价方法[12-13]。
1 材料
1.1 仪器
TS7700 型分光测色仪(深圳市三恩时科技有限公司);Vanquish 型超高效液相色谱仪(赛默飞公司);ME204E 型万分之一电子分析天平、XP26 型百万分之一电子分析天平(瑞士Mettler-Toledo 公司);KQ-500DE 型数控超声波清洗器(昆山市超声仪器有限公司);Milli-Q-Direc 型超纯水系统(德国Merck公司)。
1.2 试药
对照品没食子酸(批号:110831-201605,纯度:90.8%)、5-羟甲基糠醛(5-HMF,批号:111626-201912,纯度:99.2%)、儿茶素(批号:110877-202005,纯度:95.1%)、芍药苷(批号:110736-202044,纯度:96.8%)、苯甲酸(批号:100419-201703,纯度:99.9%)均购自中国食品药品检定研究院;对照品1,2,3,4,6-五没食子酰葡萄糖(批号:wkq19011402,纯度:98.3%)、芍药内酯苷(批号:wkq18052205,纯度:99.2%)购自四川省维克奇生物科技有限公司;对照品苯甲酰芍药苷(批号:ST05580220MG,纯度:96.4%)购自上海诗丹德标准技术服务有限公司;乙腈(德国Merck公司)、磷酸(天津市科密欧化学试剂有限公司)均为色谱纯;其他试剂为分析纯。
1.3 样品
经广东一方制药有限公司魏梅主任药师鉴定,15 批白芍药材均为毛茛科芍药Paeonia lactifloraPall.的干燥根。样品信息见表1。

表1 15批白芍及炒白芍样品信息
2 方法与结果
2.1 炒白芍的制备
按《中国药典》2020 年版白芍【炮制】项下的规定制备白芍饮片,再按清炒法(通则0213),取白芍饮片于炒锅内,设置电陶炉加热功率为800 W,翻炒至表面微黄,用红外测温仪测定饮片表面温度,其温度为114~128 ℃。
2.2 色谱条件
色谱柱:ACQUITY UPLC HSS T3(150 mm×2.1 mm,1.8 μm);流动相:乙腈(A)-0.05%磷酸(B),梯度洗脱(0~5 min,3%A;5~10 min,3%~12%A;10~16 min,12%~13%A;16.0~26.5 min,13%~20%A;26.5~30.0 min,20%A;30~36 min,20%~35%A;36~40min,35%~50%A;40.0~40.1min,50%~3%A;40.1~45.0 min,3%A)。检测波长:0~10 min,280 nm;10~45 min,230 nm。柱 温:30 ℃;流速:0.3 mL·min-1;进样量:1µL。
2.3 溶液的制备
2.3.1对照品溶液的制备 精密称定对照品没食子酸、5-HMF、儿茶素、芍药内酯苷、芍药苷、苯甲酸、1,2,3,4,6-五没食子酰葡萄糖、苯甲酰芍药苷适量,加甲醇制成上述8 个成分质量浓度分别为72.69、62.10、33.49、219.32、364.78、79.20、26.16、39.59 μg·mL-1的混合对照品溶液,即得。
2.3.2(炒)白芍供试品溶液的制备 取(炒)白芍中粉约1.0 g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25 mL,称定质量,超声提取30 min(300 W,40 kHz),放冷,称定质量,用稀乙醇补足减失的质量,摇匀,滤过,取续滤液。
2.4 白芍、炒白芍UPLC特征图谱的建立
2.4.1精密度试验 取按2.3.2 项下方法制备的炒白芍(CBS1)供试品溶液,按2.2 项下色谱条件连续进样6 次,参照峰(S)确定为9 号色谱峰(芍药苷),计算可得各共有色谱峰的相对保留时间RSD为0.03%~0.13%,相对峰面积RSD 为0.15%~3.09%,表明仪器精密度良好。
2.4.2稳定性试验 取按2.3.2 项下方法制备的炒白芍(CBS1)供试品溶液,分别在0、2、4、8、12、24 h 按2.2 项下色谱分析方法依次进样,参照峰(S)确定为9 号色谱峰(芍药苷),计算可得各共有色谱峰的相对保留时间RSD 为0.02%~0.41%,相对峰面积RSD为0.21%~3.96%,表明供试品溶液在24 h内稳定性良好。
2.4.3重复性试验 独立平行取6 份按2.3.2 项下方法制备的炒白芍(CBS1)供试品溶液,按2.2 项下色谱分析方法进样测定,参照峰(S)确定为9 号色谱峰(芍药苷),计算可得各共有色谱峰的相对保留时间RSD 为0.02%~0.28%,相对峰面积RSD 为0.21%~4.22%,表明该方法重复性较好。
2.4.4白芍、炒白芍UPLC 特征图谱的建立 取15 批(炒)白芍,按2.3.2 项下方法制样和2.2 项下色谱条件进样分析,以.cdf 格式导入“中药色谱指纹图谱相似度评价系统”(2012 年版),确定15 批(炒)白芍UPLC 特征图谱及其共有色谱峰。通过15批白芍、炒白芍的UPLC 特征图谱的叠加,生成白芍、炒白芍的对照特征图谱。15 批白芍UPLC 特征图谱标定了15个共有色谱峰,与之对应的15批炒白芍UPLC 特征图谱标定了17 个共有色谱峰,经对照品的保留时间和二极管阵列全波扫描光谱确定,2、3、6、8、9、11、13 和16 号色谱峰分别为没食子酸、5-HMF、儿茶素、芍药内酯苷、芍药苷、苯甲酸、1,2,3,4,6-五没食子酰葡萄糖和苯甲酰芍药苷。由结果可知,炒白芍特征图谱的1号、3号色谱峰由白芍药材炮制后产生(图1)。
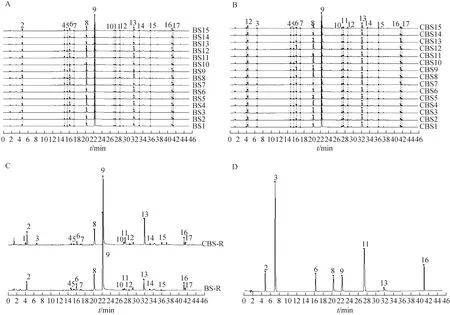
图1 15批白芍及炒白芍的UPLC叠加图谱及对照特征图谱、混合对照品色谱图
2.4.5白芍、炒白芍UPLC 特征图谱的相似度评价 经“中药色谱指纹图谱相似度评价系统”(2012版)分析,15 批白芍、15 批炒白芍样品的UPLC 特征图谱相似度分别为0.946~0.999、0.948~0.997,表明15 批白芍、炒白芍特征图谱相似度较高,炒白芍炮制过程稳定可行。
2.5 白芍、炒白芍UPLC 特征图谱的主成分分析(PCA)及正交偏最小二乘法−判别分析(OPLS-DA)
PCA 是一种可概括原始指标的无监督多元统计方法,通过对原始数据进行降维处理得到几个主要信息互不相关的综合指标,从而获得样本间的内在联系和差异性因素[14]。基于PCA 基础,进一步结合有监督的OPLS-DA,放大样本间的差异性,获得其显著性影响差异因子,应用在指纹图谱的质量控制上具有一定优势[15]。将15 批白芍和15 批炒白芍样品UPLC 特征图谱各共有色谱峰峰面积经标准化处理后导入SIMCA 14.0 软件,进行PCA(色谱峰缺失的峰面积以“0”计)。PCA 结果提取4 个主成分,主成分特征值和方差贡献率见表2。以第1、第2 主成分为变量的二维载荷图中,第1 主成分变量的权重前三名依次为15 号、1 号、11 号(苯甲酸)色谱峰,由此判定15 号、1 号、11 号(苯甲酸)色谱峰在区分白芍生品与炮制品指纹图谱中占决定性作用。PCA得分图见图2,PCA的二维载荷图见图3。

图2 白芍和炒白芍UPLC特征图谱共有峰峰面积PCA得分图

图3 白芍和炒白芍UPLC特征图谱共有峰峰面积PCA二维载荷图
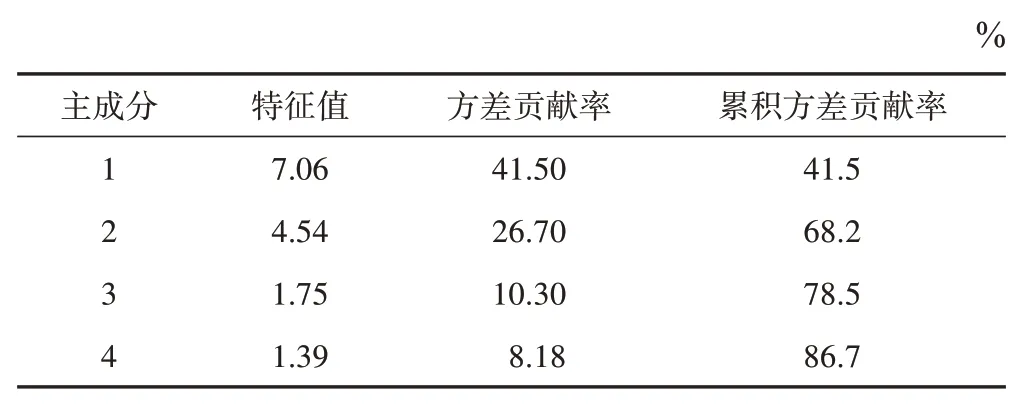
表2 白芍、炒白芍前4个主成分的特征值和方差贡献率
进一步采用OPLS-DA 进行分析,在OPLS-DA得分图中每个点分别代表1 个样品,点与点之间的距离代表各个样品之间存在的差异程度。
15批白芍药材及炒白芍在OPLS-DA模型中分类聚集明显,且两者分布在图中两个不同的区域,表明白芍、炒白芍的UPLC 特征图谱有明显差别。其中所建模型对Y 矩阵的解释率(R2Y)为1,模型的预测能力(Q2)为0.787,表示该模型拟合程度和预测能力良好;对模型中变量重要性投影(VIP)值进行分析,选择VIP 值>1 的化学成分作为区分白芍生品及炒白芍的重要特征峰,依次为峰11(苯甲酸)、峰1、峰15、峰10、峰3(5-HMF)、峰2(没食子酸)。OPLS-DA得分图、VIP值得分图分别见图4~5。结合图5 也可明显看出,这些色谱峰变量离原点的距离远,提示这些色谱峰是引起白芍炮制前后差异性的主要标志性成分。

图4 白芍和炒白芍UPLC特征图谱共有峰峰面积OPLS-DA得分图
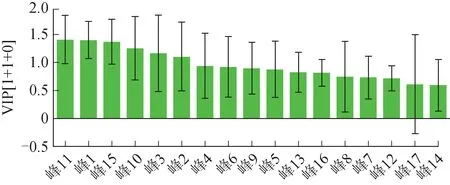
图5 15批白芍及炒白芍UPLC特征图谱共有峰峰面积的OPLS-DA VIP值得分图(, n=30)
2.6 白芍、炒白芍色度值读取
取15 批白芍、15 批炒白芍,破碎,过四号筛,取适量压制于载玻片上,压制厚度约为1 mm,色差仪设置光源为D65,采用白板进行校正,读取白芍与炒白芍的粉末色度值(L*、a*、b*),每个样品平行读取3 次,取平均值。白芍、炒白芍粉末图像见图6,15批白芍、炒白芍粉末色度值见表3,15批白芍、炒白芍粉末的色差值见表4。
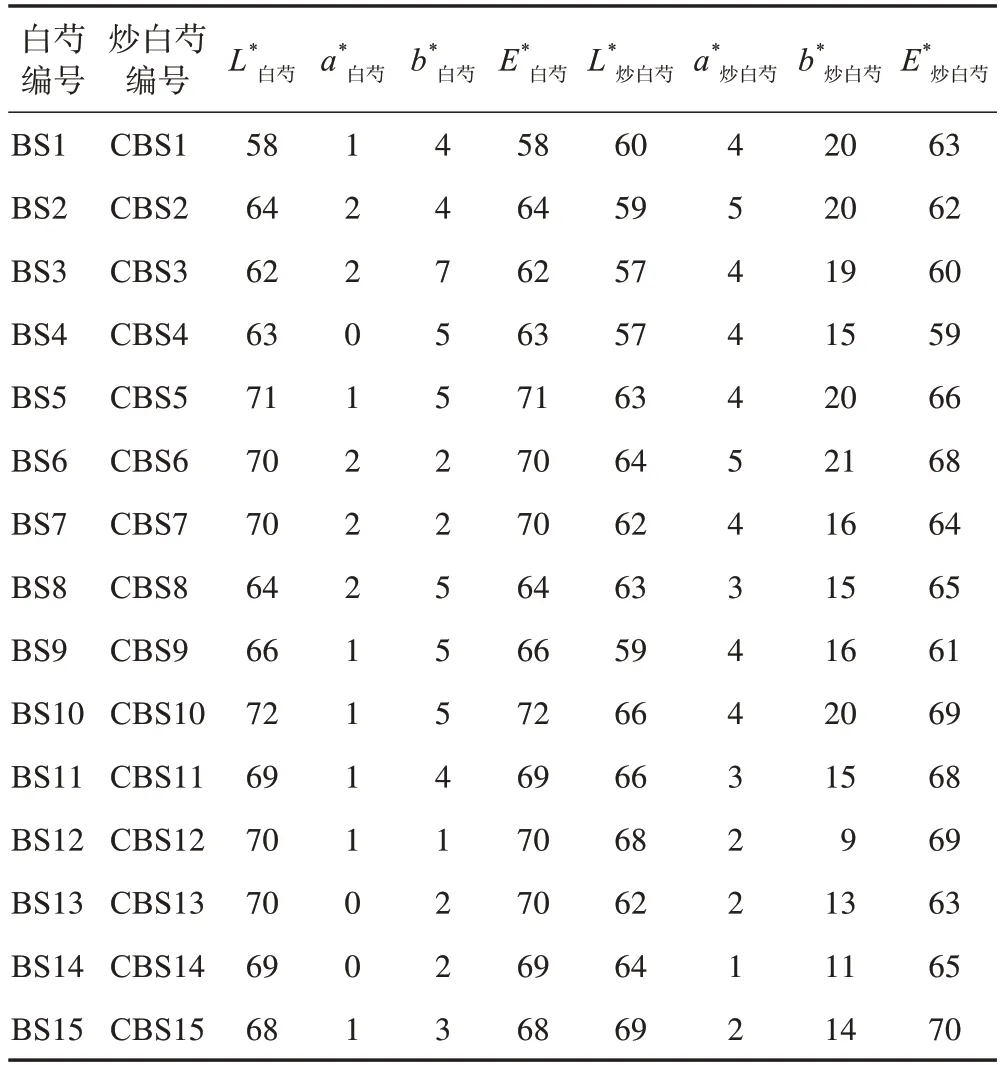
表3 15批白芍及炒白芍粉末色度值

表4 15批白芍及炒白芍粉末色差值

图6 15批白芍及炒白芍色彩图像
Lab 色彩模式中L*值表示物体明暗程度,a*、b*值代表不同色彩通道的色度(a通道包括的颜色是从低亮度值的深绿色到灰色再到高亮度值的亮粉红色,b 通道则是从低亮度值的深蓝色到灰色再到高亮度值的黄色),样品颜色可用总色值(E*)表达。

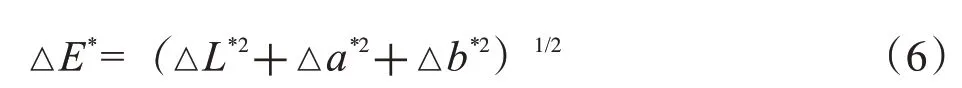
△E*用于表达生品到炮制品的颜色变化,△E*值越大,代表炮制品与生品色度值相差越大,当△E*>3.5 时,其色差可被肉眼识别。由表2 可知,△E*为8~20,表明可明显识别同批次炒白芍炮制品与白芍生品。为1~7,为9~21,从b*范围也能看出,炮制后黄色明显加深,表明可从b*值来区分白芍的生品与炮制品。
3 讨论
3.1 供试品提取考察
本研究对不同提取溶剂进行考察,UPLC 特征图谱结果显示,以水与50%甲醇提取时,13 号色谱峰(1,2,3,4,6-五没食子酰葡萄糖)丢失;以乙醇为溶剂提取时,没食子酸的峰形不佳;以甲醇、稀乙醇为提取溶剂时,各峰峰形较好,因稀乙醇毒性较低,选取稀乙醇为提取溶剂。回流提取与超声提取2 种提取方式对特征图谱的影响较小,因超声提取较简便,选取超声提取;各共有峰提取率随着超声时间的增加有所增加,30 min后峰面积无明显变化,选取超声30 min。
3.2 色谱条件的考察
没食子酸最大吸收波长为215、275 nm,1,2,3,4,6-五没食子酰葡萄糖最大吸收波长为215、275 nm,儿茶素最大吸收波长为282 nm,芍药内酯苷、芍药苷、苯甲酸、苯甲酰芍药苷最大吸收波长为230 nm[12]。5-HMF最大吸收波长为280 nm[13]。因此,选择0~10 min时检测波长为280 nm,10 min 后为230 nm,炒白芍色谱峰丰富且5-HMF 响应值较高。本研究比较了0.5%冰乙酸、0.1%甲酸、0.05%磷酸和0.2%磷酸等流动相对白芍、炒白芍UPLC 特征图谱的影响,结果表明,流动相为0.05%磷酸溶液时,特征图谱峰信息较丰富,分离效果和响应值最优,因此选取流动相为0.05%磷酸溶液。考察了柱温25、30、35 ℃和流速0.20、0.25、0.30 mL·min-1,结果表明当柱温为30 ℃、流速为0.3 mL·min-1时,特征图谱色谱峰分离度高、峰形对称,可满足分析要求。
3.3 炒白芍炒制时间考察
本研究初步考察了炒制时间对炒白芍UPLC 特征图谱的影响。设置电陶炉功率为800 W,当锅底温度达到140 ℃时,取白芍饮片置炒锅内,分别炒5、10、15、20、30 min,结果未检测到白芍药材中有3 号色谱峰(5-HMF),炒制10 min 后5-HMF 出现,随着炒制时间继续增加,3 号(5-HMF)、2 号(没食子酸)、11 号(苯甲酸)色谱峰峰面积逐渐增加,6 号(儿茶素)、8 号(芍药内酯苷)、9 号(芍药苷)、16 号(苯甲酰芍药苷)色谱峰峰面积逐渐降低,13 号(1,2,3,4,6-五没食子酰葡萄糖)色谱峰峰面积有增有减,无明显规律;炒白芍的颜色也逐渐加深。白芍饮片经炒制后产生5-HMF,5-HMF 的产生与温度、炒制时间有关。本研究表明,饮片颜色的变化与成分含量有一定的相关性,后续可进一步探究。
5-HMF又名5-羟甲基-2-呋喃甲醛,分子中含有1个呋喃环,其由葡萄糖或果糖等单糖化合物在高温或弱酸等条件下脱水生成,在炮制的高温高热过程中随着加热时间延长其含量增加。5-HMF 存在药理活性但含有一定的不良反应。有研究发现,生脉散中的5-HMF 成分可能是益气生脉的物质基础,具有抗氧、保肝、改善血液微循环等药理作用[16]。而因5-HMF 有一定的遗传毒性、生殖毒性、致癌性,《中国药典》2020 年版对葡萄糖注射液、蜂蜜和某些含蜂蜜的制剂中的5-HMF 均进行了含量控制。本研究通过UPLC 特征图谱结合色度值,可有效鉴别白芍与炒白芍,为下一步对5-HMF 限量控制的研究、量化炒白芍炮制程度提供参考。

