虾血细胞虹彩病毒在青虾中的感染情况调查分析
曾建刚 ,郭琦 ,沈中华 ,陈杰 ,刘莉∗
(1.德清县农业技术推广中心,浙江 德清 313200;2.浙江省农业科学院 水生生物研究所,浙江 杭州 310021)
虾血细胞虹彩病毒 (Shrimp hemocyte iridescent virus,SHIV) 又称十足目虹彩病毒1(Decapod iridescent virus 1,DIV1),是双链线性DNA 病毒,基因组大小约为166 kb,其病毒粒子呈二十面体,大小约为150 nm[1-3]。SHIV 最早于2014 年在浙江某凡纳滨对虾养殖场中被发现,并鉴定和命名[1]。目前已经证实,SHIV 可以感染凡纳滨对虾、中国明对虾、脊尾白虾、罗氏沼虾、克氏原螯虾和日本沼虾,感染SHIV 的凡纳滨对虾会出现厌食、胃肠道清空、肝胰腺颜色变浅和死亡的临床症状[2-5]。
日本沼虾 (Macrobrachiumnipponense) 俗称河虾或青虾,是重要的淡水养殖品种,在众多淡水养殖虾种类中占有重要地位。德清被誉为 “青虾之乡”,日本沼虾是其重要的特色养殖品种,是农民养殖增收的主要途径[6]。近年在日本沼虾的养殖中出现较为普遍的产量不如预期甚至育苗过程也不顺利的现象,其中原因尚无报道。SHIV 在多种虾中被检测到,而对日本沼虾养殖的危害未见相关研究。鉴于此,本研究对德清县日本沼虾养殖塘中SHIV 的流行情况进行监测,分析了虾虹彩病毒感染青虾的病理特征,相关结果为后续探讨SHIV 对日本沼虾养殖的影响奠定了基础。
1 材料与方法
1.1 样品采集
2020 年在德清县设2 个采样点,分别位于下渚湖街道和钟管镇,于7—10 月共采样4 次,每次采集30 只以上青虾。2021 年在德清县设12 个采样点,分别位于下渚湖、钟管、新市、雷甸、新安和洛舍6 个乡镇或街道,于6、7 月分别进行采样,每次各点采集30 只以上青虾。
1.2 主要试剂和仪器
DNA 提取试剂盒QIAamp DNA Mini Kit (德国QIAGEN 公 司);PCR 反应试剂 (New England Biolabs 北京有限公司);引物由北京擎科生物科技有限公司合成。多样品组织研磨仪 (上海净信实业发展有限公司);PCR 仪 (北京东胜创新生物科技有限公司)。
1.3 样品处理与DNA 提取
每个养殖户取20 只以上的活虾,解剖取每只虾的肝胰腺至独立的离心管中研磨成组织匀浆,或根据实验需要混合解剖所得的肝胰腺,再研磨成组织匀浆,置于-40 ℃下保存。每个样品取25 mg,利用基因组DNA 提取试剂盒提取DNA,提取方法参照试剂盒操作手册。同时取样用于单只检测的虾肝胰腺,采用4%多聚甲醛和2.5%戊二醛固定,用于染色和电镜观察。
1.4 PCR 检测
以1.3 中提取的DNA 为模板,以SHIV-F1(5′-GGGCGGGAGATGGTGTTAGAT-3′) 和SHIV-R1(5′-TCGTTTCGGTACGAAGATGTA-3′) 进行巢式PCR 第一步扩增,反应体系为 2 × Master Mix 12.5 μL,10 μmol·L-1引物各0.5 μL,模板DNA 2.5 μL,ddH2O 9 μL。PCR 反应程序为95 ℃预变性3 min→95 ℃变性30 s→59 ℃复性30 s→72 ℃延伸30 s,共35 个循环,最后72 ℃延伸2 min。以第一步 PCR 的产物为模板,以SHIV-F2 (5′-CGGGAAACGATTCGTATTGGG-3′) 和SHIV-R2(5′-TTGCTTGATCGGCATCCTTGA-3′) 进行巢式PCR 第二步的扩增,反应体系为2×Master Mix 12.5 μL,10 μM 引物各0.5 μL,模板DNA 1 μL,ddH2O 10.5 μL。PCR 反应程序为95 ℃预变性3 min→95 ℃变性30 s→59 ℃复性30 s→72 ℃延伸20 s,共35 个循环,最后72 ℃延伸2 min,反应完毕后进行琼脂糖电泳分析。
1.5 肝胰腺的石蜡切片制作及HE 染色
将肝胰腺切割成1 mm 见方的组织块,在4%多聚甲醛中进行固定,使用不同浓度的乙醇和二甲苯对固定好的组织依次进行脱水和透明,浸蜡包埋后进行切片,将石蜡切片展平烘干后使用二甲苯脱蜡,并用不同浓度的乙醇逐级复水。分别用苏木素(Hematoxylin) 和伊红 (Eosin) 进行染色,随后将切片依次放入无水乙醇和二甲苯中进行脱水及透明,用中性树胶封片,通过光学显微镜观察,并采集图像进行分析。
1.6 透射电镜观察
将肝胰腺切割成1 mm 见方的组织块,在2.5%戊二醛固定液中于4 ℃固定过夜;弃去戊二醛固定液,加入足量磷酸缓冲液漂洗3 次,加入0.1 mol·L-1四氧化锇溶液固定2 h;弃去锇酸固定液,加入足量磷酸缓冲液漂洗3 次后,样品依次在50%、70%、80%、90%、95%的乙醇中进行梯度脱水,用无水乙醇脱水处理3 次,再在丙酮中脱水3 次。样品在丙酮与包埋剂1∶1 配置液中渗透1 h,在丙酮与包埋剂1∶3 配置液中渗透3 h,最后在纯包埋剂中渗透过夜。将样品加入纯包埋剂中,于70 ℃烘箱中加热聚合48 h。取出聚合完成的样品切片,用铜网吸附后置于透射电镜下观察,并采集图像。
2 结果与分析
2.1 日本沼虾中SHIV 的PCR 检测结果
2020 年在德清县2 个日本沼虾养殖户进行为期4 个月的病原跟踪监测,结果表明,日本沼虾中存在感染SHIV 的情况。表1 显示,在SHIV DNA的巢式PCR 检测中,7 和10 月养殖户A 和B 的日本沼虾样品的SHIV 检测结果均呈阳性;8 和9 月分别在养殖户A 和B 的日本沼虾样品中检测到SHIV 的特异性核酸片段。2021 年在对德清地区6个行政村12 个养殖户的日本沼虾的检测中发现(表2),有6 个养殖户的日本沼虾的SHIV 呈阳性。进一步选取其中3 个养殖户再次采样,分别提取单只虾的DNA 进行巢式PCR 检测,结果显示,日本沼虾SHIV 的感染率在10%~20%。

表1 不同采样时间下日本沼虾中SHIV 的PCR 检测结果

表2 不同养殖户的日本沼虾中的SHIV 的PCR 检测结果
2.2 SHIV 对日本沼虾肝胰腺组织结构的影响
肝胰腺的HE 染色结果显示,SHIV 检测为阴性的日本沼虾肝胰腺的细胞结构正常,分布较为均匀;SHIV 检测为阳性的日本沼虾肝胰腺中分泌细胞和内部转运泡数量增加,储存细胞数量有所减少,管腔体积变大,存在核固缩现象 (图1)。

图1 感染SHIV 对日本沼虾肝胰腺显微结构的影响
2.3 日本沼虾肝胰腺组织中SHIV 的电镜观察
分别取SHIV 的巢式PCR 结果为阴性和阳性的日本沼虾肝胰腺包埋并切片后,在透射电镜下进行观察。SHIV 为阴性的肝胰腺细胞中未观察到病毒粒子 (图2 中A、B)。在SHIV 检测为阳性的日本沼虾肝胰腺中,观察到直径约为150 nm 类似病毒粒子的结构,显示SHIV 能够感染日本沼虾的肝胰腺,并进入其细胞质 (图2 中C~F)。
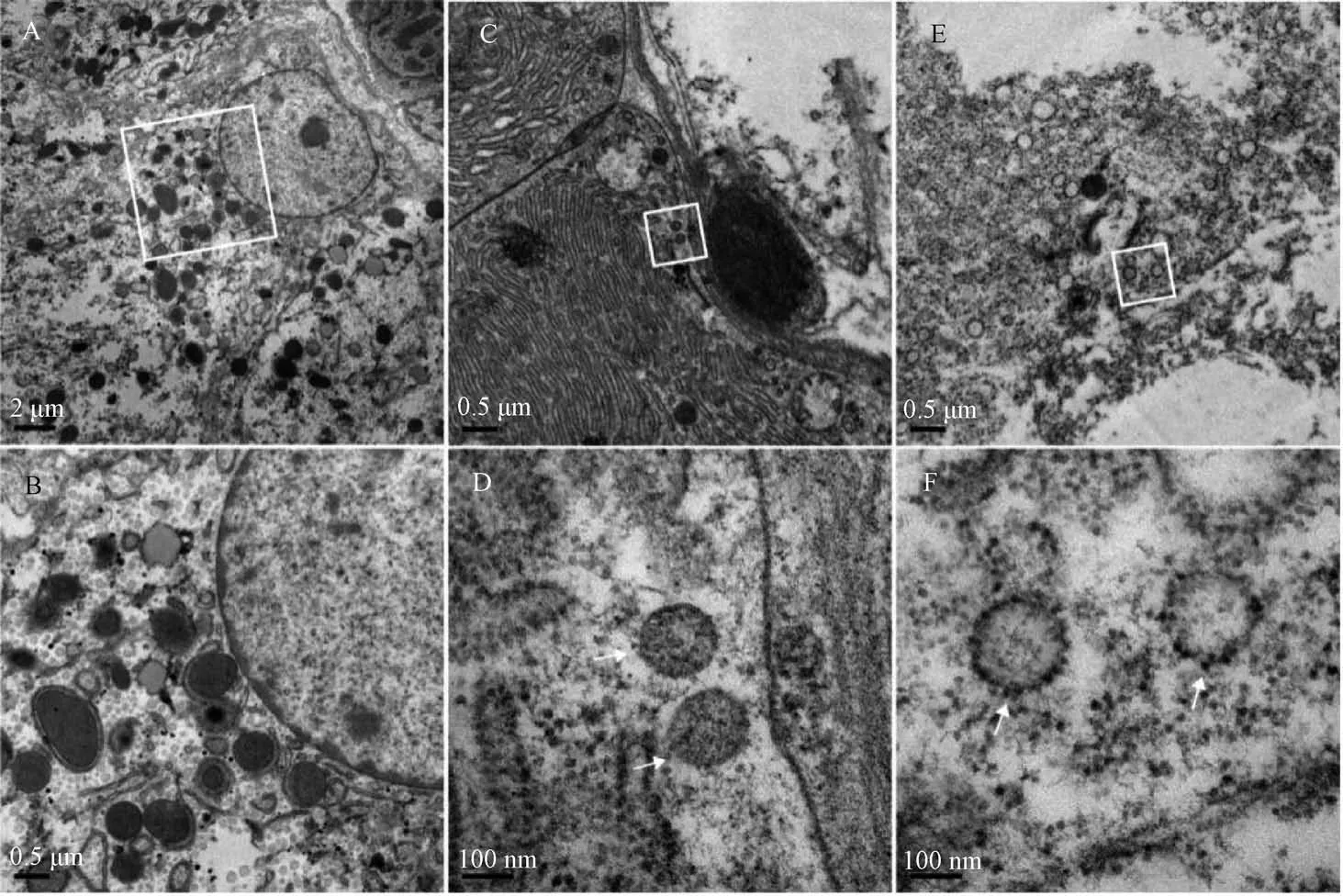
图2 日本沼虾肝胰腺肝小管上皮细胞内SHIV 的病毒粒子
3 讨论
虾血细胞虹彩病毒发现至今未满10 a,由全国的SHIV 监测结果可知,目前已在浙江、广东、河北、江苏等省市及沿海地区的对虾养殖场中检测到SHIV[1,7]。浙江德清县被誉为 “青虾之乡”,日本沼虾是该地区主要的养殖品种。2020 和2021 年的调查结果显示,SHIV 在德清地区的日本沼虾中普遍存在。其中,2020 年的养殖户A 和2021 年的养殖户1 为同一家,其SHIV 的检测结果在跟踪调查中均为阳性,显示SHIV 可以一直存在于养殖塘中,可能对日本沼虾的养殖产生威胁。德清县的青虾养殖一般采用人工培育幼虾的方式,在5 月初选择怀卵量大且较为健壮的亲虾至繁殖池塘中,待幼虾孵出20 d 后,再捕出放养,在之后的1 a 内捕大留小,产量和经济利润较为可观[8]。然而这种模式缺乏对亲虾的病原筛查,养殖时间较长,容易造成病毒传播。本研究在2021 年5—6 月及2020 年7—10 月的病原监测中均检测到SHIV 的存在,提示该模式可能存在使病毒扩散的风险。
目前对SHIV 的研究主要集中在凡纳滨对虾上,在患病虾组织切片中可以普遍观察得到嗜酸性包涵体和核固缩现象。透射电镜观察显示,患病虾的肝胰腺、造血组织、肌肉、步足和游泳足中均存在SHIV 病毒粒子,其大小约为150 nm,呈典型的二十面体形状[1]。通过投喂和反向灌肠SHIV,可使凡纳滨对虾累积死亡率高达100%[1];通过注射感染可使脊尾白虾的累积死亡率达到76%,通过投喂感染的死亡率也可达到50%[5],因此,SHIV已成为我国对虾养殖的重大威胁之一。本研究在通过巢式PCR 检测到SHIV 的日本沼虾肝胰腺组织切片中观察到核固缩现象,透射电镜观察显示,SHIV 阳性虾的肝胰腺中存在类似SHIV 病毒粒子的结构,大小约为150 nm,主要存在于细胞质中。有研究表明,日本沼虾感染SHIV 后的病毒载量显著低于罗氏沼虾和凡纳滨对虾,这可能是SHIV 对日本沼虾的影响较为有限的原因[4]。本研究仅对采样的虾进行HE 染色和透射电镜观察,初步探讨了SHIV 对日本沼虾的影响,要明确SHIV 与日本沼虾患病的关系,还需进行更深入的研究。
日本沼虾中常见的病害主要有固着类纤毛虫病、霉菌病、丝状细菌病、红体病、黑鳃病等[9]。感染SHIV 的日本沼虾的肝胰腺存在一定程度的病变,可能会影响其正常代谢功能,从而引起感染SHIV 的日本沼虾对其他病原的抵抗力降低,导致更易受寄生虫或细菌性病害的影响。虾类病害的发生与养殖环境和气温变化有关。有研究发现,水质中的总氮和水温对SHIV 在凡纳滨对虾中的发病情况具有较大的影响[10]。因此,注意日本沼虾的亲虾育种过程中的病害监测工作,加强青虾养殖过程中的水质条件管理,重视对病害的预防,能有效降低SHIV 对日本沼虾养殖的影响。

