2-取代苯基-5-取代苯甲酰胺基-1,3,4-噻二唑的合成、抑菌活性及三维定量构效关系
王三艳, 彭雅琦, 娄佳玉, 王美怡
(天津科技大学 化工与材料学院,天津 300457)
以五元杂环1,3,4-噻二唑为核心骨架的化合物具有多种生物活性[1],由此已开发出杀菌剂[2]、除草剂[3]、植物生长调节剂[4]和杀虫剂[5]等多种农药品种;而酰胺类化合物因含有易与有机体形成氢键的 -CONH- 基团而在农药领域的应用备受重视[6-7]。
基于结构的小分子三维定量构效关系 (3D-QSAR)研究,可为1,3,4-噻二唑酰胺类化合物的进一步优化以及设计开发潜在的、具有较高抑菌活性的化合物提供理论依据。Zong 等[8]将1,3,4-噻二唑与D-木呋喃糖拼接,并针对化合物结构与其对油菜菌核病菌Sclerotinia sclerotiorum的抑制活性间的关系,建立了比较分子力场分析 (CoMFA) 和比较分子相似性指数分析 (CoMSIA) 模型,提出了一种通过改变取代基的亲水性、静电性质和体积大小来增强化合物抗真菌活性的方法。Chen 等[9]将氟吡菌酰胺中的烷基链转换为1,3,4-噻二唑环,通过其所建立的CoMFA 和CoMSIA模型研究表明,氟代乙酯和砜基结构对该系列化合物抑菌活性的提高至关重要。Chen 等[10]建立了由新型诺卜衍生的1,3,4-噻二唑硫脲类化合物对番茄早疫病菌Alternaria solani抑制活性的CoMFA 模型,并进行了分析。结果表明,当连接硫脲的苯环间位取代基为硝基或溴时,化合物展现出良好的抑菌活性,在50 μg/mL 下,抑制率分别为87.9%与88.2%。
为了寻找高效、低毒的农药先导化合物[11-13],根据活性叠加原理,本研究以1,3,4-噻二唑为基本骨架,其中引入含有酰胺键的活性基团,设计合成了33 个1,3,4-噻二唑酰胺类化合物 (合成路线见图式1),其中23 个为新化合物,采用核磁共振氢谱 (1H NMR) 和高分辨质谱 (HRMS) 对其结构进行了表征;初步对目标化合物的抗真菌活性进行了筛选并进行了3D-QSAR 研究,建立了CoMFA与CoMSIA 模型,旨在为具有高杀菌活性的新农药分子的设计与合成提供有益参考。
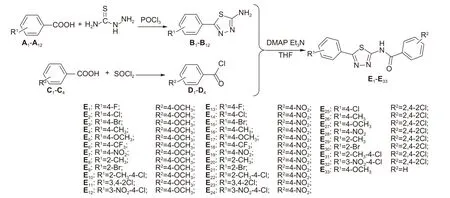
图式1 目标化合物E1~E33 的合成路线Scheme 1 Synthetic routes of target compounds E1-E33
1 实验部分
1.1 试剂与仪器
试剂均为市售分析纯,未经处理直接使用。百菌清(chlorothalonil)和多菌灵(carbendazim),均购自天津索罗门生物科技有限公司;4-二甲氨基吡啶(DMAP),购自阿拉丁化学试剂有限公司;根霉Rhizopus nigricans、青霉Penicillium glaucum、灰霉Botrytis cinerea、交链孢霉Alternaria brassicae和黑曲霉Aspergillus niger,均由天津科技大学菌种保藏中心提供。所用试剂均为市售分析纯。
ZF-20C 型暗箱三用紫外分析仪,上海骥辉科学分析仪器;JB/T5520 型电热鼓风干燥箱,上海苏达实验仪器有限公司;HWCL-3 型集热式恒温磁力搅拌浴,郑州长城科贸公司;DW-3 型数显电动搅拌器,巩义市予华仪器公司;X-4 型数字显微熔点仪,北京福凯仪器公司;ME204E/02 型精密电子天平,梅特勒-托利多仪器公司;SHZ-D型循环水式真空泵,巩义市予华仪器公司;FTIR650型傅里叶变换红外光谱 (IR) 仪,天津港东科技;Ascend TM 400 型核磁共振 (NMR) 仪,Bruker;岛津LC-IT-TOF 型高分辨液质联用 (HRMS) 仪,日本岛津公司。
1.2 化合物的合成
1.2.1 中间体B1~B12的合成 参考文献方法[14]进行,稍有改进。在250 mL 四口烧瓶中加入化合物A (40 mmol)、氨基硫脲 (40 mmol) 和1,4-二氧六环 (10 mL),室温下搅拌5 min 后,于冰水浴下缓慢滴入三氯氧磷 (14 mL),温度保持在25 ℃以下。滴毕,撤去冰水浴,于80 ℃反应1 h。撤去热源,将反应瓶置于冰水浴中缓慢加入60 mL 蒸馏水,温度保持在30 ℃以下。再升温至80 ℃反应5 h,用薄层色谱 (展开剂为乙酸乙酯) 监测至反应完全。撤去热源,加入质量分数为40% 的NaOH 溶液调节pH 值至7~8,待有大量固体析出时抽滤,用蒸馏水洗涤3 次,无水乙醇重结晶,过滤,烘干,得中间体B1~B12。
2-氨基-5-(4-氟苯基)-1,3,4-噻二唑 (B1):白色固体,产率60%,m.p. 235~236 ℃(文献[15]:238~240 ℃);IR (KBr),ν/cm-1: 3 245, 3 080, 1 608, 1 505, 1 217, 837;1H NMR (400 MHz, DMSO-d6),δ: 7.79~7.83 (m, 2H, Ar-H), 7.42 (s, 2H,NH2), 7.29~7.34 (m, 2H, Ar-H)
2-氨基-5-(4-氯苯基)-1,3,4-噻二唑 (B2):浅黄色固体,产率60%,m.p. 231~232 ℃(文献值[15]:226~228 ℃);IR(KBr),ν/cm-1: 3 279, 3 086, 1 624, 1 511, 1 262, 826;1H NMR(400 MHz, DMSO-d6),δ: 7.77 (d,J= 8 Hz, 2H, Ar-H), 7.53(d,J= 8 Hz, 2H, Ar-H), 7.48 (s, 2H, NH2)。
2-氨基-5-(4-溴苯基)-1,3,4-噻二唑 (B3):浅黄色固体,产率69%,m.p. 220~221 ℃(文献[15]:216~218 ℃);IR(KBr),ν/cm-1: 3 262, 3 086, 1 639, 1 504, 1 257, 831;1H NMR(400 MHz, DMSO-d6),δ: 7.71 (d,J= 8 Hz, 2H, Ar-H), 7.67(d,J= 8 Hz, 2H, Ar-H), 7.49 (s, 2H, NH2)。
2-氨基-5-(4-甲基苯基)-1,3,4-噻二唑 (B4):白色固体,产率57%,m.p. 210~211 ℃(文献值[15]:219~220 ℃);IR(KBr),ν/cm-1: 3 273, 3 086, 1 630, 1 505, 1 262, 814;1H NMR(400 MHz, DMSO-d6),δ: 7.63 (d,J= 8 Hz, 2H, Ar-H), 7.35(s, 2H, NH2), 7.27 (d,J= 8 Hz, 2H, Ar-H), 2.34 (s, CH3)。
2-氨基-5-(4-甲氧基苯基)-1,3,4-噻二唑 (B5):白色固体,产率52%,m.p. 184~185 ℃(文献值[15]:242~243 ℃);IR (KBr),ν/cm-1: 3 375, 3 103, 1 636, 1 505, 1 239, 826;1H NMR (400 MHz, DMSO-d6),δ: 7.68 (d,J= 8 Hz, 2H, Ar-H), 7.29 (s, 2H, NH2), 7.02 (d,J= 8 Hz, 2H, Ar-H), 3.80 (s,3H, OCH3)。
2-氨基-5-(4-三氟甲基苯基)-1,3,4-噻二唑 (B6):白色固体,产率44%,m.p. 238~239 ℃(文献值[15]:242~243 ℃);IR (KBr),ν/cm-1: 3 290, 3 126, 1 613, 1 505, 1 126, 843;1H NMR (400 MHz, DMSO-d6),δ: 7.97 (d,J= 8 Hz, 2H, Ar-H), 7.83 (d,J= 8 Hz, 2H, Ar-H), 7.61 (s, 2H, NH2)。
2-氨基-5-(4-硝基苯基)-1,3,4-噻二唑 (B7):黄色固体,产率67%,m.p. 254~255 ℃(文献值[16]:256~258 ℃);IR(KBr),ν/cm-1: 3 279, 3 109, 1 630, 1 500, 1 098, 848;1H NMR(400 MHz, DMSO-d6),δ: 8.30 (d,J= 8 Hz, 2H, Ar-H), 8.02(d,J= 8 Hz, 2H, Ar-H), 7.73 (s, 2H, NH2)。
2-氨基-5-(2-甲基苯基)-1,3,4-噻二唑 (B8):白色固体,产率52%,m.p. 189~190 ℃(文献值[15]:199 ℃);IR (KBr),ν/cm-1: 3 290, 3 109, 1 619, 1 500, 1 035, 746;1H NMR (400 MHz, DMSO-d6),δ: 7.53(d,J= 8 Hz, 1H, Ar-H), 7.35 (s, 2H,Ar-H), 7.34 (s, 2H, NH2), 7.27~7.31 (m, 1H, Ar-H), 2.48 (s,3H, CH3)。
2-氨基-5-(2-溴苯基)-1,3,4-噻二唑 (B9):浅黄色固体,产率47%,m.p. 184~185 ℃(文献值[15]:202~203 ℃);IR(KBr),ν/cm-1: 3 335, 3 069, 1 619, 1 517, 1 279, 752;1H NMR(400 MHz, DMSO-d6),δ: 7.88 (d,J= 8 Hz, 1H, Ar-H), 7.78(d,J= 8 Hz, 1H, Ar-H), 7.49~7.52 (m, 1H, Ar-H), 7.44 (s, 2H,NH2), 7.38~7.42 (m, 1H, Ar-H)。
2-氨基-5-(2-甲基-4-氯苯基)-1,3,4-噻二唑 (B10):白色固体,产率58%,m.p. 209~210 ℃(无文献报道);IR(KBr),ν/cm-1: 3 279, 3 103, 1 630, 1 505, 1 245, 791;1H NMR(400 MHz, DMSO-d6),δ: 7.29 (s, 2H, NH2), 7.26 (d,J= 8 Hz,1H, Ar-H), 7.22 (dd,J= 8 Hz, 1H, Ar-H), 7.10 (d,J= 8 Hz,1H, Ar-H), 2.15 (s, 3H, CH3)。
2-氨基-5-(3,4-二氯苯基)-1,3,4-噻二唑 (B11):浅黄色固体,产率57%,m.p. 207~208 ℃(文献值[16]:202~203 ℃);IR (KBr),ν/cm-1: 3 267, 3 080, 1 636, 1 511, 1 126, 820;1H NMR (400 MHz, DMSO-d6),δ: 7.97 (s, 1H, Ar-H), 7.71(s, 2H, Ar-H), 7.59 (s, 2H, NH2)。
2-氨基-5-(3-硝基-4-氯苯基)-1,3,4-噻二唑 (B12):黄色固体,产率62%,m.p. 198~199 ℃(文献值[15]:201~202 ℃);IR (KBr),ν/cm-1: 3 273, 3 109, 1 624, 1 500, 1 126, 826;1H NMR (400 MHz, DMSO-d6),δ: 8.40 (s, 1H, Ar-H), 8.04(dd,J= 8 Hz, 1H, Ar-H), 7.86 (d,J= 8 Hz, 1H, Ar-H), 7.67 (s,2H, NH2)。
1.2.2 中间体D1~D4的合成 参考文献方法[17]进行。在配有尾气吸收装置的250 mL 四口烧瓶中加入化合物C (50 mmol),冰水浴下缓慢滴加二氯亚砜 (13 mL)。滴毕,撤去冰水浴,升温至80 ℃反应约3 h 后,加入催化量的N,N-二甲基甲酰胺 (DMF),继续搅拌回流,用薄层色谱 (V(石油醚) :V(乙酸乙酯) = 1 : 1) 监测至反应完全。减压蒸馏,得中间体D1~D12,不经纯化直接投料下一步反应。
1.2.3 目标化合物E1~E33的合成 参考文献方法[18]进行。在250 mL 四口烧瓶中加入化合物B (5 mmol)、四氢呋喃 (THF,15 mL)、4-二甲氨基吡啶(DMAP,0.25 mmol) 和三乙胺 (5 mmol),室温搅拌5 min 后,冰水浴下逐滴加入溶解于四氢呋喃(5 mL) 的化合物D (5 mmol),温度保持在20 ℃以下。滴毕,用薄层色谱 (V(石油醚) :V(乙酸乙酯) =1 : 2) 监测至反应完全。撤去冰水浴,加入质量分数为30%的Na2CO3溶液3 mL、蒸馏水50 mL,搅拌30 min,待有大量固体析出时抽滤,用蒸馏水洗涤2 次,甲醇-DMF 混合溶剂重结晶,过滤,干燥,得目标化合物E1~E33。
2-(4-氟苯基)-5-(4-甲氧基苯甲酰胺基)-1,3,4-噻二唑(E1):白色固体,产率46%,m.p. 299~300 ℃;IR (KBr),ν/cm-1: 3 165, 2 916, 1 675, 1 250, 826, 729;1H NMR (400 MHz, DMSO-d6),δ: 12.99 (s, 1H, CONH), 8.16 (d,J= 8 Hz,2H, Ar-H), 8.03~8.06 (m, 2H, Ar-H), 7.37~7.42 (m, 2H, Ar-H), 7.11 (d,J= 8 Hz, 2H, Ar-H), 3.87 (s, 3H, OCH3);HRMS(m/z, ESI-):计算值C16H12FN3O2S[M + Na]+352.052 6,实测值352.052 7。
2-(4-氯苯基)-5-(4-甲氧基苯甲酰胺基)-1,3,4-噻二唑(E2):白色固体,产率47%,m.p. 289~290 ℃(文献值[19]:291~292 ℃);IR (KBr),ν/cm-1: 3 131, 2 927, 1 670, 1 245,831, 752;1H NMR (400 MHz, DMSO-d6),δ: 13.03 (s, 1H,CONH), 8.16 (d,J= 8 Hz, 2H, Ar-H), 8.01 (d,J= 8 Hz, 2H,Ar-H), 7.62 (d,J= 8 Hz, 2H, Ar-H), 7.11 (d,J= 8 Hz, 2H, Ar-H), 3.87 (s, 3H, OCH3); HRMS(m/z, ESI-):计算值C16H12ClN3O2S[M-H]-344.026 6,实测值344.026 4。
2-(4-溴苯基)-5-(4-甲氧基苯甲酰胺基)-1,3,4-噻二唑(E3):白色固体,产率52%,m.p. 294~296 ℃,IR (KBr),ν/cm-1: 3 149, 2 927, 1 670, 1 257, 826, 758;1H NMR (400 MHz, DMSO-d6),δ: 13.02 (s, 1H, CONH), 8.16 (d,J= 8 Hz,2H, Ar-H), 7.93(d,J= 8 Hz, 2H, Ar-H), 7.75 (d,J= 8 Hz, 2H,Ar-H), 7.11 (d,J= 8 Hz, 2H, Ar-H), 3.87 (s, 3H, OCH3);HRMS(m/z, ESI-):计算值C16H12BrN3O2S[M-H]-387.976 1,实测值387.976 1。
2-(4-甲基苯基)-5-(4-甲氧基苯甲酰胺基)-1,3,4-噻二唑(E4):白色固体,产率59%,m.p. 285~286 ℃(文献值[19]:286~287 ℃);IR (KBr),ν/cm-1: 3 137, 2 933, 1 670, 1 250,814, 752;1H NMR (400 MHz, DMSO-d6),δ: 12.94 (s, 1H,CONH), 8.16 (d,J= 8 Hz, 2H, Ar-H), 7.86 (d,J= 8 Hz, 2H,Ar-H), 7.36 (d,J= 8 Hz, 2H, Ar-H), 7.11 (d,J= 8 Hz, 2H, Ar-H), 3.87 (s, 3H, OCH3), 2.38 (s, 3H, CH3); HRMS(m/z,ESI-):计算值C17H15N3O2S[M + Na]+348.077 7,实测值348.077 7。
2-(4-甲氧基苯基)-5-(4-甲氧基苯甲酰胺基)-1,3,4-噻二唑 (E5):白色固体,产率62%,m.p. 288~289 ℃(文献值[19]:290~291 ℃);IR (KBr),ν/cm-1: 3 142, 2 927, 1 608, 1 250,826, 741;1H NMR (400 MHz, DMSO-d6),δ: 12.94 (s, 1H,CONH), 8.15 (d,J= 8 Hz, 2H, Ar-H), 7.92 (d,J= 8 Hz, 2H,Ar-H), 7.12 (d,J= 8 Hz, 2H, Ar-H), 7.09 (d,J= 8 Hz, 2H, Ar-H), 3.87 (s, 3H, OCH3), 3.84 (s, 3H, OCH3); HRMS(m/z,ESI-):计算值C17H15N3O3S[M + Na]+364.072 6,实测值364.071 4。
2-(4-三氟甲基苯基)-5-(4-甲氧基苯甲酰胺基)-1,3,4-噻二唑 (E6):白色固体,产率45%,m.p. 297~298 ℃,IR(KBr),ν/cm-1: 3 160, 2 933, 1 658, 1 257, 837, 758;1H NMR(400 MHz, DMSO-d6),δ:13.11 (s, 1H, CONH), 8.17 (d,J= 8 Hz, 2H, Ar-H), 8.11 (d,J= 8 Hz, 2H, Ar-H), 7.91 (d,J= 8 Hz,2H, Ar-H), 7.11 (d,J= 8 Hz, 2H, Ar-H), 3.87 (s, 3H, OCH3);HRMS(m/z,ESI-):计算值C17H12F3N3O2S[M-H]-378.053 0,实测值378.053 1。
2-(4-硝基苯基)-5-(4-甲氧基苯甲酰胺基)-1,3,4-噻二唑(E7):白色固体,产率51%,m.p. 338~339 ℃(文献值[19]:340~341 ℃);IR (KBr),ν/cm-1: 3 137, 2 922, 1 658, 1 250,843, 746;1H NMR (400 MHz, DMSO-d6),δ: 13.18 (s, 1H,CONH), 8.37 (d,J= 8 Hz, 2H, Ar-H), 8.28 (d,J= 8 Hz, 2H,Ar-H), 8.17 (d,J= 8 Hz, 2H, Ar-H), 7.12 (d,J= 8 Hz, 2H, Ar-H), 3.87 (s, 3H, OCH3); HRMS(m/z,ESI-):计算值C16H12N4O4S[M-H]-355.050 6,实测值355.051 3。
2-(2-甲基苯基)-5-(4-甲氧基苯甲酰胺基)-1,3,4-噻二唑(E8):白色固体,产率56%,m.p. 220~221 ℃,IR (KBr),ν/cm-1: 3 126, 2 916, 1 670, 1 250, 831, 752;1H NMR (400 MHz, DMSO-d6),δ: 12.97 (s, 1H, CONH), 8.16 (d,J= 8 Hz,2H, Ar-H), 7.71 (d,J= 8 Hz, 1H, Ar-H), 7.43 (d,J= 8 Hz, 2H,Ar-H), 7.38 (d,J= 8 Hz, 1H, Ar-H), 7.11 (d,J= 8 Hz, 2H, Ar-H), 3.87 (s, 3H, OCH3), 2.54 (s, 3H, CH3); HRMS(m/z,ESI-):计算值C17H15N3O2S[M + Na]+348.077 7,实测值348.078 8。
2-(2-溴苯基)-5-(4-甲氧基苯甲酰胺基)-1,3,4-噻二唑(E9):白色固体,产率76%,m.p. 268~269 ℃,IR (KBr),ν/cm-1: 3 131, 2 922, 1 670, 1 257, 843, 758;1H NMR (400 MHz, DMSO-d6),δ: 13.04 (s, 1H, CONH), 8.16 (d,J= 8 Hz,2H, Ar-H), 7.99 (d,J= 8 Hz, 1H, Ar-H), 7.86 (d,J= 8 Hz, 1H,Ar-H), 7.55~7.59 (m, 1H, Ar-H), 7.47~7.51 (m, 1H, Ar-H),7.11 (d,J= 8 Hz, 2H, Ar-H), 3.87 (s, 3H, OCH3); HRMS(m/z,ESI-):计算值C16H12BrN3O2S[M-H]-387.976 1,实测值387.975 5。
2-(2-甲基-4-氯苯基)-5-(4-甲氧基苯甲酰胺基)-1,3,4-噻二唑 (E10):白色固体,产率34%,m.p. 223~224 ℃,IR(KBr),ν/cm-1: 3 188, 2 916, 1 658, 1 257, 843, 746;1H NMR(400 MHz, DMSO-d6),δ: 12.93 (s, 1H, CONH), 8.13 (d,J=8 Hz, 2H, Ar-H), 7.23~7.28 (m, 2H, Ar-H), 7.15 (d,J= 8 Hz,1H, Ar-H), 7.10 (d,J= 8 Hz, 2H, Ar-H), 3.86 (s, 3H, OCH3),2.2 0 (s, 3 H, C H3); H R M S(m/z,E S I-):计算值C17H14ClN3O2S[M-H]-358.049 3,实测值358.049 5。
2-(3,4-二氯苯基)-5-(4-甲氧基苯甲酰胺基)-1,3,4-噻二唑 (E11):白色固体,产率74%,m.p. 340~341 ℃,IR(KBr),ν/cm-1: 3 142, 2 922, 1 658, 1 250, 837, 746;1H NMR(400 MHz, DMSO-d6),δ: 13.09 (s, 1H, CONH), 8.23 (s, 1H,Ar-H), 8.16 (d,J= 8 Hz, 2H, Ar-H), 7.96 (dd,J= 8 Hz, 1H,Ar-H), 7.81 (d,J= 8 Hz, 1H, Ar-H), 7.11 (d,J= 8 Hz, 2H, Ar-H), 3.87 (s, 3H, OCH3); HRMS(m/z,ESI-):计算值C16H11Cl2N3O2S[M-H]-377.987 6,实测值377.986 7。
2-(3-硝基-4-氯苯基)-5-(4-甲氧基苯甲酰胺基)-1,3,4-噻二唑 (E12):浅黄色固体,产率63%,m.p. 299~300 ℃,IR(KBr),ν/cm-1: 3 137, 2 922, 1 670, 1 262, 837, 752;1H NMR(400 MHz, DMSO-d6),δ: 13.09 (s, 1H, CONH), 13.16 (s, 1H,CONH), 8.63 (d,J= 8 Hz, 1H, Ar-H), 8.27 (dd,J= 8 Hz, 1H,Ar-H), 8.15 (d,J= 8 Hz, 2H, Ar-H), 7.93 (d,J= 8 Hz, 1H, Ar-H), 7.11 (d,J=8Hz, 2H, Ar-H), 3.87 (s, 3H, OCH3);HRMS(m/z, ESI-):计算值C16H11ClN4O4S[M-H]-389.011 7,实测值389.010 8。
2-(4-氟苯基)-5-(4-硝基苯甲酰胺基)-1,3,4-噻二唑(E13):浅黄色固体,产率90%,m.p. 342~343 ℃(文献值[19]:343~344 ℃);IR (KBr),ν/cm-1: 3 109, 2 916, 1 675, 1 245,837, 724;1H NMR (400 MHz, DMSO-d6),δ: 13.09 (s, 1H,CONH), 13.57 (s, 1H, CONH), 8.40 (d,J= 8 Hz, 2H, Ar-H),8.35 (d,J= 8 Hz, 2H, Ar-H), 8.05~8.08 (m, 2H, Ar-H),7.39~7.43 (m, 2H, Ar-H); HRMS(m/z, ESI-):计算值C15H9FN4O3S[M-H]-343.030 7,实测值343.030 6。
2-(4-氯苯基)-5-(4-硝基苯甲酰胺基)-1,3,4-噻二唑(E14):浅黄色固体,产率63%,m.p. 337~338 ℃(文献值[19]:337~339 ℃);IR (KBr),ν/cm-1: 3 109, 2 916, 1 675, 1 245,837, 724;1H NMR (400 MHz, DMSO-d6),δ: 13.63 (s, 1H,CONH), 8.39 (d,J= 8 Hz, 2H, Ar-H), 8.34 (d,J= 8 Hz, 2H,Ar-H), 8.01 (d,J= 8 Hz, 2H, Ar-H), 7.62 (d,J= 8 Hz, 2H);HRMS(m/z, ESI-):计算值C15H9ClN4O3S[M-H]-359.001 1,实测值359.001 5。
2-(4-溴苯基)-5-(4-硝基苯甲酰胺基)-1,3,4-噻二唑(E15):浅黄色固体,产率55%,m.p. 348 ℃,IR (KBr),ν/cm-1: 3 109, 2 922, 1 670, 1 245, 837, 764;1H NMR (400 MHz, DMSO-d6),δ: 13.63 (s, 1H, CONH), 8.40 (d,J= 8 Hz,2H, Ar-H), 8.35 (d,J= 8 Hz, 2H, Ar-H), 7.95 (d,J= 8 Hz, 2H,Ar-H), 7.76 (d,J= 8 Hz, 2H, Ar-H); HRMS(m/z, ESI-):计算值C15H9BrN4O3S[M-H]-402.950 6,实测值402.950 1。
2-(4-甲基苯基)-5-(4-硝基苯甲酰胺基)-1,3,4-噻二唑(E16):浅黄色固体,产率68%,m.p. 339~340 ℃(文献值[19]:341~342 ℃);IR (KBr),ν/cm-1: 3 115, 2 927, 1 675, 1 257,843, 713;1H NMR (400 MHz, DMSO-d6),δ: 13.52 (s, 1H,CONH), 8.40 (d,J= 8 Hz, 2H, Ar-H), 8.35 (d,J= 8 Hz, 2H,Ar-H), 7.88 (d,J= 8 Hz, 2H, Ar-H), 7.37 (d,J= 8 Hz, 2H, Ar-H), 2.39 (s, 3H, CH3); HRMS(m/z, ESI-):计算值C16H12N4O3S[M + Na]+363.052 2,实测值363.054 0。
2-(4-甲氧基苯基)-5-(4-硝基苯甲酰胺基)-1,3,4-噻二唑(E17):浅黄色固体,产率58%,m.p. 346~347 ℃(文献值[19]:347~348 ℃),IR (KBr),ν/cm-1: 3 103, 2 916, 1 675, 1 257,826, 713;1H NMR (400 MHz, DMSO-d6),δ: 13.49 (s, 1H,CONH), 8.40 (d,J= 8 Hz, 2H, Ar-H), 8.34 (d,J= 8 Hz, 2H,Ar-H), 7.93 (d,J= 8 Hz, 2H, Ar-H), 7.11 (d,J= 8 Hz, 2H, Ar-H), 3.85 (s, 3H, OCH3); HRMS(m/z, ESI-):计算值C16H12N4O4S[M-H]-355.050 6,实测值355.051 2。
2-(4-三氟甲基苯基)-5-(4-硝基苯甲酰胺基)-1,3,4-噻二唑 (E18):浅黄色固体,产率83%,m.p.>390 ℃,IR (KBr),ν/cm-1: 3 115, 2 922, 1 670, 1 257, 860, 718;1H NMR (400 MHz, DMSO-d6),δ: 13.74 (s, 1H, CONH), 8.39 (d,J= 8 Hz,2H, Ar-H), 8.34 (d,J= 8 Hz, 2H, Ar-H), 8.21 (d,J= 8 Hz, 2H,Ar-H), 7.90 (d,J= 8 Hz, 2H, Ar-H); HRMS(m/z, ESI-):计算值C16H9F3N4O3S[M-H]-393.027 5,实测值393.027 4。
2-(4-硝基苯基)-5-(4-硝基苯甲酰胺基)-1,3,4-噻二唑(E19):浅黄色固体,产率81%,m.p.>390 ℃(文献值[19]:387~388 ℃),IR (KBr),ν/cm-1: 3 109, 2 916, 1 675, 1 302,848, 718;1H NMR (400 MHz, DMSO-d6),δ: 13.60 (s, 1H,CONH), 8.40 (d,J= 8 Hz, 2H, Ar-H), 8.35 (d,J= 8 Hz, 2H,Ar-H), 8.04~8.08 (m, 2H, Ar-H), 7.38~7.43 (m, 2H, Ar-H);HRMS(m/z, ESI-):计算值C15H9N5O5S[M-H]-370.025 2,实测值370.025 7。
2-(2-甲基苯基)-5-(4-硝基苯甲酰胺基)-1,3,4-噻二唑(E20):浅黄色固体,产率82%,m.p. 296~297 ℃,IR(KBr),ν/cm-1: 3 142, 2 973, 1 670, 1 307, 843, 752;1H NMR(400 MHz, DMSO-d6),δ: 13.65 (s, 1H, CONH), 8.40 (d,J= 8 Hz, 2H, Ar-H), 8.36 (d,J= 8 Hz, 2H, Ar-H), 7.72 (d,J= 8 Hz,1H, Ar-H), 7.45 (d,J= 8 Hz, 2H, Ar-H), 7.38 (d,J= 8 Hz, 1H,Ar-H), 2.51 (s, 3H, CH3); HRMS(m/z, ESI-):计算值C16H12N4O3S[M-H]-363.052 2,实测值363.051 6。
2-(2-溴苯基)-5-(4-硝基苯甲酰胺基)-1,3,4-噻二唑(E21):浅黄色固体,产率75%,m.p. 346~347 ℃,IR(KBr),ν/cm-1: 3 154, 2 927, 1 681, 1 250, 854, 764;1H NMR(400 MHz, DMSO-d6),δ: 13.65 (s, 1H, CONH), 8.41 (d,J= 8 Hz, 2H, Ar-H), 8.36 (d,J= 8 Hz, 2H, Ar-H), 8.01 (d,J= 8 Hz,1H, Ar-H), 7.88 (d,J= 8 Hz, 1H, Ar-H), 7.58~7.61 (m, 1H,Ar-H), 7.50~7.51 (m, 1H, Ar-H); HRMS(m/z, ESI-):计算值C15H9BrN4O3S[M-H]-402.950 6,实测值402.950 1。
2-(2-甲基-4-氯苯基)-5-(4-硝基苯甲酰胺基)-1,3,4-噻二唑 (E22):浅黄色固体,产率74%,m.p. 277~279 ℃,IR(KBr),ν/cm-1: 3 142, 2 916, 1 675, 1 250, 860, 718;1H NMR(400 MHz, DMSO-d6),δ: 13.55 (s, 1H, CONH), 8.39 (d,J= 8 Hz, 2H, Ar-H), 8.32 (d,J= 8 Hz, 2H, Ar-H), 7.24~7.28 (d,J=8 Hz, 2H, Ar-H), 7.16 (d,J= 8 Hz, 1H, Ar-H), 2.21 (s, 3H,CH3); HRMS(m/z, ESI-):计算值C16H11ClN4O3S[M-H]-373.024 0,实测值373.024 6。
2-(3,4-二氯苯基)-5-(4-硝基苯甲酰胺基)-1,3,4-噻二唑(E23):浅黄色固体,产率93%,m.p. 358~360 ℃,IR(KBr),ν/cm-1: 3 115, 2 922, 1 675, 1 296, 843, 706;1H NMR(400 MHz, DMSO-d6),δ: 13.66 (s, 1H, CONH), 8.40 (d,J=8 Hz, 2H, Ar-H), 8.36 (d,J= 8 Hz, 2H, Ar-H), 8.26 (d,J=8 Hz, 1H, Ar-H), 7.99~8.01 (m, 1H, Ar-H), 7.83 (d,J= 8 Hz,1H, Ar-H); HRMS(m/z, ESI-):计算值C15H8Cl2N4O3S[M-H]-393.970 0,实测值393.970 5。
2-(3-硝基-4-氯苯基)-5-(4-硝基苯甲酰胺基)-1,3,4-噻二唑 (E24):黄色固体,产率62%,m.p.>390 ℃,IR (KBr),ν/cm-1: 3 120, 2 916, 1 687, 1 307, 837, 752;1H NMR (400 MHz, DMSO-d6),δ: 13.57 (s, 1H, CONH), 8.38 (d,J= 8 Hz,2H, Ar-H), 8.29 (d,J= 8 Hz, 2H, Ar-H), 7.84 (d,J= 8 Hz, 1H,Ar-H), 7.79 (d,J= 8 Hz, 1H, Ar-H), 7.62 (dd,J= 8 Hz, 1H,Ar-H); HRMS(m/z, ESI-):计算值C15H8ClN5O5S[M-H]-403.993 4,实测值403.994 3。
2-(4-氯苯基)-5-(2,4-二氯苯甲酰胺基)-1,3,4-噻二唑(E25):浅黄色固体,产率38%,m.p. 273~274 ℃,IR(KBr),ν/cm-1: 3 149, 2 916, 1 670, 1 273, 831, 769;1H NMR(400 MHz, DMSO-d6),δ: 13.43 (s, 1H, CONH), 8.03 (d,J=8 Hz, 2H, Ar-H), 7.83 (d,J= 8 Hz, 1H, Ar-H), 7.77 (d,J=8 Hz, 1H, Ar-H), 7.64 (s, 1H, Ar-H), 7.61 (s, 2H, Ar-H);HRMS(m/z, ESI-):计算值C15H8Cl3N3OS[M-H]-381.938 1,实测值381.938 3。
2-(4-甲基苯基)-5-(2,4-二氯苯甲酰胺基)-1,3,4-噻二唑(E26):浅黄色固体,产率56%,m.p. 291~292 ℃,IR(KBr),ν/cm-1: 3 131, 2 922, 1 687, 1 307,809, 741;1H NMR(400 MHz, DMSO-d6),δ: 13.36 (s, 1H, CONH), 7.88 (d,J=8 Hz, 2H, Ar-H), 7.82 (d,J= 8 Hz, 1H, Ar-H), 7.76 (d,J=8 Hz, 1H, Ar-H), 7.59~7.62 (m, 1H, Ar-H), 7.36 (d,J= 8 Hz,2H, Ar-H), 2.39 (s, 3H, CH3); HRMS(m/z, ESI-):计算值C16H11Cl2N3OS[M-H]-361.992 7,实测值361.992 4。
2-(4-甲氧基苯基)-5-(2,4-二氯苯甲酰胺基)-1,3,4-噻二唑 (E27):浅白色固体,产率59%,m.p. 280~281 ℃,IR(KBr),ν/cm-1: 3 137, 2 927, 1 687, 1 302, 826, 729;1H NMR(400 MHz, DMSO-d6),δ: 13.28 (s, 1H, CONH), 7.93 (d,J=8 Hz, 2H, Ar-H), 7.82 (d,J= 8 Hz, 1H, Ar-H), 7.76 (d,J=8 Hz, 1H, Ar-H), 7.60 (dd,J= 8 Hz, 1H, Ar-H), 7.10 (d,J=8 Hz, 2H, Ar-H), 3.84 (s, 3H, OCH3); HRMS(m/z, ESI-):计算值C16H11Cl2N3O2S[M-H]-377.987 6,实测值377.986 3。
2-(4-硝基苯基)-5-(2,4-二氯苯甲酰胺基)-1,3,4-噻二唑(E28):浅白色固体,产率75%,m.p. 288~289 ℃,IR(KBr),ν/cm-1: 3 115, 2 922, 1 698, 1 307, 854, 746;1H NMR(400 MHz, DMSO-d6),δ: 13.57(s, 1H, CONH), 8.38 (d,J=8 Hz, 2H, Ar-H), 8.29 (d,J= 8 Hz, 2H, Ar-H), 7.84 (d,J=8 Hz, 1H, Ar-H), 7.79 (d,J= 8 Hz, 1H, Ar-H), 7.62 (dd,J=8 H z, 1 H, A r-H); H R M S(m/z, E S I-):计算值C15H8Cl2N4O3S[M-H]-392.962 1,实测值392.960 9。
2-(2-甲基苯基)-5-(2,4-二氯苯甲酰胺基)-1,3,4-噻二唑(E29):白色固体,产率65%,m.p. 234~235 ℃,IR (KBr),ν/cm-1: 3 149, 2 922, 1 693, 1 313, 826, 752;1H NMR (400 MHz, DMSO-d6),δ: 13.35 (s, 1H, CONH), 7.82 (d,J= 8 Hz,1H, Ar-H), 7.77 (d,J= 8 Hz, 1H, Ar-H), 7.72 (d,J= 8 Hz, 1H,Ar-H), 7.61 (dd,J= 8 Hz, 2H, Ar-H), 7.45 (d,J= 8 Hz, 2H,Ar-H), 7.38 (dd,J= 8 Hz, 1H, Ar-H), 2.54 (s, 3H, CH3);HRMS(m/z, ESI-):计算值C16H11Cl2N3OS[M-H]-361.992 7,实测值361.992 9。
2-(2-溴苯基)-5-(2,4-二氯苯甲酰胺基)-1,3,4-噻二唑(E30):白色固体,产率63%,m.p. 287~288 ℃,IR (KBr),ν/cm-1: 3 131, 2 922, 1 693, 1 319, 848, 752;1H NMR (400 MHz, DMSO-d6),δ: 13.43 (s, 1H, CONH), 7.99 (dd,J= 8 Hz,1H, Ar-H), 7.87 (dd,J= 8 Hz, 1H, Ar-H), 7.83 (d,J= 8 Hz,1H, Ar-H), 7.78 (d,J= 8 Hz, 1H, Ar-H), 7.60~7.63 (dd,J= 8 Hz,1H, Ar-H), 7.59~7.56 (dd,J= 8 Hz, 1H, Ar-H), 7.50~7.53 (m,1H, Ar-H); HRMS(m/z, ESI-):计算值C15H8BrCl2N3OS[M-H]-425.887 6,实测值425.886 3。
2-(2-甲基-4-氯苯基)-5-(2,4-二氯苯甲酰胺基)-1,3,4-噻二唑 (E31):浅黄色固体,产率64%,m.p. 249~250 ℃,IR(KBr),ν/cm-1: 3 165, 2 916, 1 693, 1 320, 838, 753;1H NMR(400 MHz, DMSO-d6),δ: 13.30 (s, 1H, CONH), 7.81 (d,J= 8 Hz,1H, Ar-H), 7.74 (d,J= 8 Hz, 1H, Ar-H), 7.58~7.61 (m, 1H,Ar-H), 7.23~7.29 (m, 2H, Ar-H), 7.15 (s, 1H, Ar-H), 2.20 (s,3H, CH3); HRMS(m/z, ESI-):计算值C16H10Cl3N3OS[M-H]-395.961 0,实测值395.960 2。
2-(3-硝基-4-氯苯基)-5-(2,4-二氯苯甲酰胺基)-1,3,4-噻二唑 (E32):白色固体,产率69%,m.p. 304~305 ℃,IR(KBr),ν/cm-1: 3 120, 2 905, 1 693,1 303, 826, 735;1H NMR(400 MHz, DMSO-d6),δ: 13.58 (s, 1H, CONH), 8.67 (d,J= 8 Hz,1H, Ar-H), 8.29~8.32 (m, 1H, Ar-H), 7.95 (d,J= 8 Hz, 1H,Ar-H), 7.77~7.83 (m, 2H, Ar-H), 7.60~7.67(m, 1H, Ar-H);HRMS(m/z, ESI-):计算值C15H7Cl3N4O3S[M-H]-426.923 2,实测值426.924 0。
2-(4-甲氧基苯基)-5-(苯甲酰胺基)-1,3,4-噻二唑 (E33):浅黄色固体,产率37%,m.p. 260~261 ℃(文献值[19]:261~262 ℃);IR (KBr),ν/cm-1: 3 126, 2 922, 1 670, 1 307,831, 706;1H NMR (400 MHz, DMSO-d6),δ: 13.10 (s, 1H,CONH), 8.14 (d,J= 8 Hz, 2H, Ar-H), 7.92 (d,J= 8 Hz, 2H,Ar-H), 7.87 (dd,J= 8 Hz, 1H, Ar-H), 7.55~7.59 (m, 2H, Ar-H), 7.10 (d,J= 8 Hz, 2H, Ar-H), 3.84 (s, 3H, OCH3);HRMS(m/z, ESI-):计算值C16H13N3O2S[M-H]-310.065 6,实测值310.065 9。
1.2.4 目标化合物的抑菌活性测试 采用菌丝生长速率法[20],测试目标化合物在50 μg/mL 下对5 种供试病原菌的离体抑菌活性。以多菌灵和百菌清为对照药剂。将0.05 g 待测化合物用1 mL DMSO溶解后,移取100 μL 加入至由2 mL 0.1%的吐温80 水溶液与8 mL 水组成的混合液中。取3 mL 上述溶液与27 mL 马铃薯葡萄糖琼脂培养基 (PDA)混合,最终制成质量浓度为50 μg/mL 的含药培养基。待其凝固后,接种直径5 mm 的供试菌种,置于28 ℃恒温培养箱中培养72 h。每个化合物重复3 次测量 (平均值 ± 相对标准偏差)。运用十字交叉法测量菌落直径,并与空白对照 (仅用DMSO 处理过的菌种) 进行对比,计算其抑制率。继而测定目标化合物在5、1、0.5、0.25 和0.1 μg/mL 下对黑曲霉的抑制率,采用软件GraphPad Prism 8 计算IC50值[21]。
1.2.5 CoMFA 和CoMSIA 模型的建立 使用SYBYL-X 2.0 软件,采用CoMFA 与CoMSIA 进行 3D-QSAR 分析。利用Sketch molecule 模块构造目标化合物的化学结构,利用Minimize 模块结合Tripos 力场和Gasteiger-Hüeckel 电荷,并采用Powell 能量梯度法对其进行能量最小化。最大迭代次数设置为10 000,收敛标准为0.209 2 kJ/mol,其他参数设置为默认值,创建分子表单。随机选取分子E1、E4、E8、E15、E16、E24、E25和E29为测试集,余下的26 个分子作为训练集。以抑制黑曲霉IC50值最高的分子E24作为模板分子,运用Align database 模板分别对训练集与测试集进行分子叠合,结果如图1 所示。以偏最小二乘法建模,采用留一法进行交叉验证,获得交叉验证系数q2与最佳主成分值N[22]。其中由q2可判定模型是否具有预测能力;当q2越接近于1 时,证明模型越具有统计显著性的预测能力;当0.4 <q2<1 时,说明模型可以考虑使用且具有统计显著性的预测能力;当q2<0 时,说明模型的预测能力低于均值预测能力。最佳主成分值N是通过主成分分析方法降维后得到的模型最佳的成分值,一般认为模型中的主成分数为统计样本数的1/3 左右可具有统计意义。采用非交叉验证,获得非交叉验证判定系数r2、统计方差比F、标准偏差SE。其中当r2>0.9,且接近于1 时,证明具有良好的相关性。统计方差比F代表统计数据的可信度,当F值大于临界值F0.05(9,16) = 2.55,F0.05(8,17) =4.39 时,说明该数据具有95%的可信度,随机性小于5%。标准偏差SE 越小则代表该组数据具有良好的准确性,SE 接近于0 时,模型的拟合能力最好。并通过交叉与非交叉验证得到的统计数据来评估模型的稳健性。
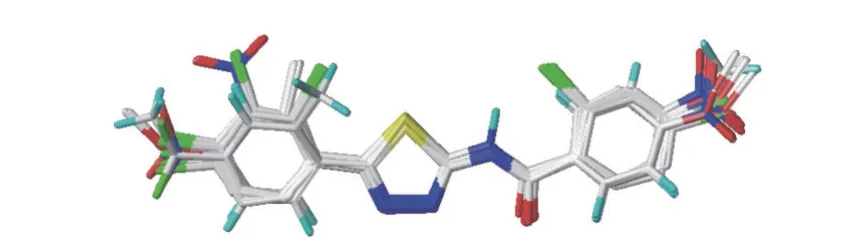
图1 1,3,4-噻二唑-2-氨基衍生物的结构叠合图Fig. 1 Superimposed image of 1,3,4-thiadiazol-2-amide derivatives structures
2 结果与讨论
2.1 目标化合物的合成及结构表征
首先尝试了以四氢呋喃为溶剂、三乙胺为缚酸剂、DMAP 为催化剂,由化合物B 与D 在加热条件下 (70~80 ℃) 进行反应生成目标化合物,但收率较低。后经优化发现,当温度保持在20 ℃左右时,反应能够顺利进行且产率较高。
在目标化合物的1H NMR 谱图中,在低场δ12.94~13.74 中出现的单峰为CONH 中的NH 质子吸收峰,在δ7.09~8.40 的多重峰为苯环上氢的吸收峰;δ3.87 处单峰是OCH3中氢的吸收峰,δ2.39为CH3中氢的吸收峰。目标化合物的HRMS 实测值与理论计算值一致,进一步确证了化合物的结构。
2.2 目标化合物的抑菌活性
结果(表1)表明,在50 μg/mL 下:化合物E24对根霉的抑制率达90.59%,与多菌灵 (98.30%) 的效果相当,且超过百菌清 (81.20%);化合物E17对青霉的抑制率为86.73%,与多菌灵 (84.55%) 的效果相当;化合物E12对灰霉的抑制率达88.18%,优于百菌清 (75.00%);化合物E7、E19、E21对交链孢霉的抑制率分别为89.16%、90.36%、90.96%,与多菌灵和百菌清的效果接近。其中目标化合物E1、E2、E29对所测真菌的抑制率均达80% 以上。通过初步分析目标化合物结构与抑菌活性之间的关系发现:取代苯甲酰氯的苯环上不同取代基的抑菌率高低排序为2,4-二氯 < 对甲氧基 < 对硝基;噻二唑环一侧苯环上连有吸电子基团,如含硝基、含氟 (化合物E1、E2、E13、E17) 时,化合物对所有菌种均有较好的抑制活性。

表1 目标化合物E1~E33 对供试病原真菌的抑制活性Table 1 Fungicidal activities of target compounds E1-E33 against tested pathogenic fungi
2.3 CoMFA 和CoMSIA 模型分析
对目标化合物的抗黑曲霉活性进行3D-QSAR的分析,如表2 所示,CoMFA 模型中立体场的贡献值大于静电场的贡献值,表明化合物的活性主要取决于范德华力的相互作用[23];而通过CoMSIA模型所计算的静电场的贡献值和疏水场的贡献值要大于其他场,由于该模型在计算相互作用时采用了与距离相关的高斯函数,可以有效地避免CoMFA 模型中由静电场与立体场函数形式所引起的缺陷,因此对目标化合物的静电场和疏水场影响最大,贡献值最多[24]。基于两种模型的训练集和测试集的实测活性数据、预测活性数据及其之间的残差如表3 所示,所有残差在 ±0.058 以内;实测和预测的pIC50值分布如图2 所示,由图可知所有数据点都分布于直线附近,说明模型具有较好的预测能力。
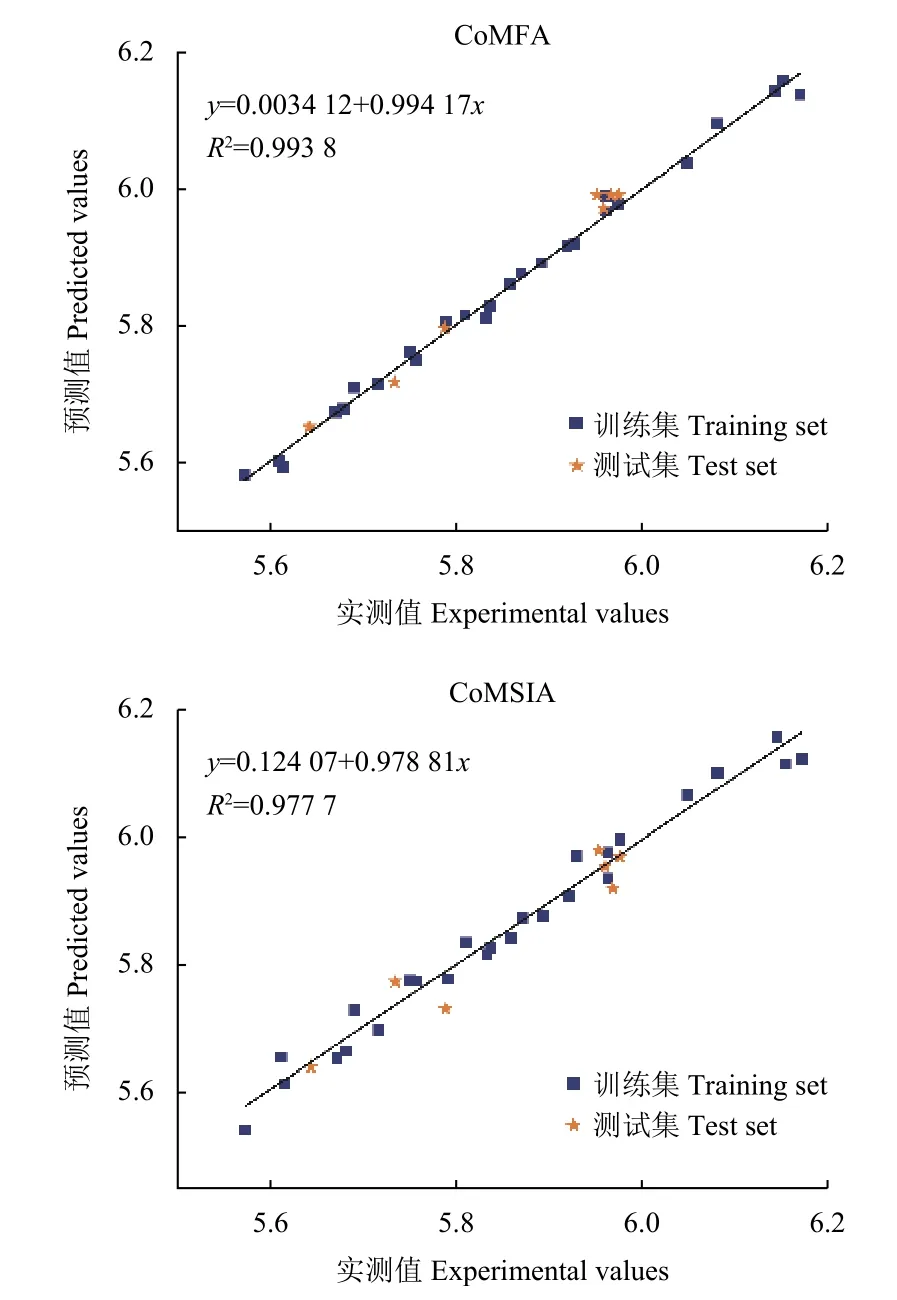
图2 实测与CoMFA 和CoMSIA 预测pIC50 值的散点图Fig. 2 Scatter plots of experimental and predicted pIC50 for the CoMFA and CoMSIA
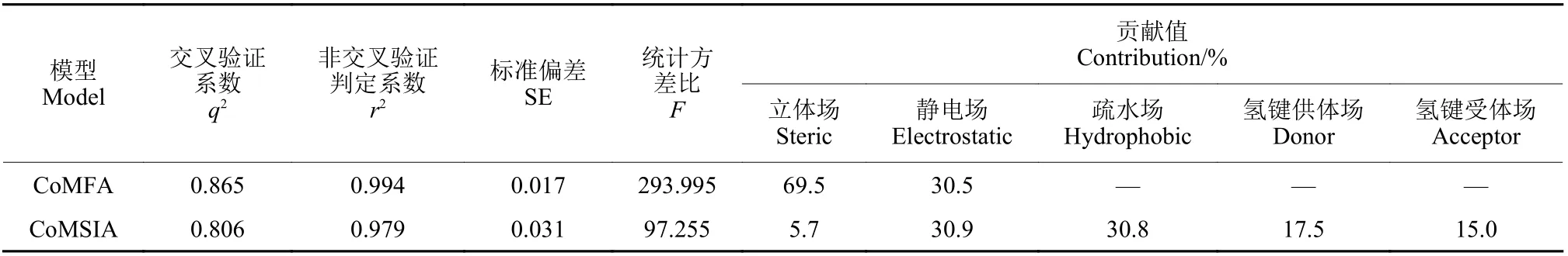
表2 CoMFA 和CoMSIA 结果分析Table 2 CoMFA and CoMSIA analysis results
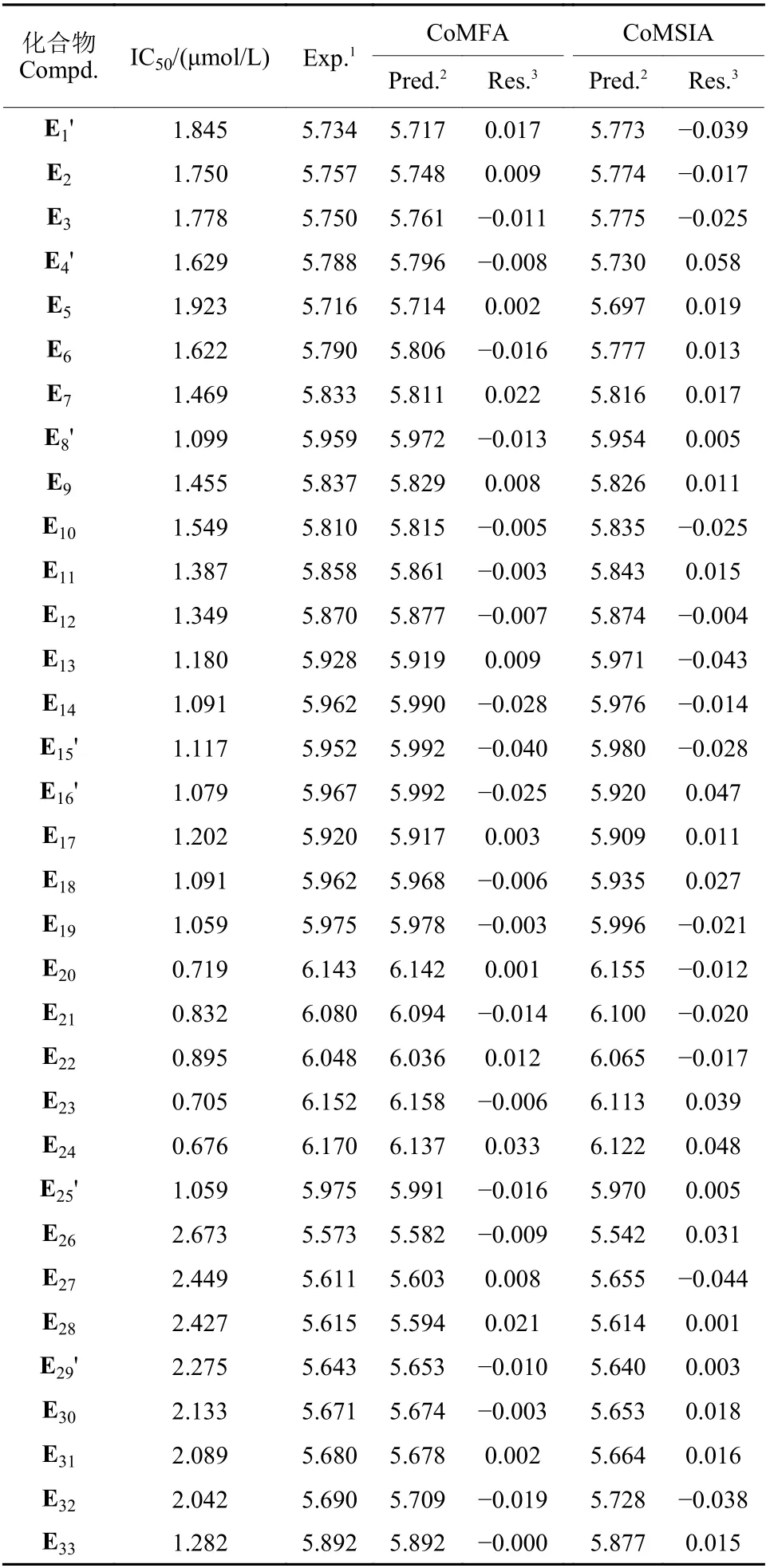
表3 实测的与CoMFA 和CoMSIA 预测的pIC50 结果值Table 3 Experimental and predicted results of pIC50 for CoMFA and CoMSIA
以目标化合物E24为模板分子 (如图3 所示),将所有目标化合物的取代基分为苯环a 与苯环b,对所有分子进行CoMFA 与CoMSIA 模型的分析。由图4 和图5 可知,两种模型分别所得的立体场和静电场分布结果基本一致。图4A 与图5A所示为CoMFA 与CoMSIA 模型所生成的立体场,绿色区域代表引入取代基为大体积时有利于化合物活性的提高,而黄色区域代表减小取代基体积有利于化合物活性的提高[11]。例如,当苯环a 的取代基不变,苯环b 的2′ 位由大体积的氯变为小体积的氢时活性增加,如CoMFA 模型中的化合物E29(pIC50= 5.653) 与E8(pIC50= 5.972)、CoMSIA 模型中E29(pIC50= 5.640) 与E8(pIC50=5.954) 的结果所示[11-13]。图4B 与图5B 所示为静电场等势图,CoMFA 模型得到的静电场分布相较于CoMSIA 模型得到的结果更丰富。图中红色区域表示引入取代基为吸电子基团有利于提高化合物的活性,而蓝色区域表示引入取代基为供电子基团有利于提高化合物的活性[11]。由两种模型得出一致的结果为:在苯环a 的4 位引入供电子基、2 位和6 位引入吸电子基,苯环b 的2′和3′位引入吸电子基,有利于提高化合物的抑菌活性[25]。图5C 所示为CoMSIA 模型的疏水场,黄色区域表明此处增加疏水基团有助于提高化合物的生物活性,即在苯环a 及苯环b 的4′ 位增加疏水基团都会使化合物的活性提高。图5D 所示为CoMSIA模型给出的氢键受体与供体等势图,青色区域表明在此处引入氢键供体基团可提高化合物的生物活性,紫色区域则表明在此处减少氢键供体可提高化合物的活性;橙色区域表明在此处引入氢键受体基团可增加生物活性,红色区域处则相反。由图5D 可得,在苯环a 的3 位增加氢键受体基团、苯环b 的4′位减少氢键受体基团可提高化合物的生物活性[26]。
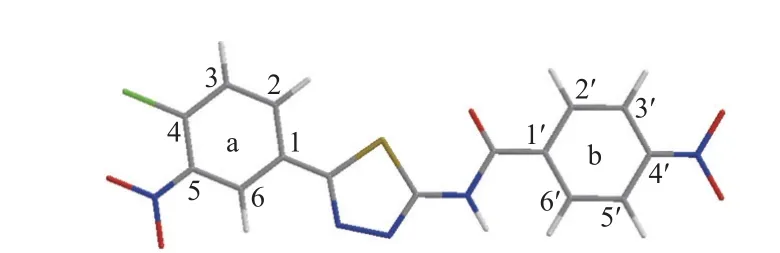
图3 模板分子E24 被分为苯环a 与苯环bFig. 3 The template molecule E24 was divided into benzene ring a and benzene ring b
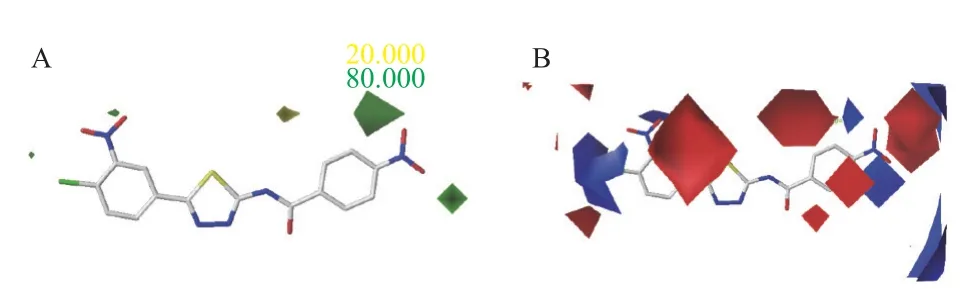
图4 CoMFA 等势图的立体场 (A) 和静电场 (B)Fig. 4 Steric (A) and electrostatic (B) field of CoMFA contour maps
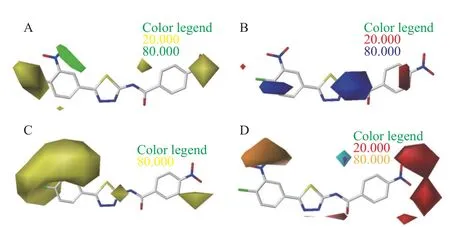
图5 CoMSIA 等势图的立体场 (A)、静电场 (B)、疏水场 (C)、氢键供体场和受体场 (D)Fig. 5 Steric (A), electrostatic (B), hydrophobic (C),hydrogen bond donor and acceptor (D) field of CoMSIA contour maps
3 结论
以取代苯甲酰氯与2-氨基-5-取代-1,3,4-噻二唑为反应物,合成了33 个2-取代苯基-5-取代苯甲酰胺基-1,3,4-噻二唑化合物,其中23 个为新化合物。离体抑菌活性测试表明,所有化合物对根霉R. nigricans、青霉P. glaucum、灰霉B. cinerea、交链孢霉A. brassicae和黑曲霉A. niger均有较好的抑制活性,在质量浓度50 μg/mL 下,化合物E1、E2、E29对所有供试菌种的抑制率均在80%以上。目标化合物对供试菌种的抑菌活性顺序为:黑曲霉 > 根霉 > 灰霉 > 交链孢霉 > 青霉。通过建立的CoMFA 与CoMSIA 模型对目标化合物进行了3D-QSAR 研究,综合两种模型给出的结果为:1) 增大苯环a 的2、3 位与苯环b 的3′ 位取代基的体积,减小苯环a 的4 位与苯环b 的4′ 位取代基的体积,可提高化合物的抑菌活性;2) 苯环a 的4 位引入供电子基,苯环a 的2 位和6 位以及苯环b 上引入吸电子基,有利于化合物抑菌活性的提高;3) 苯环a 及苯环b 的4′ 位增加疏水性基团会使化合物的抑菌活性增加;4) 苯环a 的3 位增加氢键受体基团,苯环b 的4′ 位减少氢键受体基团可提高化合物的抑菌活性。

