华蟾素对肺癌患者免疫功能及血清肿瘤标志物的影响研究
孙晨,汪硕敏,夏云红
(安徽医科大学第四附属医院,安徽合肥 230000)
肺癌是全球发病率最高的恶性肿瘤,其中,非小细胞肺癌(non-small cell lung cancer,NSCLC)的发病率高达80%。近年来随着空气质量的改变,肺癌发病率呈快速上升趋势,对各国人民的身体健康造成了严重影响[1-3]。手术是治疗肺癌的最佳选择,但是由于肺癌发病早期仅表现为轻微咳嗽等症状,对患者无明显影响,往往不能得到足够重视,多数患者在发现时已处于中晚期,失去手术治疗的最佳时机,只能依靠内科治疗方法维持生命[4-5]。吉西他滨联合顺铂是治疗肺癌较有效的化疗方案,但长期治疗患者会出现耐药而导致疗效下降,同时副作用增大,对患者的免疫功能造成较大影响。华蟾素为一种中成药,可有效抑制肿瘤生长,改善患者免疫功能,在肺癌等恶性肿瘤的治疗中具有一定疗效[6-7]。基于此,本研究采用华蟾素联合常规化疗对NSCLC患者进行治疗,旨在探讨NSCLC的更佳治疗方案,为临床治疗NSCLC提供可靠依据。现将研究结果报道如下。
1 对象与方法
1.1 研究对象及分组选取2018年9月至2020年8月安徽医科大学第四附属医院肿瘤科收治的97例NSCLC患者为研究对象。按病理类型和TNM分期,采用分层随机方法,将患者随机分为对照组48例和观察组49例。
1.2 病例选择标准
1.2.1 纳入标准 ①经临床、影像学和病理学检查确诊为中晚期NSCLC;②预计生存期>6个月;③Karnofsky功能状态评分(KPS)>60分;④意识清醒,愿意配合研究的患者。
1.2.2 排除标准 ①合并有其他肿瘤的患者;②其他脏器严重功能不全的患者;③预计生存期<6个月的患者;④不愿意接受化疗方案治疗的患者;⑤沟通障碍,无法配合研究的患者。
1.3 治疗方法
1.3.1 对照组 给予常规化疗。①吉西他滨(江苏豪森制药有限公司,批准文号:国药准字H20030104)+0.9%生理盐水静脉滴注,剂量为1 000 mg/m2,治疗时间为疗程的第1天和第8天,60 min内滴注完毕;顺铂(江苏豪森制药有限公司,批准文号:国药准字H20040813)+0.9%生理盐水静脉滴注,剂量为75 mg/m2,治疗时间为疗程的第1天和第3天。1个月为1个疗程,共治疗3个疗程。
1.3.2 观察组 在对照组常规化疗的基础上加用华蟾素治疗。用法:华蟾素(安徽华润金蟾药业股份有限公司,批准文号:国药准字Z34020274)口服,服用时间为疗程的第1天和第14天,服用剂量为每次0.75 g,每日3次,于餐后温开水送服。1个月为1个疗程,共治疗3个疗程。
1.4 观察指标及疗效评价
1.4.1 临床疗效 根据实体瘤疗效评价标准对患者疗效进行评估。患者肿瘤病灶完全消失,且时间能够持续4周以上,评为完全缓解(CR);患者肿瘤最大直径与治疗开始时相比减少>30%,且时间能够持续4周以上,评为部分缓解(PR);患者肿瘤最大直径与治疗开始时相比减少<30%,评为疾病稳定(SD);患者肿瘤最大直径与治疗开始时相比增加>20%或出现新的病灶,评为疾病进展(PD)。其中,CR、PR患者评为治疗有效。
1.4.2 免疫功能 采集患者空腹静脉血,将血清分离,使用流式细胞仪检测血清中T淋巴细胞亚群CD3+、CD4+及CD8+水平。观察2组患者治疗前和治疗3个月后血清T淋巴细胞亚群CD3+、CD4+及CD8+水平的变化情况。
1.4.3 血清肿瘤标志物 包括神经元特异性烯醇化酶(NSE)、基质金属蛋白酶9(MMP-9),均采用酶联免疫吸附法(ELISA)进行检测。观察2组患者治疗前和治疗3个月后血清NSE、MMP-9等肿瘤标志物的变化情况。
1.4.4 不良反应 根据抗肿瘤药物不良反应评估标准进行评估,共分为4级,其中Ⅳ级最严重。观察2组患者的恶心、白细胞减少、血小板减少、肝功能异常、肾功能异常等不良反应发生情况。
1.4.5 预后情况 所有患者均随访24个月,观察2组患者的2年生存率。
1.5 统计方法 采用SPSS 20.0统计软件进行数据的统计分析。计量资料以均数±标准差(±s)表示,组内治疗前后比较采用配对样本t检验,组间比较采用两独立样本t检验;计数资料用率或构成比表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 2组患者基线资料比较观察组49例患者中,男27例,女22例;年龄34~72岁,平均(51.36±8.21)岁;病理类型:腺癌35例,鳞癌14例;TNM分期:Ⅲ期33例,Ⅳ期l6例。对照组48例患者中,男25例,女23例;年龄36~74岁,平均(51.84±8.42)岁;病理类型:腺癌37例,鳞癌11例;TNM分期:Ⅲ期35例,Ⅳ期13例。2组患者的性别、年龄、病理类型、TNM分期等基线资料比较,差异均无统计学意义(P>0.05),表明2组患者的基线特征基本一致,具有可比性。
2.2 2组患者临床疗效比较表1结果显示:治疗3个月后,观察组的总有效率为77.55%(38/49),对照组为56.25%(27/48),组间比较,观察组的疗效明显优于对照组,差异有统计学意义(P<0.05)。
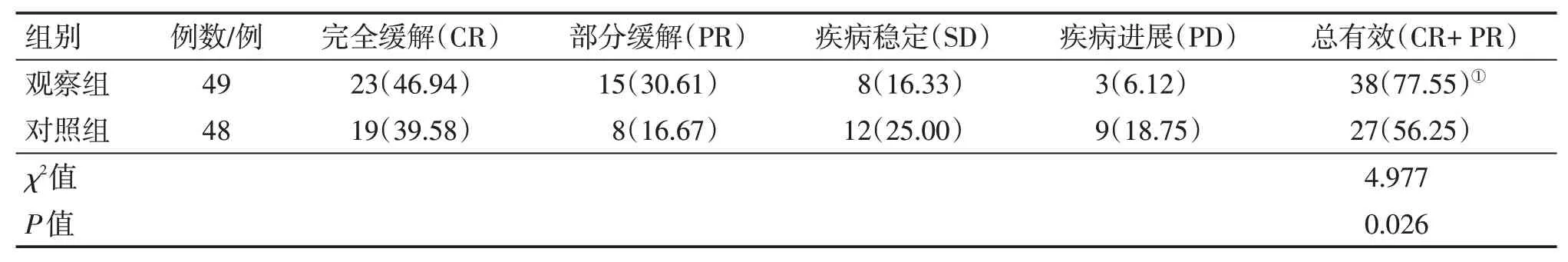
表1 2组非小细胞肺癌(NSCLC)患者临床疗效比较Table 1 Comparison of clinicalefficacy in the two groups of patients with non-smallcelllung cancer [例(%)]
2.3 2组患者治疗前后免疫功能指标比较表2结果显示:治疗前,2组患者血清T淋巴细胞亚群CD3+、CD4+及CD8+水平比较,差异均无统计学意义(P>0.05)。治疗3个月后,观察组患者血清T淋巴细胞亚群CD3+、CD4+及CD8+水平均较治疗前升高(P<0.05),而对照组患者均无明显变化(P>0.05);组间比较,观察组对血清T淋巴细胞亚群CD3+、CD4+及CD8+水平的升高作用均明显优于对照组,差异均有统计学意义(P<0.05或P<0.01)。
表2 2组非小细胞肺癌(NSCLC)患者治疗前后血清T淋巴细胞亚群比较Table 2 Comparison of serum levels of T lymphocyte subsets in the two groups of patients with non-small celllung cancer before and after treatment (±s,%)
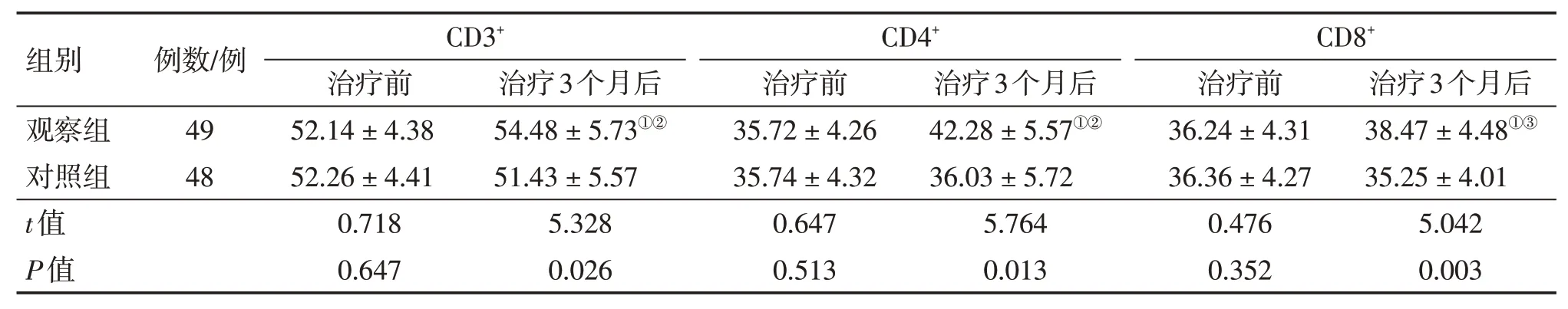
表2 2组非小细胞肺癌(NSCLC)患者治疗前后血清T淋巴细胞亚群比较Table 2 Comparison of serum levels of T lymphocyte subsets in the two groups of patients with non-small celllung cancer before and after treatment (±s,%)
①P<0.05,与治疗前比较;②P<0.05,③P<0.01,与对照组治疗3个月后比较
组别观察组对照组t值P值例数/例49 48 CD3+治疗前52.14±4.38 52.26±4.41 0.718 0.647治疗3个月后54.48±5.73①②51.43±5.57 5.328 0.026 CD4+治疗前35.72±4.26 35.74±4.32 0.647 0.513治疗3个月后42.28±5.57①②36.03±5.72 5.764 0.013 CD8+治疗前36.24±4.31 36.36±4.27 0.476 0.352治疗3个月后38.47±4.48①③35.25±4.01 5.042 0.003
2.4 2组患者治疗前后血清肿瘤标志物比较表3结果显示:治疗前,2组患者血清NSE、MMP-9等肿瘤标志物比较,差异均无统计学意义(P>0.05)。治疗3个月后,2组患者血清NSE、MMP-9水平均较治疗前明显降低(P<0.05),且观察组对血清NSE、MMP-9水平的降低作用均明显优于对照组,差异均有统计学意义(P<0.01)。
表3 2组非小细胞肺癌(NSCLC)患者治疗前后血清肿瘤标志物比较Table 3 Comparison of serum levels of tumor markers in the two groups of patients with non-small celllung cancer before and after treatment(±s)
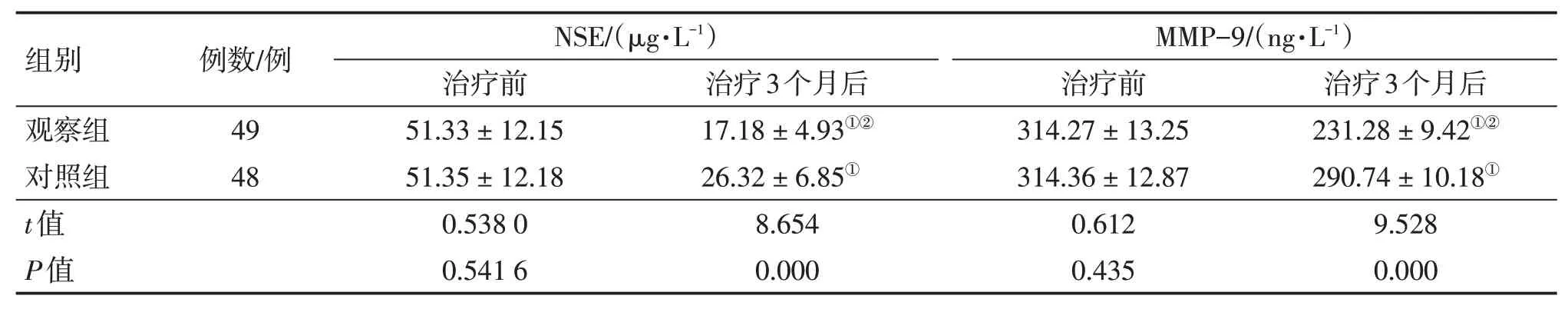
表3 2组非小细胞肺癌(NSCLC)患者治疗前后血清肿瘤标志物比较Table 3 Comparison of serum levels of tumor markers in the two groups of patients with non-small celllung cancer before and after treatment(±s)
①P<0.05,与治疗前比较;②P<0.01,与对照组治疗3个月后比较
组别观察组对照组t值P值例数/例49 48 NSE/(μg·L-1)治疗前51.33±12.15 51.35±12.18 0.538 0 0.541 6治疗3个月后17.18±4.93①②26.32±6.85①8.654 0.000 MMP-9/(ng·L-1)治疗前314.27±13.25 314.36±12.87 0.612 0.435治疗3个月后231.28±9.42①②290.74±10.18①9.528 0.000
2.5 2组患者不良反应发生率比较表4结果显示:治疗过程中,患者的不良反应均以Ⅰ~Ⅱ级为主,其中,2组患者的恶心、血小板减少、肝功能异常、肾功能异常发生率比较,差异均无统计学意义(P>0.05);而2组患者的白细胞减少发生率比较,观察组[12.24%(6/49)]明显低于对照组[29.17%(14/48)],差异有统计学意义(P<0.05)。

表4 2组非小细胞肺癌(NSCLC)患者不良反应发生率比较Table 4 Comparison of the incidence of adverse reactions in the two groups of patients with non-smallcelllung cancer [例(%)]
2.6 2组患者预后情况比较随访24个月,观察组患者的2年生存例数为25例,占52.08%;对照组患者的2年生存例数为19例,占38.78%;组间比较,差异无统计学意义(χ2=1.280,P>0.05)。
3 讨论
晚期肺癌患者的治疗方法以内科化疗等为主,其中作为治疗NSCLC的标准方案的铂类药物是一种金属化合物,对细胞周期的不同时相均有影响,可通过影响细胞DNA嘧啶及碱基的形成,损伤细胞膜结构,从而起到抑制肿瘤生长的作用[8-11]。吉西他滨作为一种新型的胞嘧啶核苷衍生物,注射入人体后,可产生磷酸盐类,进而抑制肿瘤细胞DNA合成,降低肿瘤细胞中脱氧核苷酸三磷酸酯含量。顺铂联合吉西他滨对肺癌的治疗效果获得临床普遍认可,但是对患者副作用较大,且对患者免疫功能造成较大损害,是提高肺癌疗效的一个障碍[12-13]。华蟾素是干蟾皮中的一种成分,主要由蟾蜍苷元与华蟾蜍精组成,具有较好的抑制肿瘤细胞增殖效果,并可有效调节患者免疫功能,减少患者不良反应发生率,在肝癌、肺癌等多种恶性肿瘤的治疗中疗效较佳[14-16]。
本研究采用华蟾素联合常规化疗方案对中晚期NSCLC患者进行治疗,结果显示,治疗3个月后,观察组的总有效率为77.55%(38/49),对照组为56.25%(27/48),组间比较,观察组的疗效明显优于对照组,差异有统计学意义(P<0.05)。同时,观察组对血清T淋巴细胞亚群CD3+、CD4+及CD8+水平的升高作用均明显优于对照组,差异均有统计学意义(P<0.05或P<0.01)。提示华蟾素可有效促进顺铂和吉西他滨对肺癌的抑制作用,3者联合使用具有协同作用。分析原因,可能是由于华蟾素本身对肿瘤具有一定的抑制作用;另外,华蟾素对患者免疫功能具有一定的调节作用,从而促进了对NSCLC的抑制作用。
在肿瘤标志物方面,本研究结果显示,治疗3个月后,2组患者血清NSE、MMP-9水平均较治疗前明显降低(P<0.05),且观察组对血清NSE、MMP-9水平的降低作用均明显优于对照组,差异均有统计学意义(P<0.01)。提示华蟾素可有效降低NSCLC患者体内的肿瘤标志物水平,使患者体内肿瘤的细胞增殖能力、侵袭能力降低。与其他研究[3,5,10]相比,均显示了华蟾素对肿瘤具有较好的抑制作用。
在不良反应方面,本研究结果显示,治疗过程中,2组患者的不良反应均以Ⅰ~Ⅱ级为主,其中,观察组的白细胞减少发生率明显低于对照组,差异有统计学意义(P<0.05)。提示华蟾素可降低化疗对NSCLC患者免疫功能的损伤,故患者体内的白细胞水平较高,机体免疫力较强。
在预后方面,本研究结果显示,经随访24个月,观察组患者的2年生存例数为25例,占52.08%;对照组患者的2年生存例数为19例,占38.78%,组间比较,差异无统计学意义(P>0.05)。提示使用华蟾素后患者预后获得一定改善,但是尚未显示出显著性差异,这可能与病例选择较少、随访时间较短等有关。为给临床NSCLC提供更多可靠的治疗方案,我们今后将会从病例数量、研究细节、研究深度等方面,完善研究方案,进而为华蟾素对NSCLC的治疗提供更多可靠的依据。
综上所述,华蟾素能够提高NSCLC患者临床疗效,改善患者免疫功能,降低患者血清肿瘤标志物水平,减少患者不良反应发生率,改善患者预后。

