浸提条件对土壤溶解性有机碳测定结果的影响
李亚林,练金山,任凤玲,孙楠,徐明岗
(中国农业科学院农业资源与农业区划研究所/耕地培育技术国家工程实验室,北京 100081)
随着全球气温和大气温室气体浓度的升高,学者对土壤碳库和全球碳循环的研究日益增多[1]。土壤有机碳(Soil organic carbon,SOC)储量约为大气中的3倍,并以CO2、HCO-3和土壤溶解性有机碳(Dissolved organic carbon,DOC)的形式进入相邻圈层[2]。DOC 是指能够溶解于水或盐溶液的一系列结构、大小不同的有机化合物[3]。土壤中适当的DOC 含量在维持生态系统营养库的稳定性和降低环境污染方面均具有重要作用。一方面,DOC 是土壤碳库最为活跃的组分之一[4],其主要来源于腐殖化的有机质、植物凋落物、根系分泌物以及土壤微生物[5],参与土壤C、N、P 等养分元素的生物化学循环过程;另一方面,DOC 具有较高的移动性,溶解后可随水体迁移,导致环境污染[6];此外,DOC 是微生物可直接吸收利用的有机碳源,通过影响微生物代谢对CO2、CH4等温室气体的排放产生一定影响[7]。目前,国内外学者对DOC 的来源、结构组成、影响因素以及生态环境效应进行了大量研究[8-10],在研究过程中不同的学者采用不同的研究方法测定DOC 含量。李忠佩等[11]通过室内试验发现在红壤水稻土中,以去离子水作为浸提剂测定的DOC含量更接近田间实际情况,但去离子水浸提会导致土壤黏粒分散从而很难获得可供分析的清澈溶液[12]。HANEY 等[13]利用去离子水和0.5 mol·L-1K2SO4试剂作为浸提剂测定DOC 含量,结果表明室温条件下,在低pH 土壤中用去离子水测定的DOC 含量比用0.5 mol·L-1K2SO4试剂提高290%,在高pH 土壤中则减少17%。也有研究发现用低浓度的盐溶液测定的DOC含量比用去离子水高[1],但DOC 含量的高低与浸提温度、水土质量比等密切相关[14]。通常情况下,DOC 含量会随着温度的升高显著增加[15-17],CHRIST等[18]对土壤淋洗发现DOC 含量随温度升高呈指数性增加,但也有一些学者认为温度对DOC含量没有显著影响[19]。
综上所述,DOC 的测定容易受浸提剂类型、浸提温度、水土质量比和土壤前处理方式等因素的影响[20-21],因而测定含量差异较大,导致很多研究结果之间无法进行横向比较。目前,对DOC 含量的测定尚无统一的方法,因此,本研究通过搜集现有关于浸提方法对DOC 含量影响的研究结果,采用整合分析(Meta-analysis)的方法,系统评价不同浸提方法对DOC 测定含量的影响及其差异,以期为DOC 测定方法的选择提供科学依据和参考。
1 材料与方法
1.1 数据搜集
本研究所用数据来自中国知网的中文文献以及Web of Science 核心数据库的英文文献,通过输入检索词“土壤溶解性有机碳/Dissolved organic carbon”“浸提条件/Extraction conditions”“水土质量比/Waterto-soil ratio”和“浸提温度/Extraction temperatures”,筛选了2000—2020年发表的关于浸提方法对DOC测定含量和浸提率影响的相关研究文献。以25 ℃和2∶1水土质量比作为对照组,其余温度和水土质量比条件下(处理组)DOC 含量与对照组DOC 含量的差值为DOC 增加量(ΔCDOC,mg·kg-1)。DOC 测定含量(mg·kg-1)为不同浸提条件下提取的土壤中DOC 含量的测定值;DOC 浸提率(DOC 与SOC 含量之比,%)为土壤中DOC 测定含量(mg·kg-1)占土壤有机碳含量(SOC,g·kg-1)的百分数,其计算公式:

为了避免搜集文献带来的偏差,本研究采用以下标准进行文献筛选:①同一独立试验必须包含明确的处理组和对照组(表1);②至少有SOC、DOC 和浸提率等指标中的两个;③每个处理重复次数≥3;④所有试验均采用表层土壤(0~20 cm)。此外,对于每个独立试验还收集了试验时间、气候类型、地理位置(经度和纬度)、土壤基础理化性质等相关信息。经筛选,共获得31 篇符合标准的研究文献,包含547 组DOC 测定含量数据和390 组DOC 浸提率数据。在数据提取过程中,根据文献中直接给出的平均值和标准误(SE),转换为相应的标准差(SD):

表1 土壤溶解性有机碳测定含量综合分析涉及的因素Table 1 Factors involved in the Meta-analysis of soil dissolved organic carbon(DOC)concentrations

式中:n是重复次数。若该文献中无SD 或SE,则根据本研究所收集的文献中给出的SDs(SDx1、SDx2、…、SDxi、…、SDxk)或SEs(SEx1、SEx2、…、SExi、…、SExk)和相对应的重复次数(Nx1、Nx2、…、Nxi、…、Nxk)计算得出SD[22],具体公式为:
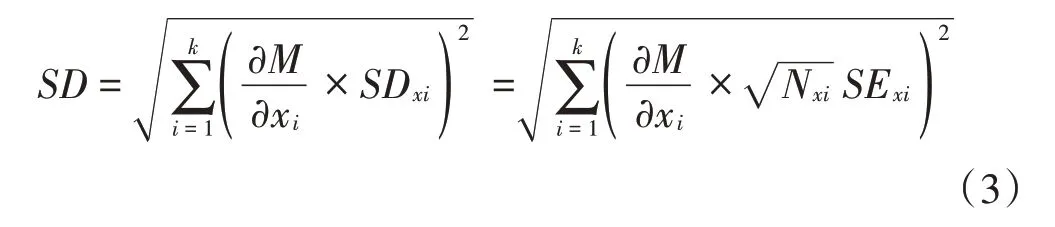
1.2 研究方法
整合分析是利用同类研究的多个相互独立的研究结果进行定量分析,从而获得相对综合性结论的研究方法。由于整合分析增大了分析样本量,同时也提升了统计的检验效能,因此,其结论较单一研究结论更具参考价值。本研究使用Metawin 2.0 进行整合分析,采用效应比值的自然对数(lnRR)来量化不同浸提方法对DOC测定含量和浸提率的效应[23]:
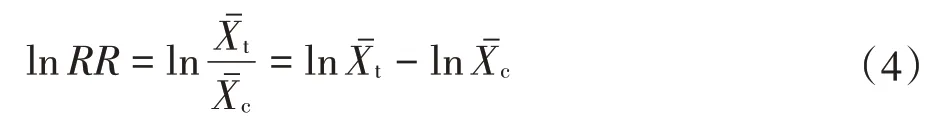
式中:RR为响应比;为处理组DOC测定含量或浸提率的平均值;为对照组DOC 测定含量或浸提率的平均值。平均值的变异系数V、权重系数wij、权重响应比RR++、RR++的标准误(S)以及95%CI可通过以下公式计算[24]。

式中:SDt和SDc分别代表处理组和对照组的标准差,nt和nc分别代表处理组和对照组的样本数。通过分析得到每一组数据的效应比值,利用数据标准差计算权重加权平均数后得出其95%置信区间(95%CI)。若置信区间包含0,说明不同浸提方法对DOC 测定含量或浸提率无显著影响;若置信区间全部大于0,说明不同浸提方法对DOC 测定含量或浸提率具有显著正效应,即显著增加DOC 测定含量或浸提率(P<0.05);若置信区间全部小于0,说明不同浸提方法对DOC测定含量或浸提率具有显著负效应,即显著降低了DOC测定含量或浸提率(P<0.05)[25]。
由于纳入整合分析的文献在研究条件、地点、时间、对象和研究者等方面不尽相同,不同研究异质性的存在使各研究中变量关系效应的估计也不同。因此,在合并技术资料的响应比得出加权平均数之前,需要对各试验处理及各试验结果间进行异质性检验。如果各研究之间的差异很大,即存在明显的异质性,直接计算合并得出效应量会造成结果的不可靠和不稳定。异质性检验结果(表2)表明,各试验数据结果间存在明显异质性,因此选用随机效应模型(P<0.001)。

表2 不同处理间的异质性(Qt)自由度和显著性检验Table 2 Heterogeneity(Qt)and probability among observations in different treatments
1.3 数据分析
为了进一步分析某一特征因素对DOC 测定含量或浸提率的影响,将数据划分为不同的亚组,如浸提剂种类、浸提温度、水土质量比等。此外,采用SPSS 18.0进行数据分析和显著性检验(P<0.05),用Origin 2021制图,各因素对DOC测定含量的影响程度的重要度采用R语言中的软件包Random Forest进行计算[26]。
2 结果与分析
2.1 不同浸提方法对DOC测定含量的影响
整合分析结果(图1)显示,浸提剂种类和浸提条件对DOC 测定含量的影响程度存在显著差异。相比于去离子水,对不同的浸提剂种类比较发现,CaCl2浸提下土壤样品中的DOC 测定含量的提升幅度显著低于K2SO4、KCl浸提。与去离子水相比,K2SO4和KCl试剂对DOC 测定含量均有显著提升,分别提高了118.8% 和124.1%(P<0.05)。但DOC测定含量在K2SO4和KCl 浸提之间无显著差异。然而,CaCl2浸提剂显著降低了DOC 测定含量(降幅57.9%,P<0.05)。DOC 测定含量均随着浸提时间、浸提温度、土壤研磨粒径和水土质量比的增加而显著增加,相比于对照组,处理组DOC 测定含量的升幅分别为27.4%、72.5%、11.2%和79.7%。

图1 不同浸提方法对DOC测定含量的影响Figure 1 Effects of extractant methods on measured soil dissolved organic carbon(DOC)concentrations
2.2 不同浸提方法对DOC浸提率的影响
不同浸提剂种类、浸提条件对DOC 浸提能力影响显著不同(图2)。与去离子水相比,K2SO4和KCl均显著增加DOC 浸提率,升幅分别为17.2%和65.3%,但CaCl2显著降低了DOC 浸提率,降幅为45.2%。不同浸提条件下,DOC 浸提率随浸提时间、浸提温度和水土质量比的增加而升高,但升幅略有差异(图2),与对照组相比,处理组DOC 浸提率的升幅分别为27.3%、65.2%和72.3%。不同土壤研磨粒径间DOC浸提率差异较大。相比≤2 mm 土壤粒径,2 mm 以上土壤粒径下DOC 浸提率显著提高,升幅为13.2%。总体而言,浸提条件不同,DOC浸提率具有显著差异。
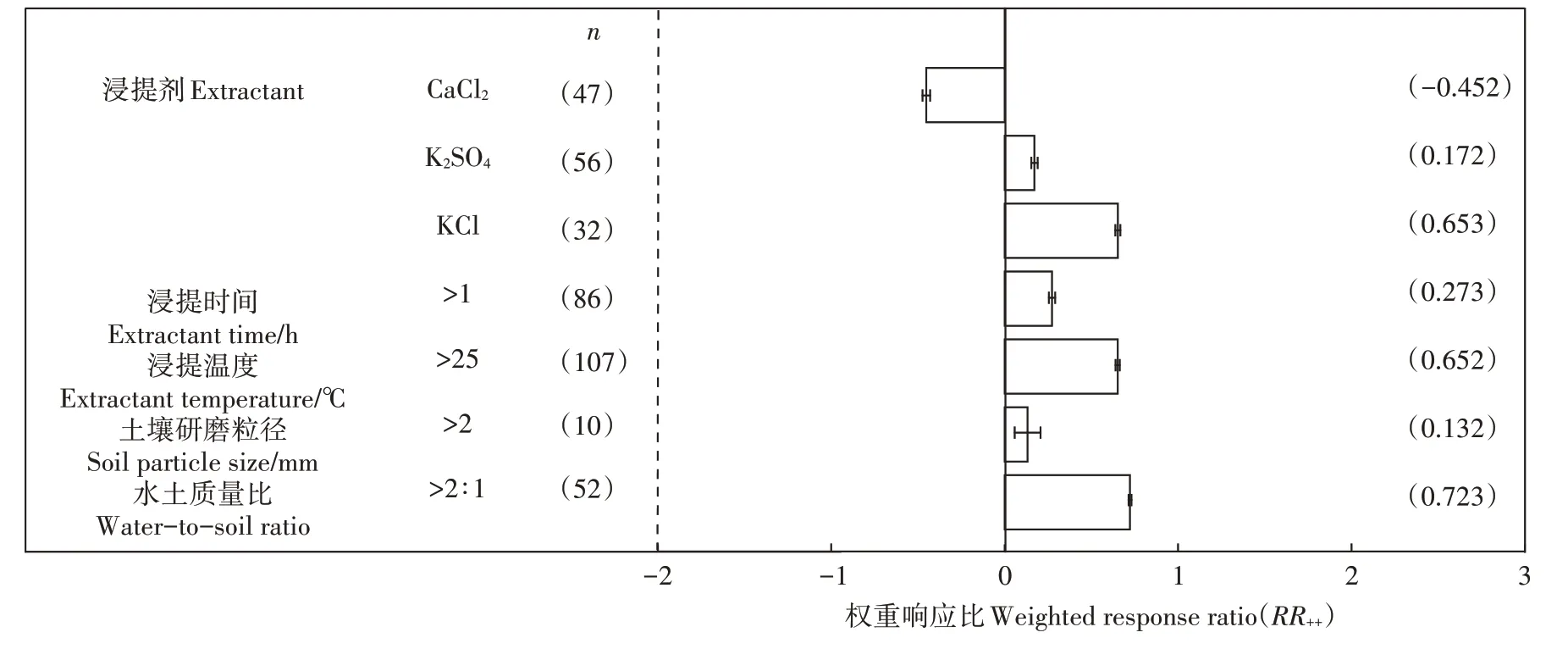
图2 不同浸提方法对DOC浸提率的影响Figure 2 Effects of extractant methods on measured soil dissolved organic carbon(DOC)extraction rate
2.3 浸提温度和水土质量比与DOC增加量的关系
图3结果表明,浸提温度对DOC增加量有显著的影响(P<0.01)。在30~80 ℃范围内,DOC 增加量随温度的升高呈现出先减小后增大的趋势,且DOC 增加量曲线和零点有两个交界点(分别为48 ℃和63 ℃),表明DOC 测定含量在48 ℃左右时达到最大值,之后随温度增加逐渐减小,并在63 ℃左右时达到最小值,随后继续增大。不同水土质量比与DOC 增加量的拟合曲线(图4)表明,随着水土质量比的增大,溶解进入到土壤溶液中的DOC 增加量呈直线增加,且达到极显著水平(P<0.01),这表明水土质量比对DOC 测定含量有重要的影响。

图3 浸提温度与DOC增加量(ΔCDOC)关系Figure 3 Relationship between DOC increment(ΔCDOC)and extraction temperature
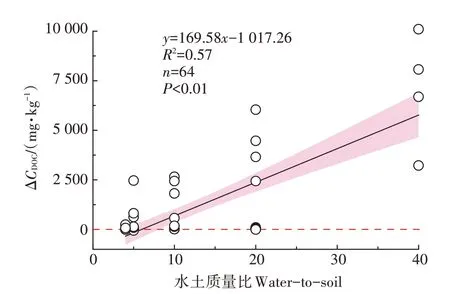
图4 水土质量比与DOC增加量(ΔCDOC)关系Figure 4 Relationship between DOC increment(ΔCDOC)and water-to-soil ratio
2.4 不同浸提剂下土壤性质对DOC 测定含量影响的重要度
由于DOC 在养分供应、物质循环等方面具有重要作用,因此,不同浸提剂下土壤性质对DOC 测定含量的影响程度能够反映出浸提剂是否适宜。整体来看,相比于其他因素,土壤pH 是影响DOC 测定含量的主要因素,其相对重要度为14.75%,其次是SOC 和全氮(TN)含量,重要度分别是11.85%和11.43%(图5a)。与去离子水相比,不同浸提剂(K2SO4、KCl 和CaCl2)下DOC 测定含量影响幅度的主控因素存在差异。对于浸提剂K2SO4,土壤pH、黏粒含量和SOC 含量是影响DOC 测定含量的主要因素,其相对重要度分别为14.62%、14.21%和13.76%(图5b);对于浸提剂KCl,TN 含量是影响DOC 测定含量的主要因素,其次是土壤容重(BD)和SOC 含量(图5c);对于浸提剂CaCl2,土壤质地对DOC测定含量的影响较大,其中粉粒、黏粒和砂粒含量的重要度分别为19.99%、17.14%和12.45%,SOC含量的重要度也达到了9.44%(图5d)。
3 讨论
3.1 浸提剂种类对DOC测定含量和浸提率的影响
本研究表明,浸提剂种类显著影响DOC 测定含量和浸提率。与去离子水相比,钾盐(K2SO4和KCl)对DOC 测定含量的提升幅度显著高于钙盐(CaCl2),这可能与部分矿物结合态有机质被释放有关[27]。RENNERT 等[28]的研究表明去离子水可以溶解出更多具有芳香性和高分子量的疏水化合物,而盐类可以提取出更多吸附在带电土壤基质表面的亲水化合物。一方面,浸提剂中的一价阳离子(K+)与多价阳离子(Ca2+和Mg2+)交换,从而使吸附在黏土矿物表面或被有机物-多价阳离子复合物固定的有机化合物溶解,进而导致更多固定的有机团聚体分解为DOC[29];另一方面,CaCl2对土壤中高缩合的有机碳素的提取能力较弱[30]。而且,CaCl2本身是一种温和试剂,溶液中的Ca2+可以同时被黏土颗粒表面的负电荷和有机化合物的羧基基团吸附,或者被来自不同有机化合物的两个负电荷吸附,从而导致CaCl2试剂浸提条件下DOC测定含量的增幅明显低于其他试剂(K2SO4和KCl)浸提[31]。与去离子水相比,KCl 试剂对DOC 测定含量的提升幅度略高于K2SO4试剂,差异不显著(P>0.05),但KCl试剂对DOC浸提率的提升幅度显著高于K2SO4试剂(P<0.05,图1 和图2)。这与杨小燕等[32]在黑土上的研究结果不一致,该研究发现K2SO4试剂对DOC 测定含量的影响显著高于KCl 试剂。产生这种现象的原因可能是不同土壤间的理化性质具有明显差异。最近的研究表明土壤对DOC 的吸附能力取决于SOC含量和铁氧化物含量,二者呈现显著正相关关系[33]。本研究还发现在不同浸提剂条件下,土壤理化性质(pH、SOC 和TN 含量)均显著影响DOC 测定含量,其重要度为17.31%~38.03%(图5)。
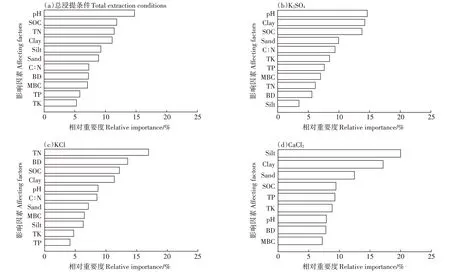
图5 影响DOC测定含量的主要因素Figure 5 The main factors affecting the DOC concentrations
3.2 浸提温度和水土质量比对DOC 测定含量和浸提率的影响
与室温(25 ℃)浸提相比,增加浸提温度使DOC测定含量和浸提率显著提高。在30~80 ℃范围内,DOC 测定含量在48 ℃左右达到最大值,之后随温度增加逐渐减小,并在63 ℃左右达到最小值,随后继续增大(图3)。温度的升高加速了分子热运动,提高了溶解性有机物在滞膜层中的分子扩散速度[22,29],进而增加了DOC 的释放速率。当温度达到一定限度(50 ℃左右)后,温度升高会导致溶解性有机物发生絮凝作用,使其分子量增加、分子扩散系数降低,因而DOC 释放速率也降低[21]。当温度继续升高(≥60 ℃)时,高温导致有机结构破坏、溶酶细胞水解,同时电离有机物质和无机胶体,使得DOC 测定含量大幅提高[34]。
水土质量比对DOC 测定含量和浸提率有重要的影响,与对照(≤2∶1 水土比)相比,处理组(>2∶1 水土比)的DOC 测定含量和浸提率显著提升,增幅分别为79.7%和72.3%(图1和图2);另外DOC测定含量随水土质量比的提高而增加(图4)。这可能是因为溶液中的离子浓度随水土质量比的增大而降低,使土壤孔隙中更多易解吸的DOC 向水体中释放;而且水土质量比的提高会增强土壤颗粒的分散性,改变土壤与DOC 交换位点的有效性,导致与土壤结合能量低的DOC 释放。此外,水土质量比的提高会打破DOC 在土壤固液两相界面的吸附-解吸平衡,促进亲水性DOC释放,进而提升溶液中DOC的测定含量[21,35]。
4 结论
本研究采用Meta分析方法探究了DOC 测定含量和浸提率对不同浸提条件的响应,结论如下:
(1)与去离子水作浸提剂相比,KCl 和K2SO4浸提剂显著提高了DOC 测定含量和浸提率,而CaCl2浸提剂显著降低了DOC测定含量和浸提率。
(2)DOC 测定含量随着浸提时间、浸提温度、土壤研磨粒径和水土质量比的增加而提高,且其提升幅度显著不同。
(3)土壤pH、SOC含量是影响DOC测定含量的主要因素,但不同浸提剂下各主控因素有所不同。
综上所述,浸提剂种类、浸提时间、浸提温度、水土质量比以及土壤性质均对DOC 测定含量和浸提率有显著影响,在测定DOC含量时适宜采用KCl作为浸提剂,在室温条件(25~30 ℃)下浸提1 h。

