110例儿童奥密克戎变异株感染恢复期血清IgG抗体变化
张平平 郭艳婷 初玉芹 齐继 连雁 李巍 姚丽娜
(天津市第一中心医院儿科,天津 300190)
自2019 年新型冠状病毒肺炎(coronavirus disease 2019,COVID‐19)首次报告以来,严重急性呼吸综合征冠状病毒2(severe acute respiratory syndrome coronavirus 2,SARS‐CoV‐2)对全球健康构成重大威胁[1]。2021 年11 月9 日南非报道首次发现COVID‐19 新变异株奥密克戎(Omicron),迅速引起全球的广泛关注[2],世界卫生组织(World Health Organization,WHO)将其列为COVID‐19 的第5 种“值得关注的变异株”(variant of concern,VOC),因为它是迄今为止SARS‐CoV‐2变异最严重的毒株,并具有更高的传播力。2022年1月8日天津市发现2 例本土SARS‐CoV‐2 感染者,天津市疾病预防控制中心对其进行了COVID‐19 全基因组测序,最终确认2 例均属于VOC/Omicron 变异株(BA.1 进化分支),属于同一传播链。随即天津全市范围开展全员核酸检测,共有430人通过SARS‐CoV‐2 核酸检测确诊为COVID‐19,根据流行病学史,均考虑为VOC/Omicron变异株感染,其中儿童(<18岁)114例(26.5%),这是中国大陆第一波奥密克戎本土疫情。至今,我国仍受以奥密克戎变异毒株为主的SARS‐CoV‐2 传播的影响,推进SARS‐CoV‐2 疫苗(简称新冠疫苗)接种是中国常态化疫情防控的重要措施之一。了解新冠疫苗在COVID‐19 流行期间的保护效力是至关重要的。SARS‐CoV‐2 基因组编码4 种结构蛋白,包括刺突蛋白(spike protein,S蛋白)、包膜蛋白、膜蛋白、核衣壳蛋白,S 蛋白是诱导SARS‐CoV‐2 特异性抗体,特别是中和抗体的关键靶标,包含2个亚基——S1 和S2,S1 包含受体结构域[3]。检测新冠疫苗免疫效果的金标准仍是中和试验(neutralization test,NT),血浆中的中和活性被认为在疫苗效力中发挥重要作用[4],但NT 对实验条件要求高,不易施行。多项研究提示抗SARS‐CoV‐2 受体结构域特异性IgG抗体(简称SARS‐CoV‐2 IgG抗体)与中和抗体滴度呈正相关[5-7]。本研究通过回顾性分析中国首次本土奥密克戎流行期间确诊COVID‐19 患儿的基本情况及SARS‐CoV‐2 IgG 抗体水平,了解新冠疫苗的保护效力,监测感染后的抗体变化,从而优化新冠疫苗接种策略和加强疫苗的接种。
1 资料与方法
1.1 研究对象
2022 年1 月8 日至2 月7 日天津市海河医院(天津市COVID‐19定点收治医院)收治了114例0~17岁奥密克戎变异株感染的COVID‐19患儿,达出院标准后转入天津市第一中心医院水西院区进行至少14 d的医学观察期及出院后门诊随访,其中4例无SARS‐CoV‐2 IgG 抗体结果,最终纳入110 例。根据患儿确诊COVID‐19 前新冠疫苗接种情况分为4组,其中加强针接种组(3剂)2例,完全接种组(2剂)90例,不完全接种组(1剂)5例,未接种组13例。COVID‐19的诊断及临床分型参照《新型冠状病毒肺炎诊疗方案(试行第八版)》[8]。本研究获我院伦理审查委员会审核通过(2022N050 KY),所有患儿家长均签署了书面知情同意书。
1.2 资料收集
通过我院电子病例系统回顾性收集患儿相关临床资料,包括性别、年龄、COVID‐19临床分型、流行病学接触史、新冠疫苗接种情况、实验室检查结果。实验室数据主要包括确诊后1个月(中位数为25 d,范围12~30 d)、确诊后2个月(中位数为43 d,范围31~52 d)SARS‐CoV‐2 IgG抗体水平,住院及随访期间鼻咽拭子SARS‐CoV‐2 核酸检测结果。其中确诊时间为天津市海河医院入院时间。
1.3 主要仪器和试剂
血 清SARS‐CoV‐2 IgG 抗 体 水 平 采 用SARS‐CoV‐2 IgG 抗体试剂盒(博奥赛斯重庆生物科技有限公司,G202110004)通过磁微粒化学发光检测,结果以待检样本发光值/临界值(signal to cut‐off,S/CO)表示。判定标准:S/CO≥1.0为阳性,<1.0为阴性。标本的检测、结果判定由检验专业人员严格按照说明书完成。
鼻 咽 拭 子SARS‐CoV‐2 核 酸 使 用 试 剂 盒(Zybio, 5203050) 检 测, 聚 合 酶 链 反 应(polymerase chain reaction,PCR)再阳性定义为间隔超 过24 h 的2 次独立PCR 阴性结果后PCR Ct 值<40。
1.4 统计学分析
采用SPSS 22.0 软件对数据进行处理与分析。计数资料采用例数和百分率(%)表示,组间比较采用Fisher 确切概率法,进一步两两比较采用Bonferroni 校正法检验。不符合正态分布的计量资料采用中位数(范围)表示,多组间比较采用Kruskal‐WallisH检验,进一步两两比较采用Bonferroni 校正法检验;抗体随时间变化情况采用Wilcoxon 符号秩和检验。P<0.05 示差异有统计学意义。
2 结果
2.1 一般资料
110 例COVID‐19 患 儿 中, 男 女 比 例 为1∶1.04,中位确诊年龄为10(范围1~17)岁;以家庭聚集感染为主(71/110,64.5%);以轻型为主(91/110,82.7%),未见危重型病例;14 例(12.7%)在恢复期出现了SARS‐CoV‐2 核酸检测再阳性。110 例患儿中97 例(88.2%)接种了新冠疫苗,完全接种新冠疫苗者最多(90/110,81.8%)。4组患儿性别、临床分型、SARS‐CoV‐2核酸检测再阳性率比较差异无统计学意义(P>0.05)。4 组间传播途径比较差异有统计学意义(P<0.05),经两两比较显示,完全接种组传播途径与未接种组比较差异有统计学意义(P=0.007),其他组间比较差异无统计学意义(P>0.05)。完全接种组确诊年龄大于未接种组(P<0.05)。加强针接种组、完全接种组、不完全接种组患儿确诊距末次新冠疫苗接种时间差异无统计学意义(P>0.05)。见表1。
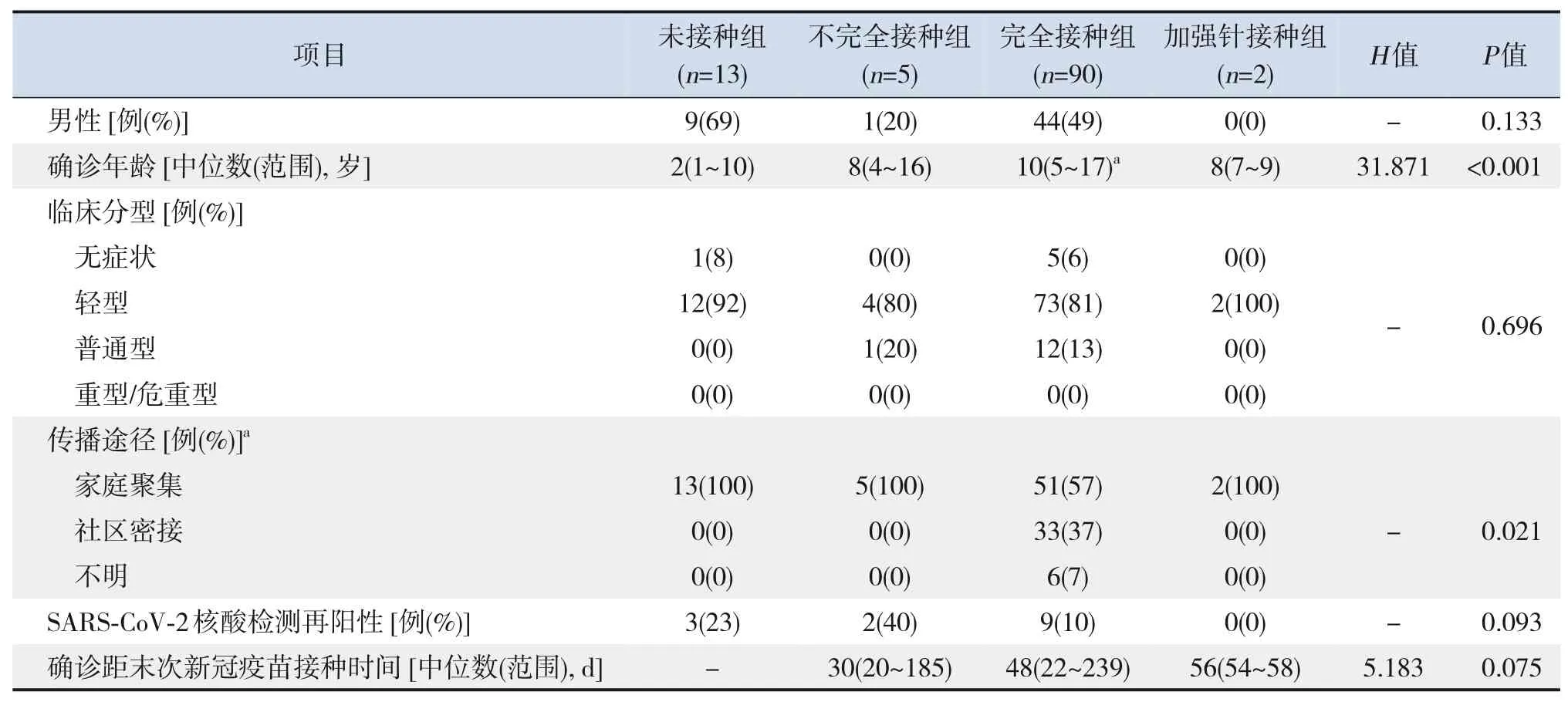
表1 4组COVID‐19患儿临床资料比较
2.2 接种疫苗厂家情况
97例患儿接种的新冠疫苗均是灭活病毒疫苗,以国药集团中国生物北京生物制品研究所(简称北京生物)疫苗接种人数最多(85/97,88%),其次为北京科兴中维生物技术有限公司(简称北京科兴)11例(11%),北京科兴/国药集团中国生物兰州生物制品研究所(简称兰州生物)仅1 例(1%),见表2。
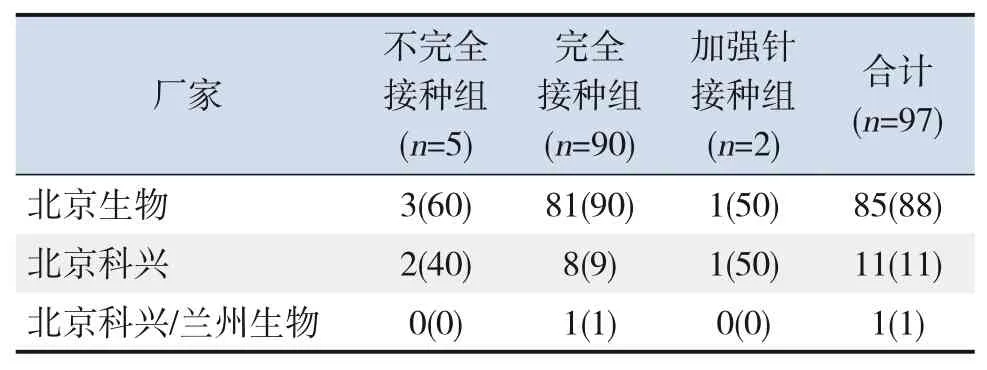
表2 97例COVID‐19患儿新冠疫苗接种厂家情况[例(%)]
2.3 4 组患儿确诊后1个月、确诊后2个月的SARS‐CoV‐2 IgG抗体水平比较
90 例患儿确诊后1个月有SARS‐CoV‐2 IgG 抗体结果,84 例确诊后2个月有SARS‐CoV‐2 IgG 抗体结果。加强针接种组、完全接种组、不完全接种组、未接种组4 组确诊后1个月、确诊后2个月的SARS‐CoV‐2 IgG 抗体水平比较差异均有统计学意义(P<0.05)。经两两比较,确诊后1个月加强针接种组、完全接种组SARS‐CoV‐2 IgG 抗体水平高于未接种组(P<0.05);确诊后2个月,完全接种组SARS‐CoV‐2 IgG 抗体水平高于未接种组(P<0.05)。见表3。
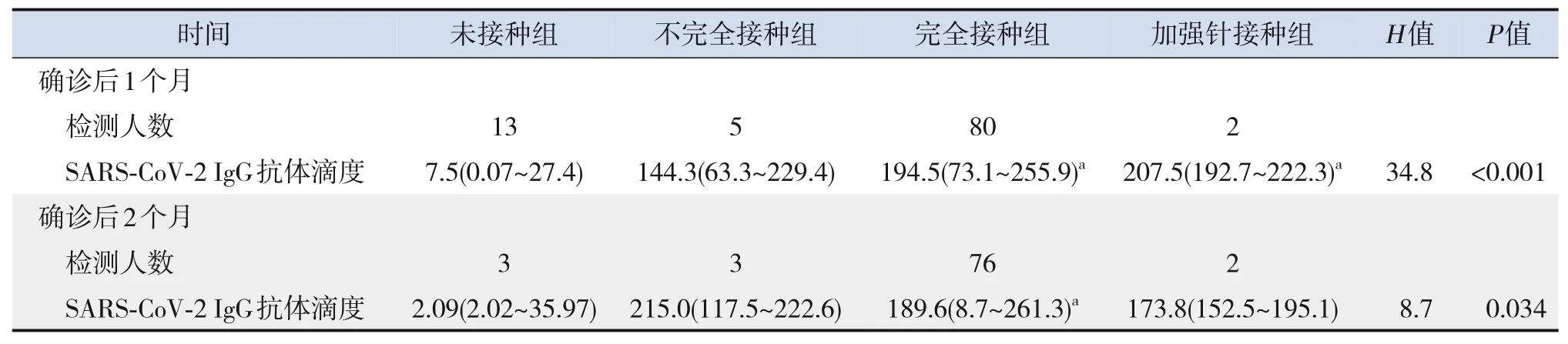
表3 4组患儿确诊后1个月、确诊后2个月的SARS‐CoV‐2 IgG抗体结果 [中位数(范围),S/CO]
2.4 4 组患儿SARS‐CoV‐2 IgG 抗体水平随时间变化情况
76 例患儿确诊后1个月及确诊后2个月均有SARS‐CoV‐2 IgG抗体结果,完全接种组确诊后2个月SARS‐CoV‐2 IgG 抗体水平低于确诊后1个月(P<0.05),加强针接种组、不完全接种组、未接种组确诊后1个月及确诊后2个月SARS‐CoV‐2 IgG抗体水平比较差异无统计学意义(P>0.05),见表4。
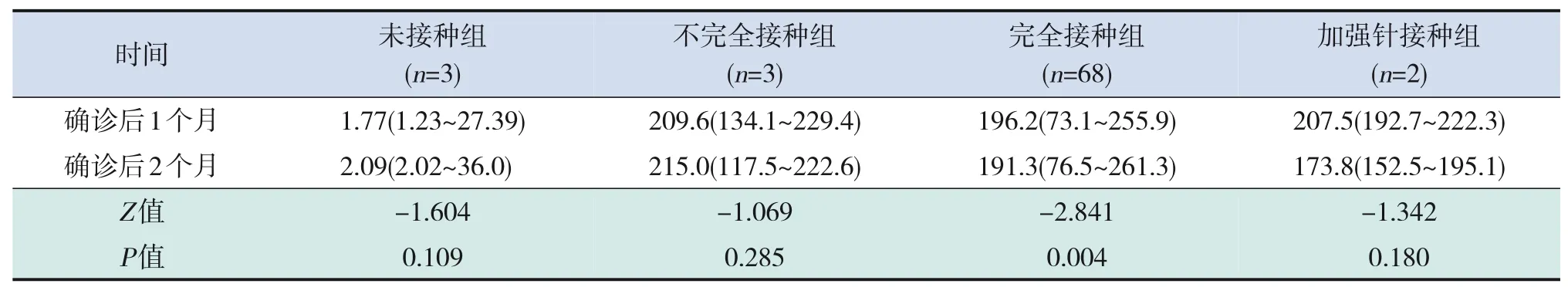
表4 4组患儿SARS‐CoV‐2 IgG抗体水平随时间变化情况 [中位数(范围),S/CO]
3 讨论
我国在2021 年7 月批准3~17岁儿童和青少年开展SARS‐CoV‐2 灭活疫苗的紧急使用[9]。截至2022 年4 月26 日,31个省(自治区、直辖市)和新疆生产建设兵团累计报告接种新冠疫苗333 628.5 万剂次[10]。此次天津市疫情发生于儿童新冠疫苗接种政策之后,本研究中,88.2%的患儿已接种了新冠疫苗,这得益于我国应接尽接的政策,接种新冠疫苗患儿与未接种新冠疫苗患儿临床分型均以轻型为主,无危重型病例,而COVID‐19 流行初期武汉华中科技大学同济医学院附属武汉儿童医院的146例患儿以普通型为主,甚至有危重型病例[11]。本研究中患儿症状普遍较轻,一方面考虑与奥密克戎变异株的自身特点有关,这与Lancet刊发的英国队列研究得出奥密克戎的致病性较Delta株有实质性下降一致[12];另一方面也与中国儿童大规模接种新冠疫苗有关。一项来自纽约的5~17岁完全接种BNT162b2疫苗的研究显示,奥密克戎时代,疫苗丧失了对5~11岁儿童感染的保护作用,但仍可以预防严重疾病[13]。
SARS‐CoV‐2 主要免疫原性成分是S 蛋白和核衣壳蛋白,在感染过程中大量产生,针对S蛋白的单克隆抗体可以中和病毒感染,中和抗体是能够灭活病毒的抗体,与许多传染性病原体的再感染保护性免疫有关[14],血浆中的中和抗体活性被认为在疫苗效力中发挥重要作用[15]。Seaman等[16]研究显示所有接种新冠疫苗的患者发生SARS‐CoV‐2 Delta 或者奥密克戎(BA.1)变体突破性感染时都有高水平的特异性抗体,本研究中接种新冠疫苗的儿童确诊后1个月及确诊后2个月也有较高水平的SARS‐CoV‐2 IgG抗体,在确诊后2个月,完全接种组有1例患儿的SARS‐CoV‐2 IgG水平明显低于同组其他患儿,提示并非所有的突破性感染会有高水平的SARS‐CoV‐2 IgG。Wang等[15]研究提示表达有效的抗S 蛋白抗体的记忆B 细胞在患者感染SARS‐CoV‐2 后至少1 年选择性地保留在体内,在接种疫苗后扩增。本研究提示接种新冠疫苗患儿感染SARS‐CoV‐2 后机体可产生较高水平的SARS‐CoV‐2 IgG 抗体,而未接种新冠疫苗的患儿在感染SARS‐CoV‐2 后SARS‐CoV‐2 IgG 抗体 水 平要低 很多,甚至有患儿的SARS‐CoV‐2 IgG 抗体为阴性。本研究中患儿确诊距末次新冠疫苗接种时间最长为239 d,确诊后1个月SARS‐CoV‐2 IgG抗体水平为173.1 S/CO。然而比较新冠疫苗不同接种剂次后再感染奥密克戎的SARS‐CoV‐2 IgG 抗体水平无明显差异,提示单剂量接种灭活新冠疫苗亦可提供保护,但并不能因此认为只需接种单剂量新冠疫苗即可,因为SARS‐CoV‐2 在不断地发生新变异,尤其是传染性最强的奥密克戎变异株推动疫情反复。迄今为止出现的所有SARS‐CoV‐2 变体中,奥密克戎对中和抗体表现出最广泛的抗性,只有少数单克隆抗体被证实可以交叉中和奥密克戎。越来越多的证据表明,额外剂量的新冠疫苗可以显著改善奥密克戎的交叉中和作用,Wang 等[17]分析了3剂疫苗接种者、2剂疫苗接种者和康复期患者的免疫情况,发现3剂疫苗接种者的抗体有更好的中和广度,可以更快速召回体液免疫,并维持较长时间,能够有效中和SARS‐CoV‐2 变异。对抗SARS‐CoV‐2是人体免疫系统必须学习而获得的能力。本研究中,对于完全接种新冠疫苗的患儿,确诊感染后SARS‐CoV‐2 IgG抗体在确诊后2个月较确诊后1个月出现轻度下降,但仍处于较高水平,因为儿童的特殊性,我们未持续监测IgG 的变化。Sughayer 等[18]研究提示接种北京生物疫苗后成人的SARS‐CoV‐2 IgG 抗 体 水 平 可 以 持 续 稳 定 至120 d,而后出现显著降低。
虽然普遍的观点认为奥密克戎的致病力较之前的变体降低,但最近发表在Pediatrics上的研究显示,奥密克戎激增期间,美国波士顿儿童医院儿童哮吼患者骤增[19],研究显示奥密克戎优先感染上呼吸道,而幼儿的鼻道相对较小,婴儿主要通过鼻子呼吸,这些因素可能会使儿童的上呼吸道疾病比成人更严重。儿童各个系统处于动态变化中,细胞免疫、体液免疫发育不完善,易受病原体感染[20],而且儿童所在托幼机构或学校是人群相对密集的场所,一旦有SARS‐CoV‐2 感染,很容易造成大范围的传播和流行。在本轮天津市疫情中,就出现了儿童在托管机构和学校的聚集性疫情,因此儿童接种新冠疫苗是非常必要的。
本研究有一定的局限性,因为3~17岁儿童已经大部分接种了新冠疫苗,纳入的未接种患儿大多在3岁以下,尚未到接种年龄;加强针接种组和不完全接种组的患儿数量均偏少,这可能是加强针接种组、完全接种组、不完全接种组之间SARS‐CoV‐2 IgG 抗体水平差异无统计学意义的原因,也是加强针接种组、不完全接种组、未接种组之间IgG抗体水平差异无统计学意义的原因;在比较确诊后1个月与确诊后2个月SARS‐CoV‐2 IgG抗体水平变化情况的时候也存在同样的问题;另外,我们无接种过新冠疫苗但未感染SARS‐CoV‐2 儿童的IgG抗体水平进行对比,因此需要更多的关于同年龄段和长期的儿童随访的数据。

