替诺福韦酯联合双重免疫方案阻断慢性乙型肝炎病毒携带孕妇母婴病毒传播的临床效果
姜先杏 洪永孟 陈 兴
广东省阳江市公共卫生医院药剂科,广东阳江 529500
乙型肝炎病毒(hepatitis B virus,HBV)是由乙型肝炎病毒持续感染所导致的肝脏慢性传染性疾病[1],母婴传播是指在围生期病原体通过胎盘、产道、哺乳等由亲代传给子代,是病毒感染的特点之一,也是HBV 最主要的传播途径,有高达50%的慢性HBV 携带者经此途径感染[2-3]。母婴传播方式复杂,包括孕妇处于妊娠期时,胎儿宫腔内感染;分娩时新生儿通过产道吸入羊水、吸吮母乳感染;此外亲密接触也可能导致感染[4-5],故母婴传播在临床中较难控制。临床现多采用乙肝疫苗与乙型肝炎免疫球蛋白联合预防方案进行干预,但仍有5%~10%发生阻断失败[6]。究其原因,孕妇分娩前血液HBV DNA 载量是影响母婴阻断效果及新生儿是否感染的主要因素[7],在妊娠后期降低孕妇HBV DNA 载量有利于提升母婴HBV 传播阻断率。本研究探讨替诺福韦酯联合双重免疫方案阻断慢性HBV 携带孕妇母婴病毒传播的临床效果。
1 资料与方法
1.1 一般资料
选取阳江市公共卫生医院2019年9月至2020年9月收治的70 例慢性HBV 携带孕妇作为研究对象,采用随机数字表法分为对照组与观察组,各35 例。对照组中,年龄20~41 岁,平均(29.73±6.32)岁;孕龄24~28 周,平均(25.08±0.63)周。观察组中,年龄20~40岁,平均(29.58±6.36)岁;孕龄24~28 周,平均(25.17±0.70)周。两组孕妇年龄、孕龄资料比较,差异无统计学意义(P>0.05),具有可比性。纳入标准:①诊断符合《慢性乙型肝炎防治指南(2019年版)》[8]中相关标准[乙型肝炎表面抗原(hepatitis B surface antigen,HBsAg)和(或)HBV DNA 阳性史>6 个月,现HBsAg 和(或)HBV DNA 结果提示阳性];②HBV DNA>2×106U/ml;③既往未服用HBV 抗病毒药物;④了解免疫应答、HBV母婴传播与阻断情况,自愿参与。排除标准:①合并艾滋病、恶性肿瘤;②其他病毒性肝炎、酒精性肝炎、药物性肝损伤、肝硬化;③精神病、语言或听力障碍。本研究经医院医学伦理委员会批准开展,所有孕妇均签署知情同意书。
1.2 方法
对照组孕期不给予抗病毒干预,观察组在孕24~28 周口服替诺福韦酯(英国Gilead Sciences Interna tional Ltd,国药准字H20180060,生产批号:CGNYP)300 mg,1 次/d,直至分娩。两组新生儿出生后均给予双重免疫方案:乙型肝炎人免疫球蛋白[华兰生物工程股份有限公司,国药准字S20023029,生产批号:201909007,规格:100 U/支(1.0 ml)]200 μg 肌肉注射+重组乙型肝炎疫苗(汉逊酵母,大连汉信生物制药有限公司,国药准字S20040016,生产批号:202004078A,规格:每瓶0.5 ml)20 μg,0、1、6 个月程序肌肉注射。
1.3 观察指标及评价标准
比较两组肝功能指标、HBV DNA 水平、新生儿HBV 感染情况、新生儿情况及用药安全性。①肝功能指标:丙氨酸转氨酶(alanine aminotransferase,ALT)、天冬氨酸转氨酶(aspartate aminotransferase,AST)采用全自动生化分析仪(日立LABOSPECT 008)进行检测,治疗前、分娩时进行分别测定。②HBV DNA 水平:采用聚合酶链式反应法检测,治疗前、分娩时进行分别测定。③新生儿HBV 感染情况:采用胶体金法检测血清标志物,分娩时,6、12 个月分别测定,HBsAg阳性率=HBsAg 阳性例数/新生儿总例数×100%,HBV阳性率=HBV 阳性例数/新生儿总例数×100%。④新生儿状态:采用Apgar 评分[9]进行测定,满分10 分,分值越高表示新生儿状态越好。⑤用药安全性:观察孕妇用药后血肌酐、血肌酸激酶、血磷等指标的水平变化情况。
1.4 统计学方法
采用SPSS 19.0 统计学软件进行数据分析,计量资料用均数±标准差(±s)表示,两组间比较采用t 检验;计数资料用率表示,组间比较采用χ2检验,以P<0.05 表示差异有统计学意义。
2 结果
2.1 两组孕妇治疗前和分娩时肝功能指标的比较
治疗前和分娩时,两组孕妇ALT、AST 水平比较,差异均无统计学意义(P>0.05);分娩时,两组孕妇ALT、AST 水平均低于治疗前,差异有统计学意义(P<0.05)(表1)。
表1 两组孕妇治疗前和分娩时肝功能指标的比较(U/L,±s)
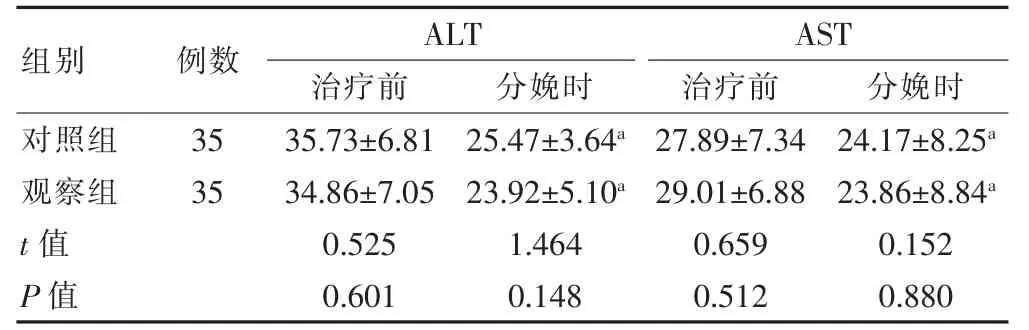
表1 两组孕妇治疗前和分娩时肝功能指标的比较(U/L,±s)
注 与本组治疗前比较,aP<0.05;ALT:丙氨酸转氨酶;AST:天冬氨酸转氨酶
组别 例数 ALT治疗前 分娩时AST治疗前 分娩时对照组观察组t 值P 值35 35 35.73±6.81 34.86±7.05 0.525 0.601 25.47±3.64a 23.92±5.10a 1.464 0.148 27.89±7.34 29.01±6.88 0.659 0.512 24.17±8.25a 23.86±8.84a 0.152 0.880
2.2 两组孕妇治疗前和分娩时HBV DNA 水平的比较
治疗前,两组孕妇HBV DNA 水平比较,差异无统计学意义(P>0.05);分娩时,观察组HBV DNA 水平低于治疗前,差异有统计学意义(P<0.05),对照组分娩时与治疗前HBV DNA 水平比较,差异无统计学意义(P>0.05);分娩时,观察组HBV DNA 水平低于对照组,差异有统计学意义(P<0.05)(表2)。
表2 两组孕妇治疗前和分娩时HBV DNA 水平的比较(lg copies/ml,±s)
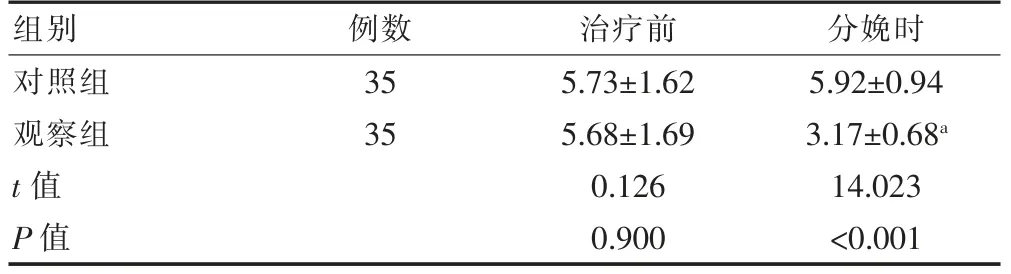
表2 两组孕妇治疗前和分娩时HBV DNA 水平的比较(lg copies/ml,±s)
注 与本组治疗前比较,aP<0.05;HBV:乙型肝炎病毒
组别 例数 治疗前 分娩时对照组观察组t 值P 值35 35 5.73±1.62 5.68±1.69 0.126 0.900 5.92±0.94 3.17±0.68a 14.023<0.001
2.3 两组新生儿不同时间点HBV 感染情况的比较
观察组HBsAg 阳性率、HBV 阳性率在分娩时,6、12 个月均低于对照组,差异有统计学意义(P<0.05);两组新生儿HBsAg 阳性率、HBV 阳性率组内各时间点比较,差异无统计学意义(P>0.05)(表3)。
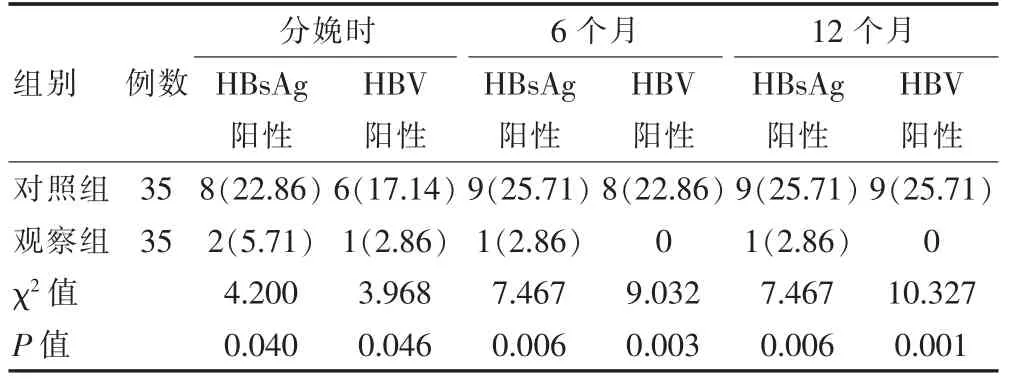
表3 两组新生儿不同时间点HBV 感染情况的比较[n(%)]
2.4 两组新生儿状态的比较
观察组新生儿Apgar 评分为(9.93±0.51)分,对照组新生儿Apgar 评分为(9.72±0.40)分,两组新生儿Apgar 评分比较,差异无统计学意义(t=1.917,P=0.060)。
2.5 两组孕妇用药安全性情况
观察组自治疗开始至分娩后,未发生血肌酐、血肌酸激酶、血磷水平明显波动,两组孕妇均未发生其他明显不良反应。
3 讨论
当前我国已全面开展疫苗接种计划,普遍的疫苗接种能够让HBV 高度流行地区的乙型肝炎流行率下降,但母婴传播引起的HBV 感染依然是世界性公共卫生问题。HBV 的传播途径最主要为母婴传播,母婴传播占现有乙型肝炎传染渠道中的50%以上。母婴传播主要包括宫内感染、产时感染、产后感染3 个方面,既往研究[10]发现,在我国有70%~90%的新生儿HBV感染来源于母婴传播,其中产时感染高达80%~85%。产时感染指的是新生儿在分娩过程中接触到含有HBV 母血、羊水、阴道分泌物等所造成的感染。新生儿出生后注射乙型肝炎人免疫球蛋白与乙肝疫苗是当前临床阻断母婴传播的首选方案,其中乙肝疫苗在接种后可刺激免疫系统产生保护性抗体,且抗体可长期发挥抗感染作用[11]。乙型肝炎人免疫球蛋白中包括了免疫球蛋白G 分子与二聚体,可有效灭杀新生儿体内的HBV[12]。但研究[13]显示,在进行上述治疗方案后仍有5%~10%的新生儿面临HBV 感染风险。对孕妇开展详细的产前检查能够降低新生儿持续性HBV感染机会,而对于HBV 阳性孕妇,在孕期接受抗病毒治疗与产后新生儿免疫接种能够有效阻断母婴传播。既往报道显示,孕妇分娩前血液HBV DNA 载量的高低将会对母婴阻断效果及新生儿感染产生直接影响,当母体血清HBV 载量大于1×106U/ml 时,新生儿采用上述治疗方案的有效保护率仅为68%。本研究结果显示,对照组在6、12 个月时HBsAg 阳性率分别为25.71%、25.71%,HBV 阳性率分别为 22.86%、25.71%,证实了上述报道结果,也说明增强HBV 母婴传播不能仅依靠分娩后方法,更需在妊娠期采用针对性药物进行干预。
本研究结果显示,治疗前,两组孕妇HBV DNA水平比较,差异无统计学意义(P>0.05);分娩时,观察组HBV DNA 水平低于对照组,差异有统计学意义(P<0.05);分娩时,6、12 个月,观察组HBsAg 阳性率、HBV 阳性率均低于对照组,差异有统计学意义(P<0.05);两组孕妇均未发生明显不良反应。提示替诺福韦酯联合双重免疫方案阻断HBV 携带孕妇母婴病毒传播效果显著,能有效降低分娩时HBV DNA 水平,降低新生儿HBV 感染率,安全性高。黄永群等[14-15]报道结果与本研究结果基本一致。替诺福韦酯是无环5′-单磷酸腺苷类似物,在经口服后能够水解为替诺福韦,再通过细胞肌酶磷酸化为替诺福韦二磷酸,可竞争于5′-单磷酸腺苷类似物,渗透入DNA 链,与HBV DNA多聚酶具有高亲和力,对DNA 链的复制过程产生抑制作用;此外,替诺福韦酯通过干扰病毒转录过程来发挥抗病毒作用,因此具有较强抗HBV 作用与高耐药性[16-17]。替诺福韦酯在妊娠期服用能够降低母体HBV DNA 水平,从源头预防HBV 母婴垂直传播,不但可降低新生儿感染风险,还能提升新生儿出生后接种疫苗阻断效果。毛创杰等[18]研究发现,妊娠期服用替诺福韦酯虽经胎盘转运,但很少进入胎儿体内,因此在妊娠期服用替诺福韦酯进行抗病毒治疗并不会对胎儿产生不利影响,可作为宫内母婴垂直传播阻断首选药物。本研究结果显示,两组孕妇治疗前、分娩时ALT、AST 水平比较,差异无统计学意义(P>0.05);两组新生儿Apgar 评分比较,差异无统计学意义(P>0.05),提示替诺福韦酯联合双重免疫方案对孕妇肝功能及新生儿影响较小,安全性较高。虽然现临床给予新生儿应用乙型肝炎人免疫球蛋白与乙肝疫苗预防性接种与妊娠中晚期给予抗病毒治疗已成为降低HBV 母婴传播的高效方法[19],但目前该治疗方案还有待进一步深入细化,如妊娠中晚期接受抗病毒治疗介入时机、药物选择、药物剂量、治疗效果监测、停药指标等,都需要大样本量的临床研究来提供数据支撑。本研究为单中心研究,所纳入样本量较小且具有一定地域性,可能导致研究所得数据存在偏倚性;在治疗方案方面没有将观察组对象分为不同治疗时间,对母亲与婴儿的随访时间比较短,无法证实停止治疗是否会引起母亲肝功能异常,后期可开展多中心、大样本、随机对照研究,对替诺福韦酯不同治疗时间及停药后对母亲肝功能的影响进行探究,进一步验证与丰富本研究成果。
综上所述,替诺福韦酯联合双重免疫方案阻断HBV 携带孕妇母婴病毒传播效果显著,能有效降低分娩时HBV DNA 水平,降低新生儿HBV 感染率,安全性高。

