靶向药物对儿童先天性心脏病合并中重度肺动脉高压肺血管反应性的治疗效果
周玲梅 许毓楷 洪钿 梁东坡 谢育梅 王树水 张智伟
1华南理工大学医学院(广州 510006);2广东省人民医院心儿科,广东省医学科学院(广州 510080);3广东省心血管病研究所(广州 510080)
肺动脉高压(pulmonary arterial hypertension,PAH)的定义是在静息状态下经标准右心导管检查测得平均肺动脉压力(mean pulmonary artery pressure,mPAP)≥25 mmHg[1]。PAH 是儿童先天性心脏病(congenital heart disease,CHD)的严重并发症之一,容易引起PAH 危象,具有较高的发病率和死亡率[2-3]。这种疾病的特点是肺血管功能进行性恶化,肺血管结构不可逆地进行性改变,导致肺血管阻力增加,最终致右心衰而死亡[4-5]。近年来,内皮素受体拮抗剂、前列环素受体激动剂等新型靶向药物的成功研发和临床应用,改善了PAH患者的生存质量[6]。然而,由于PAH 的个体化、难治性及长时间随访,靶向药物的治疗疗效评估多是基于经胸超声心动图及临床症状,多次标准心导管检查评估药物治疗效果研究甚少[7]。本研究旨在通过前瞻性的队列研究,对左向右分流CHD合并中重度PAH 患者经左右心导管检查确诊后使用靶向药物治疗,并进行规律随访,评估靶向药物对降低肺动脉压力及肺循环阻力的效果,拟达到评价肺血管反应性的目的。
1 资料与方法
1.1 研究对象 选择2017年1月至2021年3月于本中心行左右心导管检查确诊中重度PAH[肺动脉收缩压(pulmonary artery systolic pressure,PASP)>50 mmHg 且平均肺动脉压力mPAP ≥25 mmHg,予靶向药物治疗至少3月后再次行心导管检查的患儿为研究对象。纳入标准为:年龄≤18 岁;左向右分流CHD,包括房间隔缺损(ASD)、室间隔缺损(VSD)、动脉导管未闭(PDA)及上述两种以上复合畸形;所有患儿均予靶向药物治疗。药物治疗前后均完善心导管检查,根据靶向药物治疗后第二次心导管检查结果是否行手术治疗分为手术组及非手术组。第一次心导管检查后直接手术无药物治疗或手术后联合靶向药物治疗排除在外。此外排除患有复杂型先天性心脏病、心导管检查无PAH 以及靶向药物治疗后未再次行心导管检查者。本研究获得广东省人民医院伦理委员会批准(伦理号:KY-Q-2022-044-02),所有患儿行心导管检查或介入封堵、外科手术前均充分告知病情及检查手术风险,并签署手术同意书。
1.2 资料收集与随访 收集入组患儿资料,包括入组年龄、体质量、性别、解剖分型、NYHA 心功能分级、经皮血氧饱和度,六分钟步行试验、脑钠肽前体、靶向药物治疗前后经胸超声心动图资料以及心导管检查资料。靶向治疗药物主要包括内皮素受体拮抗剂ERA(波生坦、安立生坦及马昔腾坦)、5-磷酸-二酯酶抑制剂PDE-5i(西地那非、他达拉非)、人工合成前列环素PGI2 类似物(曲前列尼尔)以及前列环素IP 受体激动剂(司来帕格)。起始靶向药物治疗予二联或三联靶向药物治疗,二联药物治疗方案主要为ERA 联合PDE-5i 治疗,三联药物治疗为ERA 联合PDE-5i 及司来帕格治疗。对肺血管阻力指数(pulmonary vascular resistance index,PVRI)>6 WU·m2且肺体循环阻力比值Rp/Rs ≥0.3的患儿行急性肺血管反应试验(acute vasoreactivity testing,AVT)[8],其中第一次心导管检查时11 例行AVT 试验。CHD-PAH 中的AVT 阳性标准定义为:用药后PVRI 下降幅度>20%,并且绝对值<6 Wood·㎡,Rp/Rs 下降幅度>20%,且Rp/Rs <0.3[9]。封堵试验中肺动脉收缩压下降>20%,同时伴有PVRI 下降,而主动脉压力无明显下降,动脉血氧饱和度SaO2不下降或上升,观察20 min以上无全身不良反应,则可行永久性堵塞治疗[8]。
本研究共纳入15 例患儿,其中ASD4 例,VSD 3 例,PDA 5 例,以上两种或两种以上畸形3 例。第一次心导管前的基线特征见表1,经药物治疗后手术组8 例,非手术组7 例。靶向药物治疗前手术组的PASP,PVRI、mPAP、Rp/Rs及Pp/Ps均低于非手术组(P<0.05)。第一次心导管检查后14例予二联(波生坦联合西地那非、安立生坦联合他达拉非)靶向药物治疗,1 例予波生坦+西地那非+司来帕格治疗。
表1 一般临床资料Tab.1 General clinical data ±s
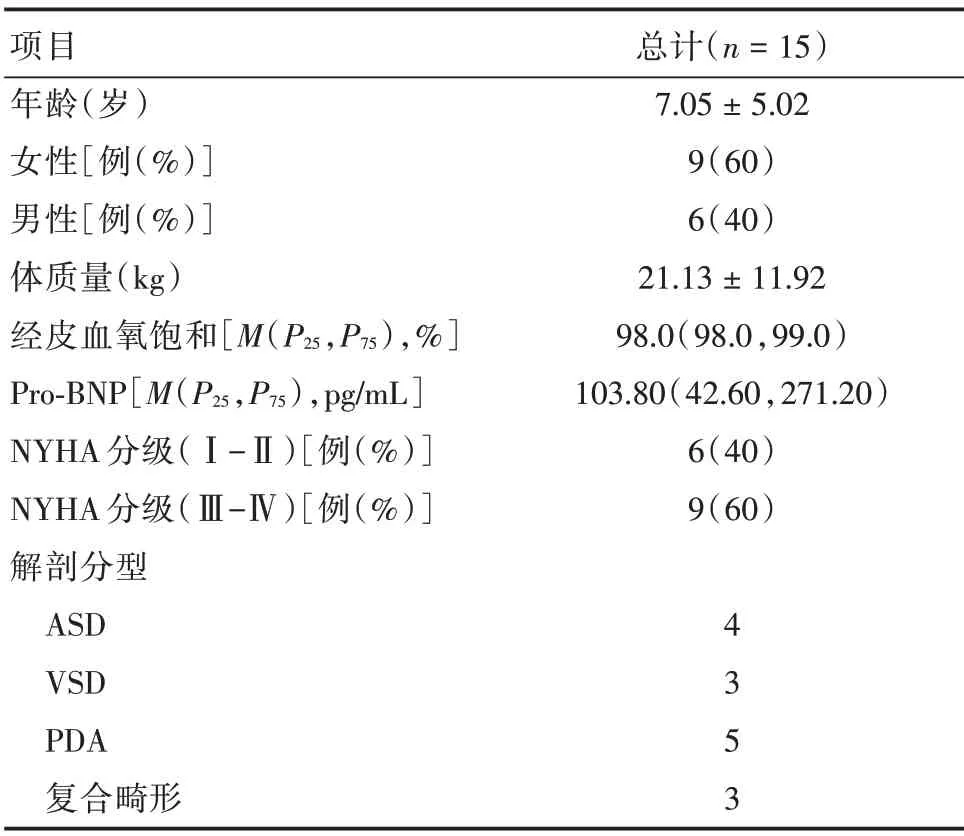
表1 一般临床资料Tab.1 General clinical data ±s
注:Pro-BNP,脑钠肽前体;ASD,房间隔缺损;VSD,室间隔缺损;PDA,动脉导管未闭
项目年龄(岁)女性[例(%)]男性[例(%)]体质量(kg)经皮血氧饱和[M(P25,P75),%]Pro-BNP[M(P25,P75),pg/mL]NYHA 分级(Ⅰ-Ⅱ)[例(%)]NYHA 分级(Ⅲ-Ⅳ)[例(%)]解剖分型ASD VSD PDA复合畸形总计(n=15)7.05±5.02 9(60)6(40)21.13±11.92 98.0(98.0,99.0)103.80(42.60,271.20)6(40)9(60)4 3 5 3
1.3 统计学方法 采用SPSS 25.0统计软件进行数据分析。计量数据正态分布以()表示,采用t检验;偏态分布以M(P25,P75)表示,采用Wilcoxon 秩和检验;计数资料以例(%)表示,采用χ2或Fisher检验。自身前后对照符合正态分布采用配对样本t检验,偏态分布采用相关样本秩和检验。以P<0.05 为差异存在统计学意义。
2 结果
2.1 靶向药物治疗效果
2.1.1 心导管检查资料 心导管检查评估血流动力学指标,包括肺动脉压力及阻力。所有患儿靶向药物治疗后mPAP、PVRI、肺体循环血流比值Qp/Qs较治疗前明显下降(P<0.05);RAP、SvO2、CI、Rp/Rs、Pp/Ps 未见明显改变(P>0.05,表2)。所有患儿经靶向药物治疗后,二次导管检查时8 例患儿行手术治疗,术后继续口服靶向药物治疗;7例患儿肺动脉压力及阻力无改善,暂无手术指征,调整药物治疗方案。
表2 CHD-PAH 患儿靶向药物治疗前后心导管检查资料Tab.2 Data of cardiac catheterization in CHD-PAH children before and after targeted drug therapy ±s

表2 CHD-PAH 患儿靶向药物治疗前后心导管检查资料Tab.2 Data of cardiac catheterization in CHD-PAH children before and after targeted drug therapy ±s
项目mPAP(mmHg)PVRI[M(P25,P75),Wood·㎡)]RAP(mmHg)SvO2(%)CI Qp/Qs[M(P25,P75)]Rp/Rs[M(P25,P75)]Pp/Ps靶向药物治疗前58.60±16.28 11.10(8.34,24.40)7.87±3.42 73.60±7.36 4.21±1.72 1.11(0.70,1.34)0.91(0.67,1.50)0.91±0.19靶向药物治疗后51.33±19.40 5.39(3.27,19.09)6.47±2.62 74.4±6.54 4.22±1.13 1.20(0.98,2.75)0.39(0.20,1.14)0.84±0.25 t/Z 值2.257-3.010 1.443-0.539-0.426-1.988-1.533-1.251 P 值0.041 0.003 0.171 0.598 0.670 0.047 0.125 0.211
第一次心导管检查时11 例(73.3%)行AVT 试验,其中18.2%(2/11)阳性。3 例封堵试验均阴性,1 例因PVRI <6 Wood·m2未行AVT 或封堵试验。第二次心导管检查3 例行AVT 试验均阴性,1 例(1/4)封堵试验阳性。
2.1.2 经胸超声心动图资料 经胸超声心动图评估患儿各房室大小、心功能情况及估测PASP。其中随访终点及二次导管检查时估测PASP 较用药前下降(P= 0.011),重复测量分析三个时间点经胸超声心动图估测的PASP 差异有统计学意义(P= 0.006)。靶向药物治疗后的肺动脉高压严重程度较前也明显下降(图1)。但心房比值RA/LA、心室比值RA/LA、肺动脉/主动脉PA/AO、肺动脉大小PA、LVEF 与用药前相比差异无统计学意义(P>0.05,表3)。

图1 靶向药物治疗前后经胸超声心动图评估肺动脉高压分度Fig.1 Transthoracic echocardiography to evaluate pulmonary arterial hypertension before and after targeted drug therapy
表3 CHD-PAH 患儿靶向药物治疗前后超声心动图资料Tab.3 Data of transthoracic echocardiography in CHD-PAH children before and after targeted drug therapy ±s

表3 CHD-PAH 患儿靶向药物治疗前后超声心动图资料Tab.3 Data of transthoracic echocardiography in CHD-PAH children before and after targeted drug therapy ±s
注:RA/LA,右房大小/左房大小;RV/LV,右室大小/左室大小;PA/AO,肺动脉/主动脉;PA,肺动脉;LVEF:左室射血分数;PASP,肺动脉收缩压
项目RA/LA RV/LV[M(P25,P75)]PA/AO PA(mm)LVEF(%)估测PASP(mmHg)靶向药物治疗前1.27±0.08 1.44(1.29,1.75)1.37±0.27 20.20±5.67 72.33±5.91 79.27±26.18第二次心导管检查1.27±0.34 1.43(1.13,1.60)1.34±0.33 20.27±5.54 71.74±7.98 68.80±27.68 t/Z 值0.015-0.568 0.383-0.080 0.583 2.913 P 值0.989 0.570 0.708 0.937 0.569 0.011随访终点1.24±0.29 1.31(1.06,1.45)1.33±0.41 20.67±7.85 70.87±7.77 66.58±30.70 t/Z 值0.445-1.363 0.356-0.376 0.719 3.240 P 值0.663 0.173 0.826 0.950 0.484 0.008
2.2 预后 15 例患儿中,8 例经靶向药物治疗后肺血管阻力及压力下降符合手术指征行手术治疗(图2),其中7 例介入封堵治疗,1 例外科手术治疗;7 例高阻力患儿药物后因肺动脉压力及阻力仍高,暂无手术指征,继续口服双联或三联靶向药物治疗。随访时间为(23.00±13.46)个月,所有患者至随访终点时无人死亡,无肺高压危象发生。药物治疗过程中无头痛等不良反应,肝功能均正常。至随访终点时,手术治疗后患儿超声心动图估测PASP 时5 例无PAH,2 例轻度PAH,1 例随访至术后1月为重度PAH;非手术患儿中6 例为重度PAH,1 例中度PAH。靶向药物治疗前手术治疗的患儿PASP,PVRI、mPAP、Rp/Rs 及Pp/Ps 均明显低于未手术患儿(P<0.05),提示这些因素将影响靶向药物的治疗效果及预后。

图2 靶向药物治疗前后手术及非手术患儿mPAP 及PVRI变化Fig.2 Changes of mPAP and PVRI in surgical and non-surgical children before and after targeted drug therapy
3 讨论
CHD-PAH 指由体-肺分流型CHD 所引起的肺动脉压力升高,是引起儿童PAH 最常见的原因。早期肺血管床损害可逆,经手术治疗后肺动脉压力可改善;长期未经治疗的严重CHD-PAH 引起不可逆损害,最终导致艾森曼格综合征,失去手术机会[9-10]。因此,在CHD 引起的PAH 早期及时予手术治疗及(或)靶向药物治疗可改善患者预后及生存时间。目前儿童PAH 靶向药物的治疗依据大多基于成人的临床试验以及临床专家的经验,但儿童CHD-PAH 的肺血管床状态及特点较成人大不相同,对于儿童患者的研究以及治疗尚未有明确的策略及标准,PAH 儿童患者的管理仍存在挑战[11-12]。
在CHD-PAH 及特发性肺动脉高压(IPAH)患儿中,通常使用AVT 试验评估患儿的肺血管反应性,但两者的标准及治疗方案均不相同。对于IPAH 患儿而言,AVT 试验阳性最新遵循Sitbon 标准定义为:试验后mPAP 下降≥10 mmHg 且绝对值≤40 mmHg,心输出量增加或不变;建议采用钙离子拮抗剂(CCB)治疗[9]。但CHD-PAH 患儿AVT 阳性有手术治疗机会。此外,CHD-PAH 患儿还可行试封堵试验评估肺血管反应性以寻求手术时机。在本研究中,并非所有的患儿均行AVT 试验或试封堵试验。一方面,多项研究表示AVT 试验阳性率低[13-14],本研究中也仅有2 例患儿阳性。另一方面,AVT 试验导致手术时间长,手术风险增加,费用增加。在本研究所有患儿经靶向药物治疗后,mPAP 及PVRI 较用药前均下降,因此笔者认为靶向药物治疗可作为一种新的评估肺血管反应性的安全方法。靶向药物治疗后再次心导管检查,若肺血管压力及阻力明显下降,提示药物治疗可改善肺血管床状态。
靶向药物可改善患者的临床症状及血流动力学指标,正广泛运用于PAH 患者的治疗[15]。目前临床常用的除波生坦、安立生坦,西地那非、他达拉非及曲前列尼尔外,新的靶向药物如马昔腾坦及司来帕格也被证实可改善患者的预后[16-18]。此外,索他西普(Sotatercept)作为逆转制剂抑制PAH中BMPR-II 信号的表达,通过新的作用机制在2 期试验中其疗效得到初步验证[19]。多项研究显示,靶向药物联合治疗相较于单药治疗而言效果更著[20-21]。因此,根据风险分层建议PAH 患者起始联合治疗,尽早达标。对于初治PAH 患者,若为低或中危状态,起始联合不同通路靶向药物治疗,若为高危状态起始联合应包括静脉前列环素类靶向药物治疗[8,22]。靶向药物起始联合治疗使用安立生坦及他达拉非,但其在儿童中有效性及安全性有待进一步研究[9,22]。在本组研究中,所有患儿起始联合治疗,未手术组二联靶向药物者第二次评估肺动脉压力及阻力后使用三联靶向药物或加用静脉曲前列尼尔。所有患儿药物治疗后mPAP、PVRI 及估测PASP 较用药前均下降,提示靶向药物治疗有效。
目前国内外CHD-PAH 儿童的样本量相对较少,且多数研究采用心脏超声或临床症状评估PAH 患者的状态,但心导管检查仍是确定PAH、评估肺动脉压力及阻力的金标准。本研究主要经过用药前后的标准心导管检查评估患儿的肺血管情况,更确切地证实了靶向药物的治疗疗效。研究表明,部分患儿经靶向药物治疗后,可获得手术机会。但本研究局限性在于样本量少,测量的指标阳性率低,而且研究过程中发现部分高阻力的未手术组PH 患者其Pro-BNP 正常或增高不显著,未来需要更多的样本量及研究证实未手术组的药物疗效。
综上,靶向药物治疗降低CHD-PAH 患儿的mPAP 及PVRI,可评估其肺血管反应性。心导管检查明确了PAH 的性质及程度,为CHD-PAH 患儿提供更加精准的治疗策略。

