锂离子电池长循环寿命Sn+Co负极材料的研究
肖开元
(湖南省冶金材料研究院有限公司,湖南 长沙 410129)
近年来,由于化石燃料的大量消耗及其不可再生的缺点迫使人们加快了可再生能源的开发[1]。但随着可再生能源的不断发展和利用,发现风能、潮汐能、太阳能等都具有不可靠性和间歇性的特点,将这些可再生能源顺利整合到现有的电网中也是一个具有挑战性的难题,这就让储能技术的研究和应用迫在眉睫[2]。一个理想的大型储能系统需要具有低成本、长循环寿命、高功率、高能量密度等特点,利用二次电池的储能技术是目前最有前途的方法之一[3]。
锂离子电池由于具有高能量密度和长循环寿命等优点,已作电化学储能设备广泛应用于运输、便携式电子、航空航天和军事设备等众多领域[4]。目前锂离子电池正极材料如锰酸锂、钴酸锂、磷酸铁锂及三元材料等已广泛实现商业化,而商业化的负极材料极少,多采用商业化的石墨(372 mAh/g),但其理论比容量不高,直接影响了商业锂电池的整体能量密度。锡金属负极材料由于具有较高的理论比容量(992 mAh/g)和自然界中含量较为丰富等优势被认为是商业化石墨最有前景的替代材料之一。但锡基负极材料在实际应用的过程中往往受限于较差的循环性能和倍率性能,其重要原因是锡基负极材料在充放电过程中存在严重的体积膨胀,导致负极材料容易粉碎。目前提高锡基负极材料循环稳定性的方法主要是集中在材料结构改变和空间设计上,如制备纳米材料以减少离子扩散的路径和增强结构的稳定性[5]。
本研究着重于解决锡基负极材料循环稳定性不佳的情况,通过恒流/脉冲电化学沉积方法制备了Sn+Co、Sn-Co合金负极材料,并采用XRD、SEM和EDX等方法研究了材料的结构,CV、EIS及恒电流充放电循环测试等研究了其电化学性能,得到了性能优良的Sn+Co复合负极材料,该电极在0.1C的电流密度下循环120次后容量保持率可以达到81.43%,为以后锂电池锡基负极材料的商业化提供了一定的理论基础和实际参考意义。
1 试验部分
1.1 Sn+Co复合电极的制备
Sn+Co复合电极在室温下通过恒流/脉冲电沉积法制备。电沉积时使用10μm厚的铜箔作为阴极,并在沉积前使用稀硫酸(5%)纯化,然后依次用乙醇和去离子水清洗铜箔。电沉积过程采用Maccor系列MC-16系统进行,阳极为铂箔电极。将铜箔裁剪成尺寸为4 cm×5 cm的小片置于SnSO4和柠檬酸混合液中,在2 mA/cm2恒电流密度的条件下电沉积10 min,随后用乙醇和去离子水清洗极片置于CoSO4和柠檬酸混合液中,在5 mA/cm2脉冲电流密度的条件下电沉积5 min。最后用乙醇和去离子水清洗极片烘干即得到了Sn+Co复合电极。
1.2 Sn-Co合金电极的制备
Sn-Co合金电极在室温下通过恒流电沉积法制备。电沉积时使用10μm厚的铜箔作为阴极,铂箔为阳极,采用Maccor系列MC-16系统进行。铜箔在沉积前使用稀硫酸(5%)纯化,然后依次用乙醇和去离子水清洗。将铜箔裁剪成尺寸为4 cm×5 cm的小片置于SnSO4、CoSO4和柠檬酸混合液中,在2 mA/cm2恒电流密度的条件下电沉积10 min,最后用乙醇和去离子水清洗极片烘干即得到了Sn-Co合金电极。
1.3 材料表征
通过XRD来研究Sn+Co复合材料及Sn-Co合金材料的晶体结构(Cu Kα;λ=1.541 6Å)。采用扫描电子显微镜(SEM;ZEISS SUPRA-55)和能量色散X射线光谱(EDX;Oxford X-Max)来研究Sn+Co复合材料及Sn-Co合金材料的微观形貌结构、化学组成及元素分布等。
1.4 电化学表征
电极的电化学性能以例如Sn+Co//Li组成的CR2032型扣式电池(充满氩的手套箱中组装)来表征,电解液为1 M的六氟磷酸锂(LiPF6),溶剂为碳酸乙酯(EC)、碳酸二甲酯(DMC)和碳酸乙酯(EMC)的混合液(体积比1∶1∶1)。扣式电池的CV、EIS曲线由辰华CHI-660E电化学系统测试,其循环性能由新威电池测试系统通过恒电流充放电手段来测试。
2 结果与分析
2.1 结构、形貌表征
在SnSO4、CoSO4和柠檬酸混合液中,2 mA/cm2恒电流密度的条件下于铜箔阴极上电沉积10 min制备得到了Sn-Co合金电极材料。在SnSO4和柠檬酸混合液中,2 mA/cm2恒电流密度的条件下于铜箔阴极上电沉积10 min后再置于CoSO4和柠檬酸混合液中,在5 mA/cm2脉冲电流密度的条件下电沉积5 min制备得到了Sn+Co复合电极材料。对电沉积合成的产物进行结构分析,具体结果如图1所示。
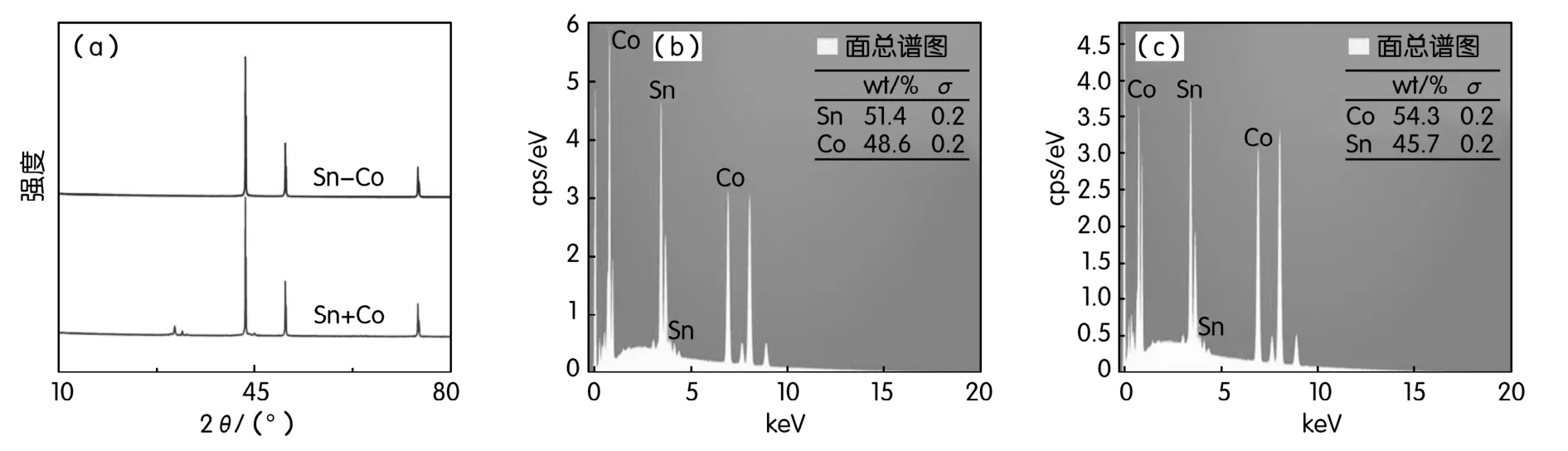
图1 Sn+CO、Sn-Co材料的XRD图和元素含量图
由图1(a)所知,Sn+Co及Sn-Co材料结晶良好且无杂质,峰形上的差异主要由晶型差异导致,Sn-Co为单晶和合金混合物而Sn+Co则为单独的Sn、Co晶体。图1(b)、图1(c)是EDX识别的元素类型及含量,可以清晰看到材料均由Sn、Co组成,佐证了XRD图中高纯度、无杂峰的试验结果。除此之外,Sn+Co中Sn的含量高于Sn-Co,由于Co在其中充当惰性元素,而Sn则为提供容量的有效成分,这也为后续两者容量上有差异提供了证据。
为了进一步了解两种材料的形貌信息,采用SEM来观察Sn+Co及Sn-Co材料的微观形貌,具体结果如图2所示。
由图2的SEM图可以看出,Sn+Co复合材料由极小的纳米颗粒聚集而成且表面致密,而Sn-Co合金材料由具有几百个纳米的较大粒子组成且表面较为疏松。较小的粒径可以大大缩短锂离子的运输距离从而提高材料的倍率性能,致密的Co表面可以阻挡Sn材料与电解液的接触,从而减少副反应达到提高循环性能的效果。除此之外,致密的Co表面层还可以缓冲Sn材料在充放电过程中的体积变化,保护材料的结构稳定性。

图2 Sn+Co、Sn-Co材料的SEM图
为了进一步了解两种材料的元素分布信息,采用EDX来观察Sn+Co复合材料及Sn-Co合金材料的微观元素分布情况,具体结果如图3、图4所示。
由图3的EDX图可以看出,Sn+Co复合材料中Cu、Sn、Co元素分布均匀。而由图4的EDX图可以看出,Sn-Co合金材料中Cu、Sn元素分布均匀,但Co元素分布存在不均匀区且存在部分Sn晶体,也为后续充放电过程中产生较大体积膨胀埋下了隐患。

图3 Sn+Co复合材料的EDX图

图4 Sn-Co合金材料的EDX图
2.2 电化学表征
通过上述的结构、形貌表征结果分析可以得知Sn+Co复合材料的性能应该优于Sn-Co合金材料,为了验证这一结果,采用CV、EIS及恒电流充放电等电化学手段进一步测试。
由于两个材料作为锂电池负极储能的有效成分都是Sn,所以此处只对Sn+Co复合材料进行了CV测试,如图5所示,分析其电化学上是否可逆。而材料的表面及组成都会影响电化学反应过程中的电阻,所以对两个电极材料都进行了EIS测试,如图6所示,分析其溶液电阻、电化学电阻等数据。

图5 Sn+Co复合材料在1 M LiPF6中的CV图

图6 两个材料在1 M LiPF6中的EIS图
由图5的CV图可知,Sn基材料在作为锂离子电池负极材料时高度可逆,具有多对氧化还原峰,其中一对为主,其他为辅。在第一圈CV图中,还原峰峰位约为0.2 V(vs.Li)略低于后续循环的还原峰峰位(0.35 V vs.Li),而后续氧化还原峰峰位基本重合,主要是因为在第一圈放电过程中形成SEI膜所导致,也是首圈充放电效率较低的主要原因。
图6则由Sn+Co、Sn-Co材料和锂片组成的扣式电池在1 M LiPF6电解液中的EIS图。由图6可知,两个材料的EIS曲线几乎重合,这说明两个材料的电化学阻抗接近,Sn+Co复合材料略低于Sn-Co合金材料,但总体来说阻抗都偏大,不利于电池进行高倍率运行。分别将Sn+Co复合材料、Sn-Co合金材料、Sn与锂片、1 M LiPF6电解液组成扣式电池并进行恒电流充放电测试以检验各个材料的循环性能。Sn+Co复合材料在0.1C电流密度下的电池循环图如图7所示。由图7可知,Sn+Co复合材料的首圈放电比容量高达541.66 mAh/g,充电比容量达到483.97 mAh/g,充放电效率为89.35%,首圈后效率迅速提高至97%以上(得益于首圈SEI膜的形成)。前期充放电比容量呈现上升趋势是因为材料活化所致,而波动性是因为早晚气温的变化,其中该材料的最高放电比容量高达563.33 mAh/g,充电比容量为547.73 mAh/g,充放电效率为97.23%。
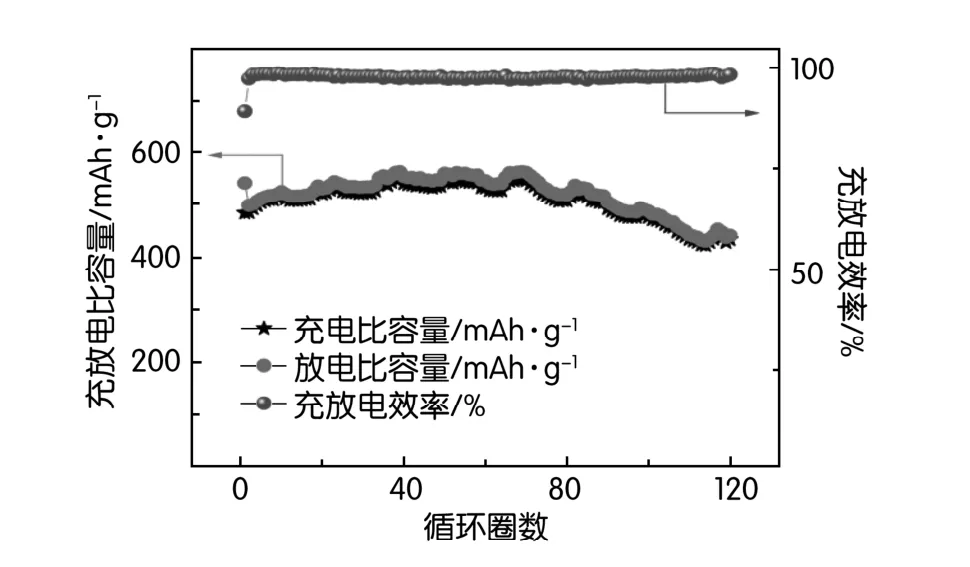
图7 Sn+Co材料的电池循环图
Sn+Co、Sn-Co及Sn材料在0.1C电流密度下的电池循环对比图如图8所示。由图8可知,Sn+Co复合材料比Sn-Co合金材料具有更高的放电比容量(首圈541.66 mAh/g vs.340.01 mAh/g),得益于更佳的纳米结构和更高的Sn含量,这与之前SEM及EDX含量分析结果是一致的。且Sn+Co复合材料比Sn-Co及Sn材料具有更好的循环稳定性(120圈放电比容量保持率81.43%vs.60.48%vs.9.09%),得益于更佳的纳米结构和致密的Co表面保护层,这与之前SEM分析结果是一致的。

图8 Sn+Co、Sn-Co及Sn材料的电池循环对比图
3 结 论
通过恒流/脉冲沉积在铜箔上制备了一种锡基锂离子电池负极材料(Sn+Co),其中Co主要作用是在锡表面形成致密保护层。该致密的电惰性层不仅可以缓冲Sn的体积变化,还避免了充放电过程中Sn与电解质的反应,提高了固体电解质界面(SEI)的稳定性。材料的结构表征和电化学表征表明了Sn+Co复合材料负极比Sn-Co合金材料负极及Sn负极具有更大充放电比容量和更优异的循环性能。Sn+Co电极在0.1C电流密度下的首次放充电比容量分别为541.66 mAh/g和483.97 mAh/g,效率89.35%,且Sn+Co电极在循环120次后容量保持率高达81.43%,远高于Sn-Co合金电极和Sn电极60.48%、9.09%的保持率,为Sn基锂离子电池负极材料的商业化提供了思路和实际参考价值。

