特殊医学用途全营养配方食品干法混合工序的工艺验证
刘宝华,徐庆利,巴宁宁,杜玲玲
青岛圣桐营养食品有限公司北京技术中心,北京 101100
0 引言
特殊医学用途配方食品是为了满足进食受限、消化吸收障碍、代谢紊乱或特定疾病状态人群对营养素或膳食的特殊需求,专门加工配制而成的配方食品;该类食品必须在医生或临床营养师指导下,单独食用或与其他食品配合食用[1]。依据《GB 29922—2013 食品安全国家标准 特殊医学用途配方食品通则》,特殊医学用途配方食品包括全营养配方食品、特定全营养配方食品及非全营养配方食品,其中全营养配方食品指可作为单一营养来源满足目标人群营养需求的特殊医学用途配方食品。截止到2022年2月统计,国家市场监督管理总局已批准注册81 款特殊医学用途配方食品,其中10岁以上特殊医学用途全营养配方食品15 款(其中粉剂14款)。依据《GB 29923—2013 食品安全国家标准 特殊医学用途配方食品良好生产规范》[2],粉末状产品的生产工艺包括湿法、干法及干湿混合工艺。干法混合是指把两种或两种以上不同物性的粉粒体,依靠外加的适当操作,尽量使各成分的浓度分布达到均匀化的一种操作[3],其特点是能耗低,工艺操作简单,生产过程中营养素基本不发生损失[4],是特殊医学用途配方食品常用的混合工艺。但由于产品物料差异大,混合过程会存在不均匀的情况,如果混合不均匀将会影响产品的质量,进而引起目标人群营养不良。因此,须对特殊医学用途全营养配方食品的生产工艺进行工艺验证以保证各批次产品的稳定性、营养充分性及安全性。
工艺验证指对商业化生产的产品质量进行监控和趋势分析,以确保工艺和质量始终处于受控状态,其在药品中的应用较为广泛[5]。2016年原国家食品药品监督管理总局发布总局令第24号《特殊医学用途配方食品注册管理办法》,对特殊医学用途配方食品注册做出规定,并在配套文件《特殊医学用途配方食品注册申请材料项目与要求(试行)(2017修订版)》中提出注册材料需提交工艺研究材料,包括工艺参数确定和工艺验证等。另外GB 29923—2013[2]中增加“需对生产过程进行验证以确保整个工艺的重现性及产品质量的可控性”的要求,相似内容在《特殊医学用途配方食品生产许可审查细则》中也予以明确[6]。综上,特殊医学用途配方食品必须对生产过程进行验证以确保整个工艺的重现性及产品质量的可控性。
特殊医学用途配方食品干法工艺中混合机为关键设备且混合工序为生产关键控制环节,其对产品营养素控制起着关键作用,因此本试验主要对干法混合工序进行工艺验证。原国家食品药品监督管理总局2017年第65号公告《婴幼儿配方乳粉产品配方注册申请材料项目与要求(试行)(2017修订版)》中提出,商业化生产工艺验证报告包括对样品均匀性、工艺稳定性及营养成分符合性的分析。由于《特殊医学用途配方食品注册申请材料项目与要求(试行)(2017修订版)》中未对工艺验证进行详细阐述,因此,参考婴幼儿配方乳粉的注册要求,本研究通过混合均匀性、营养成分符合性及工艺稳定性三方面对特殊医学用途全营养配方食品的干法混合工序进行工艺验证,旨在为使用干法混合工艺生产特殊医学用途配方食品的企业提供工艺验证的方案。
1 试验方法
为了保证特殊医学用途全营养配方食品生产工艺的稳定性和可靠性,确保商业化条件下生产的产品符合质量标准及注册要求,因此,本研究通过分析连续三批次相同批量试验样品的混合均匀性、工艺稳定性和营养成分符合性,完成对混合工序的工艺验证。
1.1 材料及设备
由植物脂肪粉、固体玉米糖浆、乳清蛋白粉、复合维生素、复合矿物质等通过干法工艺加工制成的、适用于10岁以上需要营养补充人群食用的粉状特殊医学用途全营养配方食品。
混合机,秦皇岛燕大源达机电科技股份有限公司;电子天平,梅特勒-托利多公司;气相色谱质谱联用仪、原子吸收光谱仪,赛默飞世尔科技公司;高效液相色谱仪,沃特世科技有限公司;紫外可见分光光度计,岛津仪器有限公司;等。
1.2 生产工艺
依据相关法规,特殊医学用途全营养配方食品干法生产工艺流程见图1。
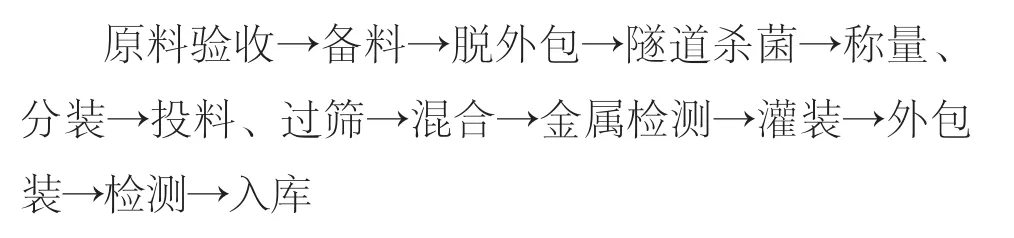
图1 工艺流程
1.3 检测方法
按照GB 29922—2013中规定的国家安全标准分析方法进行检测,检测方法具体见表1。
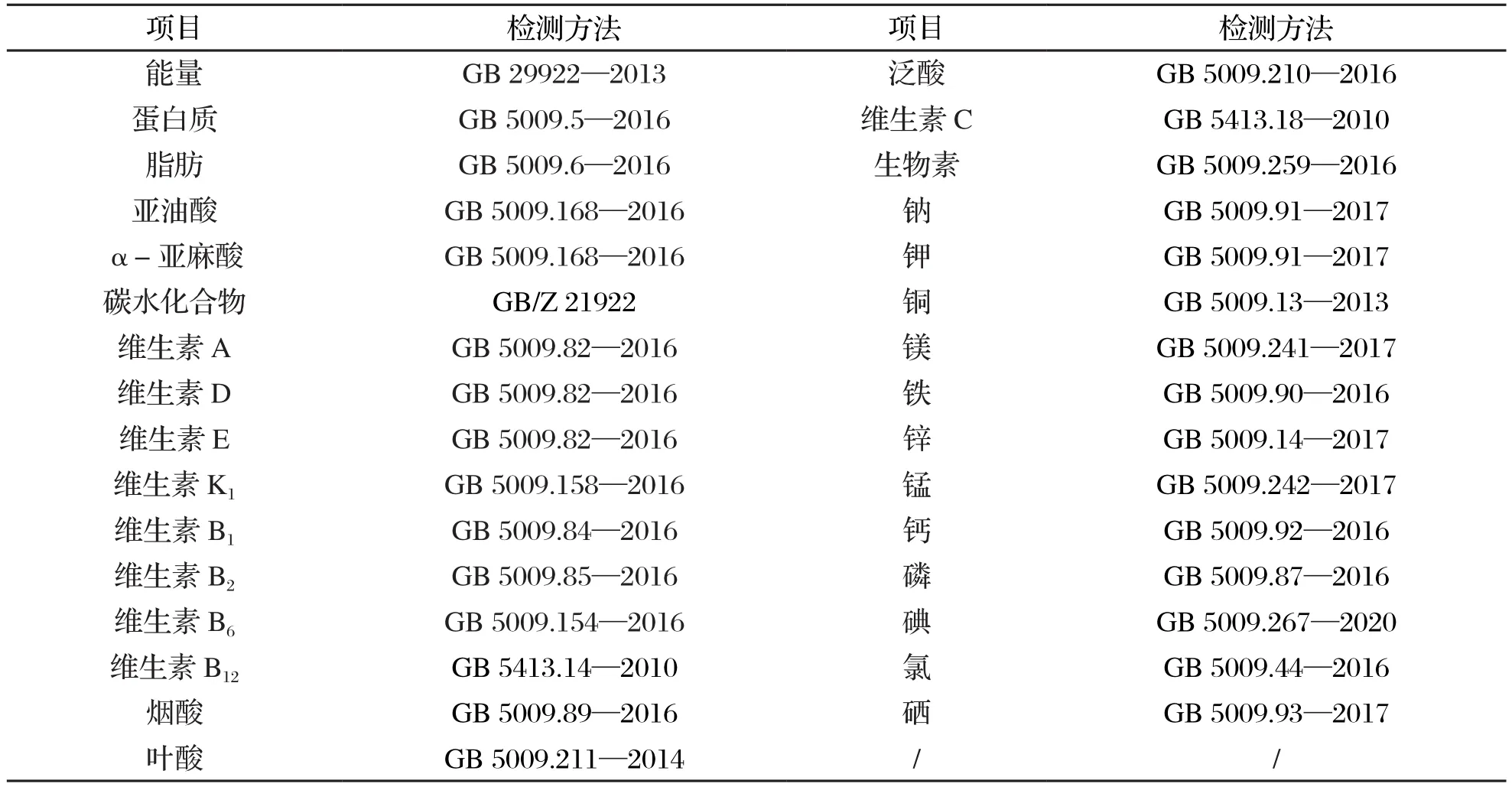
表1 营养素检测方法
1.4 混合均匀性
1.4.1 确定代表性营养素
由于各原辅料的颗粒状态不一致,极易造成物料混合不均匀而影响终产品质量。因此,各营养素的混合均匀度是否得到有效控制,是验证干法混合工艺可行性的重要指标[7]。混合均匀性应选择具有代表性的营养素(不易混匀、添加量较小的维生素、矿物质等)进行验证,本试验选取的代表性项目见表2。
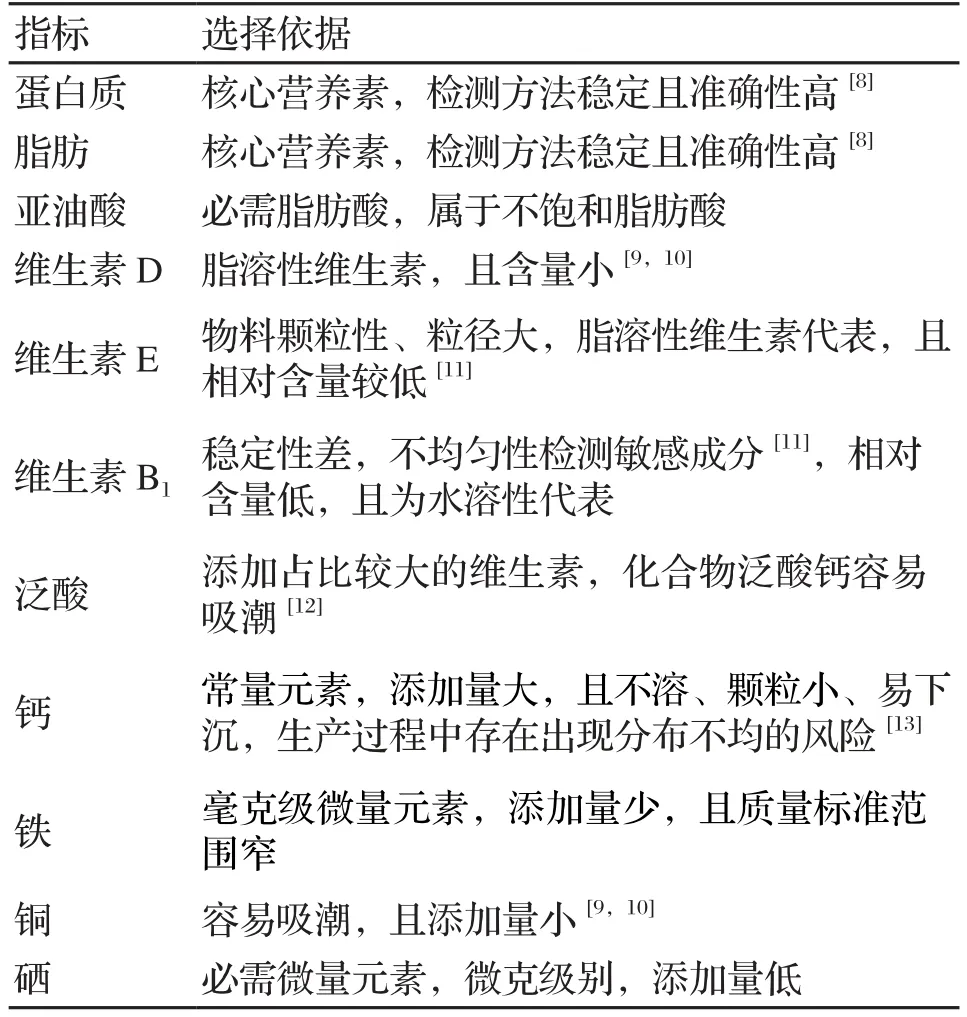
表2 代表营养素的确定依据
1.4.2 取样方案
依据《CNAS-GL03 能力验证 样品均匀性和稳定性评价指南》[14]《GB/T 10649—2008 微量元素预混合饲料混合均匀度的测定》[15]《GB/T 21122—2007营养强化小麦粉》[16]《药品GMP指南:口服固体制剂》[17]及相关文献[18],物料混合完成后在混合机出口抽取10 个代表性的原始样品(既包括产品的表层,又包括内部),且首尾两个样品应在开始出料和最后粉尾时取样,每个点取样量相对适中,取样时不允许有任何翻动或再混合。
1.4.3 计算方法
对所取样产品检测代表性营养成分,参考GB/T 5918—2008[19]中混合均匀度的计算方法,混合均匀度值以变异系数(CV)表示,通过不同位置产品的营养素指标的差异化分析,验证工艺的混合均匀性[20],CV值越大,混合均匀度越差[13],理想混合状态下的变异系数应为零[21]。GB/T 21122—2007中强化营养素的混合均匀度变异系数≤10%[16],原国家食品药品监督管理局药品认证管理中心编写的《药品GMP指南:口服固体制剂》中混合均匀度变异系数的接受标准≤5%[17],美国食品药品监督管理局(FDA)《混合均匀性取样和评价指南》规定混合均匀度的变异系数≤5%[22]。评价特殊医学用途全营养配方食品中营养成分的均匀性成为反映工艺是否科学的依据,同时也是判断产品是否合格的重要前提。
1.5 营养符合性
按照国家有关规定随机抽取样品,并对三批次的特殊医学用途全营养配方食品进行全项目检验。依据相关文献可知,干法工艺生产过程中各营养素基本不发生损失[4],因此,可通过产品营养素检测值与配方设计值的偏差验证产品干法混合工艺条件下的成分营养符合性[10]。美国FDA提出检测值应在均值的±10%以内[22],检测值与设计值的偏差在检测方法的精密度范围内[23~25],均说明产品设计合理、可控。
1.6 工艺稳定性
同一配方连续三批次重复性生产,对产品的营养指标进行全项目含量测定,分析不同批次的差异情况,以验证工艺的稳定性[26]。工艺稳定性以相对标准偏差(RSD)表示。参照美国FDA《混合均匀性取样和评价指南》[27]的规定,同一产品配方不同批次的营养素指标RSD在5%以内,说明该产品的工艺稳定性好,可满足实际生产要求。
2 结果与分析
2.1 混合均匀性
产品混合结束后进行取样,分别检测10 个不同位置产品中代表性营养素(蛋白质、脂肪、亚油酸、维生素D、维生素E、维生素B1、泛酸、钙、锌、铜和硒)的含量以计算变异系数,同时比较不同批次间的差异情况,具体见表3。
由表3可知特殊医学用途全营养配方食品不同批次的代表性营养素的变异系数均在5%以内,其中宏量营养素和脂肪酸小于1.5%,数据相对稳定,说明产品物料的组织状态较为均匀一致;维生素类变异系数在4%以内,表示现有工艺设计可以保证维生素类营养素混合均匀;矿物质类营养素变异系数在5%以内,说明其混合均匀度良好,该工艺设计可以保证矿物质类营养素混合均匀,其中一批次硒变异系数明显高于其他,可能原因为检测偏差,后期对其加以监测和控制。综合发现所有代表性营养素的变异系数均符合美国FDA《混合均匀性取样和评价指南》和《药品GMP指南:口服固体制剂》中对粉末混合的评价标准(5%以内),同时经过三批次重复的生产,因此可以表示现有干法混合工序条件下物料已充分混合且均匀,达到相应的添加效果,并能有效控制产品质量安全。
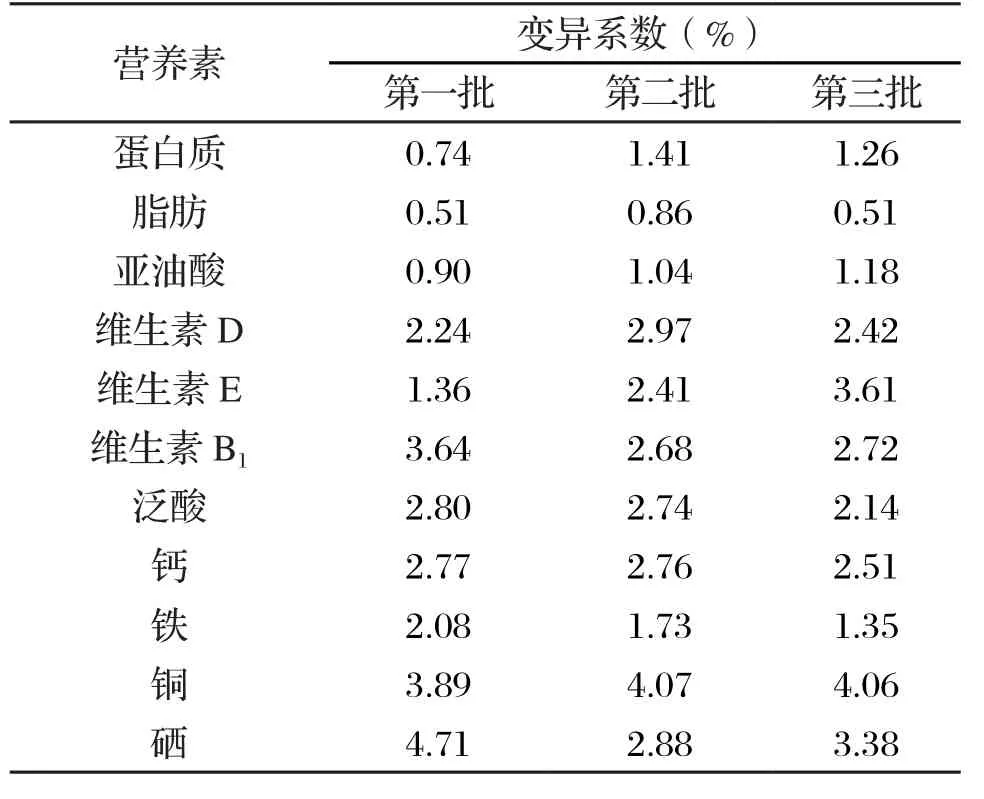
表3 不同批次代表性营养素的变异系数
2.2 营养成分符合性
将三批次产品进行全项目检测,并与产品设计值进行比较,检测值与设计值的偏差统计见表4。
检测值与设计值的偏差存在负值,其原因可为检测误差。由表4可以发现产品中各营养素的检测值与设计值均存在一定偏差,其中一批次矿物质硒的偏差为13.05%,主要原因为检测误差和硒添加量少对混合有一定影响,但由于其小于检测精密度(20%),因此判定其可控;其余指标的偏差均同时符合美国FDA要求(10%)和检测精密度的要求,因此,经验证可判定现有干法混合工序条件下生产的产品可以达到开发设计要求,同时符合GB 29922—2013技术指标的要求,能保证临床使用的安全性及有效性。
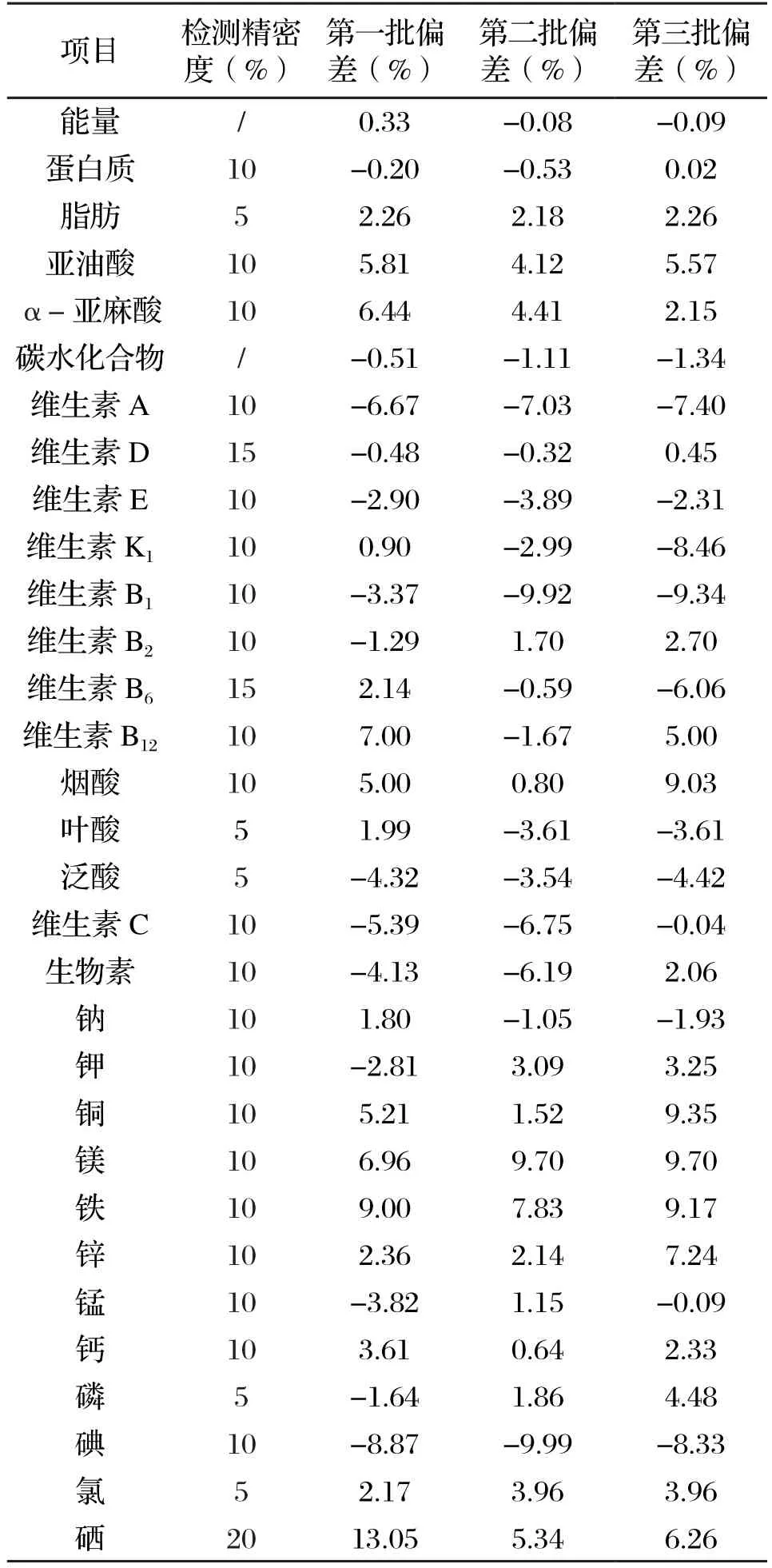
表4 检测值与设计值的偏差
2.3 工艺稳定性
按照现有工艺参数对同一配方进行三批次重复性生产,对三批次产品中营养素进行检测并计算相对标准偏差(RSD),具体见表5。
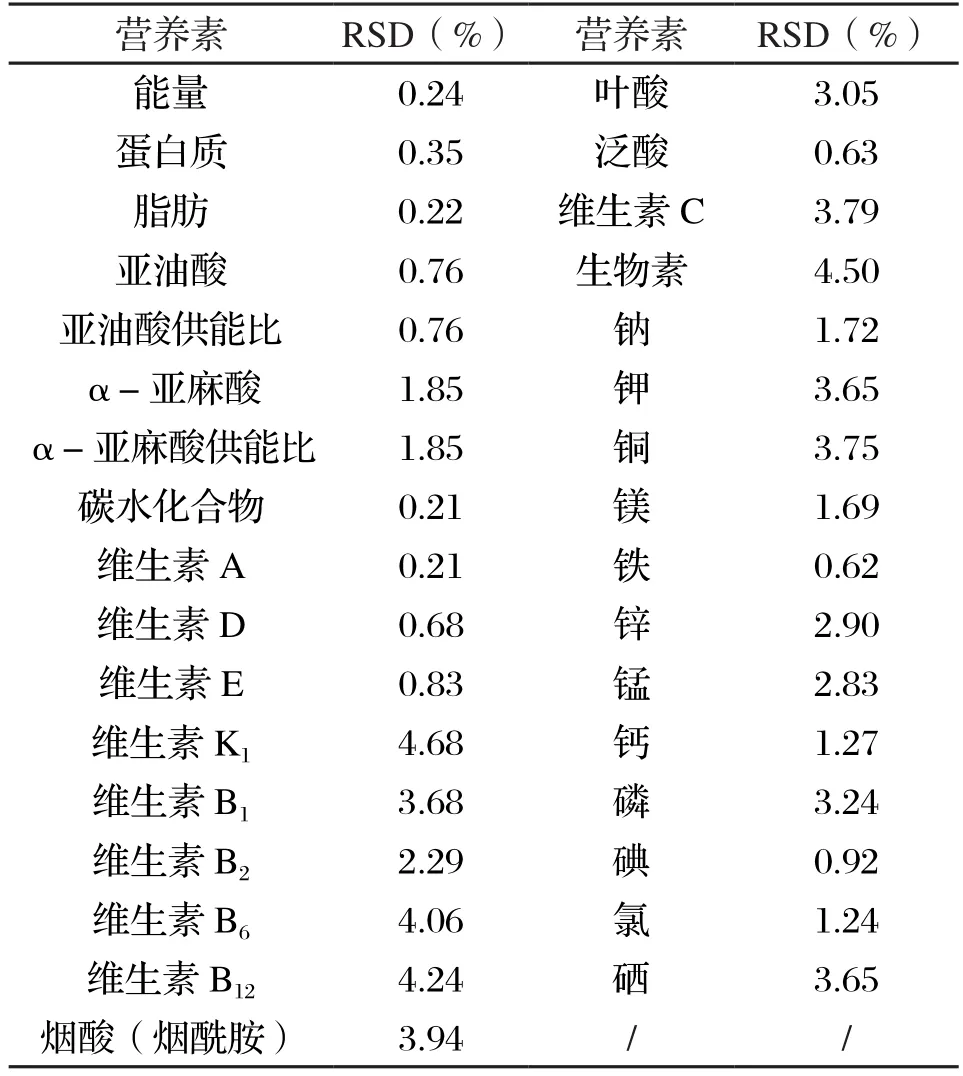
表5 相对标准偏差
干法混合工序条件下,生产批次差异对产品的营养素指标有一定程度影响,但是由表5可知,不同批次产品中各营养素的相对标准偏差均在5%以内,符合美国FDA《混合均匀性取样和评价指南》中对同一配方不同批次样品的营养素指标相对标准偏差在5%以内的要求,说明该干法混合工序重现性好,工艺稳定。因此,经验证现有干法混合工序具有良好的重现性和可靠性,并能有效控制产品的质量安全。
3 结论
本文以混合均匀性、营养成分符合性及工艺稳定性为指标对特殊医学用途全营养配方食品的干法混合工序进行工艺验证。结合试验数据可知,代表性营养素不同位置的CV均在5%以内、产品营养成分的检测值与设计值偏差在±10%以内(第一批次硒的偏差13.05%在检测方法的精密度内)、批次间的相对标准偏差(RSD)均在5%以内。得出结论,现有干法混合工序物料可充分混合均匀且可连续稳定生产,同时产品质量可控,可保证临床使用的有效性及安全性。

