通电电流密度对氧化铱pH电极性能的影响
路志博,李格格,王鹏刚,2,*,田 砾,2,隋晓萌
(1.青岛理工大学 土木工程学院,青岛 266525;2.山东省高等学校蓝色经济区工程建设与安全协同创新中心,青岛 266525)
钢筋腐蚀会引起钢筋混凝土结构耐久性劣化,影响其服役安全性,进而导致钢筋混凝土结构达不到设计服役年限[1]。在普通硅酸盐水泥混凝土中,pH值在12.5~13.5之间,钢筋表面附着一层致密钝化膜。但是,当外部环境中的Cl-,CO2等侵蚀性物质到达钢筋-混凝土界面区时,会导致钢筋钝化膜破坏。钢筋-混凝土界面处的pH值和Cl-浓度影响钢筋腐蚀过程和腐蚀速率。在一般大气环境、带有酸性气体和酸性液体的工业环境中,混凝土中性化是引起混凝土内部钢筋锈蚀破坏的主要因素。混凝土内部pH值的降低主要由混凝土碳化或者酸性气体、酸性液体的侵蚀等因素导致,钢筋附近pH值的大小则会影响钢筋钝化膜的状态,pH值较低会导致钢筋产生锈蚀。当pH<11.5时,钢筋钝化膜就开始脱钝,钢筋锈蚀速度随着pH值的下降而逐渐增大[2]。当pH<9时,钢筋完全处于活化状态,钢筋的锈蚀速度不受pH值影响[3-4]。因此,准确测试混凝土中性化过程中的pH值,对研究钢筋混凝土的腐蚀与防护,以及钢筋混凝土的可靠度预测具有重要意义。
混凝土内部pH值的测试方法包括磨粉滴定法、挤压孔隙液法等在内的破坏性方法和使用埋入式pH传感器进行原位测试的非破坏性方法。使用破坏性方法检测,需要到现场采集数据,不可避免地破损混凝土保护层,费时费力,并且危害混凝土结构的安全性。非破坏性方法主要使用埋入式pH传感器进行原位测试。相关研究学者陆续研制出用于pH监测的氢电极、玻璃电极、醌氢醌电极、光纤pH电极和金属/金属氧化物电极等。然而,氢电极结构复杂、对测试环境要求高;玻璃电极脆性高、易破损、不易微型化[5];光纤pH电极有高pH下化学不稳定、测量范围窄、染料浸出和寿命短等不足[6-7];固态金属/金属氧化物电极具有良好的长期稳定性,响应时间短,可在较极端环境使用等优势。目前适合作为pH电极的金属氧化物包括IrOx,PbO2,OsO2,TiO2,WO3,PtO2,Sb2O3和RuO2等。其中氧化铱电极在稳定性、响应时间、温度影响等方面表现更好。制备氧化铱电极的方法主要有电化学氧化法,电化学沉积法,溅射涂层法,溶胶-凝胶法,以及在碳酸盐中的热氧化法。
近年来,随着电化学沉积理论及试验研究的不断深入,电化学沉积技术被大量用于纳米材料、氧化物薄膜等非常规性能新材料的制备及环境保护等领域[8-9]。电化学沉积法通过调整沉积电流、电压、沉积液的pH值、沉积液组成成分等因素来控制氧化物沉积膜的厚度、组成、形貌等特征[10]。在实验室中,恒电流沉积法和恒电压沉积法得到广泛使用。在恒电流沉积法沉积过程中电流稳定,沉积基体表面生成沉积膜的速度稳定,具有试验重复性高的优点。YAMANAKA[11]研究发现沉积效率随着沉积液的pH值增加而增加,并在pH为10左右时达到恒定值,且pH值在10~11之间时沉积液最稳定,故选用pH值为10.5的沉积溶液进行研究。此外,沉积液中加入草酸可能起到稳定剂的作用[12]。YAMANAKA[11]认为电流密度大于0.2 mA/cm2时,制备的氧化铱薄膜的性能缺乏一致性。KIM等[13]研究了0.03,0.16,0.32 mA/cm2电流密度下沉积的氧化铱薄膜在热处理之后的性能,并认为0.32 mA/cm2,400 ℃条件下制备的电极性能最优。可见,文献中关于氧化铱pH电极恒电流极化参数的研究结果存在一定争议。针对上述问题,本文采用恒电流沉积法,在不同的沉积电流密度下制备了氧化铱pH电极,确定了最优沉积电流密度,为混凝土用高精度固态pH电极制备与应用提供依据。
1 pH电极制备
1.1 试验原材料
沉积液配制原材料为粉末状四氯化铱分析纯,草酸,H2O2(30%,wt),K2CO3分析纯,去离子水。沉积基体选用导电性能优异,且惰性较石墨更好的金属铂,纯度为99.99%,直径为Ф=1 mm。
1.2 pH电极制备过程
对沉积基体铂丝预处理:首先用细度为1600号、2000号的碳化硅砂纸依次对铂丝进行打磨,然后分别用无水乙醇、去离子水清洗干净,待铂丝干燥后,将铂丝每段截为20 mm,铂丝一端留出5 mm与铜导线焊接,并且焊点用PVC管和环氧树脂进行密封,另一端留出15 mm。待环氧树脂凝固后,将铂丝置于干燥器中保存。
沉积液配制:将0.15 g IrCl4·H2O溶于100 mL蒸馏水中。室温下用磁力搅拌机磁力搅拌30 min。先向溶液中加入1 mL的H2O2(30%,wt)磁力搅拌10 min,然后加入0.15 g草酸并且磁力搅拌10 min。最后一次加入少量K2CO3以调节混合溶液的pH值至10.5,得到金黄色的沉积液,如图1所示。新配置的沉积液在室温避光处下放置2 d,期间沉积液由金黄色逐渐转变成蓝黑色,如图2所示。这是因为草酸与四氯化铱形成了稳定的铱络合物[Ir(OH)4C2O4]2-。
电极制备:使用Princeton VersaSTAT 3电化学工作站,沉积体系为三电极体系。沉积基体铂丝为工作电极,饱和甘汞电极(SCE)为参比电极,铂片电极为对电极。将三电极体系浸入制备的沉积液中,然后在室温下对电极通电40 min,所采用的通电电流密度为0.16,1,2 mA/cm2。每沉积一个电极,更换新的沉积液。恒电流沉积结束后,用蒸馏水对工作电极进行洗涤,冷风吹干,放入真空干燥箱中保存。
1.3 电极表征及性能测试
从真空干燥箱中取出电极,截取3~5 mm样品,使用FEI Quanta 200型扫描电子显微镜,在5000倍放大倍率下分析氧化铱镀层的表面形貌,研究通电电流密度对电极形貌的影响。同时通过能谱(EDS)分析电极表面镀层成分。采用Princeton VersaStat3 电化学工作站三电极体系测试刚制备完成未经老化的pH电极的响应时间、能斯特响应,测试电极在饱和Ca(OH)2溶液中的稳定性。
2 试验结果分析
对沉积前后电极的表面形貌进行对比,沉积基体铂丝表面变黑,分析其成分为一层氧化铱薄膜,如图3所示。并且沉积层形成的速度随着电流密度的增加而增加。
2.1 通电电流密度对pH电极微结构的影响
pH电极的微结构对电极的性能有很大的影响。图4为三种通电电流密度下制备的pH电极表面SEM和EDS图。从图中看出,0.16 mA/cm2电流密度制备的pH电极表面平整均匀,覆盖完整,呈现出“泥裂”状形貌。根据EDS能谱显示,黑色的沉积物主要由Ir,C,O元素组成,推测其成分主要为氧化铱,C元素可能来源于溶液中的K2CO3,并且在基体产生少量沉积。沉积产物生长速率随着电流密度增大而增大,沉积产物的结构更加松散且孔隙更大。电流密度为1 mA/cm2时制备的pH电极,表面粗糙且形貌较为复杂,存在大量分布不均匀的黑色沉积物,以及少量长条状的白色沉积物。电流密度为2 mA/cm2时制备的pH电极的沉积层覆盖完整,表面不规则分布着大小为1~10 μm、粒径变小的白色颗粒。通过EDS图谱分析可知,不同电流密度下制备的pH电极表面的黑色沉积产物成分主要为铱氧化物(IrOx),白色颗粒成分主要为K2CO3。随着通电电流密度增大,沉积层生长速度变快,沉积产物结构疏松,存在孔隙大或K2CO3过多现象,可能会导致电极和溶液的反应时间延长。
2.2 通电电流密度对pH电极响应时间的影响
根据IUPAC标准,电极达到稳定状态(电位值变化<1 mV)所需要的时间即为电极的响应时间[10]。响应时间越短,pH电极的灵敏度越高。
将刚制备完成未老化处理的不同通电电流密度下制备的pH电极浸泡在pH值不同的缓冲溶液中,电极的电位-时间关系曲线如图5所示。从图中可以看出,相同的电极在不同pH值缓冲溶液中的响应时间基本相同,0.16,1,2 mA/cm2沉积电流密度制备的电极的平均响应时间分别为73,67,170 s。然而不同电流密度下制备的电极在相同pH值缓冲溶液中的响应时间不同,较大电流密度下制备的pH电极响应时间较长。电流密度越大,沉积物生成的速度也越快,沉积膜厚度也随之增加,但是生成的沉积膜的质量较差,存在裂缝等缺陷。沉积膜与溶液中离子的反应过程被延长,因此电极响应时间也变长[14]。电极的响应时间与电极表面沉积膜的形貌有一定联系,1 mA/cm2条件下沉积的电极响应速度最快,这是因为其高低起伏的粗糙表面形貌为电极与溶液的反应提供更多的活性点。
2.3 通电电流密度对pH电极能斯特响应的影响
pH电极的电位响应与IrOx的氧化还原之间的平衡有关,HUANG等[15]提出氧化铱pH电极在氧化还原反应过程中涉及的三种可能的反应如式(1)—(3)所示:
Ir2O3+6H++6e-↔2Ir+3H2O
(1)
IrO2+4H++4e-↔Ir+2H2O
(2)
2IrO2+2H++2e-↔Ir2O3+H2O
(3)
氧化还原电位可以确定如下:
(4)
式中:E为测试电势,mV;E0为标准电极电势;R为气体常数,8.314 J/(K ·mol);T为绝对温度;F为法拉第常数,96 480 C/mol;n为在氧化还原反应中转移的电子数。
温度为25 ℃时,RT/F可用25.69 mV代替。因此,可以推断pH电极的灵敏度仅受方程式中转移的电子数量影响。
对于灵敏度大于59 mV/pH 的电极,OLTHUIS等[14]认为从Ir3+到Ir4+的可逆反应中,铱离子的价态发生了变化。在温和溶液中,IrOx参与的氧化还原反应如式(5)所示:
(5)
IrOx是在混合的氧化和还原反应中发生价态的转变,式(5)氧化还原反应过程中每个质子对应的电子转移数少于1个,因此产生超能斯特响应。相反,对于灵敏度低于59 mV/pH的电极,氧化还原反应中每个质子转移1个以上的电子。
室温(25±3)℃条件下测得刚制备完成的pH电极在不同pH值溶液中的电位如图6所示。从图中可以看出,随着溶液pH值的增大,pH电极电位线性减小。对试验结果进行线性拟合得到各通电电流密度条件下所制备pH电极能斯特响应参数,见表1。从表中可以看出,0.16,1,2 mA/cm2电流密度条件下制备的电极的电位-pH曲线斜率均大于59 mV/pH,相关系数R2均为0.998,表现出超能斯特响应。上述制备的电极灵敏度随着电流密度的增加而升高,表现出超能斯特响应。原因如下:在高电流密度下,电极沉积速率快,电极表面氧化膜孔隙率大;此外在氧化还原反应过程中,高电流密度下,每个H+传递的电子更少。KIM等[13]在电流密度分别为0.16,0.32 mA/cm2时制备的电极灵敏度为61.1,69.3 mV/pH,同样表现出超能斯特响应。
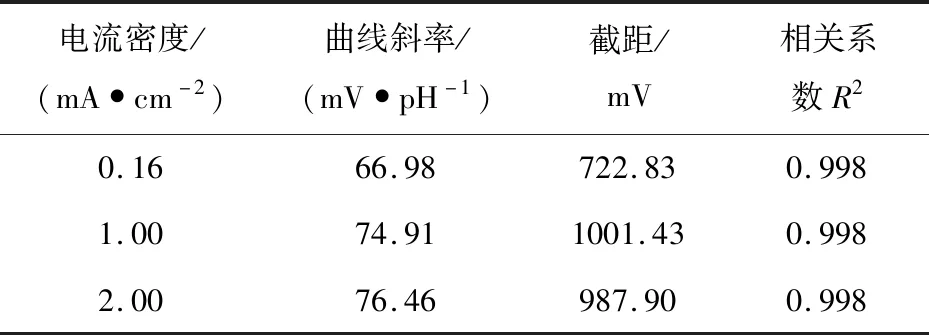
表1 不同沉积电流密度下制备的电极能斯特响应数据
2.4 稳定性
pH电极的稳定性是衡量电极性能的一个重要指标,大多数电化学电极存在电位漂移的问题,因此需要足够的老化时间,确保电极电位的稳定。图7为电沉积法制备的电极在饱和Ca(OH)2溶液中的长期电位测试图,从图中可以看出,不同通电电流密度下制备的电极在饱和Ca(OH)2溶液中前12 d内电位都呈现下降趋势,0.16 mA/cm2沉积电流密度下制备的电极电位漂移数值最大,达到了170 mV左右,且趋于稳定的时间最长。1 mA/cm2沉积电流密度下制备的电极在前3 d电位漂移较大,为100 mV左右,但其趋于稳定的时间最短。HITCHMAN等认为电位漂移过程是电极表面高低价态的铱化合物之间达到平衡的过程。王鹏刚等[1]认为电极表面的结合水影响电极的稳定性。1 mA/cm2沉积电流密度下制备的电极表面不同价态的铱化合物距离平衡状态较为接近,并且沉积层的水化程度比0.16 mA/cm2电流密度较高,仍需要时间达到平衡状态,因此在趋于稳定后,存在10 mV以内的电位波动。针对电位漂移问题,可采用预先老化处理、现场校正的方法进行改善,降低电极电位随时间的漂移幅度。
在电极长期稳定性的试验过程中,沉积层易产生脱落现象,影响电极的相关性能。电极在沉积过程中可能会受到结合水的影响,导致沉积层和基体间的结合力较差。可以采用电化学沉积之后再热处理的方法,提高沉积层与基体的结合力,同时可以减少沉积层的孔隙,提高电极的相关性能。需开展系统研究,以解决沉积层脱落问题。
3 结论
针对电化学沉积法制备pH电极过程中电流密度对电极性能的影响,本文从pH电极的微观形貌、响应时间、能斯特响应、稳定性方面进行了分析。恒电流沉积法的主要产物为K2CO3和IrOx,电流密度越大沉积层产生速度越快,沉积产物堆叠越无序,结构越疏松。1 mA/cm2电流密度制备的电极在响应时间、能斯特响应、稳定性等方面表现良好,比较适合作为pH监测的工作电极。电化学沉积法制备的IrOx电极具有广阔的应用前景,但由于其存在电位漂移较大,灵敏度、稳定性易受干扰,电极表面沉积层易脱落等问题,需要开展更为深入的研究。

