高通量血液透析联合厄贝沙坦对尿毒症患者的治疗效果*
张君琳 吴晶 王友云
尿毒症的发生是由慢性肾脏病发展所引起,从而致使患者肾脏功能出现严重衰竭。其中,机体内酸碱平衡失调及电解质紊乱是尿毒症发生的重要因素[1-2],而对于尿毒症的治疗,通常以透析为主要治疗手段。高通量血液透析(HFHD)是近年来较为常用的,HFHD是指应用高通量血液透析器进行透析,高通透性透析膜能从血液中将大量的毒素进行过滤,能够更有效地将中分子毒素清除,使透析患者得到更好的疗效[3]。而厄贝沙坦能够减少尿蛋白,延缓肾功能恶化,具有肾脏保护作用[4]。本文主要研究高通量血液透析联合厄贝沙坦对尿毒症患者疗效,为临床研究提供参考。
1 资料与方法
1.1 一般资料
选取2018年5月-2021年5月江南大学附属医院收治的尿毒症患者106例,纳入标准;符合文献[5]《慢性肾衰竭诊疗指南》中对尿毒症诊断的标准;年龄25~75岁;患者透析频率为3次/周;维持性血液透析短于半年,1次/周;自愿参与本次研究。排除标准:(1)有严重出血倾向;(2)对厄贝沙坦药物有禁忌;(3)凝血障碍。按照随机数字表法分为对照治疗组和联合治疗组,各53例。两组患者的性别、年龄、病程、体重、原发病分类等一般资料对比,差异均无统计学意义(P>0.05),有可比性,见表1。所有患者及家属对本次研究均知情,并签署知情同意书;研究经本院伦理委员会批准。
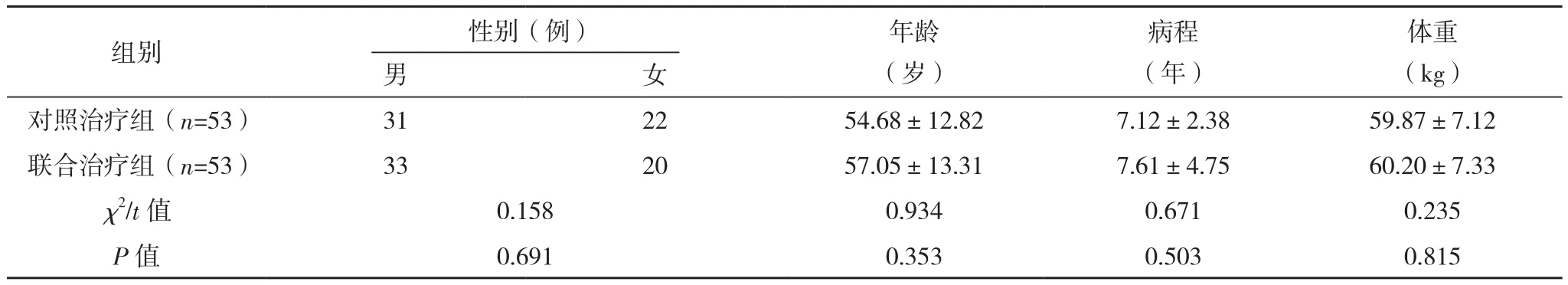
表1 两组一般资料对比
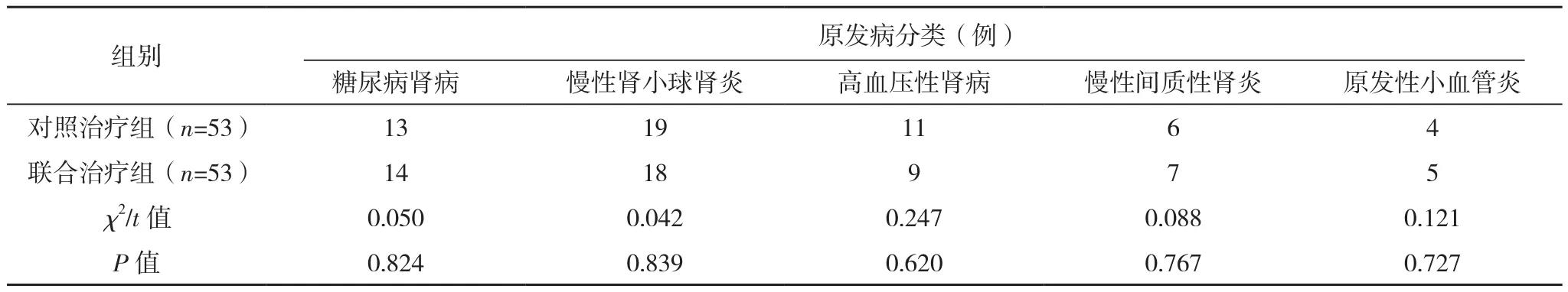
表1(续)
1.2 方法
对照治疗组采用高通量血液透析治疗,进行透析前30 min,对患者注射低分子肝素(生产厂家:深圳赛保尔生物药业有限公司,国药准字H20060191)60~80 IU/kg进行抗凝处理,并使用促红细胞生成素[生产厂家:麒麟鲲鹏(中国)生物药业有限公司,国药准字J20030074]1万U皮下注射,1次/周,多糖铁复合物[生产厂家:优时比(珠海)制药有限公司,国药准字J20160027]150 mg口服,1次/d。采用德国费森尤斯4008B型超滤透析机,颈内建立静脉透析通道,超滤系数为40 ml/(h·mmHg),透析膜面积为1.5 m2,血流量为300 ml/min,透析液流量为500 ml/min,治疗频率为3次/周,4 h/次,治疗周期为3个月。联合治疗组在对照治疗组基础上联合厄贝沙坦治疗,使用厄贝沙坦片(浙江华海药业股份有限公司,国药准字J20130049,规格:75 mg×28片),起始剂量为150 mg,1次/d,治疗6个月。
1.3 观察指标及评价标准
1.3.1 LVEDD、IVST、LVPWT、TG、HDL、LDL水平 采用贝克曼库尔特Power Express全实验室自动化生化免疫流水线检测甘油三酯(TG)、高密度脂蛋白胆固醇(HDL)、低密度脂蛋白胆固醇(LDL)水平。采用行超声心动图检测左心室舒张末期容积(LVEDD)、室间隔厚度(IVST)、左心室后壁厚度(LVPWT)水平。
1.3.2 尿素氮、尿酸、血肌酐 受试者于治疗前后清晨空腹并坐位抽取静脉血5 ml,通过离心半径10 cm、转速2 500 r/min离心处理10 min,分离上层血清,-80 ℃保存、待检。采用酶法检测血清内尿素氮、尿酸、血肌酐表达水平。
1.3.3 hs-CRP、IL-6、TNF-α、AKP、sTfR、PTH水平检测 采用双抗体一步夹心法酶联免疫吸附试验(ELISA)检测超敏C反应蛋白(hs-CRP)、白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α)、碱性磷酸酶(AKP)、血清转铁蛋白受体(sTfR)、甲状旁腺激素(PTH)、β2-MG水平。
1.3.4 钙(Ca)、β2-微球蛋白(β2-MG) Ca采用钙离子选择性的螯合剂(EGTA)络合滴定法检测,用EGTA标准液滴定,边加试剂边摇匀至出现杏黄色为止,记录EGTA标准液消耗量。
1.3.5 治疗效果 显效:患者临床症状消失,血肌酐、β2-MG、尿素氮、中任意一项与治疗前相比降低程度>30%;有效:患者临床症状得到显著改善,血肌酐、β2-MG尿素氮与治疗前相比降低程度≤30%;无效:相关指标无明显改善,或病情有加重的趋势。治疗总有效率=(显效+有效)/总例数×100%。
1.3.6 不良反应 对患者皮肤瘙痒、心律失常、头疼、头晕、关节疼痛等治疗过程中的不良反应发生情况进行统计比较。
1.4 统计学处理
采用SPSS 20.0统计软件进行分析处理,计量资料采用(±s)描述,两组间比较采用独立样本t检验,组内比较采用配对t检验;计数资料采用率(%)表示,组间比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组肾功能水平比较
治疗前,两组尿素氮、尿酸、血肌酐水平比较,差异无统计学意义(P>0.05);治疗后,与同组治疗前相比,尿素氮、尿酸、血肌酐水平降低,差异有统计学意义(P<0.05);治疗后,与对照治疗组相比,联合治疗组尿素氮、尿酸、血肌酐水平较低,差异有统计学意义(P<0.05),见表2。
表2 两组肾功能水平比较(±s)
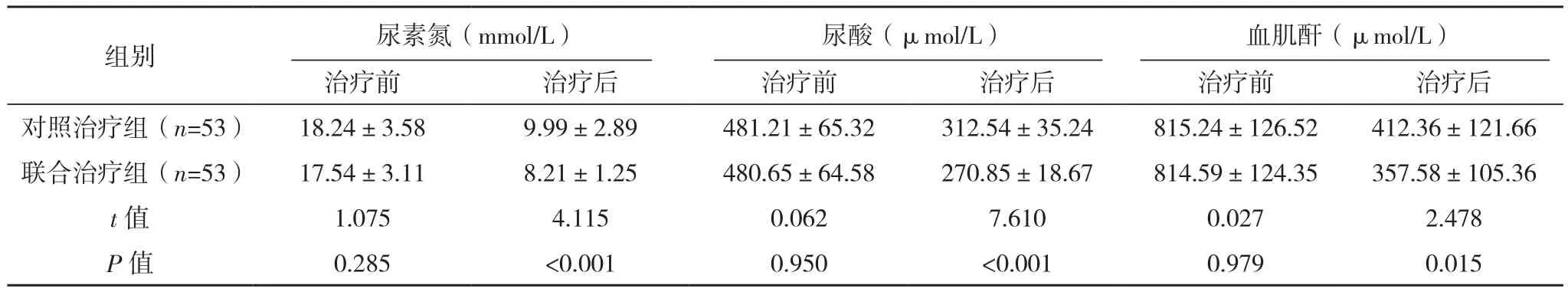
表2 两组肾功能水平比较(±s)
组别 尿素氮(mmol/L) 尿酸(μmol/L) 血肌酐(μmol/L)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照治疗组(n=53) 18.24±3.58 9.99±2.89 481.21±65.32 312.54±35.24 815.24±126.52 412.36±121.66联合治疗组(n=53) 17.54±3.11 8.21±1.25 480.65±64.58 270.85±18.67 814.59±124.35 357.58±105.36 t值 1.075 4.115 0.062 7.610 0.027 2.478 P值 0.285 <0.001 0.950 <0.001 0.979 0.015
2.2 两组LVEDD、IVST、LVPWT、TG、HDL、LDL水平比较
治疗前,两组LVEDD、IVST、LVPWT、TG、HDL、LDL水平比较,差异无统计学意义(P>0.05);治疗后,与同组治疗前相比,LVEDD、IVST、LVPWT、TG、LDL水平降低,HDL水平升高,差异有统计学意义(P<0.05);治疗后,与对照治疗组相比,联合治疗组LVEDD、IVST、LVPWT、TG、LDL水平降低,HDL水平升高,差异有统计学意义(P<0.05),见表3。
表3 两组LVEDD、IVST、LVPWT、TG、HDL、LDL水平比较(±s)
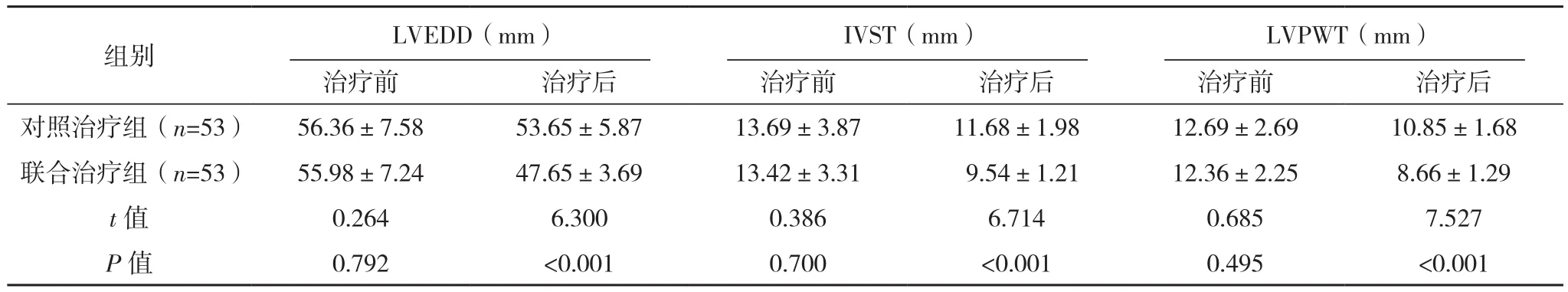
表3 两组LVEDD、IVST、LVPWT、TG、HDL、LDL水平比较(±s)
组别 LVEDD(mm)IVST(mm)LVPWT(mm)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照治疗组(n=53) 56.36±7.58 53.65±5.87 13.69±3.87 11.68±1.98 12.69±2.69 10.85±1.68联合治疗组(n=53) 55.98±7.24 47.65±3.69 13.42±3.31 9.54±1.21 12.36±2.25 8.66±1.29 t值 0.264 6.300 0.386 6.714 0.685 7.527 P值 0.792 <0.001 0.700 <0.001 0.495 <0.001
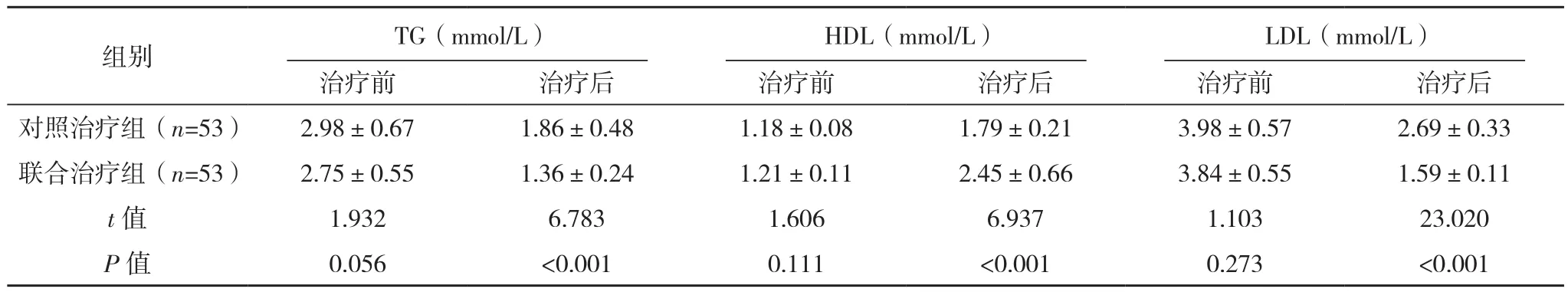
表3(续)
2.3 两组炎性因子水平比较
治疗前,两组IL-6、hs-CRP、TNF-α水平比较,差异无统计学意义(P>0.05);治疗后,与同组治疗前相比,IL-6、hs-CRP、TNF-α水平降低,差异有统计学意义(P<0.05);治疗后,与对照治疗组相比,联合治疗组IL-6、hs-CRP、TNF-α水平较低,差异有统计学意义(P<0.05),见表4。
表4 两组炎性因子水平比较(±s)
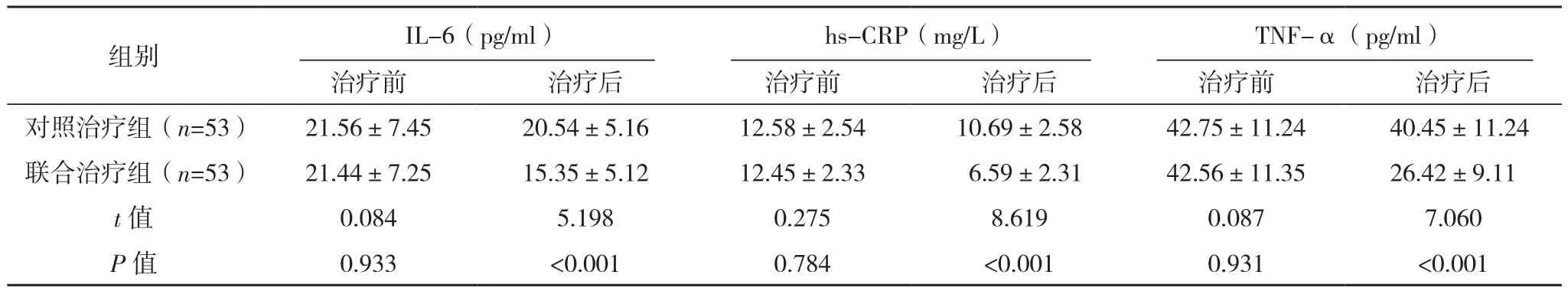
表4 两组炎性因子水平比较(±s)
组别 IL-6(pg/ml)hs-CRP(mg/L)TNF-α(pg/ml)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照治疗组(n=53) 21.56±7.45 20.54±5.16 12.58±2.54 10.69±2.58 42.75±11.24 40.45±11.24联合治疗组(n=53) 21.44±7.25 15.35±5.12 12.45±2.33 6.59±2.31 42.56±11.35 26.42±9.11 t值 0.084 5.198 0.275 8.619 0.087 7.060 P值 0.933 <0.001 0.784 <0.001 0.931 <0.001
2.4 两组AKP、Ca、PIH水平比较
治疗前,两组AKP、Ca、PTH水平比较,差异无统计学意义(P>0.05);治疗后,与同组治疗前相比,AKP、Ca、PTH水平降低,差异有统计学意义(P<0.05);治疗后,与对照治疗组相比,联合治疗组AKP、Ca、PTH水平较低,差异有统计学意义(P<0.05),见表5。
表5 两组AKP、Ca、PIH水平比较(±s)
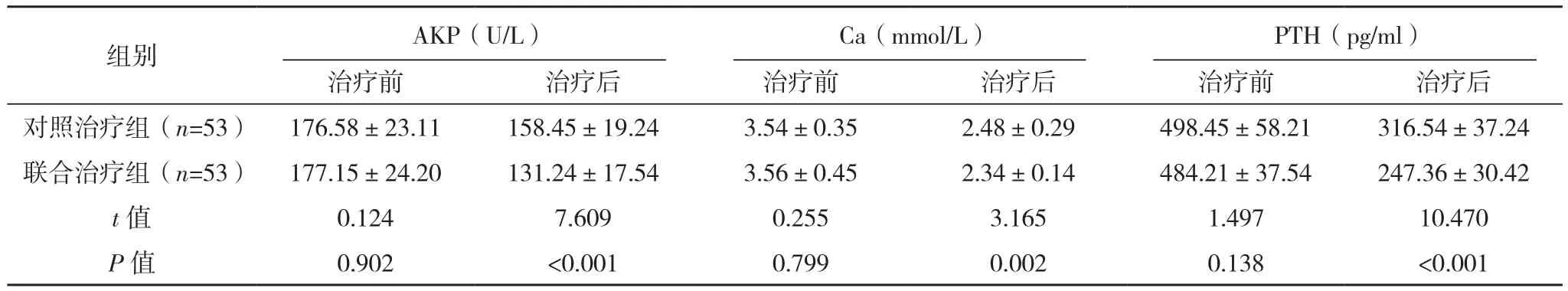
表5 两组AKP、Ca、PIH水平比较(±s)
组别 AKP(U/L)Ca(mmol/L)PTH(pg/ml)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照治疗组(n=53) 176.58±23.11 158.45±19.24 3.54±0.35 2.48±0.29 498.45±58.21 316.54±37.24联合治疗组(n=53) 177.15±24.20 131.24±17.54 3.56±0.45 2.34±0.14 484.21±37.54 247.36±30.42 t值 0.124 7.609 0.255 3.165 1.497 10.470 P值 0.902 <0.001 0.799 0.002 0.138 <0.001
2.5 两组β2-MG、sTfR水平比较
治疗前,两组β2-MG、sTfR水平比较,差异无统计学意义(P>0.05);治疗后,与同组治疗前相比,β2-MG、sTfR水平降低,差异有统计学意义(P<0.05);治疗后,与对照治疗组相比,联合治疗组β2-MG、sTfR水平较低,差异有统计学意义(P<0.05),见表6。
表6 两组β2-MG、sTfR水平比较[μg/ml,(±s)]
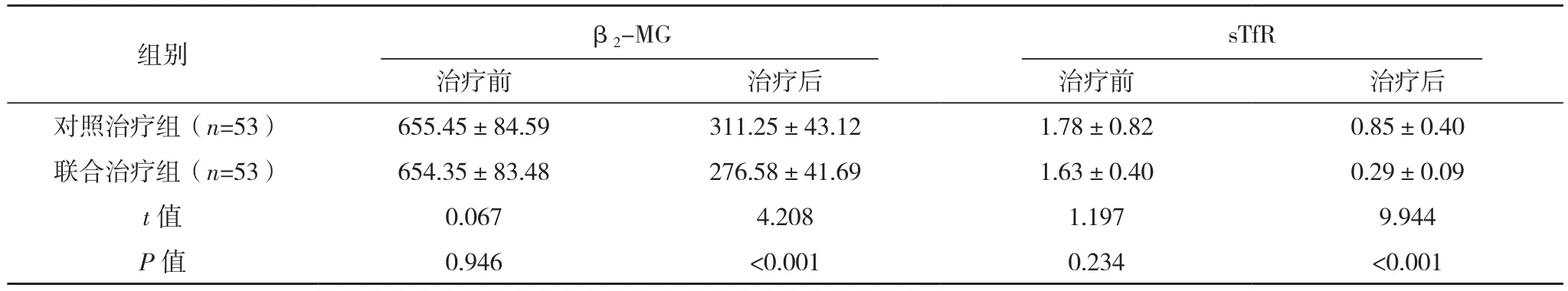
表6 两组β2-MG、sTfR水平比较[μg/ml,(±s)]
组别 β2-MG sTfR治疗前 治疗后 治疗前 治疗后对照治疗组(n=53) 655.45±84.59 311.25±43.12 1.78±0.82 0.85±0.40联合治疗组(n=53) 654.35±83.48 276.58±41.69 1.63±0.40 0.29±0.09 t值 0.067 4.208 1.197 9.944 P值 0.946 <0.001 0.234 <0.001
2.6 两组临床疗效比较
与对照治疗组相比,联合治疗组治疗总有效率较高,差异有统计学意义(P<0.05),见表7。

表7 两组临床疗效比较
2.7 两组不良反应情况比较
与对照治疗组相比,联合治疗组不良反应发生率较高,但比较差异无统计学意义(P>0.05),见表8。

表8 两组不良反应情况比较
3 讨论
高通量血液透析主要作用是对机体内的代谢物质通过弥散方式进行相应清除,同时还对机体内型分子进行清除,不仅能够有效保证患者血液中大部分有害物质得到清除,还能维持相关血液指标保持稳定状态[6]。厄贝沙坦在近几年被用于透析患者中,能够对患者的血压进行控制,如果患者合并2型糖尿病,在使用过程中初始药量可为150 mg/d,后续依照患者病情可进行适当增加到300 mg/d。一般情况下,肾功能出现损伤的患者,在服用厄贝沙坦时不需要进行剂量调整,但如果患者进行过长期透析,服用初始剂量可为75 mg,后续依照患者的临床症状进行适当调整[7]。在本文研究中,采用高通量血液透析联合厄贝沙坦治疗尿毒症,能有效降低甲状旁腺激素,使钙磷代谢紊乱有显著改善,改善血钙水平,效果显著。
LVEDD是指左心室舒张末期的充盈量,正常情况是来自左心房的血液,当主动脉瓣膜关闭不全时经主动脉瓣返流的血液也参与形成左心室舒张末期容量[8]。IVST是对患者的左心室肌壁厚度进行体现,其正常左心室肌壁厚度为9~12 mm。LVPWT能够对左心室功能进行判断,当其大于12 mm时,则表示患者左心室出现肥厚。TG升高常见于动脉粥样硬化、严重糖尿病、脂肪肝、肥胖症、高脂血症等。脂肪组织里的TG,其中一部分会分解为脂肪酸及甘油,然后运输到肝脏内,并且在肝脏内转化为TG进行储存,最后运输到血液当中,正常人妊娠时TG可升高[9]。LDL功能缺陷是伴随血浆LDL-C清除能力降低,会造成动脉内膜粥样斑块形成,通过结合其细胞膜上的低密度脂蛋白受体被转化和降解。本文研究显示,在经过治疗后LVEDD、IVST、LVPWT、TG、LDL水平显著降低,HDL水平显著升高。通过这一研究结果可以得出,对尿毒症患者行高通量血液透析联合厄贝沙坦这一联合方案进行治疗,能够改善患者心功能和血脂水平,使患者病情得到更好的恢复。
hs-CRP是机体受到组织损伤或微生物侵入等炎症性刺激时肝细胞合成的急性相蛋白,随着病变消退、功能、结构等恢复降至正常水平[10-11]。IL-6为活化的成纤维细胞和T细胞产生的淋巴因子,可增强自然杀伤细胞的裂解功能,促进原始骨髓源细胞的分化和生长[12]。TNF-α主要由巨噬细胞和单核细胞产生,是一种单核因子[13]。本文研究显示,治疗后,hs-CRP、IL-6、TNF-α水平显著降低,提示对尿毒症患者行高通量血液透析联合厄贝沙坦联合方案进行治疗,能够改善减轻患者机体炎症反应水平,更加有助于患者病情得到更好恢复。
AKP是一种磷酸单酯酶,存在于人体体液和组织中[14]。其可使RNA或DNA片段的5-P末端转换成5-OH末端,催化核酸分子脱掉5-磷酸基团。Ca是检查血清中钙离子浓度的试验。血浆钙有扩散性钙及非扩散性钙两部分。扩散性钙主要为离子钙(Ca2+),还有小部分的钙盐(如柠檬酸钙、碳酸氢钙及有机酸钙盐等)。非扩散性钙与蛋白质结合(大约1 g蛋白质结合0.87 mg的钙),占血浆总钙的40%~50%,在生理状态下保持平衡,非扩散性钙与扩散性钙之间受浓度和H+浓度的影响[15-17]。PIH主要作用为增高血钙,抑制肾小管对磷的吸收,促进肠钙和血钙水平升高,使破骨细胞活性和数目增加[18]。本文研究显示,治疗后AKP、Ca、PIH水平显著降低,透过这一研究结果可以得出,对尿毒症患者行高通量血液透析联合厄贝沙坦治疗,能够有效催化机体内的核酸分子,改善患者的血钙水平情况,抑制肾小管吸收。
β2-MG是由多形核白细胞、淋巴细胞和血小板产生的一种小分子球蛋白,分子质量为11 800,由99个氨基酸组成的单链多肽[19]。sTfR在血清中和不同的转铁蛋白以复合物的形式存在,是通过细胞表面受体的蛋白水解作用生成。铁缺乏时会引起sTfR合成的增加红细胞生成活性随之增加,会使血清中sTfR浓度的逐渐升高。血清中的sTfR大约80%来源于早期的红细胞[20]。本文研究显示,经过高通量血液透析联合厄贝沙坦治疗尿毒症能够清除中大分子毒物,减少炎症反应,保护肾功能,消除代谢性酸中毒表现。
综上所述,高通量血液透析联合厄贝沙坦能够有效改善尿毒症患者肾功能、心功能状态,改善患者的血脂水平,减轻患者机体炎症反应,降低Ca、β2-MG水平,治疗效果显著。

