应用外对照的单臂试验现状分析
刘佳宁,蔡明远,卢临博,思金华,李 戈,孙 凤
1. 天津中医药大学中药学院(天津 301617)
2. 天津中医药大学图书馆(天津 301617)
3. 天津中医药大学健康科学与工程学院(天津 301617)
4. 北京大学公共卫生学院流行病与卫生统计学系(北京 100191)
随机对照试验(randomized controlled trial,RCT)是评估干预措施疗效的“金标准”[1],常设置平行对照。将所有纳入对象均作为试验组的临床试验设计方法称为单臂试验(single-arm trial,SAT)[1],可作为临床试验的备选方案。单臂试验以研究之外的一组患者作为对比,称外部对照(external control,EC),可来自于RCT数据、真实世界数据(real world data,RWD)或文献中收集的数据,按时间轴分为历史外对照、同期外对照、混合外对照[2-5]。单臂试验可减少临床试验所需样本量,降低试验成本,显著缩短试验时间[6],但其混杂因素多且难以控制,试验结论不易解释,仅效应量具有显著临床意义时才能用于证据与决策[3]。目前单臂试验主要用于罕见病、效果极其显著或高需求药物的临床试验初步探索[7]。外对照的应用可通过调整匹配的间接比较(matchingadjusted indirect comparisons,MAICs)等方法控制混杂因素、增加可比性[8],在中等强度临床效应时增加证据和决策的可靠性[3]。目前,美国FDA[9](Food and Drug Administration)、日本 PMDA[10](Pharmaceuticals and Medical Devices Agency)、欧盟 EMA[11](European Medicines Agency)及中国NMPA[12](National Medical Products Administration)均有基于单纯的单臂试验数据审核通过药品注册申请的案例,鉴于外对照的应用有上述优点,应用外对照的单臂试验或将受到更多重视。
本文对国内外应用外对照的单臂试验进行系统检索,提取有关信息并进行可视化分析,便于直观分析应用外对照的单臂试验发展趋势、地区分布及重点研究领域现状,为我国单臂试验领域的进一步发展提供参考。
1 资料与方法
1.1 纳入与排除标准
纳入标准:①应用外对照的临床单臂试验,且必须与外对照比较;②对照要求为外对照,对研究对象、干预措施、结局指标均不做要求。排除标准:①重复发表的文献;②无法获取全文。
1.2 文献检索策略
计算机检索PubMed、SinoMed、中国知网(CNKI)、万方(WanFang)及维普(VIP)数据库,检索时间为建库至2021年7月21日。PubMed限定研究对象为人类,研究类型为临床试验,采取Title/Abstarct检索。中国知网、万方、维普选用篇名/题名、关键词、摘要检索。SinoMed进行智能检索,未通过其他方式如参考文献、灰色文献等对相关文献进行检索。
中文检索词包括单臂、真实世界、非同期、拓展、平行对照、历史对照、外部对照、外对照;英文检索词包括external control、historical control、parallel control、contemporaneous control、single arm、real world*、extensi*、non-contemporary。 以PubMed为例,检索策略见框1。

框1 PubMed检索策略Box 1. Search strategy in PubMed
1.3 文献筛选与数据提取
文献筛选及数据提取由2名研究者按照纳排标准独立进行,交叉核对提取资料,如遇分歧则通过讨论或与第3名研究者协商解决。提取内容包括第一作者、发表年份、文章类型、对照方法、基线控制手段、全部作者机构、研究疾病名称、临床试验分期和研究目的(安全性/有效性)等。
1.4 统计学分析
以Excel 2016进行数据提取与整合,并以VOSviewer 1.6.16与CiteSpace 5.7.R5W进行可视化分析。VOSviewer以距离解构相互关系[13],能采用较为一致的姓名缩写[14],故用VOSviewer进行作者合作共现分析。由于数据库导出限制,无法提取文献作者所属国家地区,故用CiteSpace对国家地区转化后进行分析。
疾病领域根据2019年国际疾病分类(ICD-10)标准[15],方法为提取疾病名称并网页检索,记录其所属大类;未提及疾病或针对两种及以上疾病归于其他。利用CiteSpace提取第一作者国籍信息,未成功获得者手动检索,并手动提取全部作者的机构信息,机构信息统一规范至大学或医院,大学附属医院视为独立机构。临床试验分期由文章直接报告,否则在文章中查找其临床试验注册号,并检索其注册信息,均未找到则归为未提及。
2 结果
2.1 文献筛选流程及结果
初检获得文献373篇,去除重复文献后剩余341篇,阅读文章题目及摘要初筛,阅读全文复筛,最终获得文献67篇,其中中文11篇、英文56篇,文献筛选流程见图1。

图1 文献筛选流程Figure 1. Flowchart of literature screening
2.2 纳入文献的基本特征
2.2.1 纳入文献基本情况
纳入文献基本情况如表1所示,文章类型包括药物治疗类(40/67)、医疗器械类(16/67)、手术治疗类(6/67)、临床路径类(临床路径等综合管理方式,6/67)、指导治疗类(治疗方式的选择依据,1/67)。在外对照选择上,除1篇文献未明确提及使用何种对照、1篇文献同时选用两种对照外,纳入研究多选择历史对照(55/67),其次为同期对照(10/67)。27篇进行基线比较,40篇未进行;42篇文章未提及混杂因素的控制,14篇设置外对照时进行匹配,11篇以统计分析处理混杂,包括协变量分析(2篇)、回归分析(8篇)、亚组分析(1篇)。
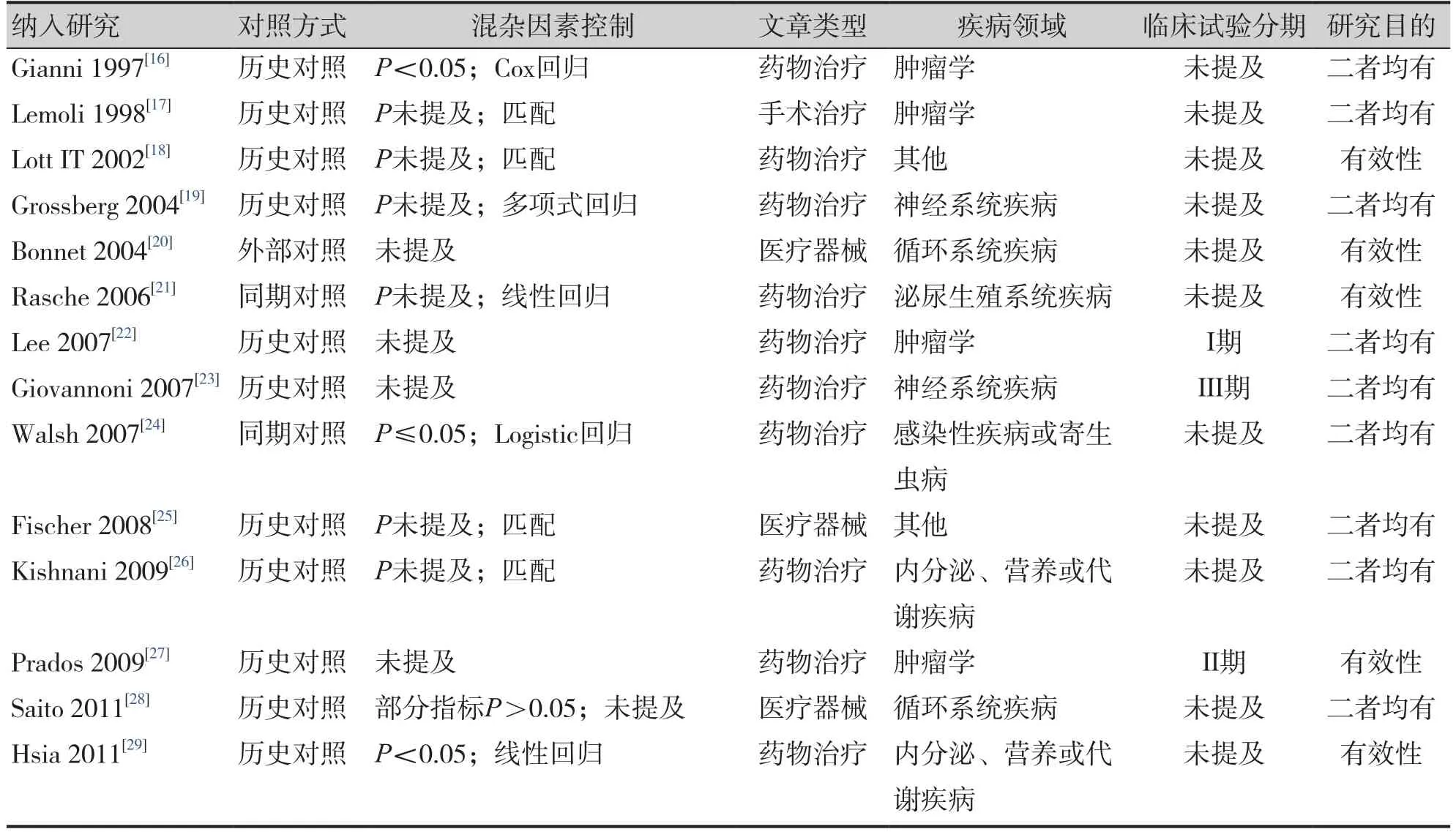
表1 纳入文献基本信息Table 1. Basic information of the included literatures
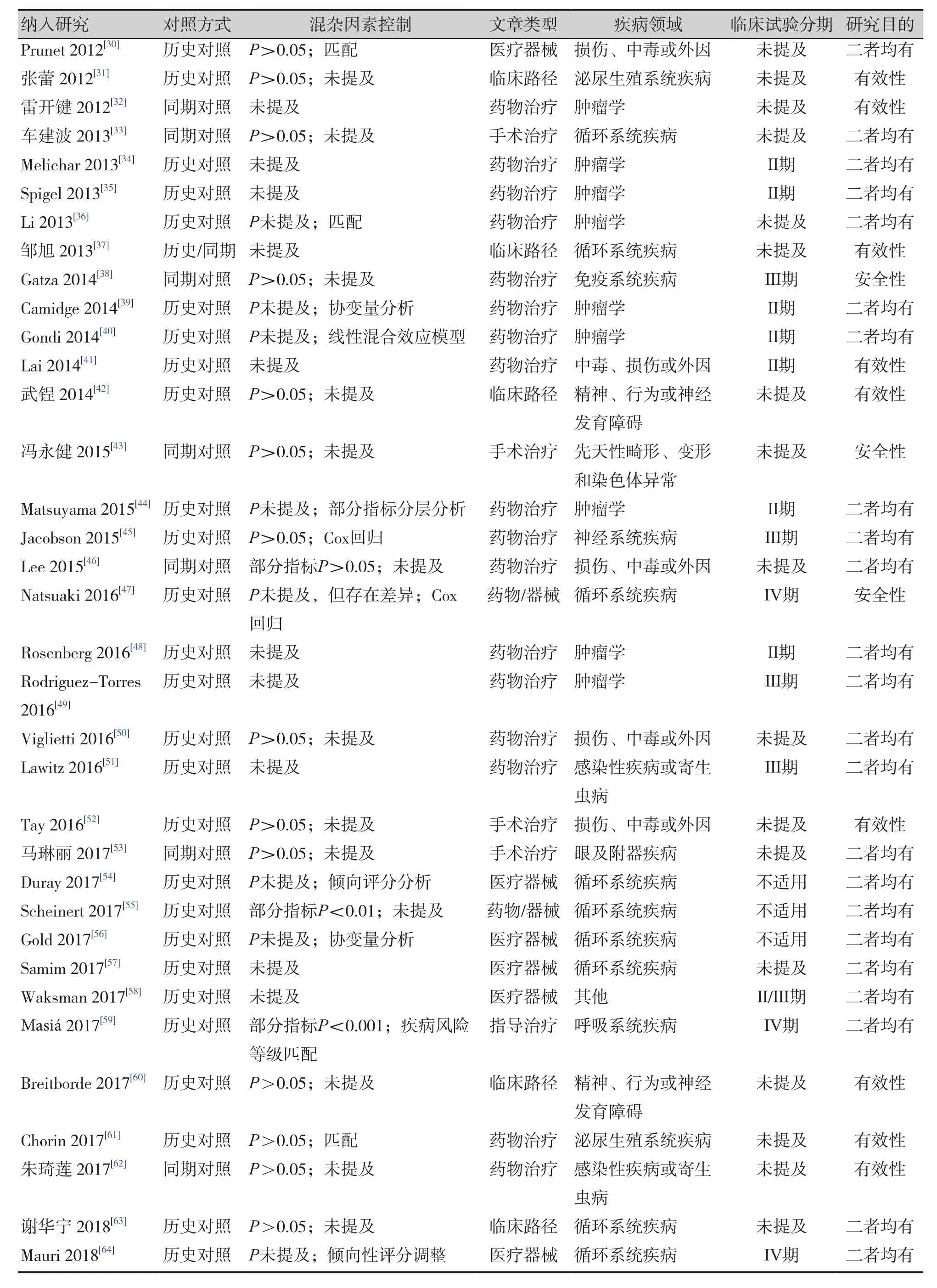
续表1

续表1
纳入研究均为临床试验,33篇文章未提及临床试验分期,包括14篇药物治疗类、7篇医疗器械类、6篇手术治疗类、6篇临床路径类;提及临床试验分期的研究中,5篇临床试验分期标明“不适用",1篇为Ⅰ期临床试验,18篇为Ⅱ期,5篇为Ⅲ期,2篇为Ⅱ/Ⅲ期,3篇为Ⅳ期。研究目的主要为评价安全性(46/67)或有效性(63/67)。
纳入文献首发于1997年,2002—2010年呈小高峰,但整体文章数量仍较少;2011—2017年发文量波动上升,2017年高达10篇;2018年短暂下降,次年迅速升高,后呈降低趋势(图2)。英文年发文量与总体基本一致;中文相关研究首次发表于2012年,发文量整体处于较低水平(图3)。
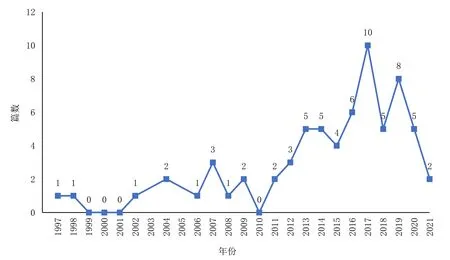
图2 应用外对照的单臂试验相关文献发文量时间分布Figure 2. Time distribution line chart of the number of publications related to the single-arm trial with external control
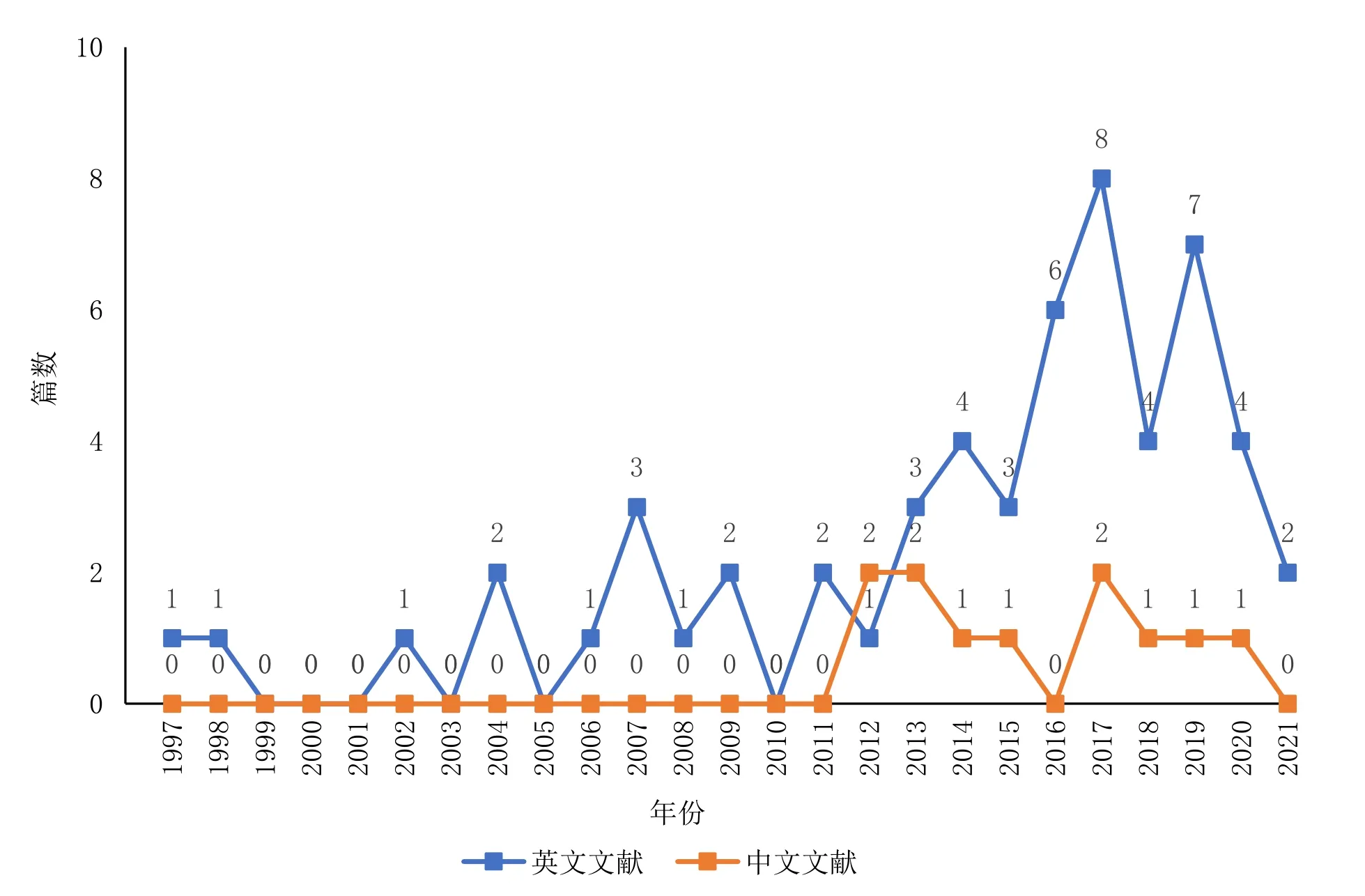
图3 应用外对照的单臂试验中英文献发文量时间分布对比Figure 3. Comparison chart of the time distribution of the number of publications in Chinese and English literature in the single-arm trial with external control
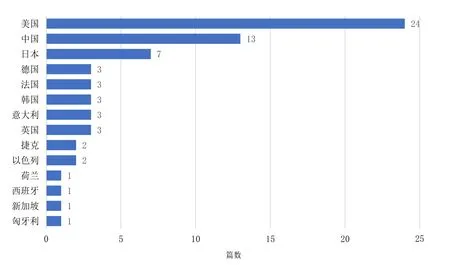
图4 应用外对照的单臂试验相关文献累计发文量国家地区分布柱形图(第一作者)Figure 4. Country and region distribution histogram of the cumulative number of publications related to the single-arm trial using external control (first author)
2.2.2 发表国家机构情况
应用外对照的单臂试验相关论文产出数量排名前三的国家分别为美国(24篇)、中国(13篇)、日本(7篇),详见图4。2篇文献未能将作者机构对应,其余机构内部作者数量以美国、以色列、德国、意大利为多(表2)。
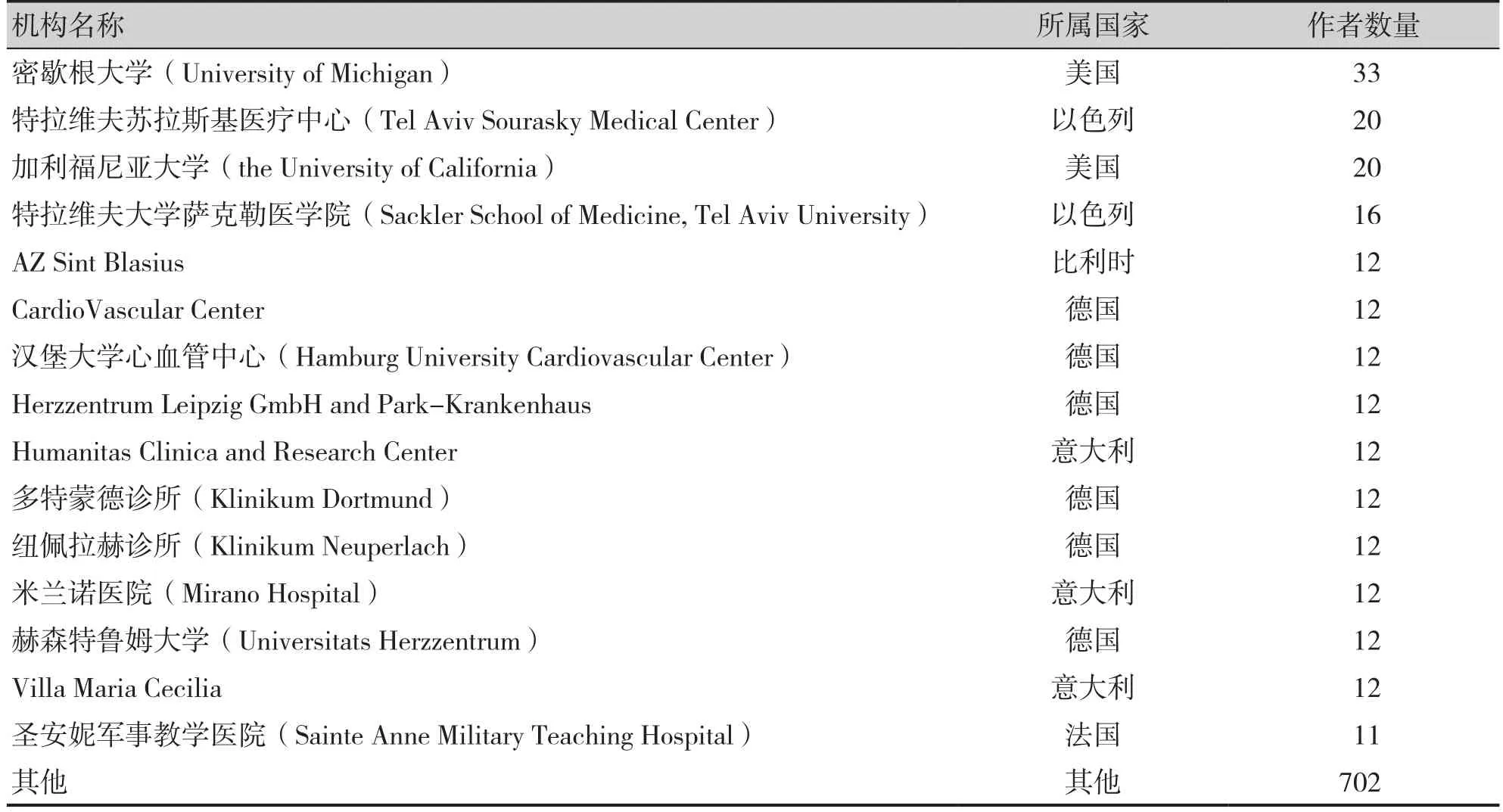
表2 应用外对照的单臂试验相关机构内部作者累积数量Table 2. Cumulative number of authors within relevant institutions of single-arm trials using external controls
2.2.3 作者合作关系
纳入文献涉及作者718人,多数作者仅发表1篇文献,11位作者发表2篇文献,无作者发表3篇及以上文献。图5为发表2篇及以上文献的作者合作网络共现图。

图5 作者合作网络共现图(阈值n≥2)Figure 5. Author collaboration network co-occurrence graph (threshold n≥2)
2.2.4 研究疾病领域
应用外对照的单臂试验涉及多种疾病领域,包括肿瘤学(24/67,35.82%),循环系统疾病(16/67,23.88%),损伤、中毒或外因(4/67,5.97%),感染性疾病或寄生虫病(4/67,5.97%)等,详见图6。
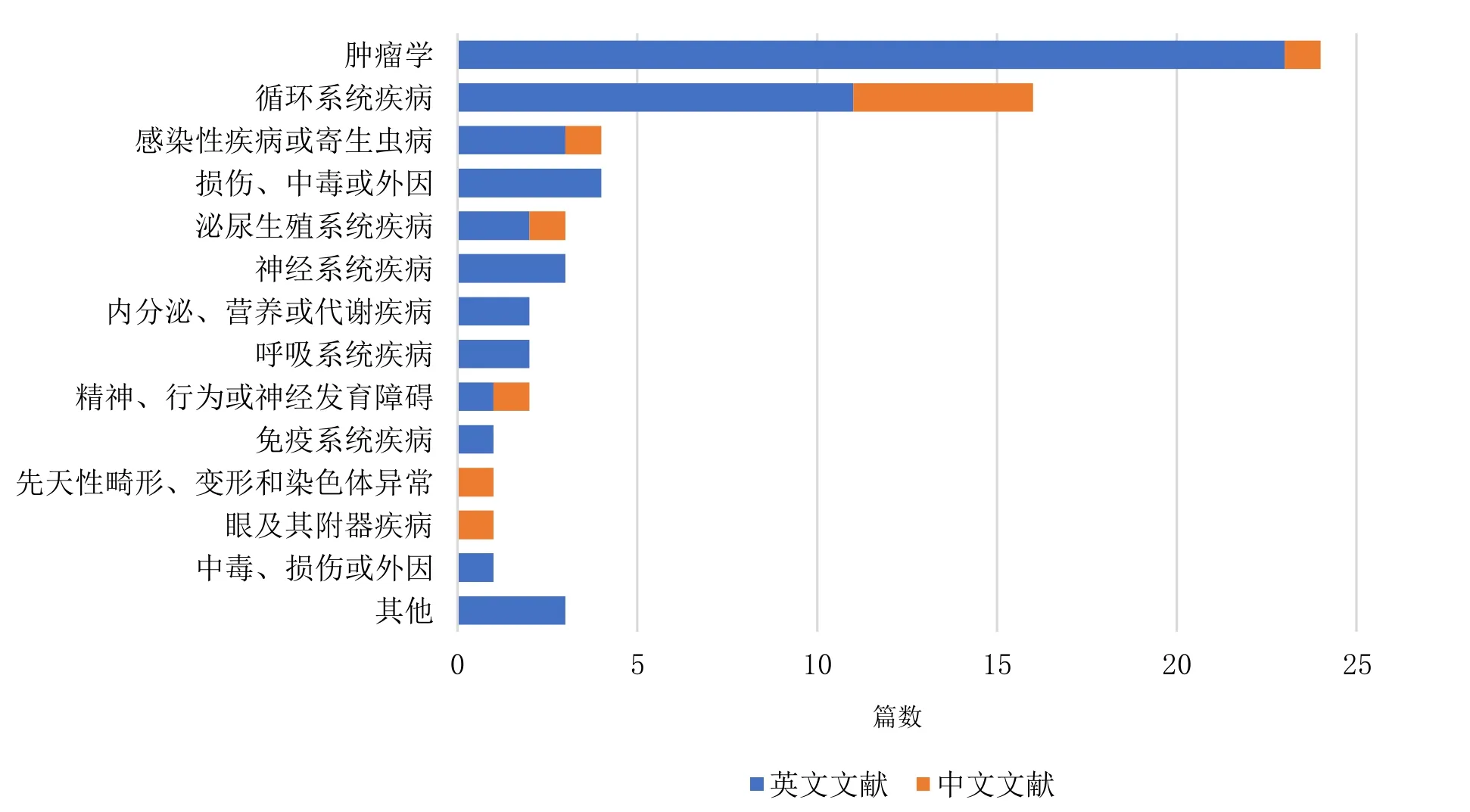
图6 应用外对照的单臂试验所属疾病领域中英文发文量对比图Figure 6. Comparison of Chinese and English publications in disease areas of single-arm trials using external controls
3 讨论
本研究纳入文献以肿瘤学及循环系统疾病领域发文量最多,表明相关领域关注度较高。肿瘤学相关文献主要关注新型治疗方法或新型药物,循环系统疾病与医疗器械相关文献联系密切。英文文献以肿瘤学最多,其次为循环系统;中文文献中循环系统疾病占比较大,其原因可能在于:2015年以前,国内抗肿瘤活性成分相关研究全球占比相对较小,2016年后占比显著增加,但仍与国外存在一定差距[83-84]。由于肿瘤学相关疾病多见难治性疾病或罕见病,其RCT设置存在伦理问题;循环系统疾病仅能选择一种器械或手术方式,难以设置对照组[85],故应用外对照的单臂试验在该领域有一定优越性。
应用外对照的单臂试验用于药品注册研究时,主要用于临床Ⅱ期,且研究目的主要为探究有效性,与Ⅱ期临床试验初步评价有效性试验目的相符合[86]。部分文章未提及临床试验分期,可能有如下原因:并非所有的医疗器械均需进行临床试验[87];国内临床路径相关指导原则未提及需进行试验注册[88];手术治疗未有相关要求;药物治疗类文章为已上市药物再研究,如联合用药或疗效对比,而非药物注册研究。在外对照方式的选择上,中文文献未在历史/同期对照的选择上有明显偏向,英文文献更多的选择了历史对照而非同期对照,可能由于国外电子病历协作互通性强,历史对照数据较易获得[89]。但历史对照可导致众多偏倚[90],有一定的局限性,故在选择历史对照时可在患者基线特征、诊断标准等方面谨慎选择[91];采用倾向评分匹配[90]或分层分析方法[8]减少混杂因素。
研究表明,应用外对照的单臂试验相关文献以美国及日本发表较多,可能与二者较早发布了单臂试验数据支持药品注册的决议有关;自首篇文献发表以来,相关文献发文量整体呈波动上升趋势,近年来各国药品审评中心陆续出台相关政策,对单臂试验数据支持新药注册做出指导,在一定程度上显示出各国对应用外对照的单臂试验这一临床试验设计的认可。在混杂因素的控制上,多数文献在设置外对照时进行匹配以平衡基线,或采用一些统计分析方法,但并未形成统一趋势,仍待相关方法学指导。
与RCT相比,单臂试验中的混杂因素难以控制,结果可预见性差,存在多方面的局限性。故NMPA要求单臂试验数据用于支持抗肿瘤新药注册时,受试者必须满足“复发/难治”的定义,并要求充分体现出其“充分治疗、缺乏标准治疗手段”的特点[6],以规范单臂试验的适用范围。在晚期非小细胞肺癌相关指导原则[92]中,NMPA指出单臂试验可以采用更少的样本量,并对目标值的选取提出建议,且已有针对单臂试验样本量选择[7]及单臂试验连续型数据处理方法[93]的研究,单臂试验在我国已有较好的发展环境。自2012年首见应用外对照的单臂试验相关文献发表后,年发文量始终保持较低水平;检索时发现,若对中文数据库进行主题检索则无法检索到相关文献,提示我国应用外对照的单臂试验尚处于起步阶段。
本研究存在一定局限性。首先,在筛选文献时,部分中文文献提供的信息不足以判断其是否为试验性研究,为避免误筛,故将相关文献纳入研究,可能对中文文献发文量及疾病领域分布产生一定影响,敏感性分析结果表明其影响较小。其次,在提取数据时,2篇文献由于杂志限制,作者机构未能对应,可能有一定影响,但敏感性分析表明此影响亦可接受。最后,本文仅对中英文数据库进行检索,未通过其他方法获得相关文献,且非公开文献难以检索,可能存在语言偏倚及发表偏倚。
本研究发现,外对照在单臂试验的应用存在不足,有待相关方法学进一步发展,以便产出高质量的研究证据,为临床应用和政府决策提供支持。

