Convey指引导管联合球囊跟踪辅助技术通过异常桡动脉路径的应用体验
李文迪 周力 姚道阔 梁思文 赵慧强 陈晖
目前,经桡动脉路径行经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)以其创伤小、血管并发症发生率低、止血操作简便,术后不需要卧床等诸多优点,已成为我国绝大多数冠心病介入手术的路径,欧美地区的各大指南也相继将桡动脉推荐为PCI的首选路径[1-2]。相较于股动脉,桡动脉存在解剖异常发生率高以及易发痉挛的特点。一旦桡动脉严重迂曲或痉挛,导管通过极其困难;暴力操作则会导致桡动脉损伤、痉挛进一步加重,局部疼痛或者前臂局部血肿甚至引发骨筋膜室综合征。有时术者不得不更换路径重新进行动脉穿刺,给患者带来额外的痛苦。实践证明,球囊跟踪辅助(balloon-assisted tracking,BAT)技术是一种可以有效解决经桡动脉行PCI时遇到桡动脉路径异常且指引导管难以通过的方法[3];但在一些桡动脉严重迂曲甚至成袢的患者中也无法保证可以成功通过。Convey指引导管因其独特的Comfortcoat SL亲水涂层,具备良好的通过性,在经桡动脉路径行PCI中体现出一定的优势。本文作者在面对桡动脉路径异常的患者时,采用Convey指引导管联合BAT技术进行操作,取得了满意的效果,现将应用体验总结如下。
1 临床资料
1.1 研究对象(表1)

表1 异常桡动脉路径应用BAT 技术通过15 例
纳入并分析2019年7月至2020年7月于首都医科大学附属北京友谊医院心脏导管室经桡动脉路径行PCI的15例患者。该15例患者均穿刺成功,并顺利置入鞘管且回血满意,但无法送入J型导丝,桡动脉造影提示桡动脉严重迂曲或顽固性痉挛。15例患者中男性7例,女性8例;平均年龄(70±12)岁;包括不稳定型心绞痛11例,急性前壁心肌梗死2例(病例编号5,病例编号8),急性非ST段抬高型心肌梗死2例(病例编号6,病例编号10)。桡动脉路径具体状况为:桡动脉狭窄1例(病例编号3),桡动脉痉挛1例(病例编号2),桡动脉迂曲13例,包括桡动脉成袢6例。
1.2 手术方法
1.2.1 桡动脉穿刺 患者均采用常规体位,右侧上臂外展,穿刺部位以1%利多卡因局部麻醉。15例均应用Terumo公司桡动脉穿刺套件[20 G穿刺针、0.025 in(1 in=2.54 cm)直导丝及6 F动脉鞘管],采用Seldinger法穿刺桡动脉成功,鞘管均能够完全置入且回血良好。沿动脉鞘管注入肝素盐水100 U/kg。
1.2.2 桡动脉造影 采用5 F Terumo MP造影导管、J 型导丝,推送造影导管,因桡动脉路径异常,导丝在前臂部位遇到阻力无法通过时,退出导丝,经造影导管注入体积比1∶1稀释的对比剂行血管造影显示桡动脉痉挛、狭窄或迂曲(如考虑痉挛所致,可经导管反复给予硝酸甘油200 μg/次,直至血压不能耐受或患者出现明显心悸、头痛,平均给药2~3次,再次造影显示痉挛仍无改善)。
1.2.3 BAT技术 经血管造影明确桡动脉狭窄、迂曲或痉挛后,换用Convey指引导管沿其送入0.014 in导丝(如runthrough)通过阻力段并送导丝至肱动脉近心段,之后沿导丝送入2.0~2.5 mm预扩张球囊至导管开口处,突出导管口5~10 mm,给予压力6~8 atm(1 atm=101.325 kPa)保持球囊扩张。扩张球囊的近端部分伸出Convey指引导管,球囊远端和Convey指引导管紧密接触,由于前端呈梭形,减少了指引导管头端的阻力,故对血管内膜一般无明显损伤。Convey指引导管和球囊作为一个整体(指引导管球囊复合体)通过阻力段后,球囊回抽,与导丝一同撤出,换用超滑导丝或 J 型导丝继续将Convey指引导管前送,若是桡动脉袢(图1,病例编号5)则需旋转导管将血管袢“拉直”,再将指引导管送至主动脉窦底,从而完成PCI。
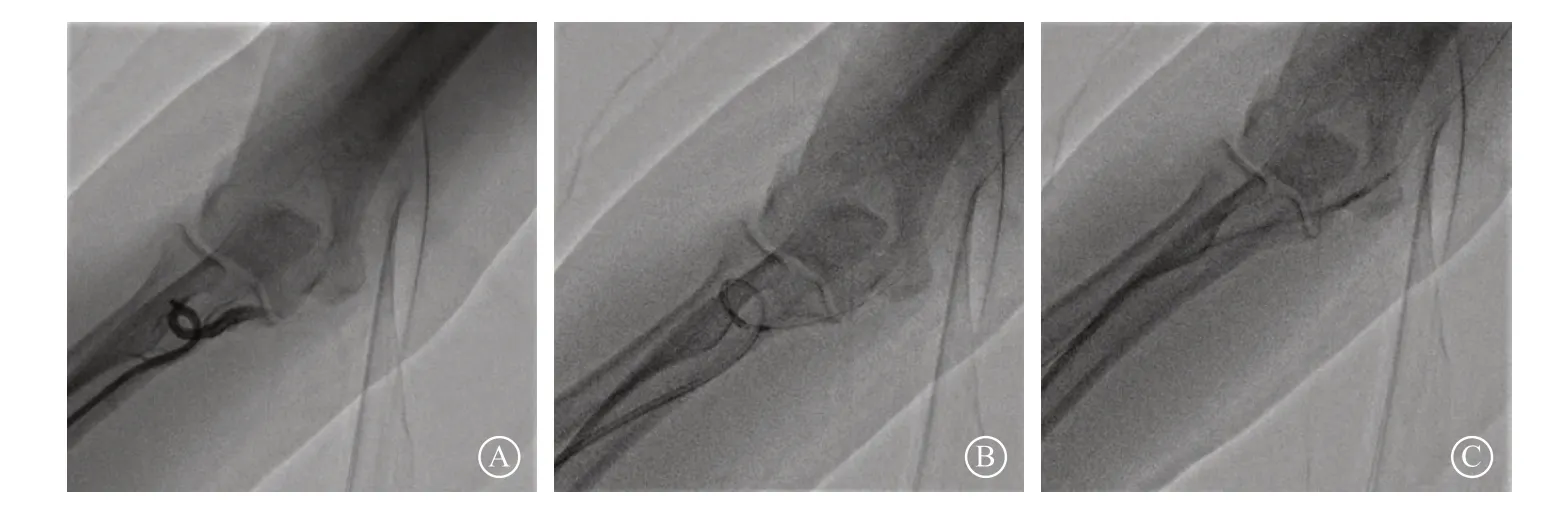
图1 病例编号5,女,75 岁,急性前壁心肌梗死 A.急诊PCI 术中桡动脉鞘管成功置入后J 型导丝无法通过,造影提示桡动脉迂曲成袢;B.送runthrough 导丝通过桡动脉袢,以2.0 mm×12 mm 预扩张球囊引导Convey 6 F Left BU 3.25 指引导管通过血管袢;C.应用BAT 技术顺利通过桡动脉袢并旋转导管将其“拉直”,完成LAD-PCI 术
1.3 手术结果
2019年9月至2020年7月,经桡动脉路径行冠状动脉造影示:桡动脉严重痉挛1例(图2,病例编号2),桡动脉狭窄1例(病例编号3),桡动脉迂曲13例,未见桡动脉损伤导致对比剂外渗。15例均应用临床上现已广泛使用,在我国经桡动脉路径行PCI比率目前已达90.5%[5],成为PCI的主要路径,在复杂冠状动脉病变介入治疗、急性心肌梗死(acute myocardial infarction,AMI)急诊PCI中也已作为首选路径[6]。与传统股动脉路径相比,桡动脉路径的优势在于它位置表浅、邻近无重要的组织器官、容易压迫止血[7],而且由于手掌为桡动脉和尺动脉双重供血,故不易出现手部缺血,术后护理工作量较股动脉明显减轻。相较于股动脉路径,即使在P C I 术前及术中应用了大量的抗血栓药物,但术后桡动脉鞘管仍能被立即拔出,应用桡动脉压迫器能够快速而安全地止血。采用桡Convey指引导管联合BAT技术成功完成PCI,除2例患者(病例编号2,病例编号6)术后出现前臂轻度皮下淤肿、经加压包扎后好转外,其余病例观察至术后2~3 d均未出现穿刺点出血、迷走神经反射、前臂血肿、骨筋膜室综合征、假性动脉瘤等不良并发症。

图2 病例编号2,男,59 岁,不稳定型心绞痛 A.动脉鞘管成功置入后J 型导丝无法送入,造影显示桡动脉纤细,考虑痉挛,经鞘管反复推注硝酸甘油200 μg/次,重复造影显示无缓解;B.送runthrough导丝通过桡动脉痉挛段,以2.0 mm×12 mm 预扩张球囊引导Convey 6 F Left BU 3.25 指引导管通过;C.应用BAT 技术成功送导管通过桡动脉痉挛处,随后完成LAD-PTCA 术
2 讨论
目前在PCI中,常用的路径为桡动脉路径,其次为股动脉路径,极少采用肱动脉或尺动脉路径。随着医疗器械的创新及冠状动脉介入诊疗技术的不断发展,以及双联抗血小板药物的广泛应用,尽管传统的经股动脉路径具有血管走行较直、血管直径较大、穿刺容易、学习曲线较短等优点,但术后需较长时间卧床和穿刺侧肢体制动,且严重血管并发症(如血肿、假性动脉瘤、动静脉瘘、下肢静脉血栓形成等)发生率较高。20世纪90年代,Neumann等[4]开展了经桡动脉路径介入治疗技术。该技术在动脉路径还能够显著降低穿刺点出血并发症的发生率,减少住院时间,患者术后无需卧床制动,可以避免因长时间卧床、下肢制动以及强力压迫而导致下肢静脉血栓形成的风险。但是由于桡动脉直径比股动脉明显较细,且作为人体平滑肌的特性动脉,血管壁弹性纤维较多,血管动力活动以β1受体兴奋为主,β2受体较少,使血管舒张的β受体很少,在紧张、疼痛及血管直接刺激等情况下,血液中儿茶酚胺水平升高,使β1受体兴奋;而桡动脉对于人体循环中的儿茶酚胺又较为敏感,很容易发生痉挛[8]。另外桡动脉本身发育异常多见,如桡动脉袢形成或桡动脉迂曲、纤细、狭窄,导致指引导管无法顺利通过,致桡动脉内膜损伤,严重者还会发生管腔闭塞、血管夹层或者上肢血肿等并发症[9],影响PCI的效果。为了缓解痉挛,反复桡动脉内注射硝酸甘油,可能造成低血压发生;有时不得不于对侧桡动脉、尺动脉或股动脉进行二次穿刺,增加了手术时间及操作难度。
为应对桡动脉路径困难,B A T技术应运而生。其最早是被用于处理桡动脉细小和迂曲的病例[10],之后应用越发广泛,在处理桡动脉发生严重痉挛或桡动脉袢时也有一定的成功率。该技术是利用球囊扩张后的锥形头端置于导管开口处,一体化推进导管通过阻力段。由于置于导管开口的球囊增加了导管的顺滑性,避免了导管开口所致的嵌顿及内膜损伤;同时也增加了导管头端的灵活性,易于通过桡动脉迂曲段、痉挛,甚至穿孔损伤段。Convey指引导管独特的Comfortcoat SL亲水涂层使其外壁更加顺滑,该涂层是一种具有良好生物相容性的功能涂层。在干燥状态下,涂层厚度在5 μm以内,有良好的韧性,其在医疗器械表面均匀附着,无色透明,肉眼不易观察到;在润湿状态下,该涂层被激活形成无色透明的水凝胶附着于管壁,该水凝胶涂层高度润滑且可以承受反复摩擦,能够明显减少导管推送时的阻力,提高输送性。
总之,Convey导管在BAT技术中应用时,因其独特的亲水涂层,具备良好的通过性,成为一种解决经桡动脉路径介入治疗中因桡动脉路径异常无法通过导管时的安全有效方法。
利益冲突 所有作者均声明不存在利益冲突

