非布司他治疗痛风的快速卫生技术评估
刘 琛,白向荣,门 鹏,杨毅恒,翟所迪,闫素英*
0 引言
痛风是一种单钠尿酸盐结晶沉积所致的关节病,与高尿酸血症相关。在发达国家的患病率为1%~2%,且呈逐年增加趋势[1]。我国尚缺乏痛风流行病学调查数据,不同时间不同地区报道的痛风患病率为1%~3%,并呈逐年上升趋势[2]。急性痛风首选非甾体抗炎药和秋水仙碱,次选口服糖皮质激素[1]。慢性痛风首选抑制尿酸合成的药物,包括别嘌醇和非布司他,也可选择促进尿酸排泄的药物苯溴马隆。意大利、英国、美国和中国的痛风治疗指南指出,非布司他是别嘌醇不耐受或肾功能不全足量使用别嘌醇血尿酸仍不达标的患者二线治疗选择[3-7]。
非布司他是一种黄嘌呤氧化酶抑制剂,通过抑制尿酸合成降低血清尿酸浓度。然而,相比于一线治疗药物别嘌醇,非布司他价格较高,需从有效性、安全性和经济性3个维度对其进行评价。卫生技术评估(Health technology assessment,HTA)是利用循证医学和卫生经济学的方法,对卫生技术的技术特性、有效性、安全性、经济性和社会适应性进行系统评价,为卫生和医保决策者及医药卫生人员提供合理选择卫生技术的科学信息和循证依据[8]。其中,快速HTA可相对高效地对现有主要证据进行梳理和分析,日益被重视并用于决策制定[9]。本研究旨在通过对非布司他治疗痛风进行快速卫生技术评估,为医疗机构药品遴选和使用提供参考。
1 资料与方法
1.1 文献检索策略 计算机检索PubMed、the Cochrane Library等英文数据库和CNKI、万方等中文数据库,补充检索NHS EED和CADTH等卫生技术评估数据库。检索词:(1)英文数据库。①PubMed:(febuxostat)AND(systematic review OR meta analysis OR cost OR economic);②Cochrane:febuxostat。(2)中文数据库。CNKI/万方:(“非布司他”or“非布索坦”)and[(系统评价 or 荟萃分析 or meta分析)or(成本 or 经济 or 费用)]。(3)卫生技术评估数据库:febuxostat。语种:中文和英文。检索时间:自建库至2020年3月。
1.2 纳入与排除标准
1.2.1 纳入标准:(1)研究人群(P):年龄>18岁的痛风患者。(2)干预措施(I):非布司他单药或联合其他常规治疗。(3)对照措施(C):别嘌醇、安慰剂单独或联合其他常规治疗。(4)结局指标(O):①有效性指标:血尿酸达标的情况,包括末次随访血尿酸降低水平、末次随访血尿酸浓度达标率、随访最后3个月血尿酸持续达标的患者比例;②安全性指标:不良反应发生情况,包括治疗相关不良事件发生率、心血管事件发生率;③经济性指标:增量成本、增量成本效果比。(5)研究类型(S):①既往发表的卫生技术评估报告;②系统评价/Meta分析;③药物经济学研究。
1.2.2 排除标准 痛风合并慢性肾脏病患者;无法获得全文文献。
1.3 文献筛选 由2位评价者独立筛选文献,共同决定纳入的文献;如遇分歧,通过讨论或咨询第3位评价者解决。
1.4 数据提取 按照预先设计好的数据提取表,由2名评价者独立提取数据。提取的数据包括研究的基本信息、纳入人群、样本量、用药方案(干预vs.对照)、结局指标和结论等。
1.5 质量评价 采用国际卫生技术评估组织协会制定的HTA checklist对HTA报告进行质量评价。采用系统评价评估测量工具(A measurement tool to assess systematic reviews,AMSTAR)量表对系统评价/Meta分析进行质量评价。采用综合卫生经济评价报告标准(Consolidated health economic evaluation reporting standard,CHEERS)量表对经济学研究进行质量评价。
1.6 数据分析 对于纳入的HTA 报告、系统评价/Meta分析和经济学研究,根据纳入研究的类型以及结局指标,采用定性分析方式对研究结论进行分类汇总。
2 结果
2.1 文献检索结果 检索获得241篇文献,其中PubMed 101篇、The Cochrane Library 4篇、CNKI 80篇、万方56篇。去重后有182篇,阅读标题和摘要初筛后有41篇,进一步获取全文,根据纳入排除标准进行复筛,最终纳入8篇,其中HTA报告2篇,系统评价/Meta分析3篇,经济学研究3篇。
2.2 纳入文献基本特征 共纳入3篇系统评价/Meta分析。发表时间2017-2019年,纳入原始研究9~18个,样本量1 816~7 757。涉及5个主要的结局指标,其中有效性指标3个,安全性指标2个。文献总体质量良好。纳入系统评价/Meta分析文献基本特征见表1。

表1 纳入系统评价/Meta分析文献基本特征
共纳入3篇经济学研究和2篇HTA报告。发表时间为2014-2016年,其中,2014年发表的两项研究为HTA报告。涉及的国家有西班牙、美国和英国。文献总体质量良好。纳入经济学研究和HTA报告文献基本特征见表2。
2.3 非布司他治疗痛风的有效性和安全性研究
2.3.1 有效性 末次随访血尿酸降低水平:40 mg非布司他与别嘌醇疗效相当(MD=35.92,95%CI:-3.77~75.61,P=0.08);80 mg非布司他优于别嘌醇(MD=-34.68,95%CI:-61.35~-8.00,P=0.01)[10]。
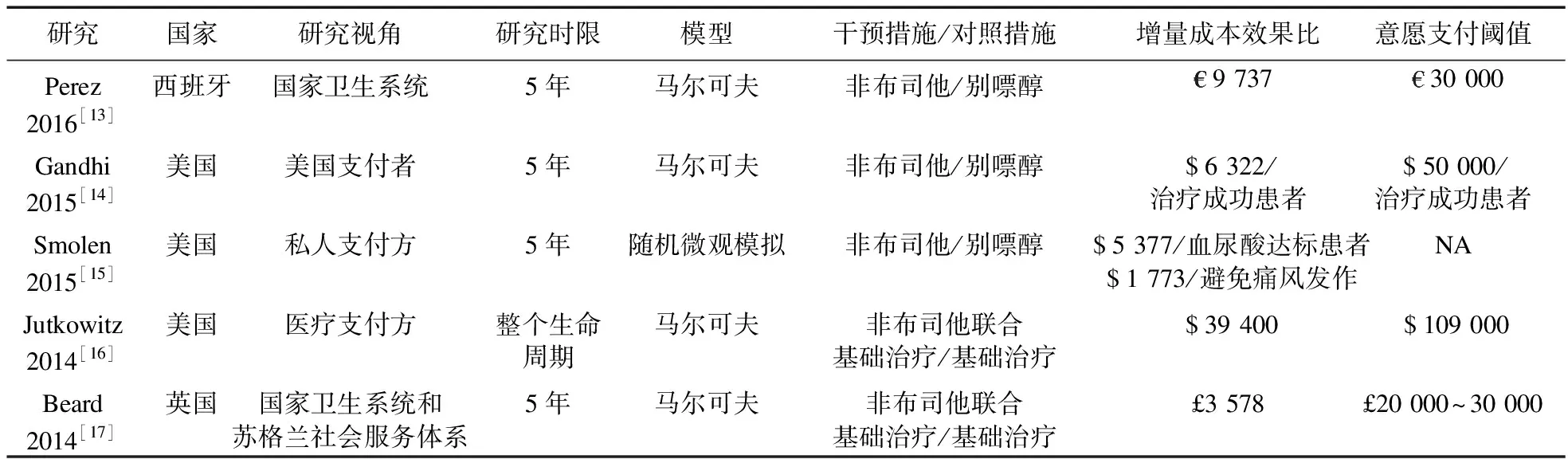
表2 纳入经济学研究和HTA报告文献基本特征
末次随访血尿酸浓度达标率:40 mg非布司他与别嘌醇疗效相当,其中一项研究报告两药差异接近显著性水平(RR=1.10,95%CI:1.00~1.21,P=0.050;RR=0.88,95%CI:0.64~1.21,P=0.41);80 mg非布司他优于别嘌醇,差异有统计学意义(RR=1.74,95%CI:1.49~2.04,P<0.001;RR=1.39,95%CI:1.04~1.85,P=0.03);120 mg非布司他优于别嘌醇,差异有统计学意义(RR=2.11,95%CI:1.87~2.38,P<0.001)[10-11]。
随访最后3个月血尿酸持续达标的患者比例:40 mg非布司他与别嘌醇疗效相当(RR=1.17,95%CI:0.89~1.54,P=0.250);80 mg和120 mg非布司他优于别嘌醇,差异有统计学意义(80 mg:RR=2.21,95%CI:1.74~2.82,P<0.001;120 mg:RR=2.91,95%CI:2.44~3.47,P<0.001)[11]。
2.3.2 安全性 治疗相关不良事件发生率:40 mg非布司他与别嘌醇相当(40 mg:RR=0.99,95%CI:0.92~1.07,P=0.860);80 mg和120 mg组优于别嘌醇,差异有统计学意义(80 mg:RR=0.94,95%CI:0.89~0.99,P=0.020;120 mg:RR=0.90,95%CI:0.84~0.96,P=0.002)[11]。
心血管事件发生率:非布司他与别嘌醇短期治疗心血管事件发生率相当(短期治疗:RR=1.69,95%CI:0.54~5.34,P=0.37),但长期治疗心血管事件发生率高,差异接近显著性水平(RR=3.90,95%CI:0.92~16.47,P=0.06)[12]。
3 讨论
通过快速卫生技术评估的方法,本研究发现,在痛风患者中,非布司他40 mg与别嘌醇有效性和安全性相当,非布司他80 mg和120 mg疗效显著优于别嘌醇,治疗相关不良事件发生率显著低于别嘌醇。从心血管风险的角度来看,短期使用非布司他与别嘌醇风险相当,长期风险高于别嘌醇,差异接近显著性水平。研究结果之间整体一致性好。从药物经济学的角度来看,非布司他的增量成本效果比在意愿支付阈值范围内,是一种具有经济性的药物治疗选择。
非布司他的药品说明书中建议起始剂量为40 mg,1次/d,可根据疗效将剂量调整至最大剂量80 mg,1次d。本研究发现,40 mg非布司他与别嘌醇相当,80 mg和120 mg非布司他优于别嘌醇,由于国内没有120 mg非布司他用药的推荐,故不建议使用更大剂量的非布司他。从安全性角度来看,非布司他长期用药增加心血管风险和全因死亡风险一直倍受关注。2016年4月,加拿大卫生部开始关注非布司他的心力衰竭风险。2017年8月,美国FDA批准非布司他药品说明书对严重肾损害患者的剂量限制在40 mg,1次/d。2017年11月,美国FDA警告非布司他与心脏相关死亡和全因死亡风险增加相关。2019年2月,美国FDA更新2017年11月的安全通告,要求非布司他的说明书中新增黑框警告,提醒对于伴有心血管疾病的痛风患者,使用非布司他会增加心血管死亡风险,并限制非布司他的适应证为别嘌醇治疗失败或不能耐受别嘌醇的患者。2019年11月,加拿大卫生部也发布了非布司他心血管死亡风险增加和限制适应证的警告,不建议非布司他用于缺血性心脏病或充血性心力衰竭的患者。国外药物经济学的研究中,非布司他均优于别嘌醇,研究结果一致。然而由于药物经济学研究中成本的计算是根据本国的经济水平来确定的,在外推时会受到影响。从现在的药品价格来看,日最大剂量的原研非布司他片价格是别嘌醇的9倍,在非布司他仿制药上市后,价格差距可能会逐渐缩小。因此,急需进行中国患者人群的药物经济学原始研究,以获得非布司他治疗痛风的最新、最佳证据,为医疗机构药品遴选提供更多决策证据。
基于现有的研究结果,对于使用别嘌醇治疗失败或不能耐受的患者,如缺血性心脏病或充血性心力衰竭等基础心血管疾病患者,在选用非布司他治疗痛风时,应从40 mg起始治疗,疗效不佳者剂量可增加至80 mg,但应关注长期用药心血管系统的风险。非布司他不同剂量治疗具有经济性,但在我国的经济性仍需进一步研究。

