微纳米气液分散体系氧化吸收CO
吴思成,李登新,2,孙红蕊,许威,郭媛媛,肖政国,叶志伟
(1.东华大学 环境科学与工程学院,上海 201620;2.上海污染控制与生态安全研究院,上海 200092;3.上海市纺织科学研究院,上海 200082)
常见的CO净化方法[1]主要有催化氧化、固体吸附、液体吸收和深冷法。其中,低温催化氧化法应用普遍,但金属催化剂造价昂贵;深冷法对混合气体组分要求苛刻;吸附法、液体吸收法对CO的吸收能力有限,液体吸收剂的稳定性也不够理想。相关研究表明,微纳米气泡具有常规气泡不具备的物理化学特性,如比表面积大、传质效率高、停留时间长、ζ电位高、自身增压溶解以及坍塌时产生大量羟基自由基(·OH)等特点[2-4],对烟气中多种污染物具有较高的净化效率[5-8]。本文通过研究微纳米气泡氧化去除烟气中的CO,探究不同条件下CO的净化效果,以期为CO气体的控制排放提供一种新的工艺方法和思路。
1 实验部分
1.1 材料与仪器
H2SO4、NaOH、(NH4)2SO4、十二烷基硫酸钠(SDS)、FeSO4·7H2O、MnSO4·H2O、叔丁醇均为分析纯。
ZJC-NM-01型微纳米气泡发生器;testo 350烟气分析仪;PHSJ-3F型便携式pH计。
1.2 实验方法
实验装置见图1。反应吸收塔有效容积200 L,微纳米气泡发生器额定进气量为1 L/min,额定进水量10 L/min。CO气体与空气经过气体减压阀与流量计后进入缓冲罐,在缓冲罐中充分混合后,与自来水同步进入微纳米气泡发生装置,产生的微纳米气泡水从底部进入吸收塔。处理前后的CO气体浓度均通过烟气分析仪检测。由于微纳米气泡在水中的停留时间较长,故整个系统持续运行1 h,1 h后关闭微纳米气泡发生装置并停止进气。
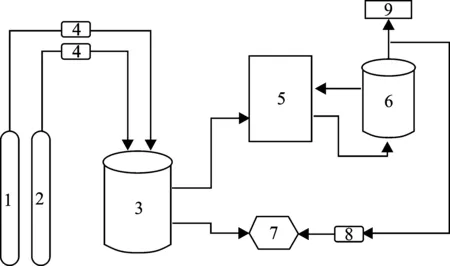
图1 实验装置示意Fig.1 Schematic diagram of the experimental setup 1.CO钢瓶;2.空气钢瓶;3.气体缓冲罐;4.气体流量计;5.微纳米气泡发生器;6.反应吸收塔;7.烟气分析仪;8.干燥器;9.尾气收集装置
1.3 分析方法
通过烟气分析仪测量处理前后的CO气体浓度,采用pH计测定溶液pH。CO脱除效率的计算公式如下:
(1)
(2)
(3)
式中,m1为进气CO的质量,m2为出气CO的质量,mg;M为CO的摩尔质量,g/mol;T1为进气口气体温度,T2为出口气体温度;P0为一个标准大气压,P1为气体减压后的压力,P2为出口气体压力,Pa;A1、A2分别为进出口CO的体积浓度,mg/L;q1、q2分别为进出口气体流量,mL/min;t为系统运行时间,min。
2 结果与讨论
2.1 CO浓度对其去除的影响
在初始水温为25 ℃,初始pH=7条件下,CO浓度对其去除的影响见图2。
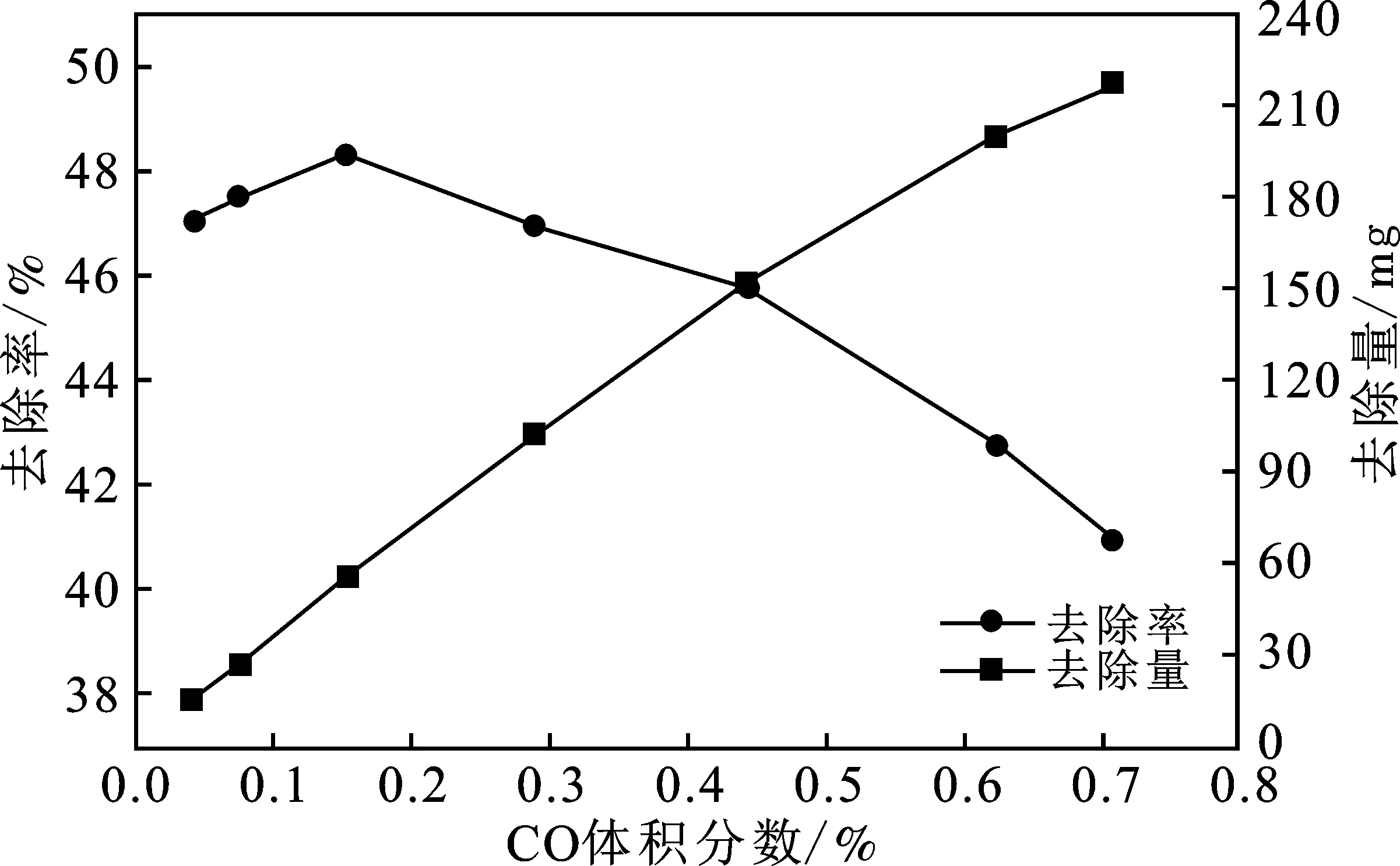
图2 CO浓度对其净化脱除的影响Fig.2 Effect of CO concentration on its removal
由图2可知,CO的去除量随着其体积分数的升高而升高,但去除率有一个先升高后降低的趋势。当CO的体积分数为0.15%时,CO气体的去除率最高,达到48.33%,随着浓度的继续增加,去除率有所下降,当体积分数上升至0.71%时,去除率为40.97%。这是因为:当CO浓度较低时,气泡中的CO分子较少,液相中的羟基自由基与其接触的概率较低[9];随着CO浓度升高,羟基自由基与CO分子接触概率有所提高,利于CO的氧化;但是当CO体积分数超过0.15%时,由于CO在水中的溶解度很低,大量的CO还没及时被氧化就从液相中逸出,不利于CO的去除,导致去除率下降。
2.2 循环次数对CO去除的影响
在初始水温为25 ℃,初始pH=7条件下,改变气体循环次数,考察其对吸收率的影响,结果见图3。
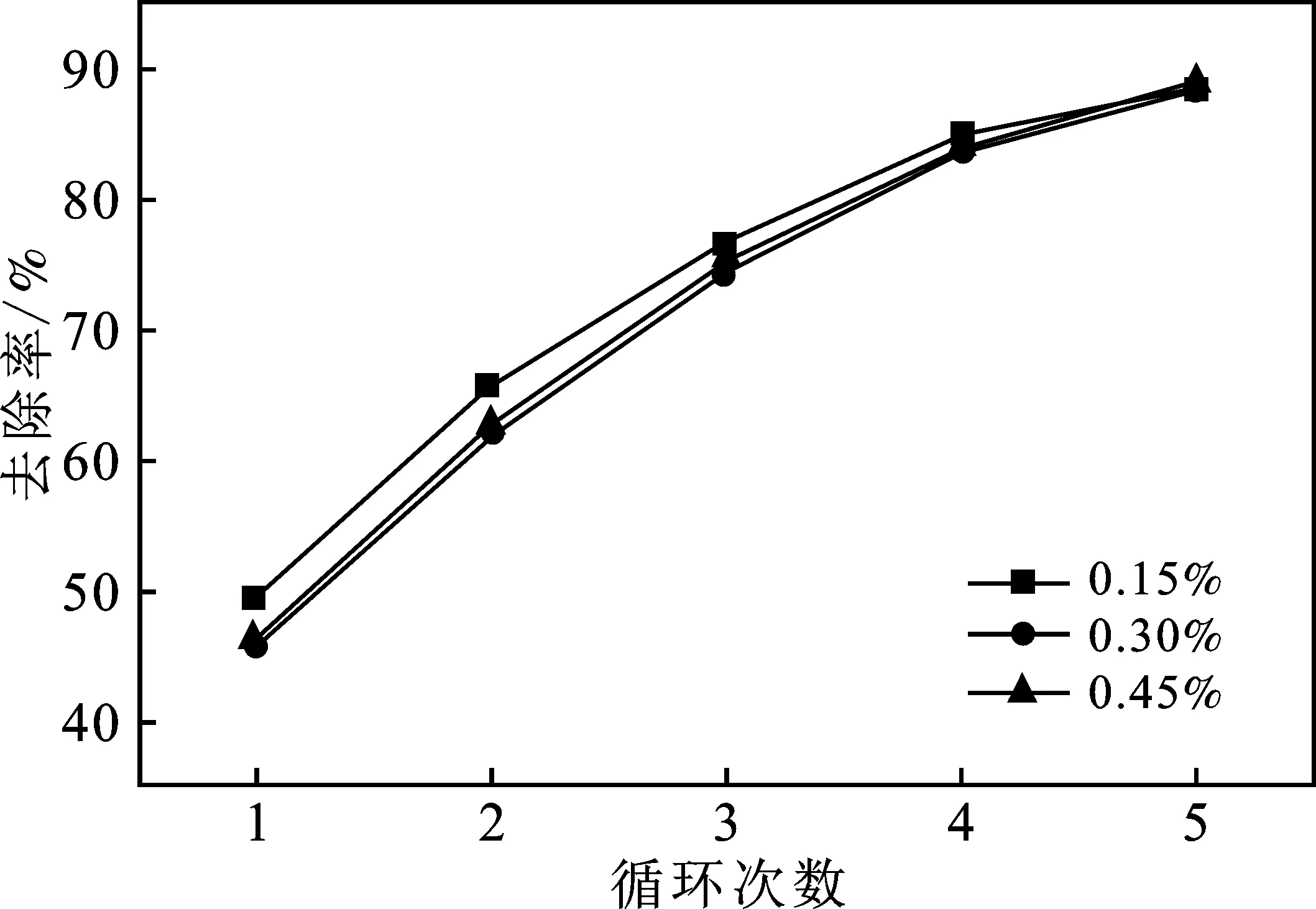
图3 循环次数对CO去除的影响Fig.3 Effect of cycle times on CO removal
由图3可知,在3种不同体积分数下,CO的去除率均随着循环次数增加而提高。当CO体积分数为0.15%时,循环5次条件下,CO去除率达到88.51%,同条件下,CO体积分数增加到0.30%和0.45%时,去除率分别为88.27%和89.06%。
循环实验中,当进气CO质量浓度升至1 951 mg/m3时,出气中CO质量浓度为224 mg/m3。为了进一步提高CO氧化吸收效率,需改进反应条件。
2.3 初始水温对CO去除的影响
在CO体积分数为0.45%、初始pH=7条件下,初始温度对CO去除的影响见图4。
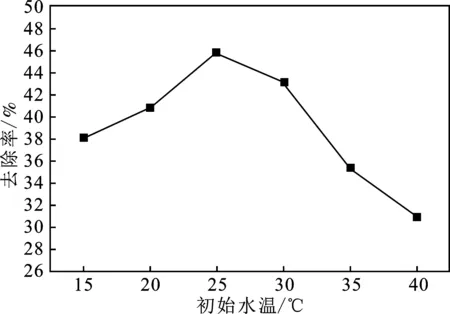
图4 初始水温对CO去除的影响Fig.4 Effect of initial water temperature on CO removal
由图4可知,随着溶液初始温度的升高,CO去除率先升高后下降。当溶液初始温度为25 ℃时,CO的去除率最高,达到45.79%,之后随着温度继续升高,CO的去除率开始下降,40 ℃水温下CO去除率仅有30.98%。相关研究表明:当初始水温较低时,微纳米气泡体系中的溶解氧含量相对较低,气泡坍塌时活化产生的自由基数目较少,随着初始水温升高(<25 ℃),溶解氧含量逐渐上升,并在25 ℃条件下达到最高值[10],CO去除率也随之提高。但是当水温继续升高(>25 ℃),温度的提升大幅降低了气体在水中的溶解度,增加了CO气体进入液相的难度。此外,较高的温度会降低微纳米气泡的稳定性,溶解氧也大量流失,影响CO的去除。
2.4 初始pH对CO去除的影响
在CO体积分数为0.45%,初始水温为25 ℃条件下,初始pH对CO去除的影响见图5。
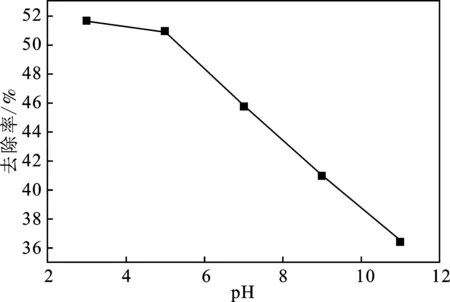
图5 初始pH对CO去除的影响Fig.5 Effect of initial pH on CO removal
由图5可知,酸性条件有利于CO的氧化脱除而碱性条件则抑制了CO的净化。在pH为3的条件下CO的去除率可达51.71%,相较于中性条件提高了5.92%;在pH为11时,CO的去除率仅为36.50%,同比中性条件降低9.29%。其原因是:酸性条件下,溶液中游离的H+促进了微纳米气液分散体系的传质效率[11],在微纳米气泡自身增压溶解(坍塌)时促进了羟基自由基的生成,提高了CO气体的去除率;碱性条件下,溶液中大量游离的OH-与气泡表面的OH-互斥[12],加剧了微纳米气泡在体系中的运动,降低了微纳米气泡的稳定性,导致整个体系的氧化能力降低,从而抑制了CO的去除。
2.5 SDS对CO去除的影响
在CO体积分数为0.45%,初始水温为20 ℃,初始pH=7条件下,SDS浓度对CO去除的影响见图6。
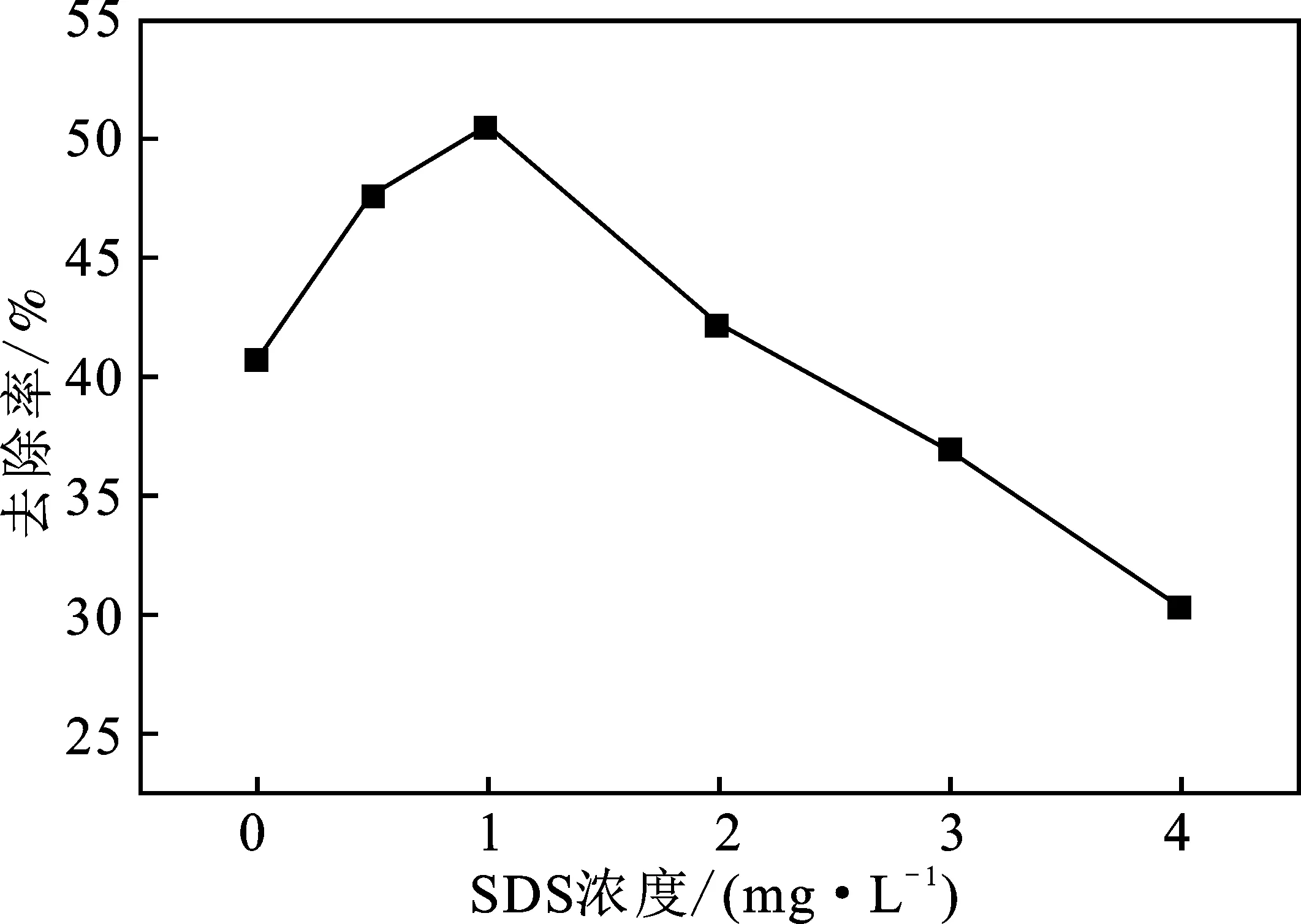
图6 SDS对CO去除的影响Fig.6 Effect of SDS concentration on CO removal
由图6可知,随着SDS浓度的增加,CO去除率先升高后下降。当SDS的浓度为1 mg/L时,CO气体的去除率最高,达到50.45%,随着SDS浓度的继续增加,CO的去除率有所下降,当SDS浓度超过3 mg/L 时,开始起抑制作用。相关研究表明,在水中投加一定量的表面活性剂可以改善液体表面张力,减少微纳米气泡的尺寸,增加比表面积,从而有助于气液两相传质。另外,微纳米气泡尺寸的减小,也有助于加快其自身增压溶解,在坍塌的瞬间产生更多的羟基自由基[13-15]。但随着SDS浓度的继续提高,微纳米气泡的稳定性降低[7],且过高浓度的SDS会争夺并消耗羟基自由基,两者导致CO氧化效率降低,甚至产生抑制作用。
2.6 金属离子对CO去除的影响
分别用FeSO4·7H2O和MnSO4·H2O配制相应浓度的溶液200 L,在CO体积分数为0.45%,初始水温20 ℃,初始pH=7条件下,Fe2+、Mn2+离子对CO去除的影响见图7。
由图7可知,随着Fe2+、Mn2+离子浓度的增加,CO去除率均为先增高后降低。当Fe2+、Mn2+离子浓度分别为1 mmol/L与1.5 mmol/L时,CO气体的去除率最高,分别为47.94%,46.12%。课题组先前研究表明:在微纳米气液分散体系中加入铁、锰等离子后,体系中大量的自由基会使Fe和Mn在Fe2+、Mn2+与Fe3+、Mn3+之间相互转化[16],从而使铁、锰离子起到催化剂的作用加快CO气体的氧化吸收。崔红斌[17]通过研究发现,微纳米气泡的直径会随着溶液离子浓度的增大而增大,且气泡数量会随溶液离子浓度的增大而减少。当溶液中Fe2+、Mn2+离子浓度分别>1 mmol/L与1.5 mmol/L时,微纳米气泡的尺寸过大,同时数量过少,体系氧化能力降低。此外本身具有还原性的Fe2+、Mn2+离子在体系中也会消耗羟基自由基,且消耗量随着离子浓度的增大而增大,使得氧化CO的自由基数目不断减少,多种因素共同影响了CO的氧化吸收效率。
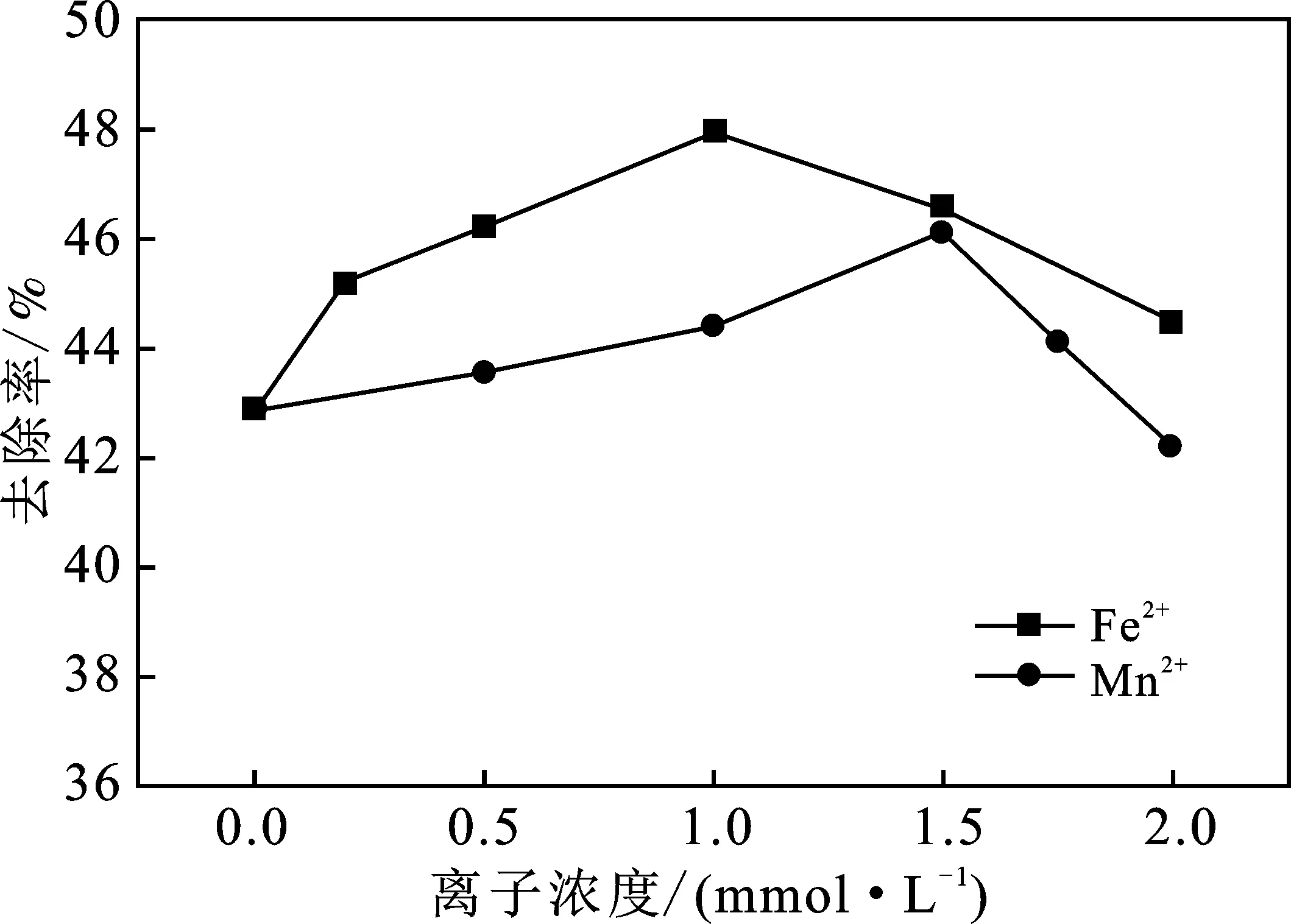
图7 金属离子对CO去除的影响Fig.7 Effect of Fe2+ and Mn2+ concentration on CO removal
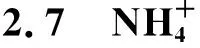

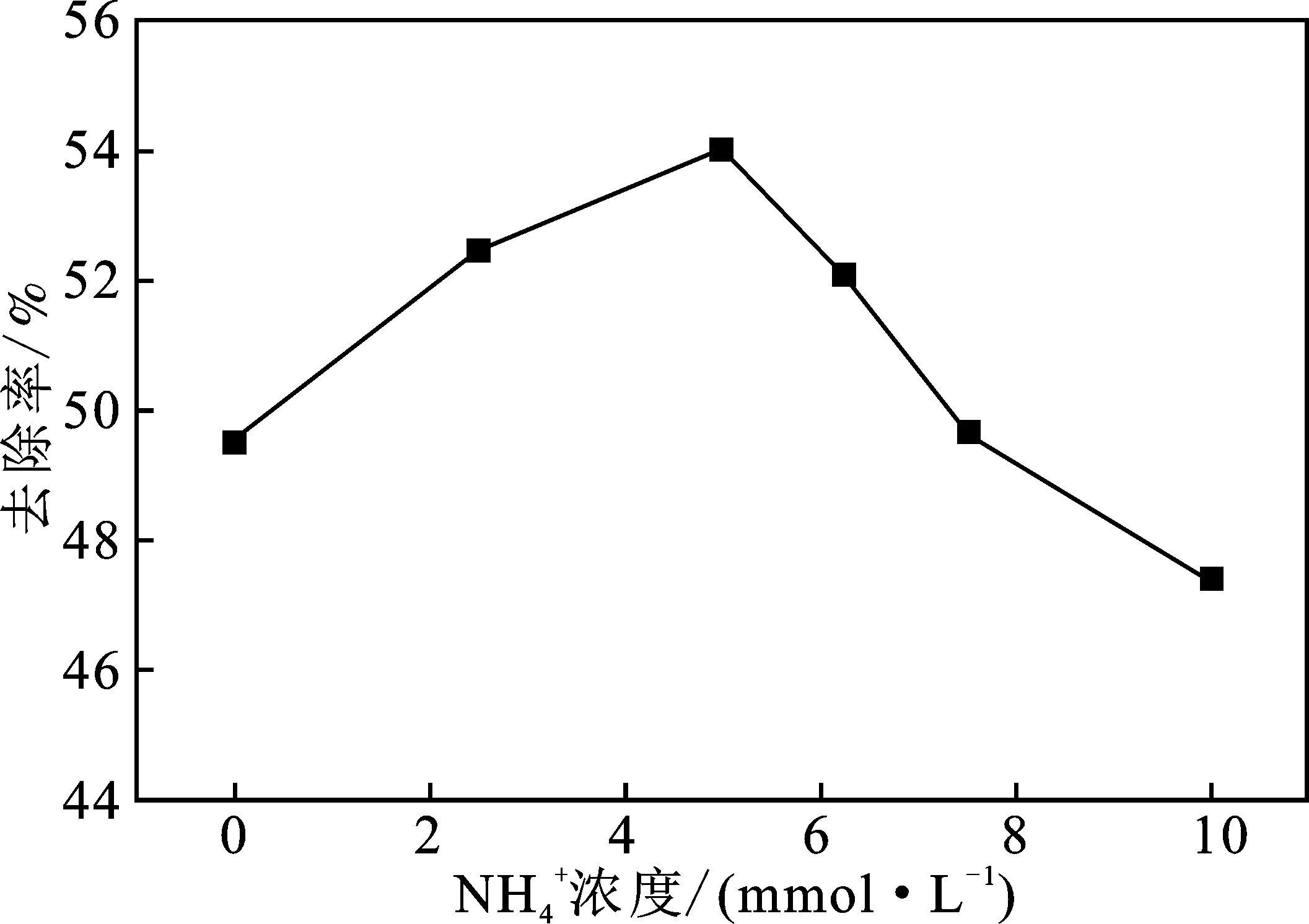
图对CO去除的影响Fig.8 Effect of concentration on CO removal
2.8 CO氧化吸收机理分析
叔丁醇是一种很强的羟基自由基猝灭剂[18],它可以快速捕捉溶液中产生的羟基自由基。分别配制质量浓度为10,20,30,40,50 mg/L的叔丁醇溶液,在CO体积分数为0.45%,初始水温20 ℃,初始pH=7条件下,CO的去除率变化见图9。
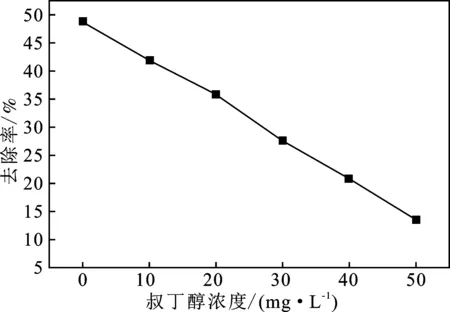
图9 叔丁醇对CO去除的影响Fig.9 Effect of tert-butanol on the removal of CO
由图9可知,随着叔丁醇浓度的增加,CO的去除率不断降低,证明在微纳米气液分散体系中,羟基自由基对CO的氧化吸收起到了关键作用,体系中主要发生的反应如下:

(1)
(2)

(3)
(4)
(5)
随着叔丁醇投加量的增加,CO去除率并没有降至0,这可能是因为叔丁醇的淬灭效率有限,无法完全消耗体系中所有的羟基自由基,也可能是由于200 L水本身也可以溶解少量的一氧化碳,或者体系中还存在着其他种类的自由基。
3 结论
(1)以自来水为水源,利用微纳米气泡氧化吸收CO,当CO体积分数为0.15%,初始温度25 ℃,初始pH=7时,CO的去除率为48.33%,在此条件下,气体经5次循环后CO去除率可以达到88.51%。

(3)体系中的羟基自由基对CO的氧化去除起到关键作用。

