发热咳嗽后大“咯血”休克
邓亮吉 熊洁 钟礼立 林小娟 肖旭平 毛志群
(湖南师范大学附属第一医院/湖南省人民医院 1.儿童医学中心儿童呼吸病学湖南省重点实验室;2.耳鼻咽喉科;3.放射科,湖南长沙 410005)
1 病例介绍
患儿,男,11岁。因间断发热15 d,咳嗽10 d,“咯血”7 d入院。患儿15 d前出现发热,热峰达41℃,伴畏寒、寒战,予头孢硫脒静脉滴注3 d,地塞米松静脉推注1次,疗效欠佳,仍有高热,且于入院前10 d后出现咳嗽,呈阵发性连声咳,有黄脓痰,改为头孢唑肟治疗,发热及咳嗽症状有所减轻。入院前7 d患儿再次出现高热,热峰为39.8℃,伴畏寒、寒战、气促,予吸氧、补液、退热、地塞米松抗炎治疗,当天患儿突发“咯血”,量约20 mL,鲜红色无血块,无食物残渣,予止血治疗后“咯血”症状缓解,改予头孢哌酮舒巴坦、阿奇霉素联合抗感染治疗,患儿热峰下降,气促缓解。入院前5 d后患儿再次出现“咯血”,量约320 mL,呈深红色,随后出现大汗淋漓、口唇苍白、四肢厥冷,心率190次/min,血压79/45 mm Hg,呼吸55次/min,血氧饱和度60%,逐渐出现意识模糊至浅昏迷。立即就诊于当地医院,完善相关检查,血常规:WBC 19.33×109/L(参考值4.3×109/L~11.3×109/L),N%89.6%(参考值31%~70%),Hb 50 g/L(参考值118~156 g/L),PLT 312×109/L(参考值167×109/L~453×109/L);C反应蛋白:312.2 mg/L(参考值0~10 mg/L);降钙素原:79.63 ng/mL(参考值0~0.5 ng/mL);甲状腺功能:游离甲状腺素(free thyroxine,FT4)33.36 pmol/L(参考值12.5~21.5 pmol/L),促甲状腺激素(thyroid stimulating hormone, TSH)0.058μIU/mL(参考值0.6~4.84μIU/mL);促甲状腺激素受体抗体阴性;凝血功能正常。甲状腺B超:甲状腺左侧叶实质光点增粗,回声减低。胸部增强CT:(1)肺动脉CT血管造影未见明显异常;(2)双肺野弥漫性磨玻璃样改变(图1);(3)甲状腺左侧叶区感染征象改变(图2)。诊断考虑肺出血、失血性休克,予0.9%氯化钠溶液扩容,肾上腺素、多巴胺、多巴酚丁胺改善循环,血凝酶、酚磺乙胺、垂体后叶素止血,予甲泼尼龙琥珀酸钠抗炎,静脉输注白蛋白补充胶体,输注浓缩红细胞及血浆补血,改为万古霉素抗感染。经积极抢救治疗,当日患儿“咯血”缓解,神志意识恢复,生命体征平稳。治疗2 d后(入院前3 d)体温正常,偶咳无痰,无咯血。为进一步明确“咯血”病因收入院。自发病以来,患儿精神、食纳欠佳,睡眠尚可,无吞咽疼痛或吞咽困难,无血尿,无黑便及柏油样便。
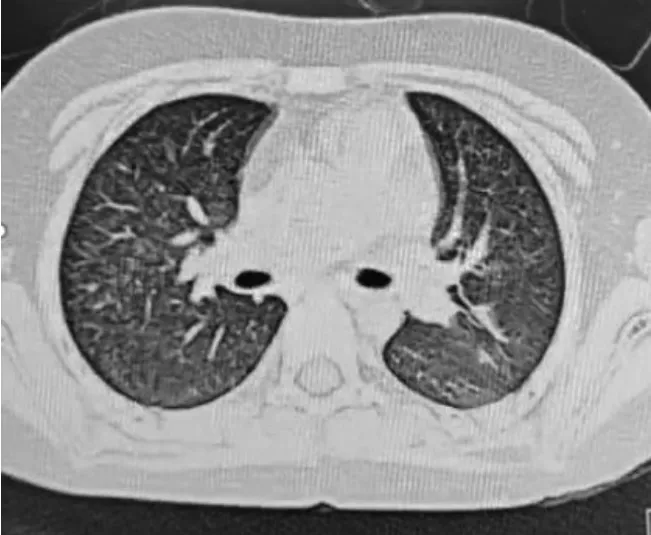
图1 肺部增强CT结果
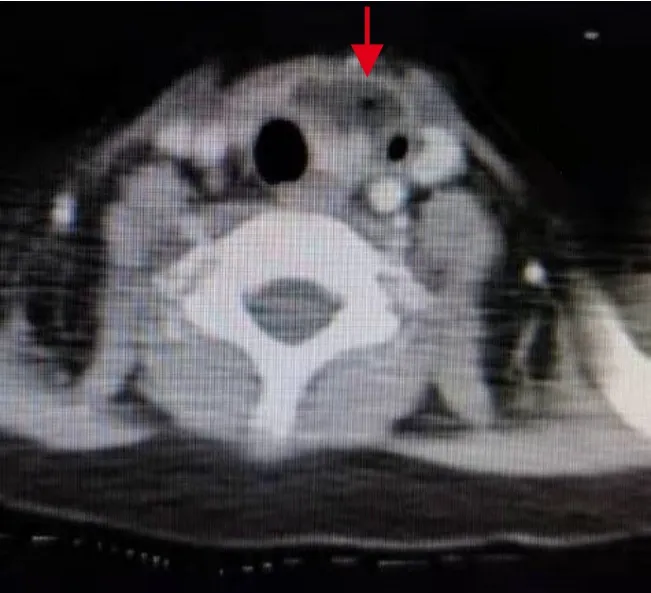
图2 甲状腺区增强CT结果
既往史、个人史、家族史:既往身体健康,无反复呼吸道感染病史,无咯血、鼻衄或活动性出血病史。否认颈部外伤及穿刺操作史,否认异物吸入史。否认新型冠状病毒肺炎、结核等传染病接触史。患儿系第1胎第1产,足月剖宫产出生,无产伤窒息史,生长发育与同龄儿相符,正常计划免疫接种。无类似疾病家族史及其他遗传病史。
入院体格检查:体温36.6℃,脉搏72次/min,呼吸24次/min,血压138/76 mm Hg,体重30 kg,经皮血氧饱和度95%,正常面容,神志清楚。全身皮肤稍苍白,无皮疹、皮下出血。左侧颈部甲状腺区深触痛,局部无异常隆起,皮温不高。鼻腔黏膜正常,口唇无发绀,牙龈无红肿出血,咽部黏膜正常。呼吸规整,无三凹征,双肺叩诊清音,双肺呼吸音粗,未闻及明显干湿啰音。心音有力,律齐,无杂音。腹平软,无压痛、反跳痛,肝脾肋下未触及。神经系统体检未见异常。
2 诊断思维
病例特点:(1)男性学龄期儿童;(2)反复高热、咳嗽起病,伴畏寒、寒战,炎症指标高,抗生素治疗有效;(3)突发大“咯血”伴失血性休克;(4)左侧甲状腺区低密度灶伴甲状腺功能异常;(5)双肺弥漫性病变(感染伴出血?)。
诊断的重点是尽快明确出血原因、出血部位。患儿出血为鲜红色,量大时深红色,无食物残渣,不伴恶心、腹痛、黑便等消化道出血症状,体格检查亦未见上呼吸道出血迹象,临床需考虑咯血可能[1]。咯血病因常有:(1)弥漫性肺泡出血症(diffuse alveolar hemorrhage,DAH):感染等多种因素均可导致DAH,咯血为最具有提示意义的症状,可伴贫血,肺部影像学多呈弥漫性浸润改变[2]。该患儿以发热、咳嗽等感染症状起病,伴咯血及贫血,CT可见双肺弥漫性磨玻璃样改变,需考虑DAH可能。但该患儿出血量大,伴休克,而肺部影像学改变不重,与病情严重程度不相符,且仅经过2 d治疗,气促缓解,肺部无明显啰音,此诊断存在疑点。拟定纤维支气管镜及胃镜检查寻找准确出血部位,必要时局部止血治疗[1-2]。(2)肺结核:肺结核发生干酪样坏死或病变累及血管可出现大咯血。肺部体征不明显,常与肺内病变程度不成比例[1]。患儿高热、咳嗽及咯血,但不伴有结核中毒症状,按计划接种卡介苗且无接触史,病原学检查有助于诊断。(3)肺血管畸形:血管畸形虽属罕见病因,却是引起大咯血的主要病因之一。临床可表现为突发性大量咯血,可出现窒息、失血性休克等,属于临床急重症[1]。该患儿临床表现高度符合此病,需警惕,完善肺血管造影检查可协诊。(4)其他:临床常见大咯血原因还有创伤、支气管异物、支气管扩张、肿瘤、凝血功能障碍等[1],但患儿无相关病史,外院初步检查已基本排除。
患儿左颈部甲状腺区触痛,追问病史发热前有左颈部疼痛,影像发现左侧甲状腺区可见低密度灶,有包膜,其内可见含气征象,结合患儿甲状腺功能检查异常,考虑并发左颈部脓肿及甲状腺化脓性感染。但甲状腺有丰富的血流和淋巴引流,且组织内含碘量高,不利于细菌繁殖,一般不容易出现化脓性感染[3]。该患儿甲状腺脓肿区有含气征象,除考虑产气杆菌感染外,应考虑脓肿与外界相通导致气体进入。先天性梨状窝瘘(congenital pyriform sinus fistula,CPSF)是一种罕见的颈部鳃源性疾病[4],临床常表现为急性化脓性甲状腺炎、颈部软组织感染并脓肿形成[3]。根据既往临床经验,高度怀疑CPSF感染并脓肿形成,颈部增强CT检查及纤维支气管镜探查寻找CPSF内瘘口有助于诊断。
3 进一步检查
入院后完善肝肾功能、心肌酶、电解质、凝血功能、免疫全套、淋巴细胞检测、狼疮全套正常;结核感染T细胞斑点试验、输血前检查、结核菌素纯蛋白衍生物试验、血培养、痰培养、肺泡灌洗液培养、大便隐血试验阴性,进一步排除特殊病原体感染及凝血功能障碍、自身免疫性疾病引发肺出血可能。甲状腺功能:游离三碘甲状腺原 氨 酸(free triiodothyronine,FT3)2.24 pmol/L(参 考 值3.88~8.02 pmol/L),FT4 16.54 pmol/L,TSH 0.033μIU/mL,考虑与感染有关,暂不需处理。
继续使用万古霉素抗感染,3 d后因出现皮疹改为利奈唑胺抗感染。患儿体温稳定,咳嗽减轻,精神明显好转,WBC计数、C反应蛋白、降钙素原正常。但Hb由入院时111 g/L下降至95 g/L,考虑仍存在持续出血,完善纤维支气管镜、胃镜检查排除消化道或下呼吸道出血,肺含铁血黄素试验阴性,不支持DAH诊断。纤维支气管镜进一步探查发现左侧梨状窝有血性液体积聚,持续吸引仍有血液渗出,继而发现左侧梨状窝存在异常瘘口(图3)。同时颈部增强CT提示甲状腺左侧部旁异常密度灶,考虑左侧鳃裂发育异常并局部感染所致;甲状腺左侧叶感染性病变(图4)。以上可明确患儿为CPSF管感染引起出血,经梨状窝内瘘口排出,因此患儿为假性咯血。但查阅文献CPSF感染未见有大出血报道,同时增强CT提示颈内静脉可见充盈缺损考虑血栓形成(图4)。该处紧邻CPSF瘘管感染形成的脓肿。患儿无颈部外伤、颈静脉穿刺等机械损伤,凝血功能、狼疮全套,以及进一步检查抗心磷脂抗体、蛋白C活性均正常,不伴有血液高凝状态及易栓症表现,分析出血及颈内静脉血栓形成存在几种可能:(1)局部感染刺激颈内静脉,但静脉壁并未破裂,仅静脉内皮损伤形成局部血栓,出血原因为CPSF瘘管感染浸润局部小血管破裂所致。但患儿瞬时出血量达320 mL且呈深红色,无血凝块,而此前并无颈部肿大等血液蓄积的表现,局部小血管破裂出血难以解释。(2)感染引起颈内静脉壁破裂出血,出血进入脓腔内,再沿着瘘管经内瘘口涌入口腔,甚至肺部、胃部形成假性咯血、假性呕血,后期随着感染控制局部形成血栓堵住破裂口止血,仅表现为少量渗血。颈内静脉血管壁是否连续是判断其出血原因的关键。为求进一步证实,完善颈部MRI,发现颈内静脉内充盈缺损考虑血栓形成,颈静脉管壁不连续(图5),存在颈内静脉壁破裂可能。

图3 纤维支气管镜探查咽腔

图4 颈部增强CT结果
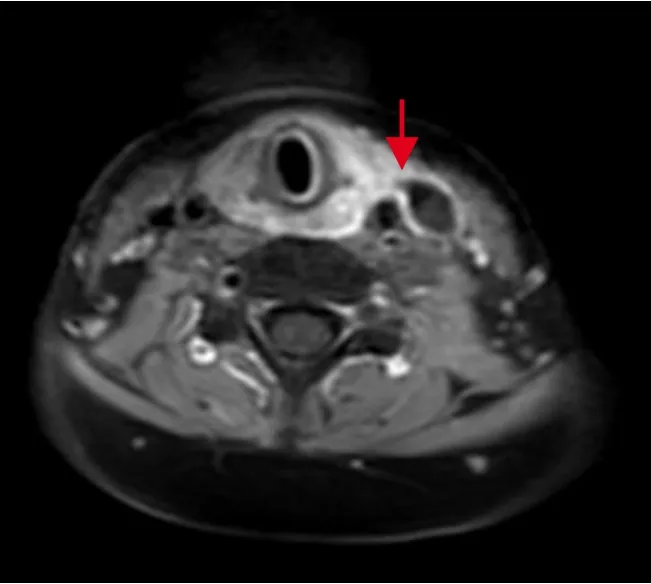
图5 颈部MRI结果
4 诊断及诊断依据
诊断:(1)CPSF管感染并大出血;(2)左颈部脓肿形成;(3)甲状腺左叶化脓性感染;(4)全身炎症反应综合征;(5)左颈内静脉壁损伤并血栓局部形成;(6)失血性休克;(7)重度贫血。
CPSF管感染并大出血诊断依据:(1)男性儿童,以感染症状起病,伴左侧颈部疼痛,病程中假性咯血,单次出血量>100 mL;(2)颈部影像学检查示甲状腺左叶呈不规则低密度灶伴特征性气泡影;(3)纤维支气管镜检查发现梨状窝内瘘口并渗血;(4)除外消化道、呼吸道出血。
5 临床经过
诊断明确后经耳鼻喉科会诊,于体温稳定5 d后选择经支撑喉镜下下咽探查术+低温等离子刀梨状窝瘘封闭术。术后患儿Hb未再下降,2周后复查纤维支气管镜,梨状窝处未见瘘口且局部无出血。
患儿左颈内静脉存在血栓,但存在血栓逐步增大,或脱落至肺动脉栓塞的风险,临床可选择溶栓或/和抗凝治疗。目前患儿无明显临床症状,且处于亚临床期,不需要溶栓治疗[5],常规抗凝治疗也有可能出现再次大出血,结合文献指南[5-6]与家长商议后选择密切监测凝血功能及颈围,未予以抗凝治疗。2周后复查颈部磁共振静脉血管成像,颈部脓肿消失,颈内静脉未见血栓,血管壁修复完整(图6)。复查炎症指标及甲状腺功能完全正常出院。随访1年半患儿未复发。

图6 颈部磁共振静脉血管成像结果
6 讨论
CPSF是一种源于咽囊结构残留的先天性畸形,内瘘口位于梨状窝并走行于同侧甲状腺背侧间,占所有鳃源性畸形的3%~10%,其中80%以上在学龄期儿童发病,男女比例相当。CPSF可分窦道型、瘘管型和囊肿型,其中窦道型最常见[4,7]。因与口腔相通,食物残渣及细菌易从内瘘口下沿,CPSF患儿常因瘘管感染而就医,初始临床表现为发热、反复发作的颈部肿痛或脓肿、急性化脓性甲状腺炎,容易误诊为颈淋巴结炎、甲状舌管囊肿、急性化脓性或亚急性甲状腺炎、甲状腺左叶肿瘤等[3,8]。CPSF有颈部炎性肿瘤之称,长期急慢性炎症刺激使颈部形成疤痕组织,影响患儿身心健康,需要引起儿科临床医生的重视[9]。本例患儿以发热、咳嗽、咯血并休克为主要表现,诊断CPSF感染并颈部脓肿形成致颈内静脉受损、大出血、休克,相关文献检索无CPSF出血报道,因此总结本例罕见病例的临床特点及诊治经过,有利于提高临床医生对本病的全面认识,指导早期诊断及治疗,以及并发症的防治。
90%CPSF发生在左颈,可能与胚胎早期双侧鳃弓发育不对称、C细胞迁移紊乱有关[4,7]。此外甲状腺由于其解剖特点不容易出现化脓性感染,如果儿童反复出现左侧颈部感染病变或化脓性甲状腺炎时,需高度怀疑CPSF[3,9-10]。应注意的是有些患儿首次发作局部症状可能不典型,本例患儿为初次发作,颈部疼痛程度不剧,体格检查并无肿块,皮温也不高,早期诊断困难。
CPSF传统的影像学检查方法为食管钡餐造影[11],可以观察窦道走行过程,但其重叠因素较多,很难分辨其与周围组织结构的关系。且急性感染期炎症和水肿可形成区域性闭合,从而阻止钡剂进入窦道,因此检查应在感染消退至少6周后进行,可能延误诊治时机。超声具有无创、简易、费用低等优势,但人为因素影响较大,并且对病灶成分的分辨率较低,对病灶位置、来源的判断较差,因此诊断具有局限性。CT及MRI对软组织位置、形态、密度、信号的表现更加清晰、具体,更有利于做出定位和定性诊断。CT及MRI影像中较典型的窦道和/或瘘管征象表现为梨状窝-甲状腺区域或颈前区皮肤异常密度影,其内往往可见含气腔[12]。加上内镜检查能直观地发现CPSF内瘘口[3,10],可以快速明确诊断。
本例患儿影像上符合CPSF,但诊治难点在于患儿局部症状不典型,以大出血为主要表现,故早期并未将出血与CPSF关联。实际上CPSF感染容易引起左侧甲状腺脓肿,而甲状腺血运丰富,感染时可能造成出血。另外甲状腺脓肿比邻颈内静脉,也可能造成血管损伤出血进一步形成血栓。另一方面,患儿出血量大,与大咯血一样存在误吸、窒息等风险,需注意防范。所以经口腔排出的大出血应尽早内镜检查明确出血部位及原因[13],除常见的呼吸道、消化道出血外,还应关注梨状窝等隐匿部位的出血。
CPSF发现时往往存在感染,早期有效控制感染是后续治疗的前提。CPSF感染往往是口腔菌群下沿至瘘管,初始治疗抗生素选择应考虑针对口腔菌群,同时积极完成血培养,文献报道常见革兰阳性菌包括草绿色链球菌、金黄色葡萄球菌、肺炎链球菌等;革兰阴性菌如肺炎克雷伯杆菌、流感嗜血杆菌、铜绿假单胞菌等,尚需注意厌氧菌感染[14]。相对于成人患者,儿童CPSF更多为革兰阳性菌感染[15]。本例患儿因外院已使用多种抗生素,故血培养阴性,改用万古霉素抗感染有效,来院时体温正常,炎症指标下降,颈部脓肿已缩小,未再切开排脓。
CPSF的治疗既往曾认为急性期抗感染治疗,切开排脓,炎症静止期颈部开放性手术切除病灶是根治的唯一手段[16]。但完整切除瘘管不仅难度较高,并发症也多,包括声带麻痹、颈部瘢痕畸形等。不恰当的外科处理使术后复发率达4.9%~39.0%。为避免开放性手术的创伤和并发症,国外学者开始探索安全、微创、美观的内镜术式。目前认为内镜下通过物理或化学方法使内瘘口及周围黏膜形成创面,形成粘连和瘢痕从而使得内瘘口闭合的术式是一线治疗手段[3,16-17]。甚至可以在急性感染期进行[3]。该患儿术前感染逐步控制,仍存在少量持续出血,采用内瘘口封闭可能形成局部血肿,但也可能由于瘘管内局部压力增加,形成压迫止血,同时封闭内瘘口减少口腔细菌进入而导致的反复感染机会,促进损伤部位愈合。经多学科联合会诊讨论,选用内镜下低温等离子射频消融封闭瘘口,预后良好。
此外,本例患儿病程中发现深静脉血栓形成,对并发症的处理,不能盲目溶栓、取栓,要系统全面地评估病情,监测凝血功能变化,尤其是面临出血、栓塞这种两难局面时,要谨慎处理,权衡利弊,充分与家长告知商议。在病情较为平稳的时期,密切监测、静待机体调节恢复可能是更稳妥的处理方案。

