哌拉西林-他唑巴坦致粒细胞减少的影响因素
赖晓琴,张素平,黄培瑜,洪 等,江艳英,陈文发
哌拉西林-他唑巴坦为广谱β内酰胺类-β内酰胺酶抑制剂复方制剂,临床常用于金黄色葡萄球菌、肠球菌、肠杆菌科细菌、铜绿假单胞菌、脆弱拟杆菌等常见革兰阳性、阴性菌及厌氧菌所致尿路感染、皮肤软组织感染及骨关节感染等。伴随着临床的广泛应用,其皮肤、胃肠道、血液学方面的不良反应报道日渐增多,血液学不良反应包括全血细胞减少[1]、中性粒细胞减少等[2-3]。中性粒细胞减少程度、持续时间与患者感染甚至死亡风险直接相关[4]。中性粒细胞减少伴发热是最主要的临床并发症,可进一步延长患者住院时间,加重患者及社会的经济负担。本文通过收集临床使用哌拉西林-他唑巴坦治疗骨相关感染的115例患者资料,采用统计学方法分析可能影响白细胞及中性粒细胞减少的相关危险因素,为临床及早采取相应的处置措施预防粒细胞减少及由粒细胞减少所致相关并发症的发生提供参考。
1 材料与方法
1.1 资料来源
2018年1月—2021年7月在福建医科大学附属第二医院和龙岩市第二医院骨科共三个病区接受哌拉西林-他唑巴坦抗感染治疗的骨相关感染成年患者。排除在治疗开始前已经出现粒细胞减少,合并使用免疫抑制剂、其他抗菌药物、非甾体类抗炎药及含巯基的血管紧张素转化酶抑制剂等其他可致粒细胞减少药物,已知与中性粒细胞减少有关的先天性异常的患者,患有人类免疫缺陷病毒感染的患者,血液系统恶性肿瘤患者及缺少治疗前、治疗中或治疗结束后任何一次血常规检测数据的患者。
1.2 数据采集
通过查看电子病历回顾性收集接受哌拉西林-他唑巴坦治疗骨相关感染患者的性别、年龄、体重,药物用法用量、疗程,治疗前血肌酐、谷丙氨酸转氨酶(ALT)、天冬氨酸转氨酶(AST),治疗前(1~3 d)、治疗中和治疗结束后血白细胞、中性粒细胞、嗜酸粒细胞情况。
1.3 定义
按照中华人民共和国卫生部(卫通[2012]23号)中华人民共和国卫生行业标准(WS/T 405-2012)血细胞分析参考区间,白细胞减少定义为绝对白细胞计数<3.5×109/L,中性粒细胞减少定义为绝对中性粒细胞计数<1.8×109/L[5]。
1.4 统计学方法
采用SPSS 25.0统计软件对数据进行分析,计数资料进行频数分析,计量资料大样本采用Kolmogorov-Smirnov法进行正态性检验,小样本采用Shapiro-Wilk法进行正态性检验,正态分布计量资料以均数±标准差表示,非正态分布计量资料以中位数(四分位数)[M(P25,P75)]表示,符合正态分布的计量资料两样本间的比较采用t检验,非正态分布计量资料两样本间的比较采用非参数的秩和检验(Mann-Whitney检验)。危险因素分析中将连续变量转换为分类变量,单因素分析确定的可能因素进一步纳入logistic 回归进行多因素分析。
2 结果
2.1 患者特征及实验室数据
根据入组标准共计115例次纳入研究,其中女性 44例(38.3 %),男性71例(61.7%);年龄18~93岁[(56.8±18.0)岁],按照WHO年龄划分新标准[6]:青年人(<45岁)30例(26.1 %),中位年龄36.5(29.0,42.0)岁;中年人(45~<60岁)43例( 37.4%),中位年龄54.0(50.0,57.0)岁;老年人(≥60岁)42例(36.5% ),平均年龄(76.2±8.8)岁。疗程2.0~35.0 d,中位数13.5 (8.0,18.0) d。哌拉西林-他唑巴坦平均日剂量:中位数13.5(9.0,13.5) g;累积使用剂量20.2~378.0 g,中位数148.5(94.5,202.5) g。白细胞及中性粒细胞减少组患者累积使用剂量及疗程均显著高于未发生白细胞及中性粒细胞减少组患者(P<0.05),两组患者年龄、性别、接受哌拉西林-他唑巴坦治疗前实验室检查数据、平均日剂量等差异均无统计学意义。见表1。

表1 患者特征及实验室数据Table 1 Patient characteristics and laboratory test results
2.2 粒细胞减少的发生
据粒细胞减少判定标准,115例次接受哌拉西林-他唑巴坦治疗的患者中,22例次(19.1%)出现白细胞及中性粒细胞减少,分布情况见表2。所有白细胞及中性粒细胞减少患者停药后两种细胞逐渐回升,其中5例因重度粒细胞减少(绝对中性粒细胞计数<0.5×109/L[4])而使用了升白细胞 药物。

表2 白细胞减少和中性粒细胞减少分布情况Table 2 Leucopenia and neutropenia distribution[n (%)]
2.3 粒细胞减少影响因素分析
按青年、中年和老年人的年龄划分标准转化为三分类变量,实验室指标ALT、AST、血肌酐根据是否高于正常值上限转换为二分类变量,疗程按人群平均疗程取整数即14 d为分界点转换为二分类变量(疗程<14 d、疗程≥14 d),累积剂量根据粒细胞减少人群平均累积剂量转化为二分类变量进行单因素分析[7],单因素分析确定的可能因素进一步纳入logistic 回归进行多因素分析。
2.3.1 单因素分析 单因素分析结果显示,不同年龄组、不同疗程、不同累积剂量(<232.4 g、≥232.4 g)对白细胞、中性粒细胞减少发生率差异存在统计学意义(P<0.05),性别、血肌酐、ALT、AST(未升高、升高)、平均日剂量各组间白细胞、中性粒细胞减少发生率差异无统计学意义(P>0.05)。见表3。
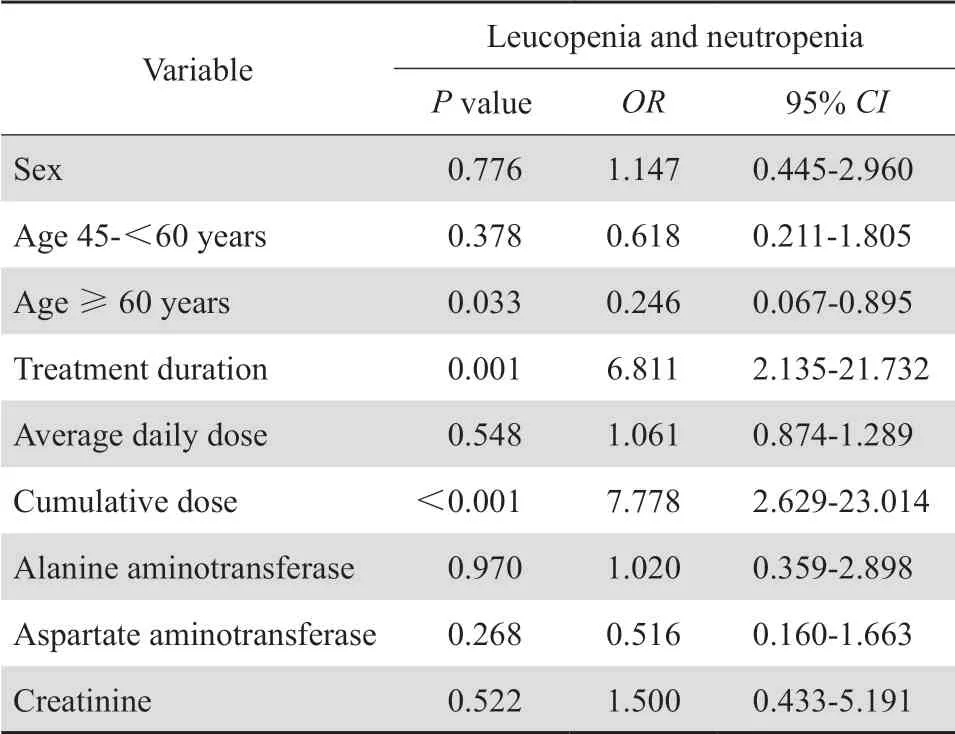
表3 白细胞减少和中性粒细胞减少单因素分析Table 3 Univariate analysis of the risk factors for leucopenia and neutropenia
2.3.2 多因素分析 以白细胞减少、中性粒细胞减少为因变量,以年龄、累积使用剂量、疗程为自变量并以协变量引入进行二元logistic回归分析。年龄与白细胞、中性粒细胞减少不存在显著相关性(P>0.05),累积使用剂量及疗程与白细胞减少的发生显著相关,疗程≥14 d患者白细胞、中性粒细胞减少的发生风险是疗程<14 d患者的4.621倍(P<0.05,OR=4.621);累积使用剂量为≥232.4 g患者的白细胞、中性粒细胞减少发生风险是累积使用剂量<232.4 g者的3.608倍 (P<0.05,OR=3.608),见图1。
3 讨论
相较于既往重点关注药物所有的不良反应研究或者单纯的个案报道[8-10],本研究回顾性调查了115例次接受哌拉西林-他唑巴坦治疗骨相关感染致粒细胞减少的情况,重点考察性别、年龄、累积使用剂量、平均日剂量、用药疗程、肝肾功能异常等对粒细胞减少的影响。19.1%的患者出现白细胞、中性粒细胞减少,用药疗程≥14 d及较高的累积使用剂量(≥232.4 g)患者其白细胞、中性粒细胞减少的发生率显著高于用药疗程<14 d及较低累积使用剂量(<232.4 g)的患者。
本研究粒细胞减少的发生率与Benli等[11]报道数据相仿,但与 Lemieux等[12]和Peralta等[13]的报道差异较大,这种差异主要与其将3级以上粒细胞减少(绝对中性粒细胞计数<1.0×109/L)[4]定义为粒细胞减少和仅将用药疗程>10 d的人群纳入研究有关。这将在一定程度上影响用药疗程对哌拉西林-他唑巴坦致粒细胞减少的评估。
本研究发现较长的用药疗程及较高的累积使用剂量与哌拉西林-他唑巴坦致白细胞、中性粒细胞减少的发生相关,这与Peralta等[13]研究一致。同样,Benli等[11]的研究亦发现总治疗时间与白细胞和中性粒细胞减少相关,并认为初始较高的嗜酸粒细胞是中性粒细胞减少的独立危险因素,本研究患者中由于初始较高的嗜酸粒细胞的病例较少,仅4例,致使本次粒细胞减少危险因素研究中未将其纳入考察因素。Fry等[1]研究并未发现全血细胞的减少与哌拉西林-他唑巴坦相关,可能是由于其纳入研究的患者用药疗程较短,平均疗程仅(5.3±3.3) d[1,14]。此外,本研究的单因素分析中发现年龄与白细胞和中性粒细胞减少相关,经多因素回归分析,未发现年龄与粒细胞减少相关。而在针对替卡西林-克拉维酸与哌拉西林-他唑巴坦的对比研究中发现哌拉西林-他唑巴坦致粒细胞减少的发生率高于替卡西林-克拉维酸,并且与年龄相关,研究观察到中性粒细胞减少病例均为年龄<13岁的患者[12]。这种差异可能是因为本次研究纳入的患者均为18岁以上的成人患者,而Lemieux等[12]研究的患者为18岁以下的未成年人。在一项主要联合使用同样可致白细胞减少的环丙沙星的研究中发现联合使用另一种抗菌药物是白细胞减少的独立危险因素[11,15],为了避免合并用药对研究的干扰,进一步提升研究结果的可信度,本次研究主要选择了辅助用药少、用药较为单一的骨相关感染患者并且将联合使用抗菌药物的病例排除在研究之外,未进行联合使用抗菌药物与粒细胞减少的相关性研究。
哌拉西林-他唑巴坦因其抗菌谱广被广泛应用于临床,其诱导的中性粒细胞减少被认为是由于髓系细胞的增殖阻滞所致[3,14],但这种不良反应通常是可逆的。本研究明确了长疗程用药(疗程≥14 d)及较高的累积使用剂量是哌拉西林-他唑巴坦诱导白细胞及中性粒细胞减少的危险因素,临床医师对接受长疗程或高累积剂量使用哌拉西林-他唑巴坦治疗的患者应注意重点监测患者血白细胞、中性粒细胞,根据监测结果及时停用、更换抗感染治疗方案,减轻粒细胞减少的程度及由此诱发的二次感染等并发症的发生,进而减少并发症带来的住院时间延长、增加患者负担。
肾功能异常易引起药物的蓄积,本次纳入调查的病例大多无法获得患者体重信息,无法计算其肌酐清除率,研究中仅简单评估了血肌酐(正常、升高)对粒细胞减少的影响。由于本次调查患者中肾功能异常病例数较少,且基本为轻度血肌酐升高患者,致使本次研究无法更准确地评估肾功能异常对哌拉西林-他唑巴坦相关粒细胞减少的影响。对于肾功能中重度异常是否与哌拉西林-他唑巴坦诱导粒细胞减少相关还需进一步深入研究。

