电子自旋密度可视化在环境化学涉自由基反应教学中的应用
洪冉,徐绘,张庆云,陈张浩,吕占傲,张宗瑞,宋珍霞,杨晓凡,唐海 ,徐大勇 ,谷成 ,3,*
1安徽工程大学化学与环境工程学院,安徽 芜湖 241000
2南京大学环境学院,南京 210023
3南京大学污染控制与资源化研究国家重点实验室,南京 210023
1 引言
环境化学是基于四大化学的专业课程,是基础化学知识的应用,也是延伸和拓展。因此要求授课教师具有扎实的化学基础,能融会贯通课程要点和难点,降低“学习能垒”,激发学习兴趣。自由基反应是环境化学中的重要内容,包括光照条件下的大气圈层和水圈层中发生的自由基反应(均相或非均相)以及高级氧化技术中所涉及的自由基过程,这些反应中包括了羟基自由基、硫酸根自由基、卤素自由基以及有机自由基等自由基物种,比较这些物种的异同是重要的学习内容。一方面有利于理解地球生态系统中最重要的能量来源——太阳辐射对环境圈层产生影响;一方面有利于建立对污染物环境归趋(迁移转化)的科学认识。
“自由基”部分往往也是教学难点,主要有如下几个原因。首先,环境化学课程往往开设在中高年级,距“有机无机分析物理化学”等基础化学课程的学习已比较“遥远”,在高强度学习氛围下,学生的基础化学概念已不够清晰。以本授课班级为例(111人),只有不到30%的同学能够在教师提问后迅速的回答出水分子(环境化学中最重要的环境介质分子)的氧原子杂化类型,对后续水分子间相互作用——氢键以及氢键笼的学习不利;只有15人回答出氧气分子的基态是三线态但无法给出解释;部分同学无法建立激发能和紫外吸收光谱的相关性;部分同学对“孤对电子”和“未成对电子”混淆不清。其次,环境化学教材中对自由基反应过程的描述通常使用的是Lewis结构式,使用居中黑点(如“·”)来表示未成对电子(式1),这种较为抽象的表达造成了一定程度理解上的困难,也缺乏和分子轨道等现代化学理论的结合。

计算化学的各种理论方法和实践手段日趋完备,特别是密度泛函概念的提出和应用直接促进了分子性质的理论计算方法的大爆发。通过对计算得到的波函数进行处理,能得到譬如“电子密度”(波函数的模方)、偶极矩、静电势以及自旋密度等分子性质,这些性质是实验数据的重要支持和有力解释,可用于验证或预测。电子自旋分为alpha和beta两种,一般作图为向上和向下的箭头(↑↓),通常情况下基态分子的alpha和beta自旋的电子数是相等的,且两两耦合(闭壳层)。自由基是具有未成对电子的物理实体(教学时仅考虑单自由基),因此必然存在具有alpha或beta自旋态的单个电子。为了定量讨论分子结构中自旋电子分布的特性,杨伟涛等人[1]将电子自旋密度定义为Q(r)= ρα(r)- ρβ(r)。通过该方程,量化计算可以定量考查电子自旋密度等值面的空间分布以及自由基反应前后电子自旋密度的变化或迁移情况,通过图形化方法对这些自由基的反应进行直观描述,应用到环境化学的课程教学中,显得生动有趣,利于理解学习。
本研究通过比较三种常见自由基分子(羟基自由基、氯自由基、甲基自由基)及其共轭闭壳层分子的自旋密度,得到单电子分布情况,通过图形化,建立了电子结构的三维图像,将自由基分子特有的未成对电子的空间分布进行了直观展示,取得了良好的教学效果。自由基反应并非环境化学所特有,高分子化学、有(无)机化学、合成化学等各门课程都广泛涉及该类反应,因此本教学方法具有推广价值。
2 授课对象、课程概况与图形化方法
2.1 授课对象与课程概况
环境科学与工程专业本科三年级学生已修的前置课程包括“有机无机分析物化”等化学课程,未修“结构化学”和“计算化学”,总人数111人。环境化学课程总计32学时,时间紧任务重。需要以教材为基础,由授课教师小组将主要授课内容凝练为八个方向,平均每方向使用4个课时进行教学,根据具体内容进行弹性调整,但最多不超过6课时/方向。八个方向分别是:1) 天然水体与土壤概述;2) 溶解沉淀与氧化还原;3) 大气扩散模型与气相反应;4) 均相与非均相光化学反应:光子、分子与界面的相互作用;5) 污染物形态与生态系统;6) 环境污染物反应机理;7) 新型污染物起源与控制;8) 环境化学与人体健康。这种做法兼顾了具体的学情和教情,在学时极度紧张的条件下,尽可能多地进行知识传递。电子自旋密度可视化的教学方法主要在第6个方向中使用。
2.2 计算与图形化方法
基态分子和自由基分子使用高斯16计算[2],波函数分析和可视化分别使用Multiwfn[3]和ChimeraX进行。鉴于教学便利性和低计算成本的要求,在M06-2X-GD3/Def2-TZVPP水平下对羟基自由、氯自由基、甲基自由基以及它们的共轭闭壳层分子进行结构优化,对羟基自由基和苯环的提氢反应进行过渡态计算。本研究主要以环境化学中最常见的羟基自由基为例,考查其电子自旋密度在提氢反应中的变化。结合分子轨道理论的轨道分析方法,剖析环境自由基过程的本质,以提高此类教学的直观性、趣味性和深刻性。
3 实施与效果
3.1 分子轨道理论与羟基自由基教学的结合
分子轨道(MO,molecular orbital)是原子轨道的线性组合,组合过程中遵守轨道数守恒原则,即组合前后轨道数不变。作为一种双原子分子,MO理论是分析羟基自由基(·OH)电子结构的理想工具。明确氧和氢的原子轨道是运用MO理论分析·OH自由基电子结构的前提。氢原子是最简单的单电子原子,基态状况下核外电子位于s壳层,写作1s1;氧原子核外总计8个电子,结构为1s22s22p4。p壳层具有3个轨道,记作pz、px、py,其中一个被一对自旋耦合电子占据,另外两个分别被2个自旋平行电子占据(洪特规则)。由于氢原子的s壳层和氧的p壳层能量接近,所以优先组成分子轨道,详细情况见图1。·OH自由基分子轨道中的非键轨道由氧原子p轨道的两个分轨道组成(图1),显然·OH自由基具有典型的未成对电子结构。
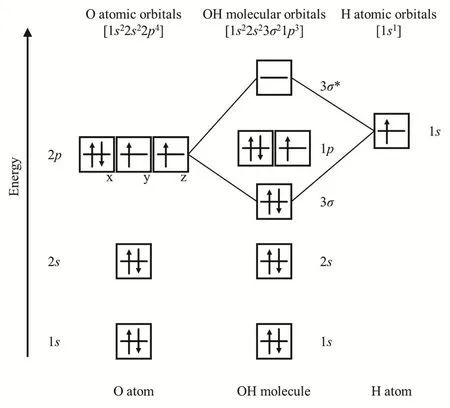
图1 氧(氢)原子轨道和羟基自由基分子轨道
为了对比氢的s轨道和氧的p轨道能量,使用量化计算得到轨道能量。计算结果表明氢的s轨道能量为−0.3750 a.u.,氧的p轨道能量为−0.5470 a.u.,与其他轨道相比,两者能量更为接近,满足轨道组合的前提要求。为了帮助学生理解·OH自由基的多重度,可以适当介绍σ态的单线态氧(1Σg+,电子均自旋耦合,但其中两个电子分布在两个独立π轨道上,实为双自由基分子)作为反例,加深学生认识,但不必深入展开(为结构化学或量子化学的内容)。MO理论可以对·OH自由基的电子结构进行非常详尽的解释,但对于多原子分子,手动推导分子轨道比较困难。为了直观体现半充满的轨道的反应活性,我们对自由基分子的自旋密度进行了可视化处理,以一个过渡态反应为例进行了深入探讨,见3.2小节。
3.2 自旋密度可视化在苯环-羟基自由基反应过渡态教学中的应用
苯分子是环境化学里较为常见的有机分子之一,常用作气相有机污染物的迁移转化的模式分子,且苯分子具有极高的对称性(D6h),便于对其进行量化计算的研究。因此,以·OH自由基和苯的提氢反应为例,考查自旋密度在反应过程中的变化情况,并将之图形化。首先为学生推演气相提氢反应的过程:·OH分子和苯分子逐渐靠近(由静电力主导)→苯环上某个H原子受到·OH作用(波函数发生相互作用)→·OH夺取苯环一个H原子形成水和苯自由基。
由MO理论分析可知(图1 hydroxyl radical molecular orbitals),·OH在氧原子上有一个未成对电子,具有很高的活性。由自旋密度的可视化可见,·OH的单电子主要分布在O原子上(图2a);提氢反应过渡态是C―H键断裂和H―O键形成的中间态,由图2b可见TS结构中的电子自旋密度同时存在于·OH和苯分子上,表明正处于旧键断裂和新键形成的过程中;产物的自旋密度等值面表明水分子是一个闭壳层分子,而新形成的苯自由基成为新的高活性反应对象。此时可对后续可能发生的·OH加成反应做进一步讨论。
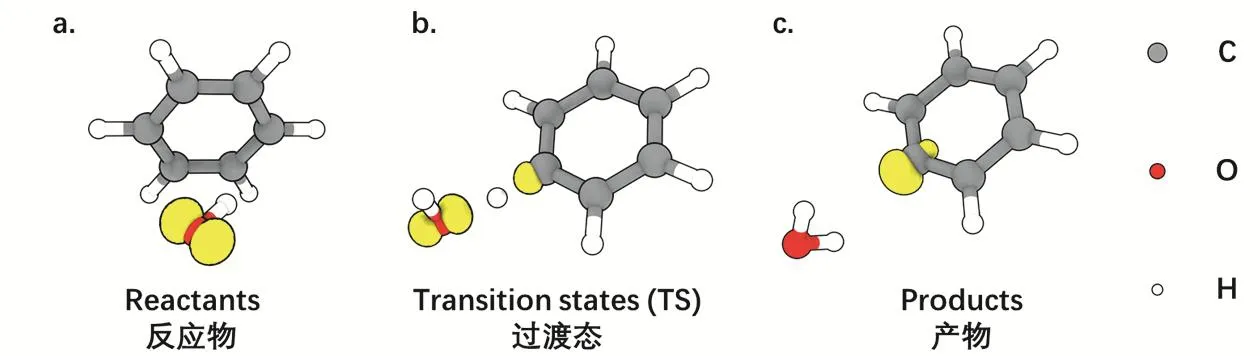
图2 羟基自由基-苯分子提氢反应中的自旋密度变化
对反应物-过渡态-产物的能量进行比较可以从能量的角度更深入的理解反应。如图3所示,提氢反应能垒较低(实际应当使用自由能垒,电子能垒用于教学足以定性正确),反应速率较大,易于发生反应,符合·OH反应特性。但此内容和自旋密度无关,不在本文讨论。
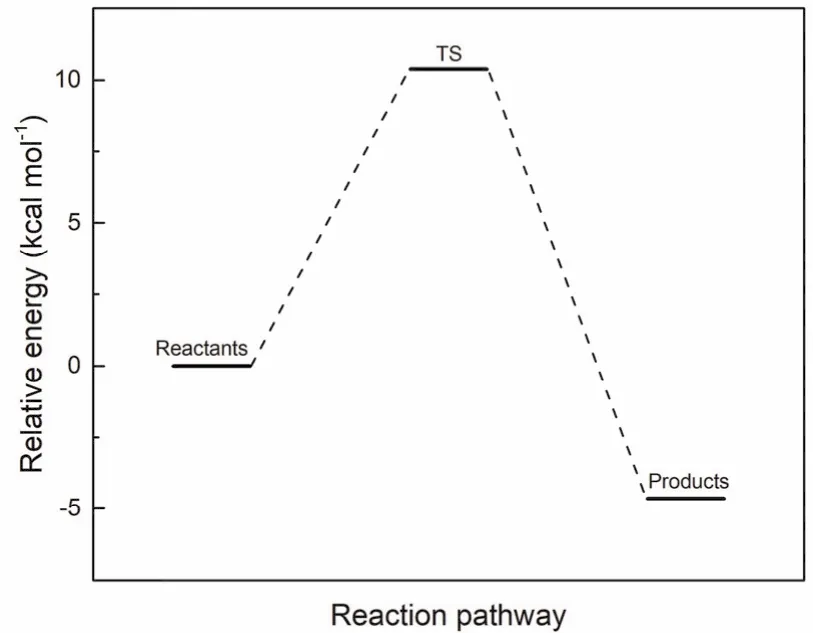
图3 密度泛函计算得到的提氢反应能垒图
3.3 自旋密度可视化方法的普适性及其与静电势耦合使用
自旋密度可视化方法适用范围很广,所有牵涉未成对电子的反应过程都能使用这种方法进行可视化的直观研究。例如,环境化学关注的其他类型自由基:卤素自由基、简单的有机自由基等活性物种都可以用自旋密度进行研究。为了比较开闭壳层分子的自旋密度差异,这里将这些自由基对应的闭壳层的共轭物种一并列出(表1),方便学习比对。

表1 环境化学中常见自由基与共轭物种分子结构
由图4可见,在本文的几个例子中电子自旋密度等值面代表着自由基分子单电子分布情况,与分子轨道方法得到的结论一致,即所有闭壳层分子的自旋密度均为零。例如,羟基自由基的单电子(自旋密度等值面)主要集中在氧原子上,分子轨道理论也指出该单电子位于氧原子的P壳层的pi轨道上(图1);氯原子(氯自由基)的3P壳层上具有一个单电子,在图4中也得到了很好的体现,存在一个典型的pi轨道节面,闭壳层的氯离子的自旋密度为零;甲基自由基及其对应的甲烷分子不仅有自旋布居差异,其结构也发生了显著变化,失去一个H原子后本来是四面体结构的甲烷分子变成了平面结构,这种现象是一个非常好的原子杂化案例,适合在学习价键理论时使用,此处不展开。甲基自由基中,C原子2P层有2个电子,因此存在2个半空1个全空轨道,接受3个H原子的电子后(回避杂化理论),必然会形成一个新的半空轨道,对应着C原子上自旋密度分布(图4甲基自由基)。
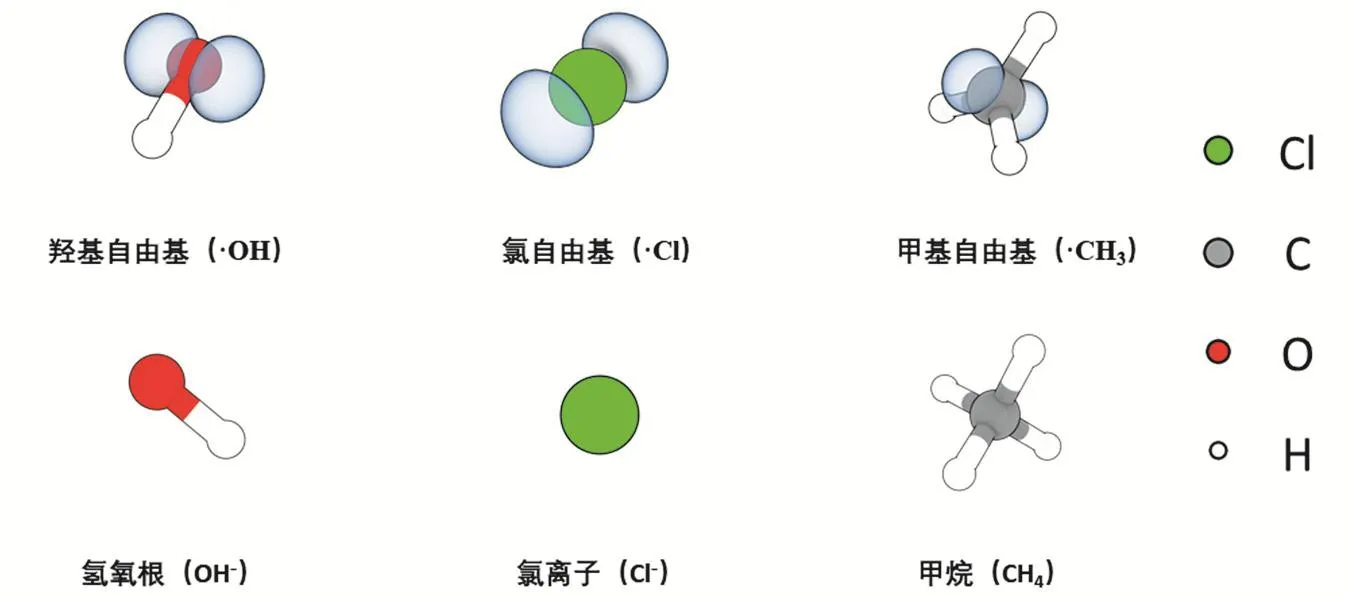
图4 自旋密度在三种自由基分子中的分布情况
由上可见,自旋密度与“活性单电子”或“半空轨道”存在良好的对应关系,对于教科书中各种电子弱相关体系而言,是很好的反应活性位点的指示参数,值得推广使用到其他化学课程中,例如卡宾自由基不同自旋态分辨、卤化氢烯烃光照加成反应过程研究等。
为了更深入地理解分子反应特性,对范德华表面(电子密度为0.001 a.u.的等值面[4])的静电势(Electrostatic potential,ESP)进行研究,并与自旋密度建立关系。静电势体现了分子表面的电性特点,对反应朝向、反应位点发挥着一定程度的影响,是最容易被学生接受的分子性质之一。通过ESP的学习可以直观理解“同性相斥,异性相吸”的分子间作用规律,将ESP和电子密度建立相关性是科学研究中的常见方法,但在教学中并不常见。
氢氧根带一个负电荷,具有较强的弥散特征,表现为整个范德华表面电势为负(图5氢氧根),其最大最小值均为负值。失去一个电子形成羟基自由基后,分子表面电荷显著增加,极大值有1处(59.59 kcal·mol−1),最小值有2处(−26.92 kcal·mol−1) (图5羟基自由基)。其极小值点和电子自旋密度分布恰好对应了,由图4可知,羟基自由基的氧原子上存在两个相对独立的自旋密度区域,结构特征与ESP很接近,ESP不仅仅受自旋电子分布影响,也受到H原子正电荷影响,整体表现出朝氧原子方向的轴端偏移的现象;氯离子的电势表现出显著的各向同性,没有结构特征(图5氯离子),氯自由基的电子自旋密度的分布受其pi轨道影响,形成了很明显的结构特征(图4氯自由基),其ESP形成了“两极高赤道低”的特征,恰好与自旋密度分布特点是互补的,这是因为极高的对称性和另外两个全满pi轨道共同导致。甲基自由基的自旋密度和ESP保持了很好的一致性,其ESP最小值点与自旋密度分布吻合。通过ESP和自旋密度的分析可知,这两者既在空间分布上保持一定的关联,也在对称性等其他因素的作用下存在互补关系。分子反应一般是以“扩散-静电作用-波函数作用”这样的空间顺序进行,ESP在静电作用和分子朝向部分发挥重要作用,自旋密度在波函数作用发挥重要作用,帮助学生建立两者之间的关系,能极大加深他们对化学反应过程的理解,以及对污染物迁移转化的理解。
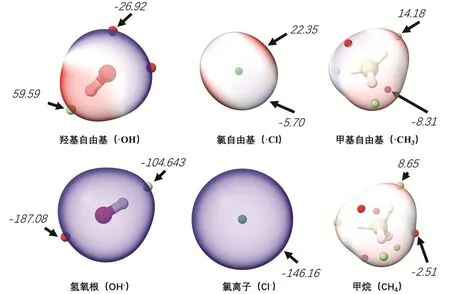
图5 三种自由基及其共轭闭壳层分子的静电势
4 结语
通过与分子轨道等现代化学理论的结合,赋予了环境自由基反应更丰富的内涵并增加了更多可供研究的“手柄”,能从各个方面对反应过程进行解读、研究乃至操纵。有利于摆脱“乏味的点线式”和“枯燥的讲解”,有利于提高“抬头率”,激发学生的主动学习热情。本研究的主要结论如下:
1) 通过图形化量化计算,将化学反应过程中的重要物种运用三维图形展示,有利于知识的传递与接受。
2) 电子自旋密度能够很好地体现自由基分子上的未成对电子分布情况,其分布结构对自由基分子的静电势分布存有一定影响。同时对两者进行考查能更全面地研究自由基分子的电子结构与反应特点,从而能够更加深入地对环境过程或环境工程中的自由基反应进行解释。
3) 在环境化学等“应用化学”专业课程的教学过程中,根据具体的学情,有目的性地回顾基础化学知识点,主动跳出专业舒适圈,能更好地激发学生的探索欲和挑战心。
致谢:感谢安徽工程大学化学与环境工程学院计算化学中心提供的硬件支持。

