数字化实验对“雷雨发庄稼”原理的深度探究
徐军 杨义洪


摘要:“雷雨发庄稼”的原理较为复杂,借助数字化实验,通过宏观辨析和微观探究,可以实现对原理的深度探究,激发学生的学习兴趣,落实核心素养。
关键词:雷雨发庄稼;注射器;传感器
文章编号:1008-0546(2022)06x-0078-03 中图分类号:G632.41 文献标识码: B
doi:10.3969/j.issn.1008-0546.2022.06x.020
2020年10月21日,江苏省优秀课大赛在江苏省靖江中学举行,B组的课题是“氮及其化合物”,笔者作为选手的指导老师,有幸学习了B组的9节课。上课内容是“氮及其化合物”新授课的第一课时。无论是苏教版还是人教版,内容都涉及氮的固定、氮氧化物的相互转化。以“雷雨发庄稼”这一情境为主线,可以把本节课的知识重难点落实到位。如何通过实验,探究“雷雨发庄稼”的原理,成为了该节课的亮点,各位选手在这方面下足了功夫,对笔者的感触也较深。
一、教材内容及实验的改进
使用2020苏教版教材的地区,上课的内容是《必修二》专题7。教材叙述的脉络为:通过“雷雨发庄稼”事例,介绍氮气在放电条件下与氧气发生反应,给出了闪电时生成氮氧化物的图片,“雷雨发庄稼”所关联的3个主要化学反应方程式。这3个反应是氮氧化物的产生及转化的重要反应,是课堂教学的重点内容,但课本上没有给出相关的实验资料。
使用2020人教版教材的地区,上课的内容是《必修二》第五章第二节“氮及其化合物”。教材叙述的脉络为:在高温和放电条件下,N2和O2化合生成NO,但没有交代“雷雨发庄稼”实例。在“一氧化氮和二氧化氮”内容中,设计实验如下:在一支50 mL的注射器里注入20 mL 的NO,然后吸入5 mL水,用乳胶管和弹簧夹封住管口,振荡注射器,观察现象,打开弹簧夹,快速吸入10mL空气后,夹上弹簧夹,观察现象。振荡注射器,再观察现象(装置如图1)。设计该实验的目的是探究NO和 NO2的相互转化。实验中巧妙使用注射器,方便灵活,微型环保,可以演示也可以分组实验,也可以对二氧化氮与水后继反应进行探究:只要把充分振荡后的溶液注入烧杯,滴加紫色石蕊溶液或测溶液的pH,就可以说明有硝酸生成。与2004旧版教材相比,这里可以说是实验的创新,有几位选手就用了该装置进行分组实验,效果较好。但由于针管的体积限制,加之吸入的是空气,因而产生的NO2量小、浓度小,实验现象不明显。
许多选手在人教版实验基础上,运用二通阀和三通阀、小储气瓶、针筒搭配(如图2、图3)改进了实验装置。用图3装置,针筒或小瓶中分别储存 NO 和纯的 O2,通过控制活塞,简便快速地实现NO、O2的混合;用小储气瓶收集气体,气体的用量增加了,这样操作更简便、可控,產生 NO2量多、浓度大,实验现象明显。图4中针筒数目增多,通过控制活塞,针筒可直接相通,可以进行多组实验,不但方便快捷,同时增加实验的安全性,可以说是对新教材实验的进一步创新。
二、问题的提出
九位选手通过放电技术进行了N2和O2化合生成 NO 的演示。两极电针高压下放电,装置中的气体颜色加深,进而说明N2和 O2在放电条件下先生成 NO,然后 NO 和 O2化合生成 NO2。有一位选手为了使现象更明显,在实验结束时在PPT上对实验过程进行了如图5的细化。但无论怎么处理,都无法说清下面几个问题:空气中成份复杂,在放电条件下就一定生成氮氧化物?实验中一定有 NO 和 NO2的转化过程(实验过程中红棕色颜色变深也可能是NO2浓度的变化引起的)?在探究NO2与水反应生成硝酸和NO时,如果实验仅仅是测溶液中酸度的变化来证明NO2气体与水反应生成的酸性物质就是硝酸,显然证据是不充分的。
三、问题的解决
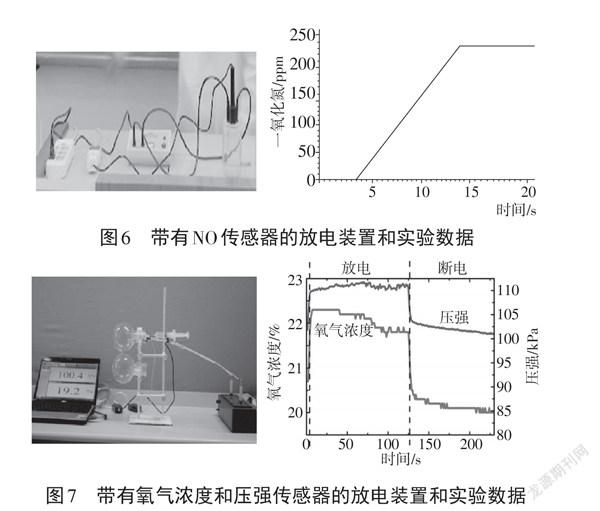
1.通过 NO传感器直接突破对放电过程中生成 NO 的理解。
通过图6装置测定玻璃容器中放电过程中NO 的浓度逐渐升高,说明了 N2和 O2在放电的条件下生成 NO,片刻后容器中颜色逐渐变成红棕色,说明了NO 又被O2氧化成NO2。现象明显直观,容易理解。
2.通过氧气浓度和压强传感器探究放电过程中反应原理
图7数据显示,放电过程和停止放电后装置中O2浓度一直减小,可以说明放电前后 O2都参加了反应,但这仍不足以说明 N2和 O2在放电下生成 NO 还是NO2。但结合压强分析就能说明问题了,放电条件下发生N2+O22NO,方程式的系数两边相等,如果温度相同,反应过程中压强不变。事实上放电过程中,整个体系温度上升不大,压强略有增加,原理和实验事实一致。放电结束后,O2浓度、压强进一步减小,气体的颜色逐渐变成红棕色,充分说明了放电后发生2NO + O22NO2,如果整个过程只发生 N2+2O22NO2,则体系的压强会一直减小。
[反思]上面的解释忽视了一个实验事实,开始放电时,压强数值瞬间增大,容器内压强增大,说明容器内瞬间微粒数目增大。经查阅相关资料可知,在放电过程中,可能发生193个基元反应。主要的反应如下: O2→O+O、N2+O→NO+N、M+NO→M+N+O ,M表示可能存在的碰撞粒子,如 N、O、H、OH、N+、N2+、O+、 O2+、O4+、NO+、H2O+、O-等。由于放电瞬间立即产生大量粒子,且粒子数目保持相对稳定,导致压强瞬间增大。另外,根据实验测得,放电过程中反应体系温度升高约为3℃。压强在瞬间增大后,因为温度的升高,压强数值继续增大,压强曲线呈现上升趋势[1]。
另一个问题是:开始放电,氧气数值瞬间增大。通过化学反应方程式分析,O2与N2可发生反应转化为 NO或NO2,放电时,O2浓度应该降低,然而实际测得数值增大。这是氧气传感器数据采集的特殊原理导致数值“不降反升”。氧气传感器的原理是使用原电池的原理,测量了氧化剂得电子的过程。根据化学反应的知识,氧气在反应中首先转化为氧原子,然后得到电子转化为-2价的氧元素。尽管O2与N2发生反应消耗一部分氧气,由于高压放电条件下,氧气更容易转化为活性氧原子,使得发生原电池反应的氧原子瞬间增加,所以实际测得数值是增大的[1]。
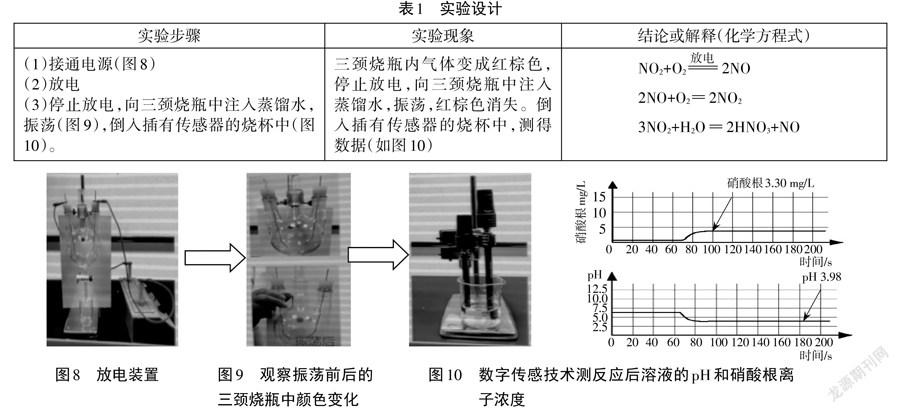
3.通过 NO-3、pH传感器数值变化突破对NO2与水反应的理解
对于NO2与水反应的原理认证,直接测定反应后溶液pH,无法充分说明生成产物中的酸一定是硝酸,但用数字化实验进行探究,就能把原理认证清楚。其中有一位选手进行了如下实验:
[实验目的]探究“雷雨发庄稼”的原理
[儀器用品]电子感应圈、带阀三颈烧瓶、50 mL针筒、硝酸根离子传感器、pH传感器、蒸馏水。
[实验设计]见表1
[反思]如果从教材中给出的反应原理理解整个实验过程,三颈烧瓶内最终气体应为NO2,注入蒸馏水振荡,发生3NO2+H2O 2HNO3+NO,得到HNO3溶液, HNO3为强酸,完全电离,溶液中 NO-3、H+浓度为定值,利用传感器测得的NO3-浓度、pH都为常数,不可能有变化的曲线。
与实验数据不相符。查阅资料,发现氮氧化物与水的反应较为复杂,可能发生反应如下[2]:
首先 NO2实为 NO2与 N2O4的混合物,溶于水时发生反应:3N2O4+2H2O 4HNO3+2NO;其次,NO2和H2O 反应生成HNO3(3NO2+H2O 2HNO3+NO);2NO2+H2O HNO2+HNO3;还有N2O4+H2O HNO2+HNO3;NO2+NO+H2O2HNO2。氮氧化物与水的反应过程中,除了生成HNO3外,还生成HNO2。无机化学教材[3]认为“亚硝酸是一种比醋酸略强的弱酸(Ka=4.6×10-4,291K),但很不稳定,仅存在于冷的稀溶液中,室温下放置时,逐渐发生歧化反应而分解(3HNO2HNO3+2NO + H2O),故立即测量NO2与H2O反应后溶液中的 NO-3、H+浓度,存在 HNO2分解过程,NO-3、H+浓度有一个变化的趋势。笔者认为,这里不适宜用数字化实验,因为如果把实验数据分析清楚,就超出了中学化学教学要求,还是直接用pH试纸测量酸碱性,作一个简单的描述为好。
四、结语
数字化传感器可以把微观反应的变化显性化、数字化、定量化。化学课堂上适度引入数字技术,发挥其优势,可以很好地弥补传统实验及仪器教学的不足。但数字化实验给人以虚拟的感觉,不利于训练学生的操作能力,难以培养学生的动手、动脑能力。笔者无法知道上述两位选手使用数字化实验时,是否考虑了图像数据中的异常。建议在教学中谨慎使用数字化实验,用常规的方法不好解决、常用的实验器材不能说明原理的时候才考虑使用。
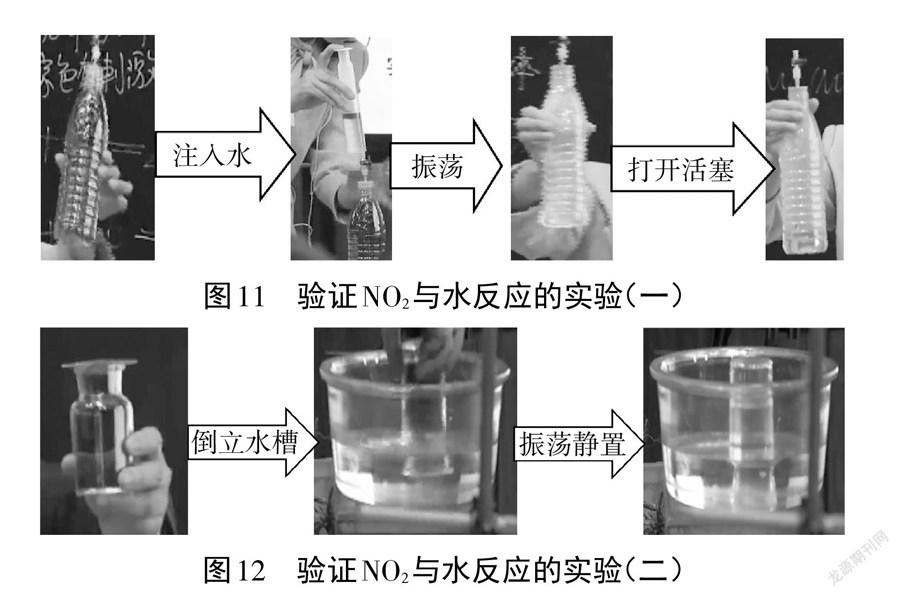
但数字化实验有机融合于课堂,能帮助学生构建从化学的视角认识事物、解决问题的思想、方法和观点。微型化实验有它独特的优势,但我们要知道同一个反应在不同装置中进行有不一样的精彩,例如:验证3NO2+H2O 2HNO3+NO,用带有活塞橡皮塞的矿泉水瓶进行实验,操作更简单,现象更明显。往收集满NO2的矿泉水瓶中注入水振荡,瓶体变瘪,瓶中气体颜色变浅,打开活塞,瓶体恢复,瓶中气体颜色变深(图11);也可直接用集气瓶做上述实验,同样观察到上述现象,水槽中集气瓶内液面上升(图12)。因此未来的实验必将是实验方法多样并举的有机融合。
(说明:本文的图片和数据主要来自教学现场。)
参考文献
[1]王保强,刘方云,李增坤.模拟雷雨条件下氮气和氧气反应的数字化实验探究[J].化学教育,2019(5):69-70.
[2]王祖浩.普通高中教科书(化学必修第二册)[M].南京:江苏凤凰教育出版社,2019.
[3]北京师范大学,华中师范大学,南京师范大学无机化学教研室.无机化学(下册)[M].北京:高等教育出版社,2004.

