含脂质体阿霉素方案治疗复发难治性多发性骨髓瘤伴继发髓外病变患者的临床研究
申曼 李新 张佳佳 汤然 詹晓凯 范斯斌 赵凤仪 黄仲夏
多发性骨髓瘤(multiple myeloma,MM)是一种浆细胞异常克隆的血液系统恶性肿瘤,其特征是单克隆浆细胞无限增殖、广泛浸润骨髓。大部分患者瘤细胞局限在骨髓内,但有少部分患者在疾病初治或复发/进展中出现髓外病变(extramedullary disease,EMD),EMD 根据发生部位分3种类型:1)骨髓瘤侵及邻近骨皮质并通过局部生长形成软组织包块;2)不与骨相连的软组织肿块或内脏肿块,通过血行转移至骨髓远处器官或组织,表现为单一或多发的结节或肿块;3)骨髓瘤细胞弥漫浸润器官而无局灶性病变,如胸水等。目前,将第 1 种类型定义为骨相关的 EMD(EMDbone related,EMD-B),第2种和第3种类型称为非骨旁 EMD(EMD-extraosseous,EMD-E)。根据出现时间分为两类:1)原发髓外病变(primary EMD,pEMD),在MM发病同时出现髓外病变;2)继发髓外病变(secondary EMD,sEMD),在MM复发或进展的疾病终末阶段[1]。多项研究结果显示,sEMD的发生率为7.5%~20%,对化疗不敏感,预后不良,考虑与肿瘤细胞的耐药性有关[2-4]。即使在新药时代,国际国内对sEMD尚无统一指南,仅部分共识可供借鉴[3,5-6]。本研究回顾性分析应用脂质体阿霉素(liposomal doxorubicin,LPD)为基础方案治疗40例复发/难治多发性骨髓瘤伴sEMD患者,记录sEMD的临床表现,并评价LPD的疗效及安全性,现报道如下。
1 材料与方法
1.1 临床资料
回顾性分析2015年1月至2020年1月北京朝阳医院西院收治的复发/难治性多发性骨髓瘤(relapsed/refractory MM,RRMM)患者,对sEMD并接受LPD患者的临床特点进行汇总。MM的确定诊断及复发/难治的评判分别参照国际骨髓瘤工作组(IMWG)制定的 MM 诊断及疗效评价标准[7-8],EMD由病理和(或)影像证实,根据是否累及骨骼而分为EMD-B与EMD-E两组,若两者同时出现则定义为EMD-E[1]。排除标准: 1)初诊时伴EMD患者;2)合并淀粉样变性或浆细胞白血病患者。本研究获北京朝阳医院医学伦理委员会批准。
1.2 方法
1.2.1 治疗方案与分组 含脂质体阿霉素方案包括:1)PDD方案:硼替佐米1.3 mg/(m2×d)d1、d4、d8、d11+脂质体阿霉素 40~60 mg d4+地塞米松20 mg d1、d4、d 8、d 11;3~4周1个疗程;2)CDD方案:环磷酰胺 0.4 g/(m2×d)d1~4+脂质体阿霉素40~60 mg d4+地塞米松20 mg d1~4;4周1个疗程;3)RCDD方案:来那度胺25 mg qod d1~21+环磷酰胺0.4 g/(m2×d)d1~4+脂质体阿霉素 40~60 mg d4+地塞米松20 mg d1~4;4周1个疗程;4)DVD方案:脂质体阿霉素 40~60 mg d1+长春地辛4 mg d1+地塞米松20 mg d1~4;4周1个疗程。
1.2.2 疗效评估 每2个疗程复查血常规,血清肌酐、血钙、血、尿M蛋白鉴定,全身低剂量CT,结合髓内指标(骨髓浆细胞及M蛋白鉴定)与髓外病灶进行综合评价,疗效判断参照IMWG评价标准[8]。
1.2.3 随访 自患者继发EMD诊断之日起开始计算随访时间,随访截至2021年6月1日,中位随访时间为26(14~62)个月。记录出现sEMD后总体生存时间(overall survival,OS):出现sEMD至死亡(任何原因)或随访终点的时间。根据下述特点进行分组比较:根据确诊MM至sEMD出现的间隔期是否达到6个月分为<6个月与≥6个月两组;根据发现sEMD时机分为有症状与无症状复查两组;根据sEMD数目分为单发与多发(同时出现≥2个部位)两组;根据EMD部位分为EMD-B与EMD-E两组。记录LPD无进展生存时间(LPD-PFS):应用LPD至疾病进展或随访终点的时间;根据LPD应用疗程分为<6个疗程与≥6个疗程两组进行比较。
1.2.4 不良反应观察 参照国际肿瘤组织毒副作用统一命名法的标准(NCI CTCAE 3.0)判断不良反应。
1.3 统计学分析
采用SPSS 24.0软件进行统计学分析。计量资料用中位数(范围)表示;计数资料以相对数表示。应用Kaplan-Meier法绘制生存曲线,采用Log-rank进行组间生存比较,对PFS分组比较时选用界标分析,界标值为6个月。应用 Cox 回归模型分析判断预测因子,以危险比(hazard ratio,HR)和 95% 可信区间(confidence interval,CI)表示。以P<0.05为差异具有统计学意义。
2 结果
2.1 基线特征
RRMM患者共256例,sEMD 71例,发病率为27.7%。满足入组标准患者共40例,初诊临床特征如下:中位年龄61(38~78)岁;男性14例,女26例;非轻链型31例(IgG型18例,IgA型10例,IgD型2例,不分泌型1例),轻链型9例(κ轻链型4例,λ轻链型5例);Durie-Salmon分期Ⅱ期5例,ⅢA期29例,ⅢB期6例;国际分期系统(International Stage System,ISS)分期,Ⅰ期4例,Ⅱ期14例,Ⅲ期22例;中位骨髓浆细胞占比为30%(10%~91%);初诊IMWG细胞遗传学分层标危19例,高危4例,17例未查。
2.2 sEMD的危险因素
本组患者自确诊MM至诊断sEMD的间隔为4.0~215.6个月,中位25.0个月。对如下指标进行sEMD危险因素的Cox多变量分析:初诊时年龄(<60岁 vs. ≥60岁)、性别(男性 vs. 女性)、MM分型(非轻链型 vs. 轻链型)、DS分期(Ⅰ~Ⅱ期 vs. Ⅲ期)、ISS分期(Ⅰ~Ⅱ期 vs. Ⅲ期),结果显示ISS分期Ⅲ期(HR=2.867,P=0.004)为sEMD的独立危险因素,见图1。
2.3 sEMD的临床表现
40例中31例患者因出现临床症状而就诊,其中20例为新发骨痛,8例为体表触及包块,3例突发截瘫。此外,9例患者无临床症状,在定期复查影像学时被检出,且其中4例经病理证实。
40例中sEMD单发19例,至少两个部位同时出现(多发)21例。
40例中sEMD-B组25例,sEMD-E组15例。骨旁病变最常分布于脊椎(20例次),其次为颅骨(7例次),再次为胸廓组成骨(6例次)与肢带骨(6例次),最后为骨盆(4例次);而非骨旁病变最常见皮肤软组织(6例次),其次为椎管(5例次)及头部(5例次),再次为胸水(3例次)及腹膜(3例次),最少见为肺脏(2例次)及睾丸(1例次)。
40例患者出现sEMD时的生化指标,见表1。
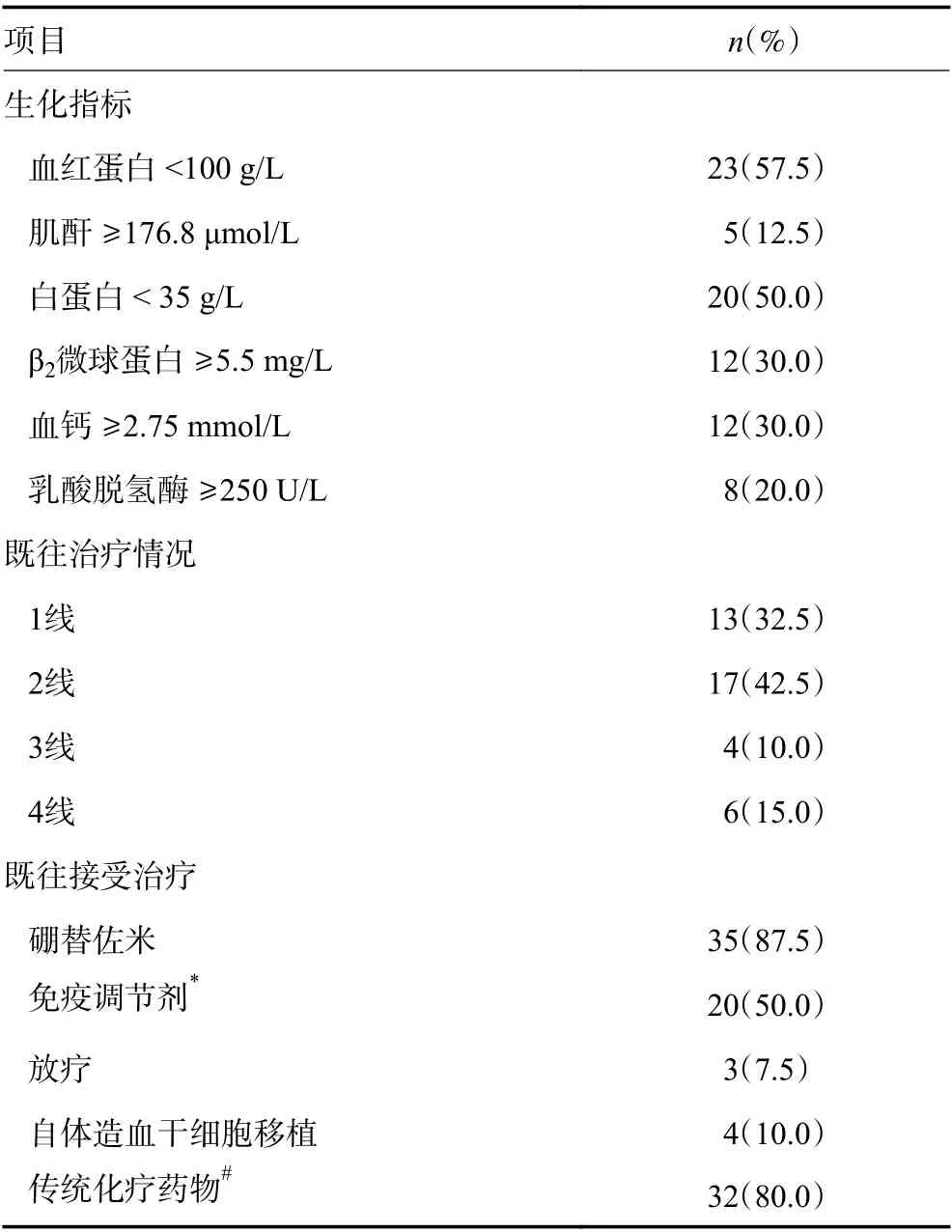
表1 40例患者出现sEMD时生化指标与既往治疗
2.4 疗效
40例患者中有6例(15%)患者在初治诱导时曾接受过LPD,其方案为PDD 5例,DVD 1例,中位疗程为5(3~9)个疗程;总体反应率(overall response rate,ORR)为100%,其中完全缓解(complete response,CR)1例,非常好的部分缓解(very good partial response,VGPR)1例,部分缓解(partial response,PR)4例;6例患者出现sEMD的中位间隔为28.5(4.0~39.0)个月;LPD再治疗中位疗程为4(3~6)个疗程,ORR为33.3%。
40例患者中位治疗线数为2(1~4)线,其中对硼替佐米耐药者7例,对免疫调节剂耐药者7例(6例为来那度胺,1例为沙利度胺),对硼替佐米及来那度胺双耐药者1例,对长春地辛耐药者2例,既往治疗方案,见表1。
在继发EMD后,40例患者接受了中位5(3~9)个疗程的LPD化疗,其中PDD方案23例,CDD 8例,DVD 7例,RCDD 2例。
每2个疗程评价疗效,结合髓内指标(骨髓浆细胞及M蛋白鉴定)与髓外病灶综合评判。2个疗程后,24例患者对治疗有反应,其中2例CR(髓内CR伴胸腔积液消失),2例VGPR(髓内CR且软组织包块缩小>90%),20例PR;疾病稳定(stable disease,SD)15例,疾病进展(progression disease,PD)1例(EMD直径增大)。本组患者2个疗程ORR为60%(24/40),≥VGPR为10%(4/40);EMD-B组ORR为68.0%,EMD-E组ORR为46.7%,两组比较差异无统计学意义(P=0.182)。
27例完成4个疗程及以上化疗,其中CR 2例,VGPR 2例,PR 19例,SD 4例,ORR为85.2%(23/27),≥VGPR为14.8%(4/27)。
13例完成6个疗程及以上化疗,其中CR 1例,VGPR 2例,PR 10例,ORR为100%,≥VGPR为23.1%(3/13)。
2例患者完成9个疗程,其中CR 1例,PR 1例,ORR为100%,≥VGPR为50%(1/2)(图2)。
2.5 LPD无进展生存时间
40例患者LPD相关预计中位PFS(median PFS,mPFS)为8.0个月(95%CI:7.5~8.5)(图3A),其中EMD-B组为9.0个月(95%CI:6.06~11.9),EMD-E组为8.0个月(95%CI:7.95~8.05);对无进展生存期≥6个月的34例患者据LPD是否达到6个疗程进行界标分析,<6个疗程与≥6个疗程的中位预计PFS分别为8.0个月(95%CI:7.6~8.5)与12.0个月(95%CI:9.3~14.7),虽然差异无统计学意义(P=0.093)(图3B),但曲线之间有离散趋势。
2.6 sEMD总体生存时间
40例患者出现sEMD后的预计中位OS(median OS,mOS)为22.0个月(95%CI:18.2~25.8),1年sEMD-OS率73.6%,2年sEMD-OS率为38.2%(图4A)。截至随访结束,17例患者死亡,9例死于疾病进展,3例死于呼吸衰竭,3例死于肺水肿,1例死于脑梗塞,1例死于脑出血。
根据sEMD与确诊的间隔、出现的时机、数目及部位等特点进行分组比较,得出:sEMD间隔≥6个月组与<6个月组的中位sEMD-OS分别为22.4个月与9.3个月,1年sEMD-OS率分别为76.8%与33.3%,差异具有统计学意义(P=0.010,图4B);有症状组与无症状复查组中位sEMD-OS分别为19.7个月与未达到(not estimated,NE),1年sEMD-OS率分别为65.6%与100.0%,差异具有统计学意义(P=0.011,图4C);单发与多发sEMD组中位sEMD-OS分别为23.2与19.7个月,1年sEMD-OS率分别为88.1%与55.9%,差异无统计学意义(P=0.073,图4D);骨旁与非骨旁sEMD组中位sEMD-OS分别为NE与11.1个月,1年sEMD-OS率分别为91.3%与33.5%,差异具有统计学意义(P<0.001,图4E)。
2.7 影响sEMD总体生存时间的预后因素分析
首先,对可能影响sEMD-OS的所有因素进行单变量分析,对各个自变量进行二分类赋值:sEMD诊断年龄(赋值:<60=1,≥60=2)、MM类型(赋值:非轻链型=1,轻链型=2)、ISS分期(赋值:Ⅰ~Ⅱ期=1,Ⅲ期=2)、血红蛋白(赋值:≥100 g/L=1,<100 g/L=2)、血清钙(校正)(赋值:<2.75 mmol/L=1,≥2.75 mmol/L=2)、乳酸脱氢酶(lactic dehydrogenase,LDH)(赋值:<250 U/L=1,≥250 U/L=2)、sEMD出现间隔(赋值:≥6个月=1,<6个月=2)、sEMD时机(赋值:复查时发现=1,有症状=2)、sEMD数目(赋值:单发=1,多发=2)、sEMD部位(赋值:骨旁=1,非骨旁=2),以sEMD-OS为因变量进行单因素分析,结果显示sEMD部位、时机、出现间隔与LDH四者的不同分组间差异具有统计学意义(P<0.05)。
随后对上述4项有统计学意义的指标进行多因素Cox回归分析,显示非骨旁(HR=4.417, 95%CI:1.026~19.005, P=0.046)与LDH>250 U/L(HR=6.904,95%CI:2.010~23.713,P=0.002)为sEMD-OS的独立不良预后因素。
2.8 不良反应
所有sEMD患者在应用LPD前完善血常规化验,若白细胞<2.0×109/L或中性粒细胞<1.0×109/L,预防性予以粒细胞集落刺激因子皮下注射,否则不予预防;应用LPD后复查血常规,参照上述标准进行升白治疗。本研究中,2例(5%)患者在应用LPD后出现3级以上不良反应而导致后续LPD停药,其中1例为粒细胞缺乏,另1例为重度贫血;其余均为2级以下不良反应,未影响化疗方案的进行。血液学毒性的发生率为47.5%,最常见的为白细胞减少(20%)与贫血(17.5%);非血液学毒性的发生率为30%,最常见的为感染(15%),未出现心脏毒性。所有不良反应,见表2。
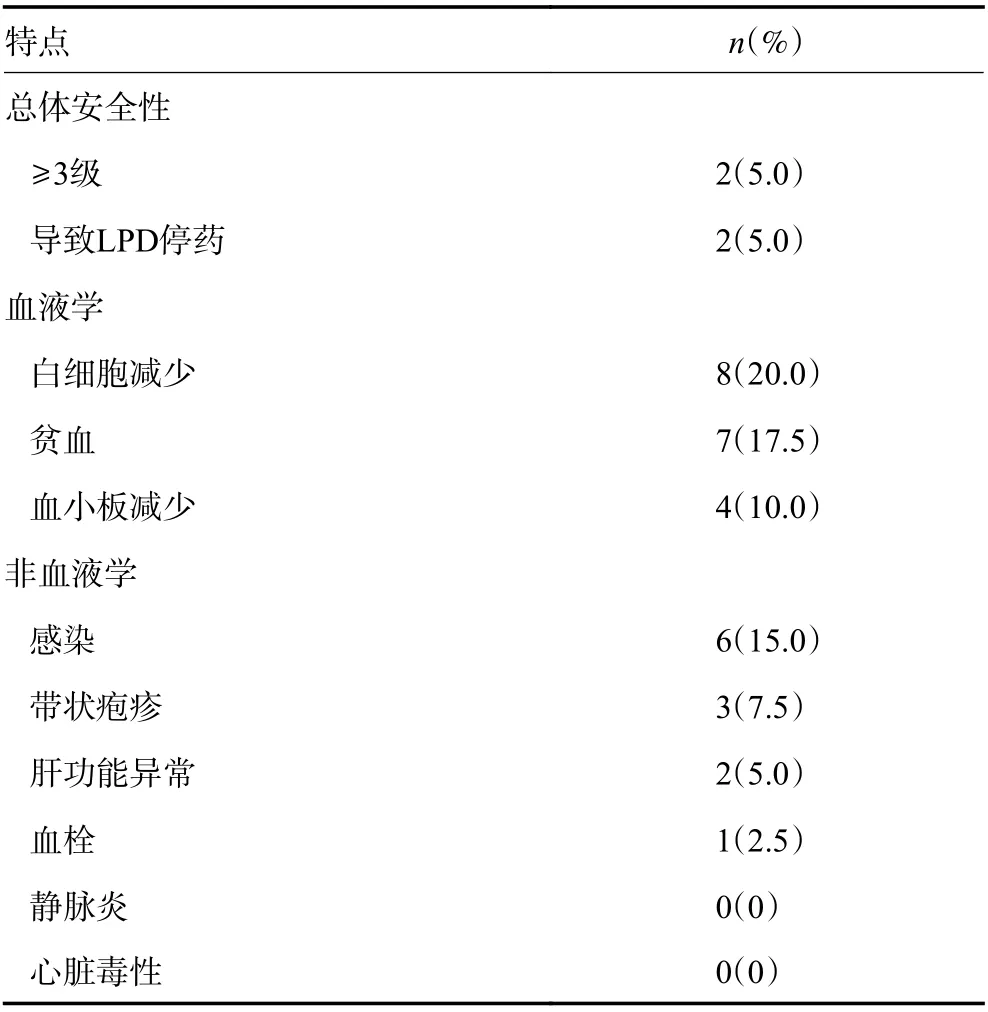
表2 患者不良反应
3 讨论
近年来,随着新药的广泛应用,MM患者的生存期逐渐延长,加之检查手段不断进步,故EMD的发生率明显升高,RRMM继发EMD对治疗不敏感,疗效欠佳。目前,国际国内仍无治疗共识,是临床医生面临的一大挑战[3,5-6,9]。阿霉素作为一种传统细胞毒药物,在2020年的《中国多发性骨髓瘤诊治指南》[10]与美国国立综合癌症网络(NCCN)指南均被推荐为骨髓瘤治疗的一线方案。美国Mayo诊所指出,对于伴EMD的适宜移植MM患者应接受VDT-PACE方案化疗2个疗程并序贯自体造血干细胞移植(autologous stem cell transplantation,ASCT),而不宜移植的患者则推荐CD38单抗类及蒽环类药物治疗[11]。相比于普通阿霉素,LPD可以选择性通过毛细血管内皮细胞间隙,在肿瘤组织内蓄积释放并发挥抗肿瘤作用,同时减少对正常组织的毒性。鉴于此,本文回顾分析40例RRMM患者,出现sEMD后接受中位5(3~9)个疗程的LPD化疗,得出含LPD方案治疗RRMM伴sEMD短期疗效好,安全性高,非骨旁sEMD及LDH>250 U/L预后不良。
有研究提示,sEMD的发生率为13%~26%[12]。本研究sEMD的检出率为27.7%,其中一线治疗后占比为32.5%,二线占比为42.5%,三线及以上占比为25%,sEMD中位诊断时间为25.0个月。相似地,一项来自土耳其的多中心真实世界研究报道继发EMD的中位诊断时间为25.1个月[13]。此外,一项既往治疗包含硼替佐米、来那度胺、沙利度胺及ASCT的回顾性研究显示,24%的患者在治疗过程中出现sEMD,其中一线、二线、三线及以上治疗后的检出率分别为53%、33%和14%[9]。目前,各中心对EMD的定义尚未统一,加之检测手段各不相同,故报道的sEMD检出率有所不同,但多学者均认同随着既往治疗线数的增多,sEMD的发生率越高[14]。
关于sEMD的危险因素,本研究发现,初诊ISSⅢ期患者在病程中较易合并sEMD,相似的结果在一项回顾性研究中也被提出[15]。多种因素被认为与sEMD有关:既往单克隆丙种球蛋白血症病史、初诊是否伴EMD、细胞遗传学异常、血红蛋白、血钙、LDH水平以及是否接受新药治疗等[15-18]。目前,较为公认的EMD复发危险因素为P53基因缺失[16]。本研究患者初诊细胞遗传学信息不全,未能将其纳入危险因素的分析中,有待于进一步扩大样本量对此进行证实。
关于治疗疗效,本研究显示2个疗程含LPD方案后ORR为60%;EMD-B组ORR为68%,EMD-E组ORR为46.7%。一项16例RRMM伴sEMD-E的研究显示,应用泊马度胺联合小剂量地塞米松的ORR为30%[5]。在另一项纳入了32例RRMM患者伴EMD的真实世界研究中,卡非佐米为基础方案的ORR为40%[19]。此外,一项非清髓造血干细胞移植伴sEMD的研究显示,在接受供者淋巴细胞回输、放疗、传统化疗及新药治疗后,ORR为45.5%[20]。由此可见二代新药、免疫治疗、放疗等对RRMM患者合并EMD的疗效也有限。本研究中有23例在4个疗程化疗后有效(23/40,ORR为57.5%),13例在6个疗程化疗后有效(13/40,ORR为32.5%),提示含LPD方案在RRMM伴sEMD短期疗效尚可,需要进一步扩大样本量及延长随访时间来证实其长期疗效。
本组研究中sEMD后mOS为22.0个月,1年生存率为73.6%;其中sEMD-E组OS为11.1个月,1年生存率为33.5%,预后不良。一项纳入456例经过第一代新药及ASCT诱导治疗sEMD的研究显示,mOS为24个月[14]。2015年Dana-Farber癌症研究所的Varga教授曾回顾分析117例MM患者的临床资料,发现sEMD-E患者的mOS为10.8个月[15],与本研究结果相近。另一项2015年的报道研究了ASCT后伴sEMD-E的55例患者,其生存期为15.6个月,较本研究结果略延长,考虑与患者的基础体能状态较好有关[17]。综上所述,sEMD-E预后不良,无论第一代、第二代新药或移植均使其获益并不显著。
关于出现sEMD后PFS,有研究报道mPFS为5.4个月,其研究对象纳入时间较早(2005年至2008年),接受的方案中包括传统化疗、第一代新药、ASCT及干扰素等[18];而另一项研究纳入的时间为2007年至2010年,其中5例患者中枢神经系统受累及,接受ASCT和(或)异基因SCT和(或)新药等治疗后,其mPFS仅2个月[21]。本研究mPFS为8.0个月,比上述文献报道明显延长,随后根据LPD应用能够达6个疗程进行界标分析,得出<6个疗程与≥6个疗程的预计mPFS分别为8.0个月与12.0个月,两组差异并不显著,但曲线有离散趋势,提示因个人因素停药的群体若继续应用至6个疗程或能获益。因未能检索到LPD治疗sEMD的研究,无法进行析因分析比较。已有学者将纳米技术与LPD结合组成智能药物运输系统对MM细胞进行精准治疗,在EMD的体外研究已取得显著疗效[22]。
LPD总体上安全性较好,本研究无1例出现心脏毒性的患者;血液学毒性方面只有2例(5%)出现了3级以上不良反应而导致停药,其中1例为粒细胞缺乏,另1例为重度贫血,其余均为2级以下不良反应,未影响化疗方案的进行。
总之,MM目前仍为不可治愈的疾病,sEMD患者极易耐药或复发,目前治疗手段有限,仍是临床上亟待解决的难题之一。即使是ASCT、CD38单抗类、Bcl-2抑制剂或嵌合抗原受体T细胞免疫疗法(chimeric antigen receptor T cell,CAR-T)等治疗仍不能完全逆转这部分患者的不良预后,关于sEMD的有效治疗手段依然在临床探索当中。本研究结果显示,LPD为基础的三药/四药方案治疗RRMM伴sEMD患者,短期疗效好,安全性高,是此类患者可供选择的有效方案之一;继发非骨旁髓外病变预后不良,需要选取更为积极的治疗策略。

