新型催化剂Er3+∶Y3Al5O12(x)/TiO2对冰毒的超声催化降解
魏春生,陈燕蝶,张江华,苏炳任,何炳晨
(1.中国刑事警察学院 禁毒与治安学院,辽宁 沈阳 110854;2.中国刑事警察学院 禁毒技术与装备研发推广中心,辽宁 沈阳 110854;3.中国刑事警察学院 公安信息技术与情报学院,辽宁 沈阳 110854)
冰毒,即甲基苯丙胺的盐酸盐,是2015~2019年全球缉获数量最多的苯丙胺类兴奋剂[1],也是我国吸毒人员滥用最为广范的一种毒品.根据《2020年中国毒品形势报告》披露,我国2020年缴获各类毒品总计55.49吨,截至2020年年底,现有180.1万名吸毒人员中,滥用冰毒等合成毒品人员有103.1万名,占比高达57.2%[2].我国每年除了缴获大量的冰毒成品以外,还在冰毒地下加工场查获巨量的含有冰毒成分的废水.冰毒作为一种强酸弱碱盐,受热后会变成液态甲基苯丙胺并进一步汽化,很难通过普通焚烧而彻底销毁.此外,冰毒极易溶解于水,而且水溶液性质稳定,毒性很强,在自然环境中很难自然降解[3].如果含有冰毒成分的废水直接排放,必然会污染环境,危及人畜安全.目前,各国的毒品销毁仍以普通焚烧、填埋和远海抛弃为主,无法彻底、有效地销毁冰毒[4-7].因此,在环保意识不断增强的今天,研发新型的绿色环保的毒品处理技术显得尤为迫切.

本研究将上转光剂Er3+∶Y3Al5O12和TiO2按一定比例混合焙烧,制备了系列新型复合材料Er3+∶Y3Al5O12(x)/TiO2并用于超声催化降解冰毒,试图建立一种绿色环保的冰毒处理方法.
1 实验部分
1.1 实验药品
硝酸铝(Al(NO3)3·9H2O)、硝酸(HNO3)、无水乙醇(C2H5OH)、氢氟酸(HF)、醋酸(CH3COOH)、柠檬酸(C6H8O7)、氧化铒(Er2O3)、氧化钇(Y2O3)等均购自国药集团沈阳化学试剂有限公司,其中氧化铒、氧化钇纯度均为99.99%,其他均为分析纯(AR).二氧化钛(TiO2, 锐钛型60 nm)购自杭州万景新材料有限公司.冰毒对照品购自公安部第二研究所.蒸馏水为二次蒸馏水.
1.2 仪器设备
JSM-6510LV扫描电镜(日本电子株式会社);XRD-6000型X射线衍射仪(Shimadzu公司,Cu Kα, λ=0.15406 nm);Agilent 7890B气相色谱仪(美国Agilent公司);TD18G型离心机(盐城市凯特实验仪器有限公司);KQ-700GVDV台式三频恒温数控超声波清洗器(昆山市超声仪器有限公司);SX2-4-10型马弗炉(天津泰斯特仪器有限公司);MYP11-2A恒温磁力搅拌器(上海梅颖浦仪器仪表有限公司);FA2004型分析天平(上海衡平仪器仪表厂).
1.3 催化剂Er3+∶Y3Al5O12(x)/TiO2的制备
上转光剂Er3+∶Y3Al5O12按文献中的溶胶凝胶法制备[19-20].之后将制备得到的Er3+∶Y3Al5O12与TiO2按照不同比例充分研磨、混合,加入蒸馏水,超声分散.再放入马弗炉中在400 ℃焙烧1 h,冷却至室温,得到催化剂Er3+∶Y3Al5O12(x)/TiO2.
1.4 超声催化降解冰毒水溶液
量取50.0 mL浓度为10.0 μg·mL-1的冰毒水溶液置于具塞锥形瓶中,添加50.0 mg Er3+∶Y3Al5O12/TiO2,静置30 min,使其均匀混合并吸附充分.然后将锥形瓶置于超声波清洗器中,考察催化剂在不同反应温度、不同超声功率下对冰毒溶液的催化降解能力.从反应开始时取样一次,此后每间隔30 min取样一次,共取样6次.用Agilent 7890B型气相色谱仪测定其中冰毒含量,根据(1)式计算降解率.其中,C0和Ct分别为反应前和反应后溶液中的冰毒含量.
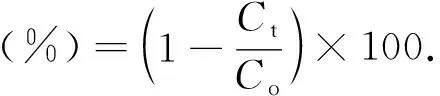
(1)
1.5 气相色谱条件
Agilent公司7890B型气相色谱仪,FID检测器,色谱柱为DB-5型毛细管柱(5%苯基和95%甲基聚硅氧烷,柱长30 m,内径0.25 mm,膜厚0.25 μm).采用程序升温的方式,柱温初始温度为80 ℃,以20 ℃·min-1的升温速率升温至220 ℃,再以40 ℃·min-1的升温速率升温至300 ℃,保持5 min.检测器温度为310 ℃,进样口温度为280 ℃,载气为高纯氮气,氮气流量为1.0 mL·min-1,H2流量为40 mL·min-1,空气流量为400 mL·min-1,尾吹流量为10 mL·min-1,分流进样,分流比为20∶1.
2 结果与讨论
2.1 温度对超声催化降解冰毒的影响
选用恒温模式,在超声波清洗器功率为700 W、水槽温度分别为20,30和40 ℃条件下,用Er3+∶Y3Al5O12(10)/TiO2对冰毒溶液超声催化降解2.5 h,结果见图1.可以看出,在20 ℃时,冰毒的降解率为47.65%;30 ℃时,冰毒的降解率高达74.43%;当温度升至40 ℃时,冰毒的降解率下降为29.17%.表明TiO2在超声波辐照下,温度对催化剂上的光生电子-电子空穴对的产生有较大影响.低温时,电子-电子空穴对产生较少,催化剂催化活性较低;温度升高时,能够产生更多电子-电子空穴对, 催化活性随之增高. 但是温度过高,电子容易与空穴发生复合,催化活性又会降低.所以,适当的温度有利于提升Er3+∶Y3Al5O12(10)/TiO2催化剂对冰毒的催化降解能力.
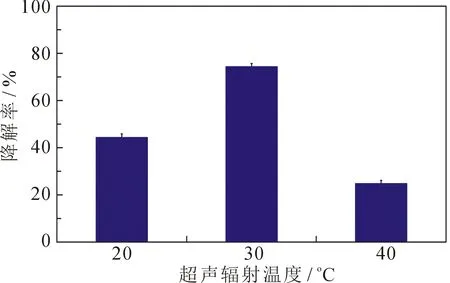
图1 不同温度下冰毒的降解率
2.2 超声功率对催化降解冰毒的影响
在温度为30 ℃,不同超声功率条件下(超声设备最大功率为700 W),超声催化降解冰毒2.5 h后的结果见图2.可以看出,随着超声波功率的增大,冰毒的降解率也随之增大.当超声波清洗器功率为280 W时,冰毒的降解率为26.41%;当超声波清洗器的功率为700 W时,冰毒的降解率达到74.43%.说明在一定范围内,Er3+∶Y3Al5O12(10)/TiO2的催化降解能力与超声波清洗器的功率密切相关.功率越大,超声所产生的声致发光及热点越强,Er3+∶Y3Al5O12转换的短波长的光越多,TiO2上产生的电子-电子空穴越多,最终冰毒水溶液的降解率越高.在一定范围内,功率越大,冰毒降解速率越大,功率越小,冰毒降解速率则越小.

图2 不同超声功率下冰毒的降解率
2.3 Er3+∶Y3Al5O12(x)/TiO2对冰毒的降解率及其反应动力学
优化上述温度与超声功率实验条件后,在超声功率为700 W、超声频率为45 kHz、溶液温度为30 ℃的条件下对冰毒水溶液(浓度为10 mg·L-1)超声2.5 h.Er3+∶Y3Al5O12(x)/TiO2催化材料对冰毒的超声降解率及其反应动力学见图3.图3A为Er3+∶Y3Al5O12(x)/TiO2对冰毒的降解率的影响,其中空白实验仅对冰毒水溶液进行超声处理,降解率为5.64%.加入Er3+∶Y3Al5O12(x)/TiO2催化剂后,随着催化剂中Er3+∶Y3Al5O12的比重增大,冰毒的降解率先增加后减少.Er3+∶Y3Al5O12比重达到10%时,冰毒的降解率最高,为74.43%.进一步增加Er3+∶Y3Al5O12的含量,催化剂Er3+∶Y3Al5O12(15)/TiO2对冰毒的降解率反而下降至51.02%.说明在一定的范围内,随着Er3+∶Y3Al5O12的不断加入,更多长波长的光被转化为可被TiO2利用的短波长光,进而提高了催化剂的性能.继续增加Er3+∶Y3Al5O12的比例,尽管转化为短波长的光持续增多,但催化剂单位质量内的TiO2比例下降,活性中心分散度降低,产生的催化活性中心变少.达到一定阈值后,复合催化剂整体催化性能反而下降.
图3B为Er3+∶Y3Al5O12(x)/TiO2复合催化材料对冰毒的超声降解反应动力学曲线.可以看出,在Er3+∶Y3Al5O12(x)/TiO2上冰毒的超声催化降解符合一级反应动力学方程:-ln(Ct/C0)=kt,Ct与C0分别为冰毒水溶液的反应浓度和起始浓度.经计算,空白实验及Er3+∶Y3Al5O12含量分别在5%,10%,15% 时催化剂的一级反应速率常数分别为0.011 0,0.167 5,0.272 8和0.136 8 s-1.其中,在Er3+∶Y3Al5O12(10)/TiO2上冰毒的一级反应速率常数最大,进一步说明在Er3+∶Y3Al5O12(x)/TiO2中,Er3+∶Y3Al5O12的加入量并不是越多越好,在5%与15%之间存在着最佳值.
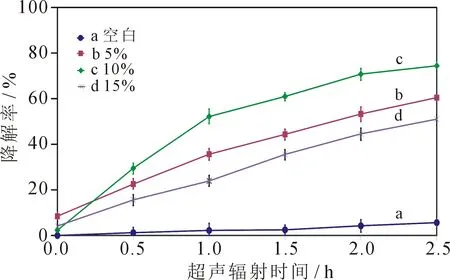
(A)Er3+∶Y3Al5O12(x)/TiO2对冰毒的降解率
2.4 Er3+∶Y3Al5O12(10)/TiO2的XRD分析
TiO2,Er3+∶Y3Al5O12和Er3+∶Y3Al5O12(10)/TiO2催化剂的XRD谱图见图4.图4a为TiO2粉末的XRD谱图,其中在2θ=25°,38°,47°,54°,55°和62°的衍射峰为锐钛型TiO2的特征衍射峰.图4b为制备的上转换发光剂Er3+∶Y3Al5O12的XRD谱图,其衍射峰与Y3Al5O12标准谱图(JCPDS 33-0040)数据一致,只有轻微的偏移.表明在Er3+∶Y3Al5O12中存在Y3Al5O12,并且少量Er3+替代部分Y3+进入Y3Al5O12晶格,从而在XRD谱图中出现轻微偏移.图4c为Er3+∶Y3Al5O12(10)/TiO2的XRD谱图.从图4c中既可以看到锐钛型TiO2的少数特征峰,也可以看到上转换发光剂Er3+∶Y3Al5O12的特征峰,说明制备的催化剂中Er3+∶Y3Al5O12与TiO2已经很好地复合在一起.

(a) TiO2, (b) Er3+∶Y3Al5O12,(c) Er3+∶Y3Al5O12(10)/TiO2催化剂
图4 样品的XRD谱图
Fig 4 XRD patterns of samples
2.5 Er3+∶Y3Al5O12(10)/TiO2的SEM表征分析
Er3+∶Y3Al5O12和Er3+∶Y3Al5O12(10)/TiO2催化剂的SEM形貌见图5.从图5a中可以清楚地看到,溶胶凝胶法制备的Er3+∶Y3Al5O12呈现不规则球状形貌,晶粒均匀,分散良好,平均粒径约为50 nm.图5b中可以看出,TiO2复合材料的粒径在60 nm左右,经400 ℃高温煅烧后,两种粒子分布均匀,已经烧结在一起.

(a)Er3+∶Y3Al5O12,(b)Er3+∶Y3Al5O12(10)/TiO2
2.6 催化降解过程中冰毒的气相色谱分析
在超声功率为700 W、超声频率为45 kHz、溶液温度为30 ℃的条件下对冰毒水溶液(浓度为10 mg·L-1)超声2.5 h.冰毒水溶液在不同超声催化时间段下的气相色谱图见图6.色谱峰1为内标物N,N-二甲基苯胺, 其保留时间为4.068 min.色谱峰2为甲基苯丙胺,其保留时间为5.053 min.由图6可知,随着超声降解时间的增加,甲基苯丙胺的色谱峰逐渐变小,说明溶液中冰毒的含量逐渐降低,甲基苯丙胺被逐渐降解.另外研究发现,在甲基苯丙胺色谱峰的前后,并未出现其他明显的峰,只检测到痕量的2-苯基环丙胺、苯丙胺、烯丙基苯,说明冰毒分子经初步降解后,被迅速矿化为H2O,CO2等无机小分子化合物[12].
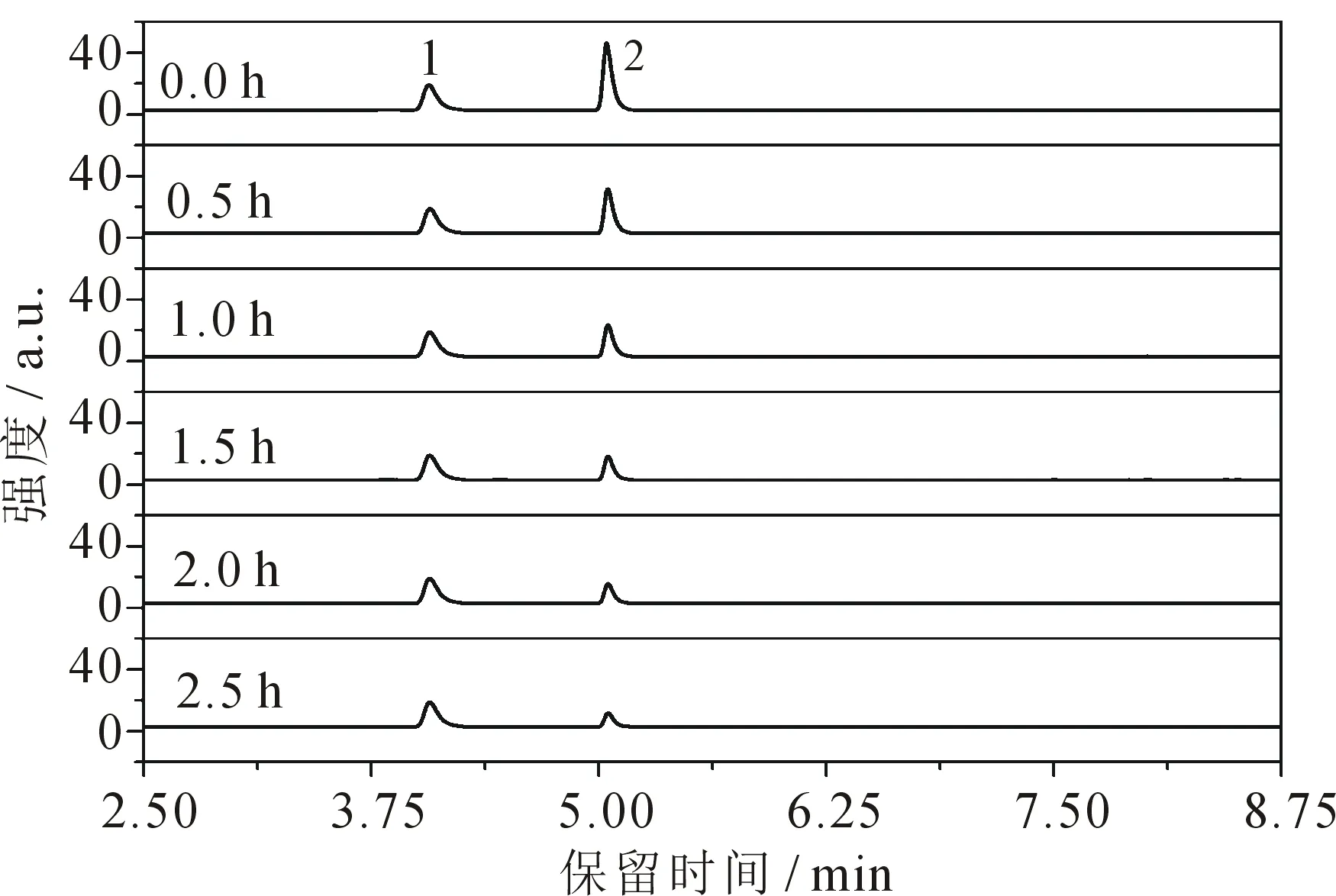
图6 不同催化降解时间下冰毒溶液的气相色谱图
2.7 Er3+∶Y3Al5O12(x)/TiO2超声催化降解毒品的机理
Er3+∶Y3Al5O12(x)/TiO2催化降解毒品的可能机理见图7,其高效降解毒品与超声空化效应产生的声致发光和“热点”机理密切相关[21-23].超声空化效应产生的声致发光可以产生范围很宽的光,但TiO2的带宽较窄(Ebg=3.2 eV),只能吸收其中波长小于365 nm的短波长的光.当受到短波长光的激发时,电子由TiO2的价带(VB)转移到导带(CB),进而在TiO2材料上产生电子空穴.电子-电子空穴对具有较高的能量,一方面电子空穴可以在TiO2材料表面直接分解毒品;另一方面电子空穴与水作用产生羟基自由基(·OH)亦可间接降解毒品.由于超声过程中产生短波长的光是有限的,故增加辐照到TiO2材料表面的短波长光的量,就会提高TiO2的声催化活性.作为上转光剂Er3+∶Y3Al5O12能够吸收无法被TiO2利用的长波长光,发出能够被TiO2利用的短波长光,进而有效提高TiO2的催化降解能力.所以,适当地添加Er3+∶Y3Al5O12而制备的Er3+∶Y3Al5O12(x)/TiO2具有更好的催化活性.
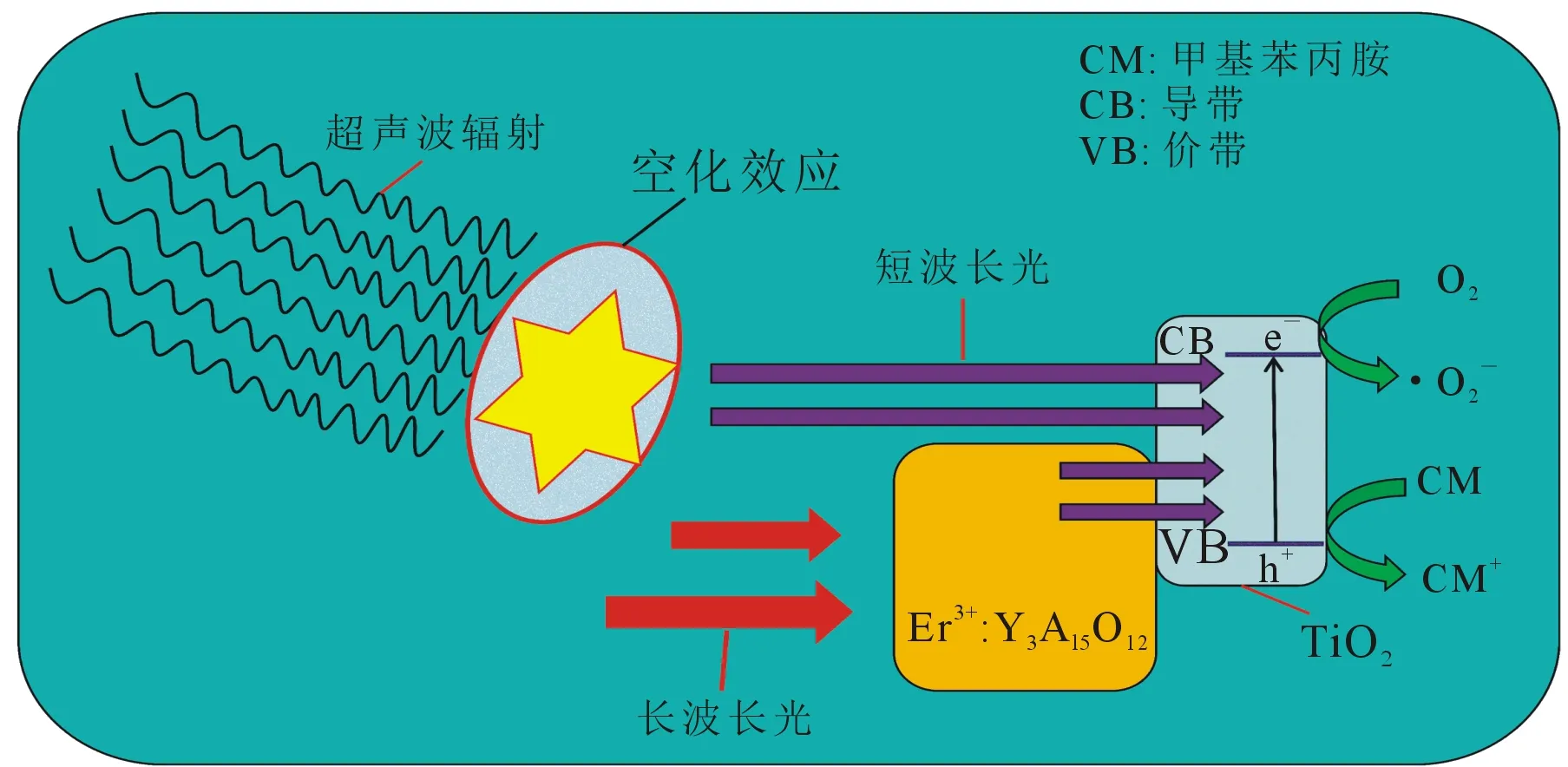
图7 Er3+∶Y3Al5O12(x)/TiO2超声降解毒品的 可能机理

3 结论
Er3+∶Y3Al5O12(x)/TiO2系列催化剂对冰毒分子具有较好的超声催化降解效果.其中,温度、超声功率和上转光剂Er3+∶Y3Al5O12的含量均影响超声催化降解冰毒的效果.当Er3+∶Y3Al5O12含量为10%、超声功率为700 W、溶液温度为30 ℃、超声频率为45 kHz的条件下,对浓度为10 mg·L-1冰毒水溶液超声2.5 h,冰毒的降解率为74.43%,达到最高.进一步研究表明,继续增大超声功率,延长超声时间,增加催化剂的用量,冰毒的降解率会进一步提高.该系列催化剂具有较高的超声催化活性,主要归因于超声空化效应产生的声致发光和“热点”.上转光剂Er3+∶Y3Al5O12能够吸收无法被TiO2利用的长波长的光,发出能够被TiO2利用的短波长的光;超高温的“热点”在水中可以破坏水分子而产生一定数量的具有较强氧化能力的·OH, 并可以像光一样激发纳米TiO2进行催化降解反应,从而有效提高TiO2的催化降解能力.本技术尤其适合透光性差的含冰毒废水的处理,且具有安全可靠、绿色环保等优点,具有良好的应用前景.

