达拉非尼联合曲美替尼治疗黑色素瘤致皮肤不良反应的Meta 分析
王瑞航,刘晓波,廖 思,华 鹏
(1.大理大学药学院,云南大理 671000;2.云南省第三人民医院药剂科,昆明 650000)
黑色素瘤是所有恶性肿瘤中最具侵袭性和复杂性的一种肿瘤,一旦扩散转移将危及患者生命。在全球范围内,每年约有5.55 万例癌症患者死于黑色素瘤〔1〕,其中原癌基因蛋白B-raf(proto-oncogene proteins B-raf,BRAF)突变型黑色素瘤约占黑色素瘤50%〔2〕。在此背景下,BRAF 抑制剂被用于治疗BRAF V600 突变型黑色素瘤,并且研究发现BRAF抑制剂与丝裂原活化细胞外信号调节激酶(mitogenactivated extracellular signal regulated kinase,MEK)抑制剂联合使用可大幅提高患者客观反应率和5年总生存率〔3-11〕。
尽管具有治疗优势,但这种治疗方法与多种皮肤不良事件相关联,从相对良性的湿疹到更严重的炎症,甚至诱发第二恶性肿瘤〔3-4〕。如果不及早发现和治疗,它不只会干扰患者对治疗的依从性,还可能导致严重的发病率和死亡风险。对此,临床医生需要了解和掌握达拉非尼(BRAF 抑制剂)和曲美替尼(MEK 抑制剂)相关皮肤不良反应的发生率和特征以进行早期预防和干预,确保患者获得最大的治疗收益并避免不必要的治疗中断。目前尚未有研究对此进行汇总分析,因此,本文对达拉非尼联合曲美替尼在临床使用过程中出现皮肤不良反应的情况进行评估,旨在为临床提供更多的循证参考。
1 资料与方法
1.1 纳入标准
1.1.1 研究对象①年龄>18 岁;②由病理学及影像学确诊为黑色素瘤。
1.1.2 研究类型国内外公开发表的达拉非尼联合曲美替尼治疗黑色素瘤的随机对照试验(randomized controlled trial,RCT)或前瞻性队列研究(Ⅱ和Ⅲ期临床试验)。
1.1.3 干预措施对于达拉非尼联合曲美替尼治疗黑色素瘤致所有等级皮肤不良反应发生率的评估,试验组:达拉非尼(150 mg,2 次/d)+曲美替尼(2 mg,1 次/d);对照组:不限。对于达拉非尼联合曲美替尼对比BRAF 抑制剂单药疗法致所有等级皮肤不良反应的评估,试验组:达拉非尼(150 mg,2 次/d)+曲美替尼(2 mg,1 次/d);对照组:BRAF 抑制剂单药疗法,如达拉非尼、威罗菲尼。
1.1.4 结局指标明确描述了是由达拉非尼联合曲美替尼引起的所有等级皮肤不良反应,包括:①皮疹;②瘙痒;③角化过度;④脱发;⑤皮肤乳头状瘤;⑥痤疮样皮炎;⑦皮肤鳞状细胞癌;⑧干性皮肤;⑨红斑。所有皮肤不良反应的严重程度均使用常见不良事件评价标准(common terminology criteria for adverse events,CTCAE)5.0 版进行分级。所有等级的皮肤不良反应包括严重等级和其他所有严重程度较低的皮肤不良反应,等级为1~5。
1.2 排除标准①综述、病例报道、会议摘要、案例报告、回顾性研究;②样本量<20;③先前已经接受过BRAF 抑制剂(有或没有MEK 抑制剂)治疗且停止治疗<12 周;④未注明药物剂量;⑤无主要结局指标;⑥重复发表、数据相同的文献。
1.3 资料来源与检索策略计算机检索PubMed、EMbase、Cochrane Library、Web of Science 以及中国知网、维普、万方、中国生物医学文献数据库中的相关文献,检索时间为自建库至2020 年12 月。中文检索词:达拉非尼、曲美替尼和黑色素瘤;英文检索词:dabrafenib、trametinib 和melanoma。
1.4 文献筛选与数据提取由2 名研究者根据纳入标准和排除标准独立筛选文献,并交叉核对,若意见不统一,请求第三方决定是否纳入。使用Excel工作表提取纳入研究基本信息:第一作者、发表年份、患者年龄、研究类型、样本量、治疗方案以及结局指标等。
1.5 质量评价对于RCT,采用Cochrane 协作网推荐的质量评价标准来评价研究的偏倚风险。采用改良版Jadad 量表〔12〕来评价纳入研究质量,内容包括:①随机序列的产生:随机数字表或类似方法计2分;描述为随机试验,但未描述随机的方法计1 分;采用交替分配的方法,如单双号计0 分。②随机化隐藏:使用的分配方案使医生和实验者无法预知分配序列的方法计2 分;只表明用随机数字表或其他随机分配方案计1 分;采取的方法均不能防止分组的可预测措施计0 分。③盲法:采用了完全一致的安慰剂片或类似方法计2 分;试验描述为盲法,但未描述方法计1 分;未采用双盲或方法不恰当计0分。④退出与失访:描述了退出与失访的数目和理由计1 分;未描述退出与失访数目或理由计0 分。总评分7 分,1~3 分为低质量,4~7 分为高质量。
对于前瞻性队列研究,采用纽卡斯尔-渥太华量表(Newcastle-Ottawa scale,NOS)〔13〕进行文献质量评价,评价内容如下:①选择性:暴露队列的代表性、非暴露队列的代表性、暴露因素的确定和研究开始前是否有研究对象发生结局事件;②可比性:是否控制混杂因素;③结局:结局事件的评估、随访是否充分和随访的完整性。满分为9 分,一般总分>5 分的研究可纳入Meta 分析,5~7 分为中等质量研究,8 分及以上为高质量研究。
1.6 统计分析采用Stata 15.1 软件计算达拉非尼联合曲美替尼治疗黑色素瘤所致皮肤不良反应的发生率;采用RevMan 5.3 软件评价达拉非尼联合曲美替尼对比BRAF 抑制剂单药治疗致皮肤不良反应的相对危险度(relative risk,RR)及95%置信区间(confidence interval,CI)。P<0.05 为差异有统计学意义。采用Q 检验和I2检验进行异质性检验,采用I2和P 值作为统计量来评价异质性的大小。当I2<50%且P>0.1 时,采用固定效应模型,反之则采用随机效应模型。若异质性较大,通过敏感性分析检验结果的稳定性。
2 结果
2.1 检索结果共检索出文献3 842 篇,通过排除重复文献及阅读题目和摘要后获得37 篇文献,再结合纳入、排除标准,最终纳入10 篇文献,均为英文文献,共2 623 例患者。文献筛选流程见图1。

图1 文献筛选流程
2.2 纳入研究的基本特征与质量评价纳入研究发表于2012—2020 年,其中包括6 篇RCT〔3-8〕,4 篇前瞻性队列研究〔14-17〕,研究对象中位年龄为47~58岁。根据纳入文献质量评价,6 篇RCT 质量评分≥4分,4 篇前瞻性队列研究质量评分≥6 分,均为中高质量的研究。纳入研究的基本特征与质量评分见表1,6 篇RCT 文献偏倚风险分布图、文献风险评估结果见图2~3。

表1 纳入研究的基本特征与质量评分
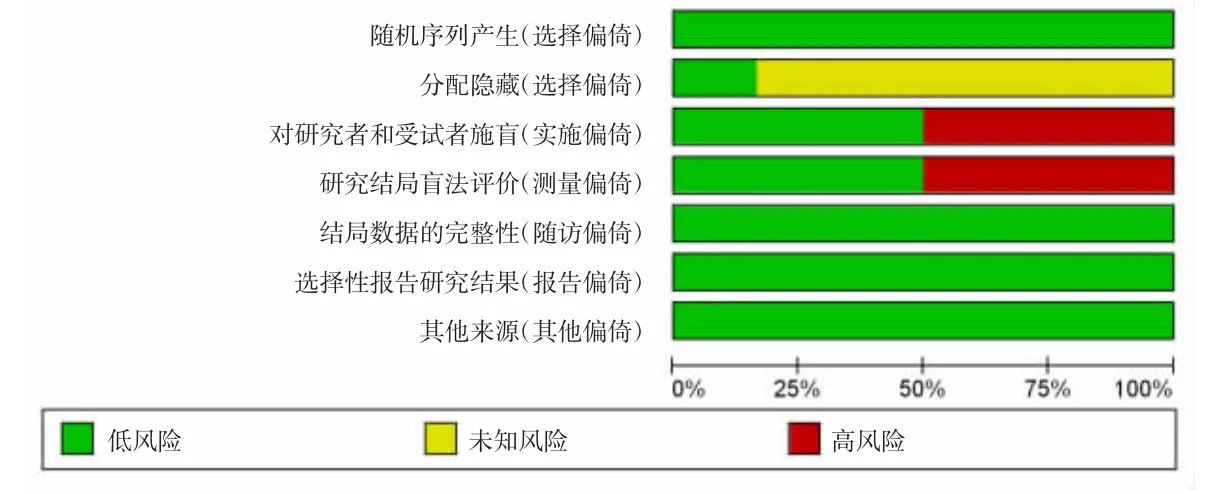
图2 文献偏倚风险分布图

图3 文献风险评估结果
2.3 Meta 分析结果
2.3.1 达拉非尼联合曲美替尼治疗黑色素瘤致所有等级皮肤不良反应的发生率(1)皮疹:9 项研究〔3-5,7-8,14-17〕(2 418 例患者)报道了所有等级皮疹的发生率。经异质性检验,I2=46.47%<50%,P=0.06<0.1,提示异质性较大,采用随机效应模型。结果显示:达拉非尼联合曲美替尼致所有等级皮疹的发生率为22%[95%CI(0.19,0.26)]。见图4A。
(2)瘙痒:6 项研究〔3-5,7,15-16〕(2 196 例患者)报道了所有等级瘙痒的发生率。经异质性检验,I2=12.32%<50%,P=0.34>0.1,提示异质性较小,采用固定效应模型。结果显示:达拉非尼联合曲美替尼致所有等级瘙痒的发生率为10%[95%CI(0.08,0.11)]。见图4B。
(3)角化过度:6 项研究〔3-4,7,14-16〕(1 354 例患者)报道了所有等级角化过度的发生率。经异质性检验,I2=48.62%<50%,P=0.08<0.1,提示异质性较大,采用随机效应模型。结果显示:达拉非尼联合曲美替尼致所有等级角化过度的发生率为7%[95%CI(0.04,0.10)]。见图4C。
(4)脱发:5 项研究〔3-5,7,15〕(2 170 例患者)报道了所有等级脱发的发生率。经异质性检验,I2=0.00%<50%,P=0.74>0.1,提示异质性较小,采用固定效应模型。结果显示:达拉非尼联合曲美替尼致所有等级脱发的发生率为5%[95%CI(0.04,0.07)]。见图4D。
(5)皮肤乳头状瘤:4 项研究〔3-4,7,14〕(1 252 例患者)报道了所有等级皮肤乳头状瘤的发生率。经异质性检验,I2=28.5%<50%,P=0.24>0.1,提示异质性较小,采用固定效应模型。结果显示:达拉非尼联合曲美替尼致所有等级皮肤乳头状瘤的发生率为1%[95%CI(0.01,0.03)]。见图4E。
(6)痤疮样皮炎:5 项研究〔3-6,15〕(2 267 例患者)报道了所有等级痤疮样皮炎的发生率。经异质性检验,I2=79.42%>50%,P=0.00<0.1,提示异质性较大,采用随机效应模型。结果显示:达拉非尼联合曲美替尼致所有等级痤疮样皮炎的发生率为10%[95%CI(0.06,0.14)]。见图4F。
(7)皮肤鳞状细胞癌:5 项研究〔3-5,7,16〕(2 120 例患者)报道了所有等级皮肤鳞状细胞癌的发生率。经异质性检验,I2=76.54%>50%,P=0.00<0.1,提示异质性较大,采用随机效应模型。结果显示:达拉非尼联合曲美替尼致所有等级皮肤鳞状细胞癌的发生率为2%[95%CI(0.00,0.04)]。见图4G。
(8)干性皮肤:5 项研究〔3-6,15〕(2 267 例患者)报道了所有等级干性皮肤的发生率。经异质性检验,I2=42.97%<50%,P=0.14>0.1,提示异质性较小,采用固定效应模型。结果显示:达拉非尼联合曲美替尼致所有等级干性皮肤的发生率为10%[95%CI(0.08,0.12)]。见图4H。
(9)红斑:4 项研究〔3-5,15〕(2 062 例患者)报道了所有等级红斑的发生率。经异质性检验,I2=0.00%<50%,P=0.63>0.1,提示异质性较小,采用固定效应模型。结果显示:达拉非尼联合曲美替尼致所有等级红斑的发生率为11%[95%CI(0.09,0.13)]。见图4I。

图4 所有等级皮肤不良反应Meta 分析森林图
2.3.2 达拉非尼联合曲美替尼对比BRAF 抑制剂单药治疗黑色素瘤致所有等级皮肤不良反应3 项研究〔3-4,7〕(1 227 例患者)报道了达拉非尼联合曲美替尼和BRAF 抑制剂单药治疗组皮肤不良反应的发生率。经异质性检验,皮疹和皮肤鳞状细胞癌I2>50%,P<0.1,提示异质性较大,采用随机效应模型分析;瘙痒、角化过度、脱发和皮肤乳头状瘤I2<50%,P>0.1,提示异质性较小,采用固定效应模型分析。Meta 分析结果显示:与单用BRAF 抑制剂相比,达拉非尼联合曲美替尼降低了瘙痒、角化过度、脱发、皮肤乳头状瘤和皮肤鳞状细胞癌的发生(P<0.05),对皮疹无影响(P>0.05)。见表2。

表2 所有等级皮肤不良反应的相对危险度
2.4 敏感性分析运用metainf 进行敏感性分析,发现2015 年Long 等〔3〕研究对达拉非尼联合曲美替尼对比BRAF 抑制剂单药治疗黑色素瘤致所有等级皮疹的发生率影响较大。将其剔除后,异质性显著降低(I2=41%,P=0.19),结果具有统计学意义[RR=0.57,95%CI(0.40,0.82),P=0.002]。其余指标剔除任意一篇,结果均无明显变化。
2.5 发表偏倚以所有等级皮肤不良反应发生率为指标绘制倒漏斗图,并进行Begg's 检验及Egger's检验,结果显示:存在发表偏倚的可能性较小(P>0.05)。见表3 和图5。

图5 倒漏斗图

表3 皮肤不良反应对称性检验
3 讨论
达拉非尼联合曲美替尼易引发皮肤不良反应导致其在黑色素瘤患者中的临床应用受到限制。许多临床试验也报道了达拉非尼联合曲美替尼在使用过程中引起皮肤不良反应的统计结果。因此,我们对现有研究进行汇总分析,旨在为临床医生提供更多的循证参考。本研究显示,达拉非尼联合曲美替尼最常发生的皮肤不良反应是皮疹,其次是红斑、瘙痒、干性皮肤、痤疮样皮炎、角化过度、脱发和皮肤鳞状细胞癌,发生率最低的是皮肤乳头状瘤(1%)。与BRAF 抑制剂单药治疗相比,达拉非尼联合曲美替尼治疗黑色素瘤会降低皮肤不良反应的发生。
非肿瘤性皮肤不良反应,如皮疹、痤疮样皮炎、脱发、干性皮肤等,其严重程度与药物的暴露和剂量成正比〔18〕。轻度或中度皮肤不良反应不需要中断治疗,可以通过调整剂量或支持治疗控制〔19〕,在某些情况下还可以局部使用糖皮质激素〔20〕。本研究表明皮疹是最常见的皮肤不良反应,通常在治疗后2~6 周内发生,表现为红斑疹和面部、头皮、躯干受累区域的脱屑〔21〕。角化过度发生率约为7%,通常在治疗后几天到几周内发生,表现为麻木、红斑、细软的角化斑块、水泡或老茧〔21〕,外用糖皮质激素通常可以缓解症状〔20〕。脱发通常在治疗后2~16 周内发生,表现为轻度稀疏或斑驳的头发,可使用0.05%的丙酸氯倍他索治疗〔22〕,其发病机制可能是BRAF 抑制剂中断了毛发基质细胞的生长,导致毛囊消退〔20〕。肿瘤性皮肤不良反应(如:皮肤鳞状细胞癌、皮肤乳头状瘤)被认为是BRAF 抑制剂单药治疗的特征性不良反应,发生率约为14%~26%〔23〕,其特点是角质形成细胞过度增殖,通常在用药约16 周后出现,可以通过简单的切除术进行治疗〔20〕,也有研究表明口服维甲酸类维生素A 可能有预防效果〔24〕。目前认为原因可能是丝裂原活化蛋白激酶(mitogenactivated protein kinase,MAPK)途径的反常激活与先前存在的原癌基因突变引起上游信号激活〔25〕,诱导了角化过度症、角化棘皮瘤向鳞状细胞癌的演变。另外,相比于BRAF 抑制剂单药治疗,联合用药整体上降低了所有等级的皮肤不良反应的发生。这可能是因为曲美替尼的加入抑制了下游MEK,防止MAPK 途径的反常激活〔25〕。总之,对于达拉非尼联合曲美替尼所引起的皮肤不良反应,临床医生应该加强管理和监测并定期随访。本研究具有一定局限性:(1)部分纳入研究样本量相对较小,较小的样本量更有可能导致对毒性反应的高估;(2)由于Meta分析中研究人员对皮肤不良反应的观察和记录存在差异,可能会增加研究的临床异质性;(3)由于纳入研究大多来自西方,缺乏亚洲国家的数据,可能造成一定的选择偏倚;(4)基于漏斗图和对称性分析,没有发现显著的发表偏倚,但证据并不充分。因此,需要进一步的大规模试验来验证我们的发现。
研究显示皮疹的发生与激活表皮生长因子受体抑制剂治疗反应呈正相关〔26〕,作为相同作用途径的BRAF 和MEK 抑制剂,推测皮疹的发生与达拉非尼和曲美替尼治疗反应可能也存在相同的关联,需要进一步验证。除此之外,使用糖皮质激素管理免疫相关不良事件可能会影响免疫疗法的疗效〔27〕,因此,糖皮质激素用于管理达拉非尼和曲美替尼致皮肤不良反应是否也会影响其疗效值得进一步探索。

