吡唑醚菌酯原药中硫酸二甲酯测定方法的改进
颜 聪,孙海建,薛建强,潘朝晖
(江苏龙灯化学有限公司,江苏昆山 215300)
吡唑醚菌酯(pyraclostrobin),化学名称为N-[2- [[1-(4-氯苯基)吡唑-3-基]氧甲基]苯基]-N-甲氧基氨基甲酸甲酯,是德国巴斯夫公司于1993年发现的一种兼具吡唑结构的甲氧丙烯酸甲酯类线粒体呼吸抑制剂,通过抑制病原菌线粒体呼吸作用,最终导致细胞死亡,具有保护、冶疗、叶片渗透传导作用,主要用于防冶多种作物真菌病害[1]。硫酸二甲酯是生产吡唑醚菌酯的一个重要原料,为无色或微黄色,略有葱头气味的油状易燃性液体。硫酸二甲酯高毒,具有强烈的刺激性和腐蚀性,对眼睛、上呼吸道有强烈刺激作用,对皮肤有强腐蚀作用。
欧盟规定吡唑醚菌酯原药中硫酸二甲酯质量分数≤1 μg/g,国内规定硫酸二甲酯质量分数≤3 μg/g,因此需要对硫酸二甲酯量进行控制。HG/T 5235—2017[2]中有关于硫酸二甲酯的测定方法,但灵敏度低,吡唑醚菌酯原药试样浓度为1 g/mL 才能满足定量要求,对仪器和色谱柱影响大,且该方法选用的三氯甲烷溶剂属于易制毒管制类试剂,不便于实际生产使用。基于此,本文采用气相色谱-质谱联用仪按照农药产品质量分析方法确认指南[3]要求开展了吡唑醚菌酯原药中硫酸二甲酯含量的测定方法验证。
1 材料与方法
1.1 仪器与试剂
GCMS-QP2010NC PLUS 气相色谱-三重四级杆质谱联用仪,岛津(中国)有限公司;XS 205 型分析天平,梅特勒-托利多国际贸易(上海)有限公司;SK5200型超声波清洗器;有机过滤器(孔径0.22 μm);硫酸二甲酯标样(质量分数≥98.0%,上海安谱实验科技股份有限公司);吡唑醚菌酯原药(山东康乔生物科技有限公司);乙酸乙酯,色谱纯(美国天地有限公司)。
1.2 色谱条件
色谱条件:色谱柱为Agilent DB-5MS (30 m ×0.32 mm,0.25 µm);柱温为程序升温,起始温度50 ℃,保持8 min,以50 ℃/min 的速率升至250 ℃后保持13 min;进样模式为分流比10;载气为氮气,纯度≥99.999%;流速为1.0 mL/min;进样口温度为150 ℃;进样体积为1.0 µL;
质谱条件:电离方式为电子轰击源(EI);电离能量1 500 eV;接口温度为250 ℃;离子源(EI)温度为230 ℃;扫描模式:定性分析时采用全扫描方式,质量数范围为 30~500,硫酸二甲酯碎片离子m/z=66、95、125;定量时采用提取离子方式,硫酸二甲酯提取离子m/z=95;溶剂为乙酸乙酯;硫酸二甲酯的保留时间约3.7 min。
1.3 溶液配制
1.3.1 标准溶液的制备
称取约10 mg 硫酸二甲酯标样(精确至0.2 mg)于50 mL 容量瓶中,加入适量乙酸乙酯,超声溶解,冷却至室温定容,移取20 µL 于50 mL 容量瓶中,乙酸乙酯定容,摇匀备用。
1.3.2 试样溶液的制备
称取约2 000 mg 试样(精确至0.2 mg)于50 mL容量瓶中,加入适量乙酸乙酯,超声溶解,冷却至室温后定容,摇匀备用。
1.4 测定
在上述操作条件下,待仪器稳定后连续注入数针标样溶液,直至相邻2 针硫酸二甲酯标样溶液的响应值相对变化<10%后,按下列顺序进样:标样溶液、试样溶液、试样溶液、标样溶液。根据外标法计算杂质的含量。硫酸二甲酯标样的提取离子色谱图见图1,吡唑醚菌酯原药中硫酸二甲酯(加标测定)的提取离子色谱图见图2。
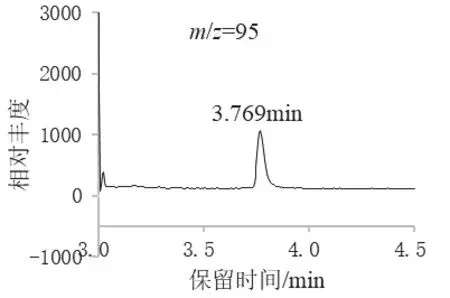
图1 硫酸二甲酯标样离子色谱图

图2 吡唑醚菌酯原药中硫酸二甲酯离子色谱图
1.5 计算
对2 次试样溶液及2 次标样溶液中硫酸二甲酯的定量峰面积[提取离子(m/z)=95]进行平均,试样中硫酸二甲酯的质量分数ω(µg/g)按下式计算:
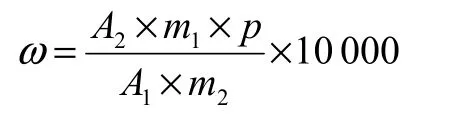
式中:A1为标样中硫酸二甲酯的峰面积;A2为试样中硫酸二甲酯的峰面积;m1为硫酸二甲酯标样的质量(mg);m2为试样的质量(mg);p为硫酸二甲酯标样的纯度(%);10 000 为%转换为µg/g。
2 结果与讨论
2.1 色谱条件的设定
影响气相色谱方法开发的主要参数为:色谱柱固定相、色谱柱规格、进样口温度、色谱柱温度、检测器温度等,其他参数可采用气相色谱分析的典型情况确定,如0.32 mm 内径的色谱柱柱流速约为1 mL/min 等。下面将从色谱柱选择、仪器参数设定两方面详细讲述。
2.1.1 色谱柱的选择
根据相似相溶原理选择固定相,即分离非极性化合物时应选择非极性固定液,分离极性化合物时应选择极性固定液。相同条件下极性越大的固定相色谱柱寿命越短,故在能够达到分离要求时,选择极性弱的固定相色谱柱。硫酸二甲酯分子极性弱,根据以上原理,应选择非极性或弱极性的色谱柱,本文选择极性弱的Agilent DB-5MS。
2.1.2 仪器参数的设定
GCMS 初始色谱条件仪器参数的设定主要包括:进样口温度、离子源温度、柱流速、分流比、色谱柱温度及定量和定性质荷比。进样口温度主要由试样的沸点范围决定,还要考虑色谱柱的使用温度。进样口温度高一些有利,一般要接近试样中沸点最高的组分的沸点,但要低于易分解组分的分解温度。硫酸二甲酯在188 ℃进行分解,因此进样口温度选择150 ℃。
根据GCMS 条件下硫酸二甲酯标准品的碎片离子选择合适的定性及定量质荷比。
2.2 方法验证
2.2.1 分析方法的线性关系
配制5 个不同质量浓度的硫酸二甲酯标准溶液,按上述色谱条件进行测定,见表1,以质量浓度(μg/mL)为自变量(x),提取离子模式下,硫酸二甲酯m/z=95 时的相对丰度作为因变量(y)进行回归分析,结果表明硫酸二甲酯质量浓度为0.02~0.60 μg/mL,其相对丰度与质量浓度之间的线性回归方程式为y=27 880x-3.154,相关系数为0.999 9。
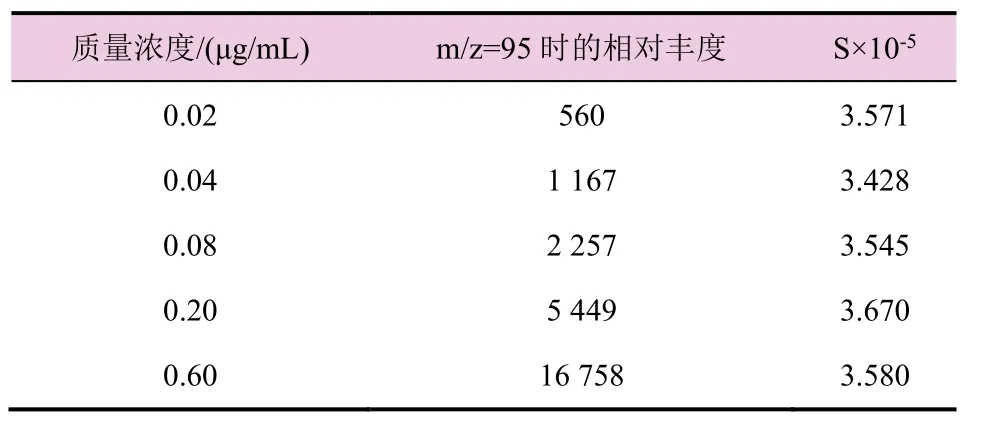
表1 分析方法的线性关系
2.2.2 分析方法的精密度
分别准确称取7 份吡唑醚菌酯原药2 g,分别加入12.0 µg/mL 的硫酸二甲酯标准溶液0.4 mL,定容后测定,见表2。可见,测得被测目标的相对标准偏差和变异系数分别为2.38%和9.33%。

表2 分析方法的精密度
2.2.3 分析方法的准确度
分别称取3 份吡唑醚菌酯原药2 g,分别加入12.0 µg/mL 的硫酸二甲酯标准溶液0.3、0.4、0.5 mL,再按1.3 节处理后上机进行分析,每个试样重复进样2 次,测得各目标被测物回收率为95.6%~106.2%,平均回收率为101.3% (表3)。
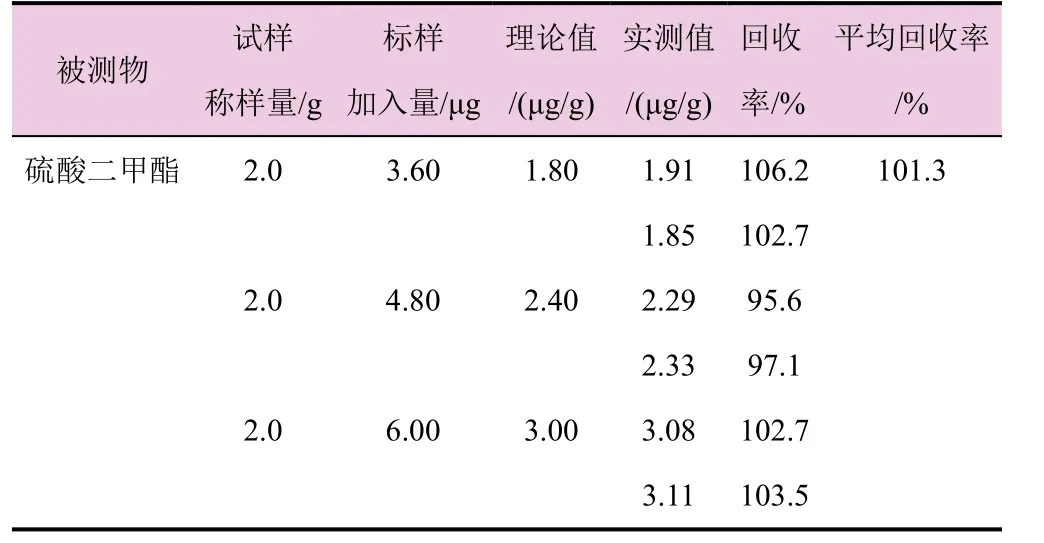
表3 分析方法的准确度
2.2.4 分析方法的检出限及定量限
本方法中硫酸二甲酯定量限为0.15 μg/g,满足国内要求≤3 μg/g 和欧盟要求≤1 μg/g。
硫酸二甲酯的定量限提取离子色谱图见图3。
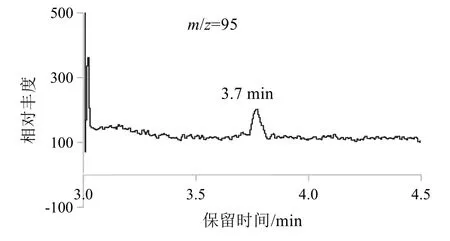
图3 硫酸二甲酯定量限的提取离子色谱图
3 结 论
本文采用气相色谱-三重四级杆串联质谱仪建立了测定吡唑醚菌酯原药中硫酸二甲酯的定性定量分析方法。该方法对HG/T 5235—2017 推荐方法的改进,采用Agilent DB-5MS 色谱柱,选用非易制毒管制类、对试样溶解性好的乙酸乙酯作为溶剂。相对于HG/T 5235—2017,该方法使所使用的吡唑醚菌酯原药试样浓度减少至0.04 g/mL,检出限降低至0.05 μg/g,灵敏度提高200 倍以上,且目标物在测试浓度范围内线性关系良好,非常适于生产实际中简便快捷地测定吡唑醚菌酯原药中硫酸二甲酯含量。

