基于超声图像形态学定量特征的乳腺肿块恶性风险列线图预测模型构建及应用
侯 银 张盼盼 张青陵
乳腺癌居女性恶性肿瘤发病率首位且呈逐年上升趋势[1],早期准确诊断乳腺癌对于临床制定治疗决策至关重要[2]。超声是我国乳腺癌筛查的主要方法,乳腺影像报告和数据系统(BI-RADS)的普及应用使得超声报告逐渐规范和统一。但BI-RADS 采用人为规定的特征描述来分类图像,缺少量化参数,导致诊断高度依赖于超声医师的经验积累和培训经历,不同水平或年资的操作者对图像的解读具有主观性,不利于临床精准决策[3-4],因而如何实现对乳腺肿块超声图像的定量评估和精准量化预测是临床面临的重要问题。在临床实际工作中,不同品牌、型号或等级的超声仪器在图像后处理方法不同,乳腺肿块图像的分辨率及成像质量也有所区别,而乳腺肿块超声图像的形态学特征受仪器型号和图像参数设置影响较小,且与病理组织学特征关系密切[5-6]。本研究旨在应用机器学习技术构建基于超声图像形态学定量特征的乳腺肿块恶性风险列线图预测模型,并以互联网在线应用程序的方式呈现,增强其实用性。
资料与方法
一、研究对象
选取 2019 年 1 月至 2020 年 10 月我院经病理确诊的乳腺肿块患者1046 例,均为女性,按7∶3 比例随机分为模型训练集和外部验证集,其中训练集732例,患者年龄18~79 岁,良性302 例,中位年龄37(26,45)岁;恶性 430 例,中位年龄 53(42,65)岁。验证集 314 例,患者年龄19~71 岁,良性115 例,中位年龄41(28,47)岁;恶性199例,中位年龄52(42,61)岁。训练集与验证集中恶性肿块占比比较差异无统计学意义。将训练集和验证集按年龄段分为<40 岁、40~50 岁、≥50~60 岁和≥60 岁 4 组,训练集中分别为 159、265、201、107 例,验证集中分别为56、110、98、50例,两数据集各年龄段例数的分布比较差异无统计学意义。所有患者均在超声检查之后行超声引导下细针穿刺活检术或手术切除,且取得明确的病理诊断结果。排除标准:①病理结果不确定;②临床资料缺失;③有放疗或化疗史;④图像记录为宽景或全景成像;⑤单幅B 型超声图像不能完整显示肿块边界。本研究经我院医学伦理委员会批准,所有患者均签署知情同意书。
二、仪器与方法
1.图像采集:使用西门子Acuson S 3000 彩色多普勒超声诊断仪,线阵探头,频率4.0~12.0 MHz。患者取平卧位,充分暴露乳房和腋窝,由两名超声医师调节优化图像质量后,采集病灶最大径线切面图像并以JPEG格式存储。
2.图像形态学特征定量分析:对于多发性乳腺肿块的病例,仅保留有病理结果的肿块图像作为目标病灶用于测量分析。由同一超声医师使用ImageJ 分析软件(美国国立卫生研究院开发,下载地址:https://imagej.nih.gov,版本号2.0.0-rc-69)描记肿块轮廓,自动输出形态特征定量数据(图1A),分别为:①长短径比值(AR),表示沿着肿块轮廓拟合一个最近似的椭圆形,计算椭圆形长径与短径比值(图1B);②圆润度(C),是兼顾肿块形状和边缘光整程度的度量,取值范围0~1;肿块形状越接近正圆形、同时边缘越光整,C值越接近1(图1C);③凹凸度(S),表示肿块边缘的凹凸程度,取值范围0~1,边缘越光整,S 值越接近1(图1D);④费雷特角度修正(MFA),表示肿块轮廓线最远两点之间的连线与图像水平轴之间的夹角,取值范围0°~90°,用以度量肿块的方位,当MFA 为0°时,表示肿块长轴在图像上呈水平位,MFA 为90°时表示呈垂直位(图1E)。
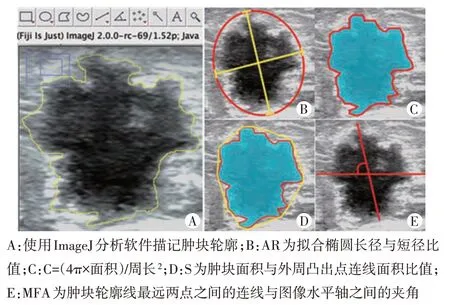
图1 乳腺肿块超声图像形态学定量特征参数测量示意图
3.重复性检测:随机选取60 例患者,由该医师和另一超声医师于2周后再次对其图像形态特征定量分析,进行观察者间及观察者内重复性检验。
4.质量控制:两名超声检查医师分别具有7 年和9 年乳腺超声检查经验。两名进行图像描记的超声医师分别具有4 年和3 年乳腺超声规范化培训和从业经历,并接受统一的ImageJ 分析软件操作培训。描记图像前,将良、恶性乳腺肿块全部图像放置在同一文件夹,使用R 语言软件添加随机索引编号并重新混合排列文件次序;两名医师均在双盲情况下完成图像描记。
5.病理诊断:病理组织均来自超声引导下细针穿刺活检标本或手术标本,通过标准诊断程序进行组织学处理,由高年资病理医师完成病理报告。
三、统计学处理
应用R-Studio(R4.0.2)软件,计数资料比较行Pearsonχ2检验。根据Shapiro-Wilk 正态性检验结果,计量资料以M(QR)表示,单因素分析行Wilcoxon 秩和检验。以病理结果为标准,采用机器学习广义线性模型(generalized linear model,GLM)分析筛选诊断乳腺恶性肿块的定量特征,构建多元回归预测模型并绘制列线图(Nomogram)[7]。采用组内相关系数(ICC)评估观察者间及观察者内重复性,ICC>0.75 表示重复性较好。绘制受试者工作特征(ROC)曲线评价模型的区分度,曲线下面积(AUC)比较行Delong 检验;绘制校准曲线评价模型预测恶性风险的校准度。P<0.05 为差异有统计学意义。
结 果
一、单因素和多因素分析
1.单因素分析显示,训练集和验证集中乳腺恶性肿块 AR、C 和 S 均低于良性,MFA 高于良性,差异均有统计学意义(均P<0.05);且患者年龄比较差异均有统计学意义(均P<0.05)。见图2和表1,2。
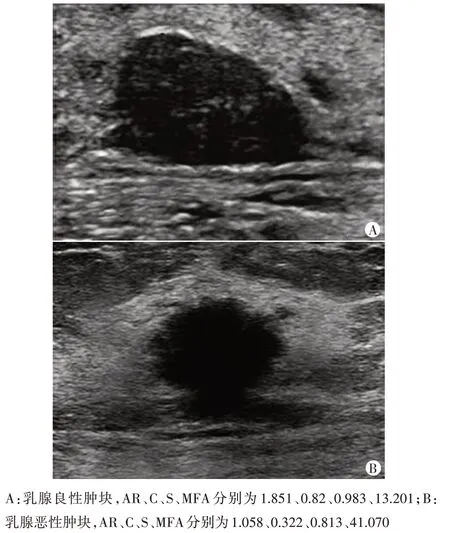
图2 训练集中良、恶性乳腺肿块声像图
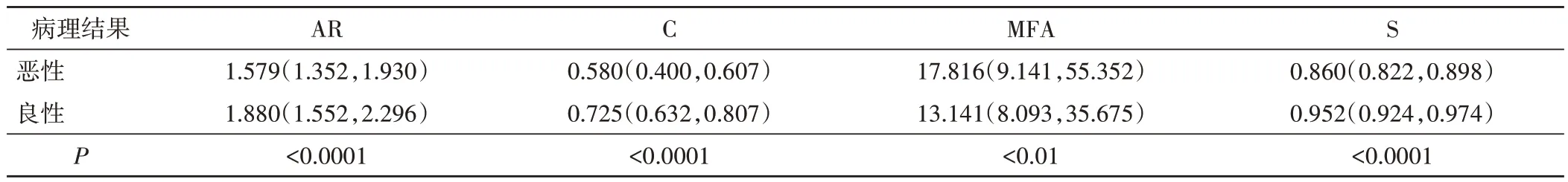
表1 单因素分析训练集中良、恶性乳腺肿块超声图像形态学定量特征参数比较[M(QR)]
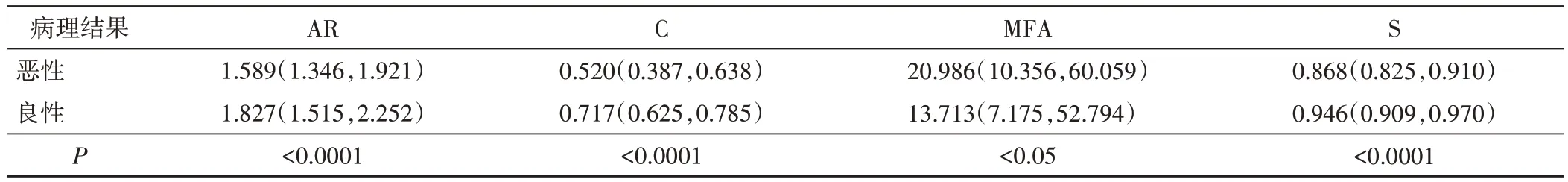
表2 单因素分析验证集中良、恶性乳腺肿块超声图像形态学定量特征参数比较[M(QR)]
2.将单因素分析差异有统计学意义的变量,即AR、C、MFA、S和患者年龄数据全部纳入机器学习广义线性模型GLM算法,采用逐步回归法进行多因素分析,剔除无效变量,结果显示AR、C和患者年龄是预测乳腺肿块恶性风险的独立危险因素;随着AR、C下降及患者年龄增大,乳腺肿块恶性风险呈上升趋势(均P<0.05)。见表3。
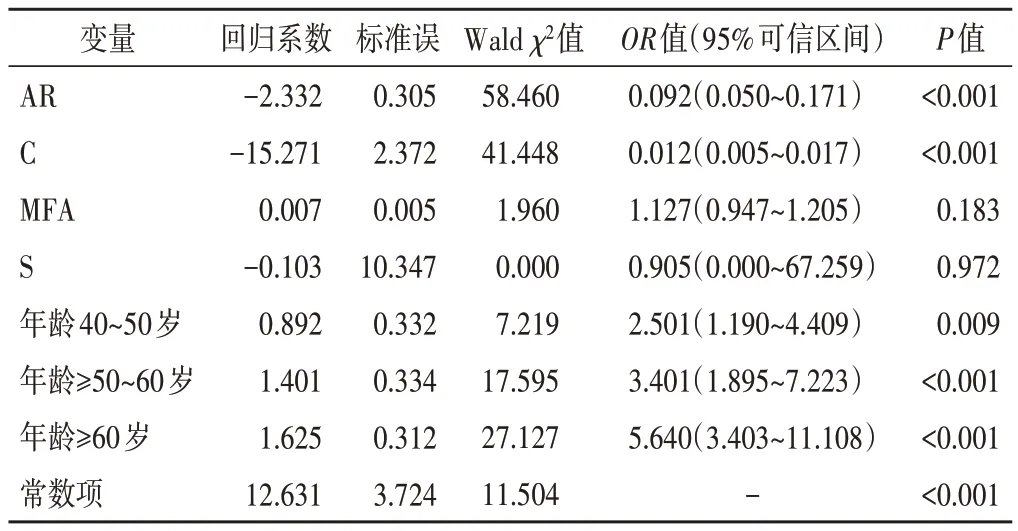
表3 机器学习GLM多因素分析结果
3.各乳腺肿块超声图像形态学定量特征参数在观察者内和观察者间ICC均>0.75,具有较好的可重复性。见表4。
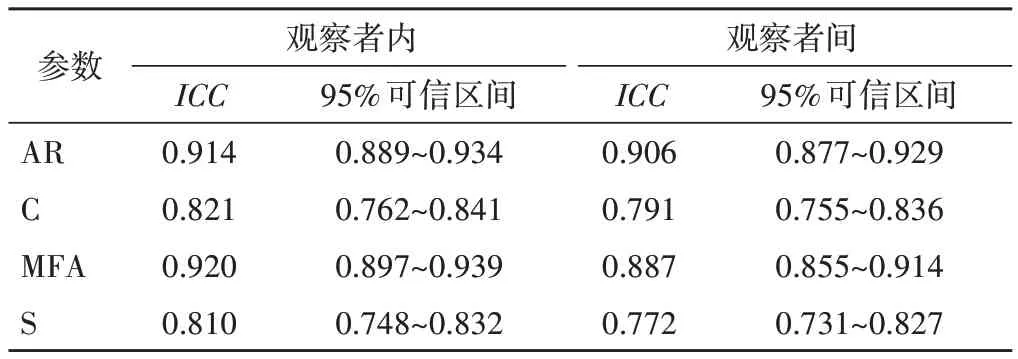
表4 乳腺肿块超声图像形态学定量特征参数的重复性检验
二、列线图模型及在线应用程序
1.根据机器学习GLM 算法分析筛选出的独立危险因素AR、C 和患者年龄构建列线图模型,模型中AR、C 和患者年龄均被赋予相应的分值,计算三者总得分即可在列线图上标记获得对应的恶性风险概率预测值。见图3。
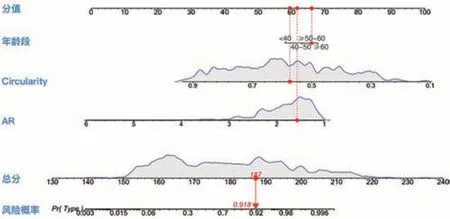
图3 基于超声图像形态学定量特征的乳腺肿块恶性风险预测列线图
2.为进一步提高该列线图模型的可操作性,设计制作并发布了一款互联网在线免费应用程序(网址:https://qingling.shinyapps.io/BreastSonoNomogram/。注 :该程序当前仅用于研究目的)。研究人员通过登录该网址,按照本研究介绍的方法提取并输入相关特征数据,即可获得对应乳腺肿块的恶性风险概率和95%可信区间,见图4。如图中蓝色标记所示某病例,输入乳腺肿块AR 为2.494,C为0.92,模型预测显示≥50~60岁组恶性风险概率为96.8%,95%可信区间为93.2%~98.5%。
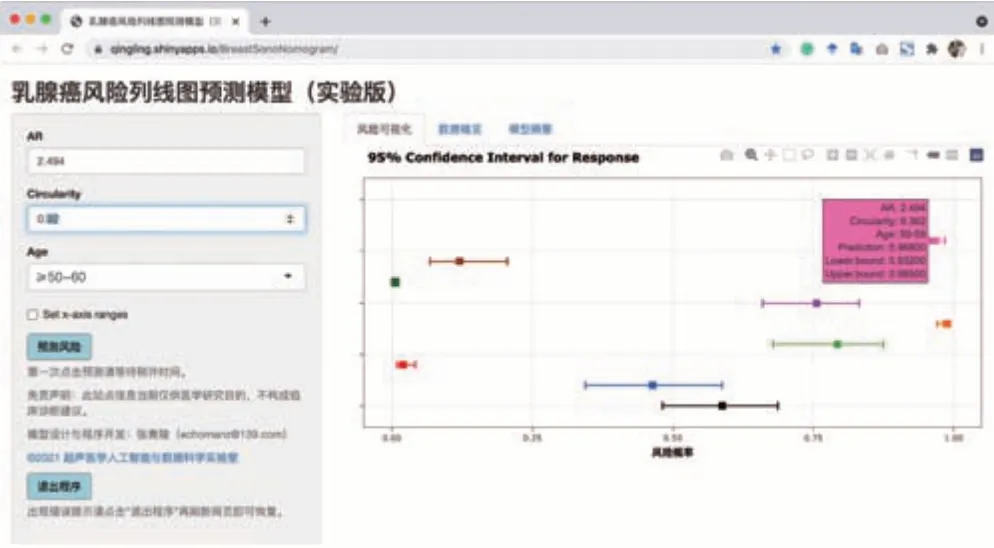
图4 互联网在线应用程序显示界面。左侧为数据输入区;右侧为可视化显示乳腺肿块恶性风险概率及95%可信区间
三、ROC曲线和校准曲线分析
1.ROC 曲线分析显示,训练集内部验证的AUC 为0.931,敏感性为88.1%,特异性为85.4%;验证集外部验证的AUC 为0.901,敏感性为84.2%,特异性为85.8%;二者AUC比较差异无统计学意义(P=0.121)。见图5A。
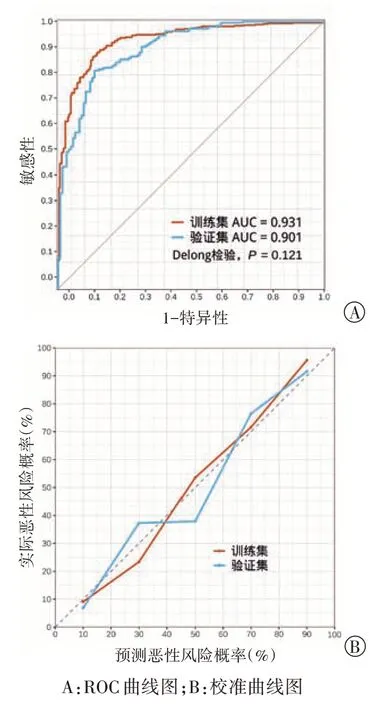
图5 列线图预测模型效能分析
2.校准曲线分析显示,训练集和验证集的校准曲线均与图像对角线方向基本一致,且与对角线重合度较好,尤其当实际恶性风险值>50%时,模型预测值未出现明显高估或低估,显示预测模型的校准度良好,其预测恶性风险概率与实际恶性风险无明显偏离。见图5B。
讨 论
BI-RADS 采用特征术语对乳腺肿块超声图像进行描述[8],这种描述性定性方法高度依赖于超声诊断医师的视觉感受、经验积累和规范化培训经历,不同水平或年资的超声医师对图像的解读具有主观性。多项研究[3-4,9]显示,超声 BI-RADS 在观察者间Kappa值为0.28~0.83,因此亟需构建一种更加客观的图像量化分析方法。既往研究[10-12]多综合乳腺肿块的回声和形态学特点进行分析,但在临床实际工作中,不同品牌、型号或等级的超声仪器在图像后处理方法上有所不同,乳腺肿块图像的分辨率及成像质量也有所区别。而乳腺肿块超声图像的形态学特征则受仪器型号和图像参数设置影响较小,可以基本反映乳腺病灶的大体病理形态。本研究采用ImageJ 分析软件对乳腺肿块的超声形态学特征进行定量分析,定量参数包括AR、C、MFA 和S,分别用精确数值度量了肿块图像的长短径比值、圆润度、生长方向和边缘光整度4项形态学特征,且测量结果具有良好的可重复性(ICC均>0.75)。既往研究[5]表明,恶性肿块的形态学特征包括不规则形态、浸润性纵向生长及边缘呈针状、微叶状或成角。本研究中,良、恶性乳腺肿块各项形态学特征定量参数比较差异均有统计学意义(均P<0.05),与上述研究结果一致,表明形态学定量特征参数能够对肿块的形状、边缘及生长方向进行更为精准量化,从而更加准确地反映肿块形态的不规则程度和边缘的不规整程度。
对于乳腺肿块患者个体而言,治疗决策具有异质性,受多种因素的影响,因此建立一个针对个体的、精准的癌症预测模型具有重要的临床价值。而随着数据采集和分析技术的日益提高,临床预测模型作为风险与获益评估的量化工具,采用更大量、更丰富的数据和更加复杂的机器学习模型算法,以更精准的结果服务于医师、患者及医疗决策者,因此其应用也越来越普遍。本研究通过机器学习GLM 模型算法筛选出乳腺恶性肿块形态学定量特征参数中的独立危险因素即AR、C 和患者年龄,构建列线图风险预测模型,并分别进行内部验证和外部验证,达到了良好的良、恶性乳腺肿块区分度和校准度。新近一些关于乳腺癌超声预测模型的研究[13-15]中,均使用了BI-RADS 定性描述作为构建模型的预测因子,分别对肿块的良恶性及进一步降低4A 类肿块风险做出了预测,各模型的AUC 为0.747~0.955。与上述研究构建的模型相比,本研究使用更客观的定量参数作为模型预测变量,应用机器学习技术构建模型,同时为了进一步提升模型的实用性,本研究还创新性地以互联网在线应用程序的方式呈现模型,使得预测过程和结果可视化,模型更具有可操作性,方便对患者进行评估。
本研究的局限性:①为回顾性研究,尚缺乏前瞻性、多中心数据的进一步验证;②入组对象排除了尺寸较大导致单幅B型超声图像不能完整显示轮廓的肿块,可能产生偏倚。本研究所得临床预测模型及其应用价值有待前瞻性及更大样本数据的评估和验证。
综上所述,本研究对乳腺肿块形态学特征实现了定量表达,且测量结果具有良好的可重复性,其中AR、C 和患者年龄是预测乳腺肿块恶性风险的独立危险因素。应用机器学习技术构建的乳腺肿块恶性风险列线图预测模型具有较高的诊断效能,而以互联网在线应用程序方式呈现模型使其更加具有可操作性和实用性,将有助于对患者进行个体化预测和治疗决策。

