来曲唑对多囊卵巢综合征患者性激素水平的影响
徐淑静,王小燕
(1.无锡市锡山人民医院鹅湖分院妇产科;2.无锡市锡山人民医院鹅湖分院检验科,江苏 无锡 214116)
多囊卵巢综合征(polycystic ovary syndrome,PCOS)是一种多病因、临床表现多态性的内分泌疾病,多见于育龄期女性,临床主要表现为月经失调、月经不规律或者闭经、月经来潮后淋漓不止、毛发浓密及面部痤疮等,且PCOS所引起的患者机体内排卵功能异常是导致育龄期女性不孕的常见病因之一。氯米芬通过竞争性占据下丘脑雌激素受体,干扰内源性雌激素的负反馈,且正反馈可促进排卵前促性腺激素的释放,从而发挥促进排卵的作用,但该药物会造成患者的宫颈黏膜粘连与子宫内膜受损[1-2]。来曲唑是非甾体选择性第三代芳香酶抑制剂,其通过抑制芳香化酶活性来阻止雄激素向雌激素转化,使雌激素水平降低,进而增加患者体内内源性促性腺激素水平,最终促进患者卵泡得以正常发育[3-4]。但目前对于来曲唑促排卵的最佳应用剂量是具有争议的,在不同的研究报道中,所推荐的最佳使用剂量各有不同。基于此,本研究旨在探讨来曲唑对PCOS患者血流搏动指数(PI)、血流阻力指数(RI)及血清雌二醇(E2)、催乳素(PRL)、黄体生成素(LH)、卵泡刺激素(FSH)水平的影响,现报道如下。
1 资料与方法
1.1 一般资料 回顾性分析2019年1月至2020年6月就诊于无锡市锡山人民医院鹅湖分院的78例PCOS患者的临床资料,按不同的治疗方案分为氯米芬组(给予100 mg/d氯米芬治疗)、来曲唑A组(在氯米芬组的基础上给予2.5 mg/d来曲唑治疗)及来曲唑B组(在氯米芬组的基础上给予5.0 mg/d来曲唑治疗),各26例。氯米芬组患者年龄20~34岁,平均(28.46±5.16)岁;病程1~4年,平均(2.81±0.62)年;体质量指数(BMI)20.4~30.3 kg/m2,平均(26.12±3.41) kg/m2。来曲唑 A 组患者年龄21~34岁,平均(28.94±4.43)岁;病程1~4年,平均(2.69±1.15)年;BMI 21.4~30.1 kg/m2,平均(26.32±2.41) kg/m2。来曲唑B组患者年龄21~35岁,平均(28.72±3.41)岁;病程1~4年,平均(2.47±1.22)年;BMI 21.6~31.2 kg/m2,平均(27.32±2.26) kg/m2。3 组患者年龄、病程、BMI等一般资料对比,差异无统计学意义(P>0.05),组间具有可比性。纳入标准:符合《多囊卵巢综合征中国诊疗指南》[5]中的相关诊断标准者;近期未接受激素类药物治疗者;行子宫输卵管造影或超声检查提示双侧输卵管通畅,宫腔形态未见明显异常者等。排除标准:对氯米芬、来曲唑过敏者;急性阴道炎、盆腔炎疾病者;因卵巢早衰、高泌乳素血症及垂体或下丘脑性闭经引起的排卵障碍疾病者;临床资料不全者等。本研究在院内医学伦理委员会批准下实施。
1.2 治疗方法 给予氯米芬组患者枸橼酸氯米芬片[MEDOCHEMIE LTD (CENTRAL FACTORY),注册证号H20140688,规格:50 mg/片]口服治疗,月经的第3天开始服用,50 mg/次,1次/d。来曲唑A组患者在氯米芬组的基础上给予来曲唑片(江苏恒瑞医药股份有限公司,国药准字H19991001,规格:2.5 mg/片)口服治疗,月经来潮第3天开始服用,2.5 mg/次,1次/d。来曲唑B组患者在氯米芬组的基础上给予来曲唑片口服治疗,月经来潮第3天开始服用,5 mg/次,1次/d。3组患者均连续服药5 d,并均于治疗后定期随访12个月。
1.3 观察指标 ①子宫内膜容受性,分别于治疗前后采用彩色多普勒超声仪检测3组患者子宫内膜厚度,子宫动脉RI及PI水平。②性激素水平,分别于治疗前后采集3组患者空腹静脉血5 mL,经3 000 r/min转速离心10 min取上层血清,采用化学发光法检测血清E2、LH、PRL、FSH水平。③排卵与妊娠情况,对3组患者治疗后12个月内的排卵、妊娠情况进行记录并统计,其中妊娠情况可分为流产、顺产和剖宫产,优良妊娠率=顺产率+剖宫产率。④不良反应,比较3组患者治疗期间恶心、关节痛、潮热发生情况。
1.4 统计学方法 使用SPSS 23.0统计软件对数据进行分析,计量资料以(±s)表示,两组间比较采用t检验,多组间比较采用重复测量方差分析;计数资料以[例(%)]表示,两组间比较采用χ2检验,多组间比较采用χ2趋势检验。以P<0.05为差异有统计学意义。
2 结果
2.1 子宫内膜容受性 与治疗前比,治疗后3组患者子宫内膜厚度均显著升高,3组患者RI、PI水平均显著降低;与氯米芬组比,治疗后来曲唑A、B组患者子宫内膜厚度均显著升高,且来曲唑B组显著高于来曲唑A组;而来曲唑A、B组患者RI、PI水平均显著降低,且来曲唑B组显著低于来曲唑A组,差异均有统计学意义(均P<0.05),见表 1。
表1 3组患者子宫内膜容受性比较(±s)
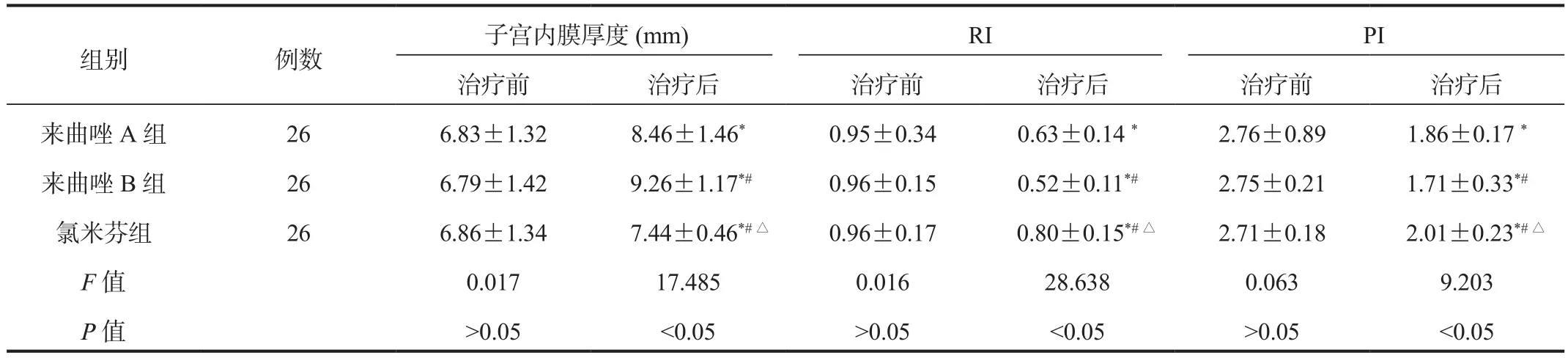
表1 3组患者子宫内膜容受性比较(±s)
注:与治疗前比,*P<0.05;与来曲唑A组比,#P<0.05;与来曲唑B组比,△P<0.05。RI:阻力指数;PI:搏动指数。
组别 例数子宫内膜厚度(mm) RI PI治疗前 治疗后 治疗前 治疗后 治疗前 治疗后来曲唑 A 组 26 6.83±1.32 8.46±1.46* 0.95±0.34 0.63±0.14 * 2.76±0.89 1.86±0.17 *来曲唑 B 组 26 6.79±1.42 9.26±1.17*# 0.96±0.15 0.52±0.11*# 2.75±0.21 1.71±0.33*#氯米芬组 26 6.86±1.34 7.44±0.46*#△ 0.96±0.17 0.80±0.15*#△ 2.71±0.18 2.01±0.23*#△F值 0.017 17.485 0.016 28.638 0.063 9.203 P值 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05
2.2 性激素水平 与治疗前比,治疗后3组患者血清E2、PRL、LH水平均显著降低,血清FSH水平均显著升高;与氯米芬组比,治疗后来曲唑A、B组患者血清E2、PRL、LH水平均显著降低,且来曲唑B组显著低于来曲唑A组,来曲唑A、B组患者血清FSH水平均显著升高,且来曲唑B组显著高于来曲唑A组,差异均有统计学意义(均P<0.05),见表 2。
表2 3组患者性激素水平比较(±s)

表2 3组患者性激素水平比较(±s)
注:与治疗前比,*P<0.05;与来曲唑A组比,#P<0.05;与来曲唑B组比,△P<0.05。E2:雌二醇;PRL:催乳素;LH:黄体生成素;FSH:卵泡刺激素。
组别 例数 E2(pmol/L) PRL(ng/mL) LH(U/L) FSH(U/L)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后来曲唑A组 26 152.61±17.43 136.03±10.11* 19.31±3.31 14.61±2.13 * 15.76±5.51 9.86±2.18* 4.76±0.89 6.21±1.43*来曲唑B组 26 153.11±19.14 129.89±11.23*# 19.37±3.26 11.54±2.11*# 15.58±3.28 8.83±1.21*# 4.62±0.71 6.97±1.16*#氯米芬组 26 153.04±16.21 145.03±10.18*#△ 19.41±3.28 16.83±2.17*#△ 15.41±4.15 11.61±1.49*#△ 4.50±0.64 5.01±1.06*#△t值 0.006 13.625 0.006 40.180 0.041 18.262 0.774 16.874 P值 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05
2.3 排卵与妊娠情况 与氯米芬组比,来曲唑A、B组患者排卵率均显著升高,且来曲唑B组显著高于来曲唑A组;与氯米芬组比,来曲唑B组患者的优良妊娠发生率显著升高,来曲唑B组优良妊娠发生率显著高于来曲唑A组,差异均有统计学意义(均P<0.05),见表3。

表3 3组患者排卵、妊娠情况比较[例(%)]
2.4 不良反应 3组患者不良反应总发生率比较,差异无统计学意义(P>0.05),见表4。

表4 3组患者不良反应发生情况比较[例(%)]
3 讨论
PCOS是一种内分泌代谢紊乱,主要累及卵巢,但可影响全身的代谢,好发于育龄期女性的生殖系统疾病,当出现该疾病时,患者机体内可出现排卵功能障碍、雄激素含量过高、卵巢增大呈多囊样等特征性改变。氯米芬是临床上常用于促进PCOS患者排卵的药物,其是一种拮抗雌激素受体的药物,一方面通过拮抗促性腺激素释放激素神经元,使内源性雌激素受体减少,抑制下丘脑的负反馈,使得FSH的分泌增加,兴奋卵巢的活性,从而刺激卵泡生长、发育[6-7];另一方面氯米芬具有较弱的雌激素作用,可使机体内的卵泡刺激素、黄体生成素及睾酮水平升高并达峰值,从而促进排卵,但临床应用时,由于其对子宫内膜和宫颈黏液的负性作用,使子宫内膜发育和胚胎发育不同步,从而影响胚胎着床和发育,同时还会出现多个卵泡同时发育、高排卵率、低妊娠率、多胎妊娠率增加等现象[8]。
来曲唑为一种人工合成的苄三唑类衍生物,通过抑制芳香化酶,使雌激素水平下降,是一种非常强的抗雌激素药物[9-10]。PCOS患者发病时,由于雄性激素分泌过多,影响孕激素的产生,致使子宫内膜缺乏性激素的支撑,从而导致子宫内膜变薄,同时影响卵泡膜厚度和子宫收缩频率,使子宫内膜出现血流灌注现象,从而影响子宫动脉PI、RI水平[11-12]。本研究结果显示,与氯米芬组比,治疗后来曲唑A组、来曲唑B组患者子宫内膜厚度、排卵率均显著升高,且来曲唑B组显著高于来曲唑A组;而来曲唑A组、来曲唑B组患者RI、PI水平均显著降低,且来曲唑B组显著低于来曲唑A组;3组患者不良反应总发生率比较,差异无统计学意义,提示相比于氯米芬单一治疗,联合来曲唑治疗PCOS,可有效改善患者子宫内膜容受性,提高排卵率和优良妊娠率,且安全性良好,5 mg剂量的来曲唑治疗效果更佳。分析其原因可能为,来曲唑通过减少合成雌激素的底物使患者雌激素降低,消除雌激素对性腺轴的负反馈,使垂体的FSH分泌增加,促进卵泡发育成熟,同时通过抑制卵巢和大脑中雌激素的合成,从而刺激垂体重新对机体内激素水平进行调节[13-15]。
PCOS患者发病时会出现代谢紊乱现象,同时造成机体内雌激素和孕激素分泌异常,使血清LH、E2水平明显升高,FSH水平明显降低;PRL是一种垂体前叶腺嗜酸细胞分泌的蛋白质激素,具有促进乳腺发育生长,刺激卵泡LH受体生长等作用[16-17]。夏蕾等[18]研究结果显示,与来曲唑2.5 mg/d的剂量比较,来曲唑5 mg的剂量治疗PCOS,可有效降低患者血清E2、LH水平,提高血清FSH水平,提示5 mg来曲唑治疗PCOS效果更佳。本研究中,治疗后来曲唑A组、来曲唑B组患者血清E2、PRL、LH水平均显著降低,且来曲唑B组显著低于来曲唑A组,来曲唑A、B组患者血清FSH水平均显著升高,且来曲唑B组显著高于来曲唑A组,提示相比于氯米芬单一治疗,联合来曲唑治疗PCOS,可有效调节性激素水平,促进病情恢复。分析其原因可能为,来曲唑可通过抑制芳香化酶活性来阻止雄激素向雌激素的转化,从而减少机体内雌激素的生成;同时雄激素蓄积在卵泡中,抑制雌激素对促卵泡生成激素的负反馈作用,使得机体内源性促性腺激素水平升高,增加卵巢的敏感度,起到刺激卵泡生长发育的效果[19-20]。
综上,相比于氯米芬单一治疗,联合来曲唑治疗PCOS,可有效改善患者子宫内膜容受性,调节性激素水平,提高排卵率和优良妊娠率,安全性良好,且治疗剂量为5.0 mg的来曲唑治疗效果更理想,值得临床推广应用。

