优质CuNiLDH的制备及结构分析
吴健松,伍世亮,简 艺
(1.广东茂名幼儿师范专科学校理学院氢能系,广东 茂名 525000;2.岭南师范学院化学化工学院,广东 湛江 524048)
0 引言
氢能已成为全球公认最环保的能源,而在氢能的研究与应用领域中,制氢催化剂的研制是重中之重[1-3].CuNiLDH是类水滑石的一种,因其具有高效快速等的优良制氢催化性能而备受关注[4].LDH的英文全称为Layered double hydroxides,即层状双金属氢氧化物,俗名“水滑石”.LDH类催化剂的结晶度、晶体的有序性和多孔结构对催化剂的催化效率和催化速度有重要的影响[5].若LDH晶体内部结构越规整、比表面越大、微孔比率越高则其吸附底物越多、催化速度和效果将越好[6].而且,催化材料的孔可更有效地“俘获”底物,能更有效地防止因底物在转化过程中迁移而致使催化反应半途而废的现象发生,这在一定程度上也将抑制催化逆反应的发生.CuNiLDH是一类很有应用前景的含铜、镍类催化剂[4,7].CuNiLDH实际上是以Cu2+和Ni2+取代镁铝水滑石中的Mg2+的一种“类水滑石”.有关水滑石或类水滑石的合成、结构与功能、晶体生长方法与技术等的报道较多[8-14],这里不做赘述.
用传统方法制备的CuNiLDH普遍存在如下问题:(i)容易生成大量的CuO单相物且CuO聚结严重,在整个产品中CuO单相物的质量分数较大,这是因为铜离子具有姜泰效应,不易进入晶格[15-18];(ii)在产物CuNiLDH中经常有少部分无定形物(如Al(OH)3)与晶体共存,结晶度不高;(iii)产物为孔状结构,但却以中孔占大比例、微孔占小比例为主,比表面积不大.这些问题均使CuNiLDH的催化效率与性能不高.因此,本文采用在缓冲体系下慢速生长质优结构的CuNiLDH.氢能作为一种高效、清洁的新能源而高度备受全球关注.然而,氢能的科学瓶颈问题就是制氢催化剂的问题,含铜、镍类的CuNiLDH是在制氢催化剂中最有前景的催化剂.
1 实验
1.1 仪器与试剂
NaOH、Cu(NO3)2·3H2O、Ni(NO3)2·6H2O、Al(NO3)3·9H2O、Na2CO3、NaHCO3等试剂均购自广州化学试剂厂,分析纯.制备仪器为KCF-10水热反应釜(快开式,烟台牟平曙光精密仪器厂).样品的表征仪器为D/Max-3C X-射线衍射仪;透射电镜采用JEM-2100F透射电镜(日本电子);Ni、Cu、Al 元素的测定采用等离子体发射光谱仪(ULTIMA型,法国JY公司);H和C元素的测定采用PE2400 SeriesⅡCHNS/O元素分析仪(美国);热失重测试采用TG-DTA320(seiko instruments),N2气氛,温度范围为50~750 ℃,升温速率为10 ℃·min-1;比表面采用ASAP 2010比表面积/空隙分析仪(美国Micromeritics公司)测定.
1.2 CuNiLDH样品的制备
(i)配制Na2CO3-NaHCO3缓冲溶液,并调节其pH值为10.3,在该缓冲溶液中Na2CO3和NaHCO3物质的量浓度均为0.5 mol·L-1;配制1.0 mol·L-1的Na2CO3溶液.
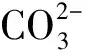
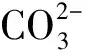
(iv)取上述第(iii)步得到的浆料于水热反应釜内,使其装满度为70%,设定一定的反应温度(T)和反应时间(t),在反应结束后过滤洗涤沉淀物,并将沉淀物于75 ℃烘箱内烘干48 h即得样品.表1列出了4个样品的制备条件.
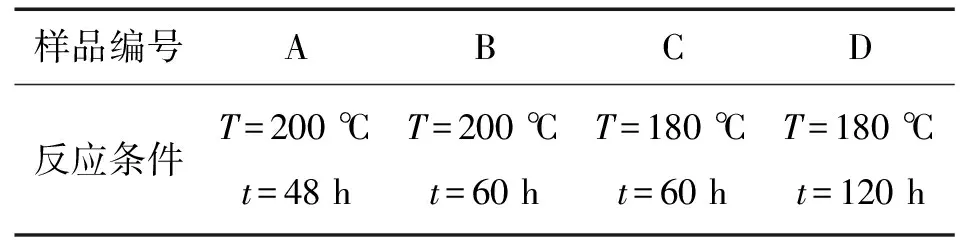
表1 4个样品的反应条件
2 结果与讨论
2.1 X-射线衍射分析
图1给出了4个样品的XRD衍射结果,图1曲线末端标注的a、b、c和d分别表示样品A、B、C和D的衍射曲线.
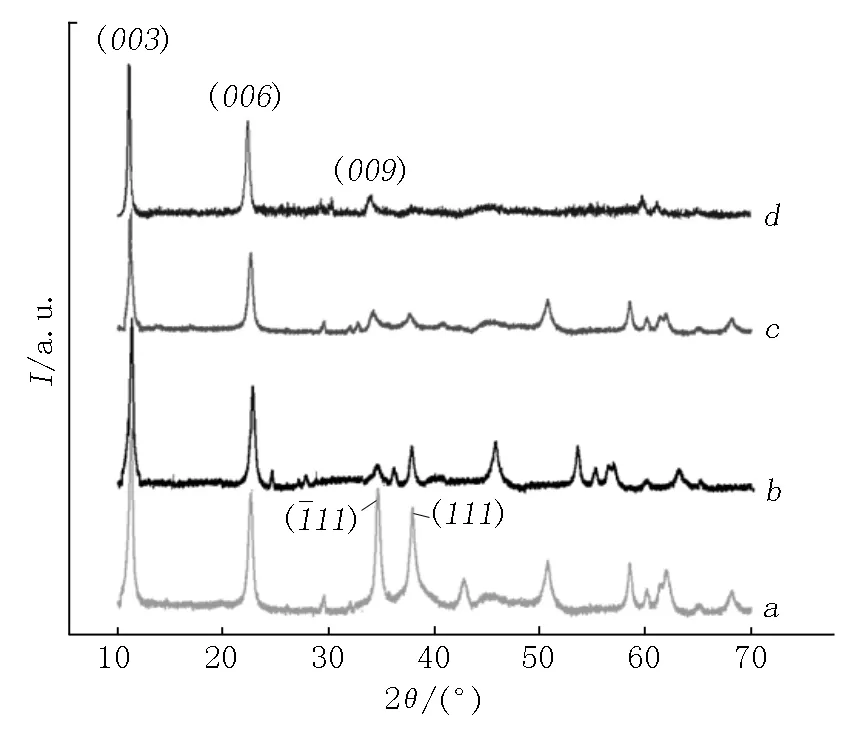
图1 4个样品的XRD衍射图
2.2 热失重分析和元素分析
样品的热失重分析结果如图2所示.由图2可知:样品有3个显著质量损失台阶,第1个台阶质量损失14.22%,对应的是化合物脱去结晶水;第2个台阶质量损失14.21%,对应的是脱羟基;第3个台阶质量损失8.66%,对应的是脱二氧化碳.样品元素分析结果如表2所示.表2列出了各元素在化学式中的比例.结合热失重分析和元素分析得知,样品D的化学式为Cu1.3Ni2.2Al(OH)8CO3·4H2O.
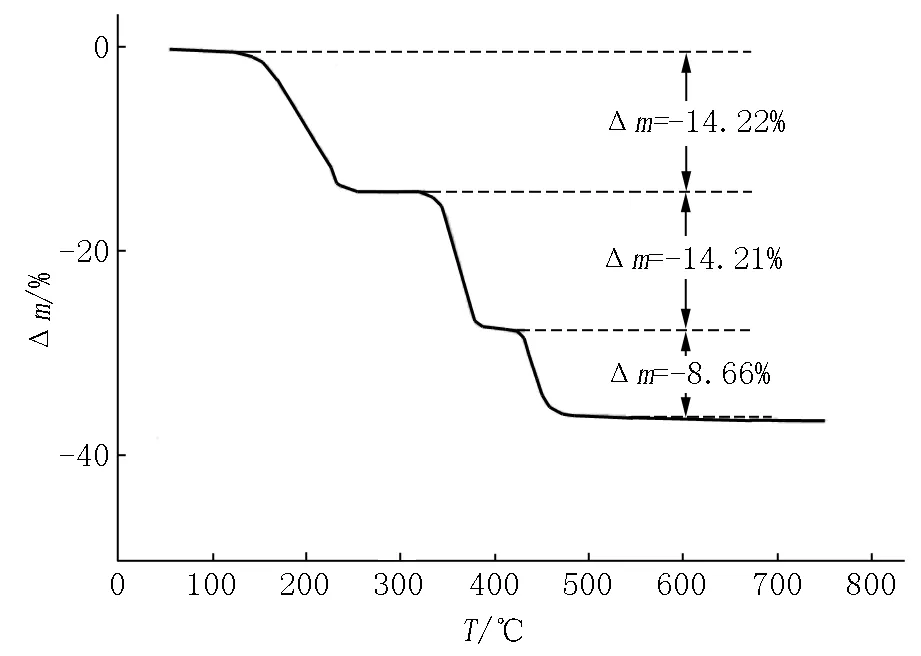
图2 样品的热失重图

表2 样品元素分析结果
样品D在脱水、脱二氧化碳之后得到的产物Cu1.3Ni2.2AlO5也是一种具有催化、吸附等多功能的材料[4-7].
2.3 透射电镜分析
图3为样品的TEM图,其中图3(a)为低倍数图,图3(b)为高分辨图,图3(c)为电子衍射图.从图3(a)可知样品呈六方状,分散性好.图3(b)和图3(c)分别是在图3(a)中圆圈圈出的粒子的高分辨透射电镜图和电子衍射图.从图3(b)可见,样品具有优良的晶格条纹,这说明分子具有规整的晶列和晶面结构,缺陷较少(若有较多的缺陷,则在图3(b)中应出现较大面积的暗区,但从图3(b)来看,暗区仅有小面积分布于圆圈圈出的左上角).图3(c)的电子衍射表明样品具有较高的结晶度和优良的晶胞结构.
2.4 比表面分析
样品的比表面分析结果如图4所示.图4显示样品具有微孔和中孔结构.样品的吸附等温线在低压范围(0.05

图3 样品的TEM图
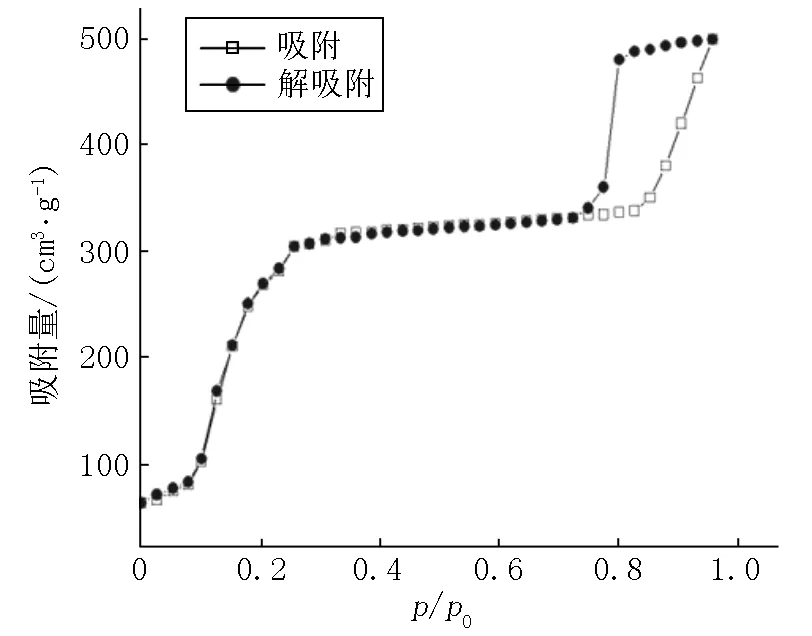
图4 样品的吸附等温线
2.5 缓冲溶液在CuNiLDH晶体生长中的作用
上述表征结果表明:在缓冲体系下可生长质优的CuNiLDH晶体.下面讨论缓冲体系对CuNiLDH晶体生长的作用.
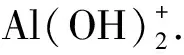
(1)
在式(1)中的OH-主要由Na2CO3提供:
Na2CO3+H2O→NaHCO3+OH-.
(2)
因在体系中有Na2CO3-NaHCO3缓冲对,NaHCO3对式(2)有同离子效应,因此式(2)的产物OH-是一个缓慢的释放过程,即在式(1)中的OH-是一个“慢速供给”的过程,OH-的慢供给有利于晶体生长[17],也符合质优的LDH晶体生长的规律.当式(1)反应向右进行时,OH-被缓慢消耗,这时式(2)也向右移动以补偿在式(1)中的OH-,这就使得质优CuNiLDH循序渐进地生长.若OH-的物质的量浓度是瞬时供给的,则会使式(1)中左边反应物CuNiAl2(OH)x+4CO3·mH2O变为形成絮凝状的Cu(OH)2和Al(OH)3而无法得到质优的CuNiLDH.图5是在不加缓冲液的条件下制备得到的样品的XRD衍射图(其他条件与样品D相同,为弥补由于没加缓冲对而缺失的Na2CO3,图5是本文采取加入与缓冲对相等物质的量的Na2CO3,若不加则效果更差).从图5可以看出:样品得不到较纯的水滑石相,杂相峰衍射比较严重,对峰的鉴别与标定较困难.在水热反应后,烘干得到的样品从外观上看也较差(如有一定量的结块现象、分散性差、有黑色物质共存等).因此,缓冲溶液在晶体生长中起了较重要的作用.
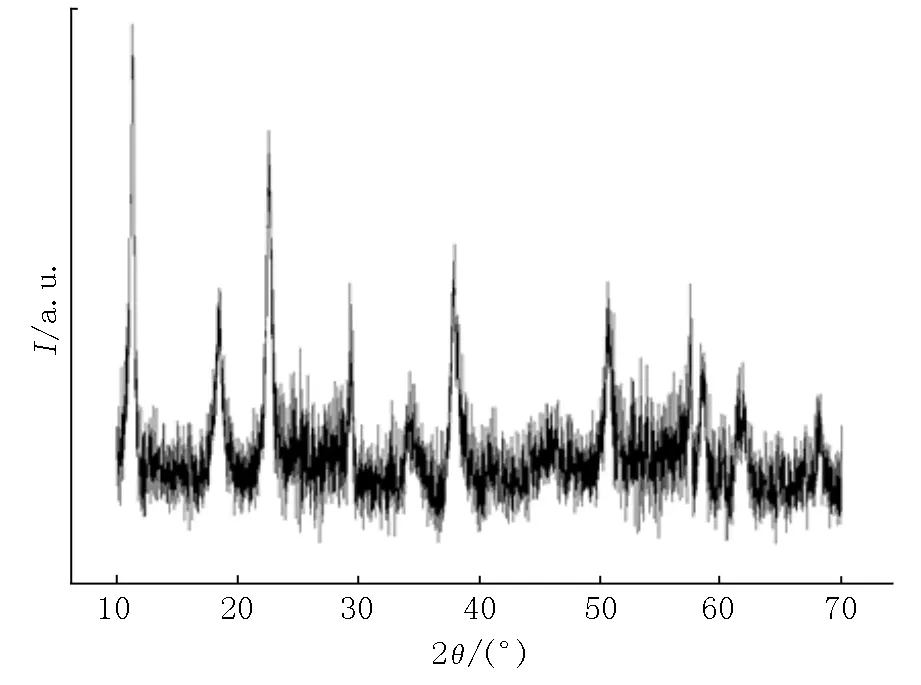
图5 在不加缓冲液情况下样品的XRD衍射图
3 结论
在缓冲介质下,可制备得到质优的CuNiLDH,其结晶度较好、无显著数量的氧化铜共存、纯度较高、晶格排列有序规整、比表面积大、具有优良的微孔结构、孔径分布均匀.CuNiLDH最优的制备条件是:加入缓冲液的体积是原体系的1/2,水热反应的反应温度为180 ℃,反应时间为120 h.

