碳纤维超微电极负载金纳米粒子高灵敏检测木犀草素
施 敏,鲍昌昊,马雯雯,程 寒,2*
(1.中南民族大学 药学院,湖北 武汉 430074;2.中南民族大学 民族药学国家级实验教学示范中心,湖北 武汉 430074)
木犀草素(Luteolin)是一类具有典型C6-C3-C6 结构的天然黄酮类化合物,存在于金银花、白毛夏枯、紫苏叶、菊花、莲花、芹菜、香菜、花生壳、胡萝卜和石榴等植物材料中[1-4]。其主要药理活性表现为抗菌、抗炎、抗过敏、抗癌、抗氧化、抗肿瘤[5-10]等方面,在临床上广泛应用于止咳、祛痰、治疗心血管系统、保护肝脏、促进免疫调节和保护神经系统[11]等。目前,木犀草素的测定方法主要有高效液相色谱法[12]、毛细管电泳法[13]及紫外分光光度法[14]等。上述方法可对木犀草素进行含量测定,但普遍存在方法繁琐、仪器昂贵、实验要求较高等问题。电化学分析法[15]具有灵敏度高、选择性好、准确度高、测量范围广、仪器设备简单等特点,逐渐成为一种不可或缺的中药有效成分测定的方法。
碳纤维超微电极(CFME)具有比表面积大、灵敏度高、制备成本低[16]等优点,在神经递质[17]、其他生物因子、金属离子[18]、活细胞释放H2O2[19]和生物活体检测[20]等方面有着广泛应用。化学修饰电极是当前电化学和电分析化学领域非常活跃的研究热点,在药物分析领域有着广阔的应用前景。纳米金为直径1~100 nm 的微小金颗粒,其制备过程简单,具有独特的光电效应,且具有比表面积大、生物相容性能优良等特点[21],其优异的电导性和生物相容性能可提升CFME 电极表面的电子转移速率,极大地改善了电极的电催化性能。杨莉莉等[22]制备了线状纳米金修饰碳纤维超微电极,用于芦荟大黄素的电化学检测,结果显示修饰后的电极具有优异的电催化活性,可用于实际样品芦荟汁中芦荟大黄素的测定。
本研究采用化学还原法制备纳米金颗粒,通过电沉积方法将纳米金修饰在碳纤维超微电极上构建电化学传感器(AuNPs/CFME),建立了一种简单、高效检测木犀草素含量的新方法(如图1),并成功应用于实际样品独一味胶囊中木犀草素的含量测定。
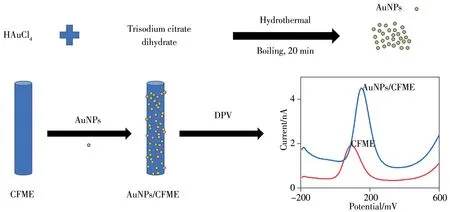
图1 基于AuNPs/CFME的木犀草素传感器的检测原理图Fig.1 Principle of luteolin sensor based on AuNPs/CFME
1 实验部分
1.1 仪器与试剂
XD-RFL 型倒置显微镜(宁波舜宇仪器有限公司);CHI660D 型电化学工作站(上海辰华仪器有限公司);SU8010 型场发射扫描电子显微镜(日本Hitachi);TECNAI G2 F20 S-TWIN 型投射式电子显微镜(美国FEI 公司);AR224CN 型分析天平(上海奥豪斯仪器有限公司);双电极系统(CFME 为工作电极,Ag/AgCl为参比电极);PHS-3C型pH计(上海仪电科学仪器股份有限公司)。
碳纤维(直径5 μm,吉林市神舟碳纤维有限责任公司);木犀草素(纯度≥98%,上海源叶生物科技有限公司);氯金酸(AuCl3·HCl·4H2O,纯度≥47.8%,国药集团化学试剂有限公司);柠檬酸三钠、单宁酸、碳酸钾、铁氰化钾、亚铁氰化钾(分析纯,国药集团化学试剂有限公司);独一味胶囊(康县独一味生物制药有限公司);AB 胶(广东爱必达胶粘剂有限公司);碳粉导电胶(自制);PBS 缓冲溶液:Na2HPO4∶KH2PO4(6∶1);以pH 1.0的PBS缓冲溶液为底液,实验用水为二次蒸馏水。
1.2 实验方法
1.2.1 AuNPs 及AuNPs/CFME 的制备AuNPs 的制备参考文献[23]。将40 mL 水加热至沸腾,边搅拌边加入500 μL 1%的氯金酸(HAuCl4)溶液。随后快速加入900 μL 1%的柠檬酸三钠(C6H5Na3O7)溶液,继续加热20 min,直至溶液呈酒红色,冷却至室温,于4 ℃下保存备用。
取10 mL AuNPs 溶胶置于50 mL 小烧杯中,将Ag/AgCl 参比电极与洁净的CFME 置于AuNPs 溶胶中,采用恒电位电流-时间法,在1.5 V电位下进行电沉积,即在CFME表面构建纳米金修饰层,制得AuNPs/CFME。
1.2.2 电化学测定电化学检测均在CHI660D 型电化学工作站上进行,采用双电极体系:以AuNPs/CFME 为工作电极,Ag/AgCl 为参比电极。循环伏安法(CV)实验参数为:电位扫描范围为-0.2~0.9 V;扫描速度0.1 V/s;采样间隔0.01 V;静置时间2 s。差分脉冲伏安法(DPV)实验参数为:电位扫描范围为-0.2~0.6 V;振幅0.05 V;脉冲宽度0.05 s;脉冲时间0.2 s;静置时间20 s。整个实验过程均在室温下进行。
1.2.3 样品预处理将独一味胶囊的外壳去除,取其内容物置于钵体中,研磨成细粉后,精密称取5.00 g 药粉,用50 mL 无水乙醇溶解后,超声振荡1 h,过滤后取上层清液制得样品溶液,于4 ℃下保存备用。
2 结果与讨论
2.1 AuNPs/CFME的制备及表征
图2A 是制备的AuNPs 的TEM 图,图中可见AuNPs 粒子大小均匀,其平均粒径约为13 nm。图2B为AuNPs 溶胶的紫外-可见吸收光谱图,在520 nm 处出现1 个特征吸收峰,为AuNPs 的特征吸收峰[24],表明AuNPs 制备成功。图2C、D 分别为CFME、AuNPs/CFME 的SEM 图。由图可知,未修饰的CFME 表面光滑平整,经AuNPs 修饰后的电极表面吸附大量球状纳米颗粒,电极直径略有增加,比表面积增大,表明CFME表面已成功键合AuNPs。
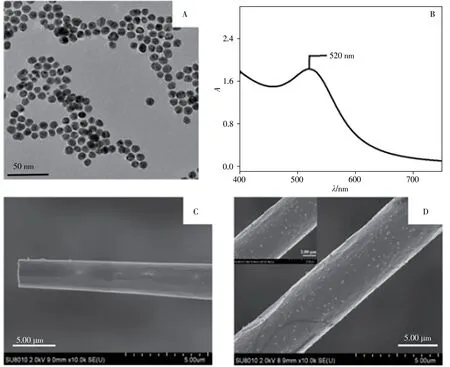
图2 AuNPs的透射电镜图(A)、AuNPs溶胶的紫外-可见吸收光谱图(B),以及CFME(C)和AuNPs/CFME(D)的扫描电镜图Fig.2 TEM image of gold nanoparticles(A),UV-Vis absorption spectrum of gold nanosol(B),SEM images of CFME(C)and AuNPs/CFME(D)
图3A 为0.01 Hz~100 kHz 频率范围内,CFME 和AuNPs/CFME 在含0.1 mol/L KCl 的5 mmol/L[Fe(CN)6]3-/[Fe(CN)6]4-溶液中的电化学阻抗谱(EIS),由图可知,CFME 的转移阻抗值(Rct)较大,为3.378×105Ω,AuNPs/CFME 修饰电极的Rct 小于CFME,为3.601×104Ω。表明AuNPs 已成功修饰在电极表面,AuNPs 降低了CFME 的界面阻抗值,主要原因可能是纳米金粒子的纳米效应及表面原子的空位效应使其具有良好的电催化活性,从而提高了电极表面的电子转移速率。采用DPV法于1 μmol/L木犀草素溶液中考察了修饰电极的电化学行为(图3B),曲线a为CFME在1 μmol/L PBS(pH 7.0)溶液中的DPV 曲线,曲线b和c分别为CFME 和AuNPs/CFME 在1 μmol/L 木犀草素溶液中的DPV 曲线。从图中可以看出,木犀草素在CFME 表面于0.1 V左右出现1个氧化还原峰,峰电流值为1.948 nA,经AuNPs修饰后,木犀草素的氧化峰电位略有正移,且峰电流值增至4.519 nA,约为CFME 电化学响应的2.3倍,表明AuNPs对木犀草素的氧化具有明显的催化作用。
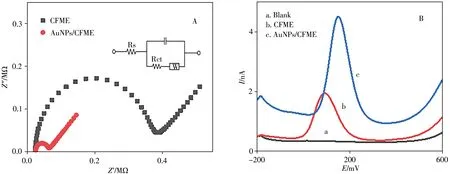
图3 CFME和AuNPs/CFME在含0.1 mol/L KCl的5 mmol/L[Fe(CN)6]3-/[Fe(CN)6]4-溶液中的电化学阻抗谱(A);CFME在1 μmol/L PBS(pH 7.0)缓冲溶液中的DPV曲线(a),以及CFME(b)和AuNPs/CFME(c)在1 μmol/L木犀草素溶液中的DPV曲线(B)Fig.3 Nyquist diagrams of CFME,AuNPs/CFME in 5 mmol/L[Fe(CN)6]3-/[Fe(CN)6]4-containing 0.1 mol/L KCl(A);DPV curve of CFME in 1 μmol/L PBS(pH 7.0)buffer solution(a),DPV curves of CFME(b)and AuNPs/CFME(c)in 1 μmol/L luteolin(B)
2.2 AuNPs/CFME电化学沉积时间的优化
采用恒电位时间-电流曲线法,保持初始电位为1.5 V,将洁净的CFME 置于10 mL AuNPs 溶胶中依次电沉积10、20、30、40、50 min(n=3)。结果显示,在1 μmol/L 木犀草素溶液中,当AuNPs 的电沉积时间为30 min 时修饰电极的氧化峰电流达到最大,超过30 min 后,氧化峰电流略有下降。可能是由于随着电沉积时间的增加,AuNPs 在碳纤维电极表面不断聚集,而时间过长则会导致电极表面修饰层脱落,从而降低其电催化活性。因此本实验选择最佳AuNPs电沉积时间为30 min。
2.3 扫速和pH值对氧化峰电流的影响
为阐明木犀草素在AuNPs/CFME 电极上的反应机理,以PBS 缓冲液(pH 7.0)为介质,考察了1 μmol/L 木犀草素在不同扫速(10、50、100、150、200、250、300、350、400、450、500 mV/s)下的循环伏安图。如图4A所示,木犀草素的氧化还原峰电流随扫速的增加而增加,且氧化峰电位随扫速的增加逐渐正移,还原峰电位逐渐负移,峰电位差逐渐增大,表明木犀草素在修饰电极表面的氧化还原反应是一个准可逆过程,且可逆性随扫速的增加逐渐变差。从图4B 可以看出,在10~500 mV/s 范围内,木犀草素的氧化还原峰电流(Ip)与扫描速率(v,mV/s)成正比,其线性回归方程为:Ipa(nA)=-0.174 3-0.009 1v(mV/s),r2=0.997 3;Ipc(nA)=0.121 9+0.006 8v(mV/s),r2=0.999 3。结果表明,木犀草素在AuNPs/CFME 电极上的氧化还原反应是吸附控制过程[25]。研究了峰值电流对数(logIp)与扫描速率对数(logv)之间的线性关系,得到线性方程为:logIp(nA)=-1.732+1.385 3 logv(mV/s),r2=0.992 6,斜率值为1.385 3,接近吸附控制的理论值1.0[26]。此外,考察了阳极(Epa)和阴极(Epc)峰值电位和扫描速率对数logv(mV/s)之间的线性关系,得到线性方程分别为:Epc(mV)= 195.7 × 10-3+50.858 × 10-3logv,r2= 0.996 0;Epa(mV)= 385.19 × 10-3-56.653 × 10-3logv,r2= 0.994 7。根据Laviron′s equation[27-28],电子转移系数(α)、电子转移数(n)可通过下列方程计算:
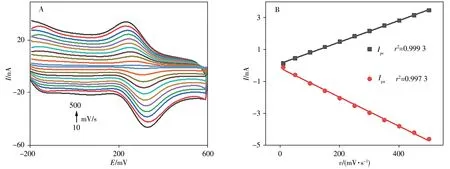
图4 AuNPs/CFME在1 μmol/L木犀草素溶液中于不同扫速下的CV图(A),木犀草素的氧化还原峰电流与扫速的线性关系图(B)Fig.4 Cyclic voltammograms of 1 μmol/L luteolin with AuNPs/CFME at different scan rate(A);plot of the anodic and cathodic peak currents of luteolin versus the scan rate(B)


其中Eθ′、R、F 和T分别代表形式氧化还原电势、理想气体常数(8.314 J·mol-1·K-1)、法拉第常数(96 485 C·mol-1)、热力学温度(298 K)。根据上述方程可计算出α/(1-α)为0.9,接近于1,α和n的值分别为0.47和2.22,n值接近于2,表明木犀草素的电化学氧化过程有2个电子参与,与文献报道的结果一致[29]。考虑到扫速过快会使充电电流变大,从而使基线噪音增加,因此后续实验均在100 mV/s 扫速下进行。
采用不同pH 值的PBS 溶液配制1 μmol/L 木犀草素溶液,在pH 1.0~8.0 范围内考察pH 值对AuNPs/CFME 电极响应的影响。结果表明,pH 为1.0 时木犀草素的氧化还原峰值电流最大,因此选择pH 1.0 的缓冲体系用于后续实验。由于质子参与了木犀草素的电极反应过程,随着pH 值的增加,氧化峰电位负移,表明木犀草素的氧化是脱质子反应。木犀草素的氧化峰电位(Ep)与pH 值呈线性关系,线性回归方程为Ep(mV)= 522.11-58.29pH,r2= 0.994 8。回归方程斜率与能斯特方程计算的理论值-59.2 mV/pH 接近,表明参与电极反应的电子数和质子数之比为1∶1,考虑到木犀草素的电子数n为2,因此木犀草素在AuNPs/CFME 上的电化学反应是双质子双电子准可逆过程[30]。
结合以上实验结果,木犀草素在AuNPs/CFME 上氧化还原反应的可能机理如图5 所示,即木犀草素苯环上的3′,4′-二羟基取代基被迅速氧化成邻苯醌基团,与文献报道相符[31]。
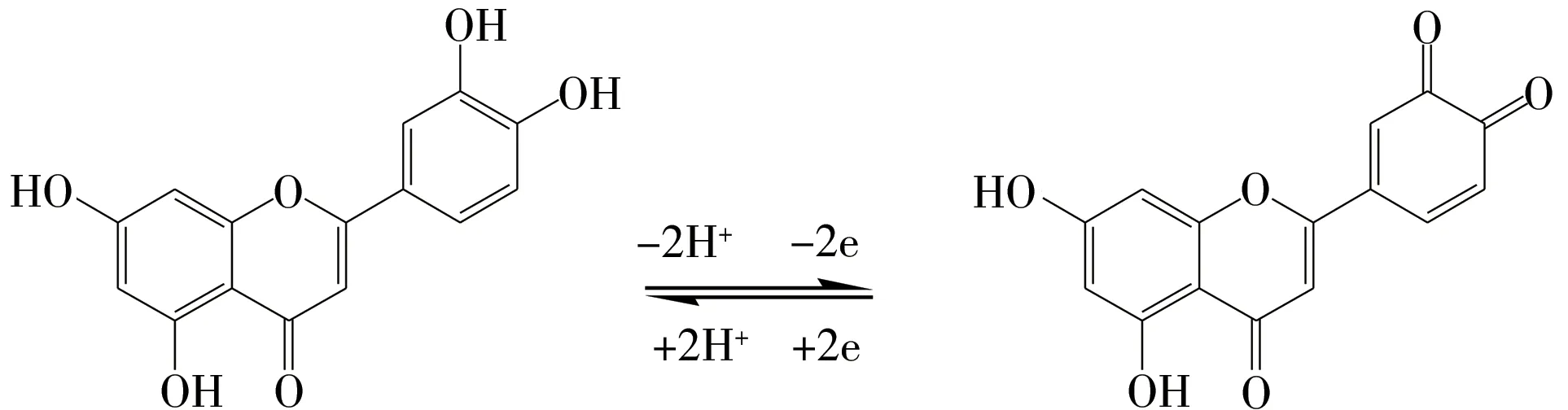
图5 木犀草素的氧化机理Fig.5 Mechanism of the oxidation of luteolin
2.4 AuNPs/CFME检测木犀草素的线性关系与检出限
最佳实验条件下,pH 为1.0 的PBS 缓冲溶液中不同浓度木犀草素的DPV 曲线如图6A 所示,其线性关系如图6B~C所示。结果表明,当木犀草素的浓度在0.01~10 μmol/L范围时,峰电流随木犀草素浓度的增加而增加,且在0.01~0.10 μmol/L 和0.10~10 μmol/L 两个范围内呈良好的线性关系,线性回归方程分别为:Ip(nA)= 0.990 1c(μmol/L)+ 1.610 5,r2= 0.994 4;Ip(nA)= 0.135 4c(μmol/L)+1.748 8,r2=0.995 1。检出限(LOD,S/N=3)为1.58 nmol/L。
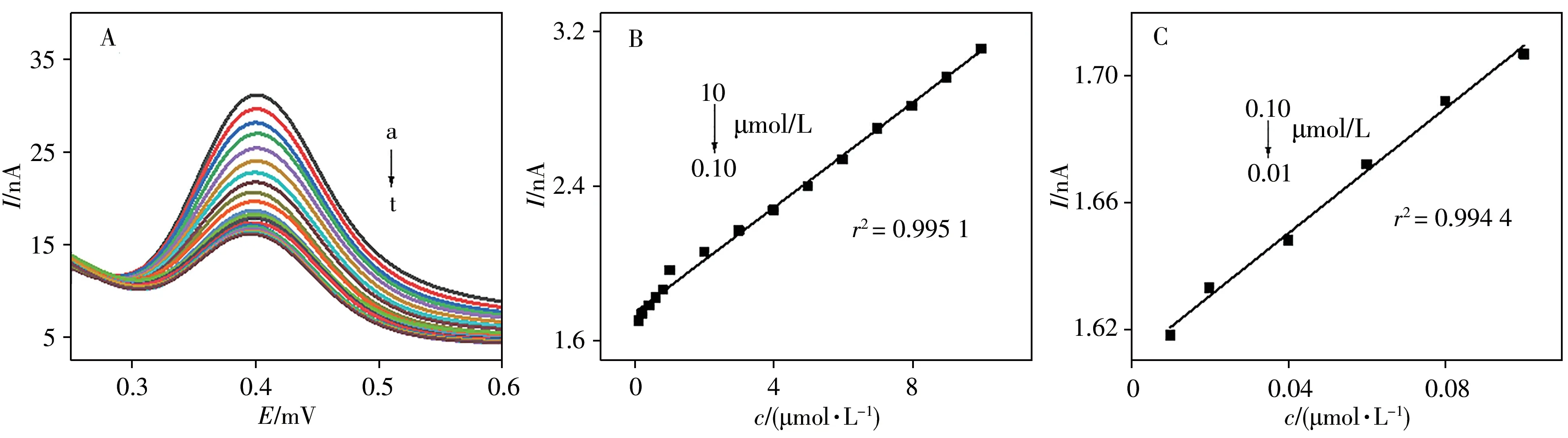
图6 不同浓度木犀草素的DPV曲线(A),0.10~10 μmol/L(B)与0.01~0.10 μmol/L(C)范围内木犀草素的氧化峰电流与浓度的线性关系曲线Fig.6 DPV curves at AuNPs/CFME in the solution of luteolin(A),linear relationship between oxidation peak current and concentration of luteolin in the range of 0.10-10 μmol/L(B)and 0.01-0.10 μmol/L(C)concentration of luteolin(curve a-t):0.01,0.02,0.04,0.06,0.08,0.1,0.2,0.4,0.6,0.8,1.0,2.0,3.0,4.0,5.0,6.0,7.0,8.0,9.0,10.0 μmol/L
比较了AuNPs/CFME 与其他电化学传感器对木犀草素检测的线性范围和检出限,结果如表1所示,AuNPs/CFME具有较低的检出限和较宽的线性范围。
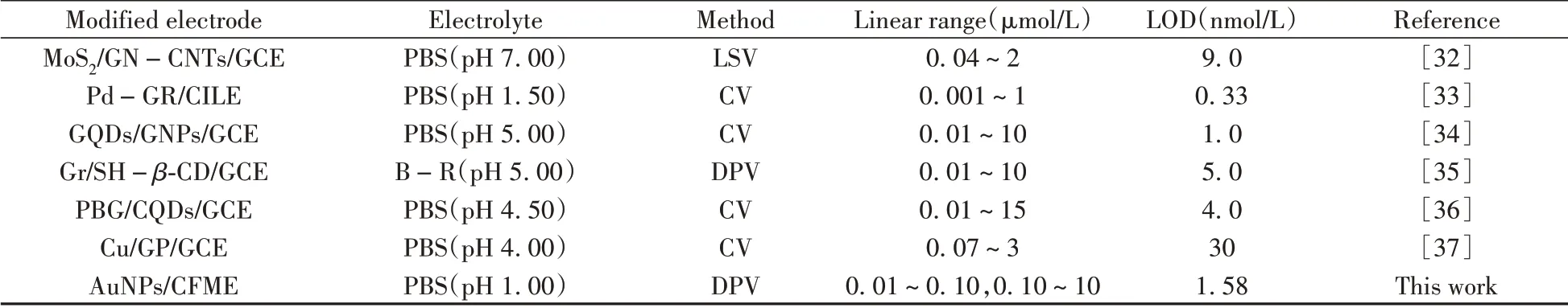
表1 不同修饰电极测定木犀草素的电化学性能比较Table 1 Comparison of the analytical performance of different modified electrodes for the determination of luteolin
2.5 干扰性与稳定性
为了将AuNPs/CFME 应用于实际样品测定,考察了检测中可能存在的各种干扰物质的影响。在10 000 倍浓度的Na+、K+、Cl-和1 000 倍SO42-存在的情况下,测定AuNPs/CFME 在1 μmol/L 木犀草素中的DPV 响应。结果显示,Na+、K+、Cl-、SO42-的加入对木犀草素的检测无明显干扰(偏差<5.0%),表明AuNPs/CFME 对木犀草素的测定具有良好的选择性。采用新制的AuNPs/CFME 修饰电极连续10 次在1 μmol/L 木犀草素溶液中进行差分脉冲扫描,木犀草素的电化学响应降低<5.0%。将修饰电极置于空气中,连续10 d 进行相同实验,木犀草素的氧化峰电流衰减较小,其氧化峰电流的相对标准偏差(RSD)降低<5.0%,表明AuNPs/CFME修饰电极的电化学性能非常稳定。
2.6 实际样品分析
取10 μL独一味样品溶液,用pH 1.0的PBS缓冲溶液稀释至10 mL,并向样品溶液中添加一系列已知不同浓度的木犀草素标样进行加标回收实验。如表2所示,木犀草素的回收率为96.0%~104%,5次平行测定的RSD 均小于5.0%,表明该方法制备的AuNPs/CFME 修饰电极可用于实际样品独一味胶囊中木犀草素的检测。
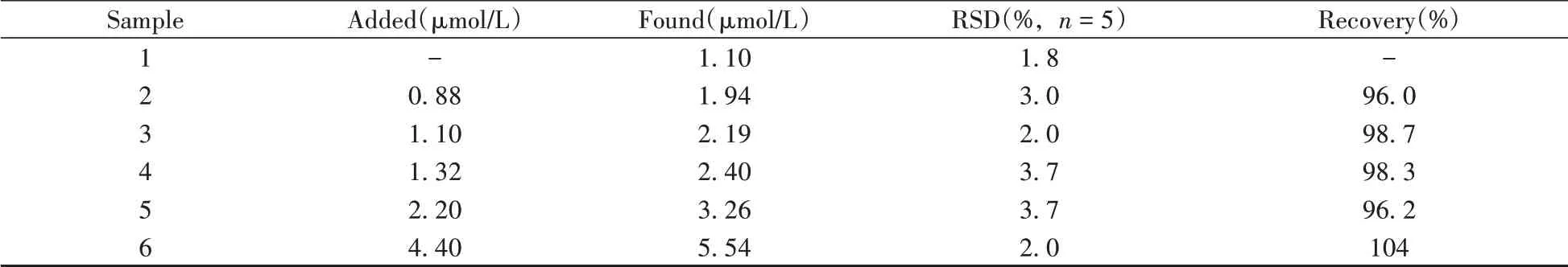
表2 独一味胶囊中木犀草素的含量测定Table 2 Determination of luteolin in Kudo capsule samples
3 结 论
本文将纳米金修饰在碳纤维超微电极表面构建了AuNPs/CFME,用于木犀草素的检测。在优化实验条件下,木犀草素的线性范围为0.01~0.10 μmol/L 和0.10~10 μmol/L,检出限为1.58 nmol/L,将其用于独一味胶囊中木犀草素含量的测定,回收率为96.0%~104%。该传感器灵敏度高、选择性好、准确度高、线性范围宽,为木犀草素在医药、食品等工业中的开发利用和深入研究提供了理论依据。
- 分析测试学报的其它文章
- 地下水中102种酸性、碱性和中性有机污染物的气相色谱-质谱法同时快速测定
- 基于超高效液相色谱-四极杆-静电场轨道阱质谱的结直肠腺瘤患者血清代谢组学研究
- 金-银双金属纳米簇@多壁碳纳米管-二氧化钛纳米材料为新型氧化还原探针构建电化学免疫传感器
- Preparation and Identification of Reference Materials of Isorhamnetin and Rutin in Seabuckthorn Fruit Powder
- 羧基微孔有机网络材料的合成及其对水中苯并三唑类污染物的快速吸附与去除
- 基于激发态分子内质子转移的新型聚集诱导荧光探针用于硫化氢的检测及细胞成像

