氢化物载体LaMg2Ni对汽车用Mg2Ni合金储氢性能的影响
郗玉平,罗志欢,2
(1.北京信息职业技术学院,北京 100070;2.北京科技大学)
镁基储氢合金由于具有吸氢量大、质量轻、成本低和环境友好等特性而具有广阔的应用前景[1],Mg2Ni 作为镁基储氢合金的典型代表,以其储氢容量高、可逆吸放氢温度低等特性而受到广泛关注,并有望作为最具发展潜力的储氢材料而应用于新能源汽车等领域[2-3]。科研工作者通过引入第三种合金元素(Cu、Co、Fe和V等)以及细化Mg2Ni合金颗粒等方法提升Mg2Ni 合金的储氢性能,但是较差的吸氢/放氢热力学和动力学性能仍然在很大程度上限制了Mg2Ni合金作为储氢材料的应用[4-6]。较为可行的办法是在Mg2Ni 合金中添加金属间化合物、轻质储氢材料等具有催化活性的添加剂,来降低储氢材料氢化物的热力学稳定性并提升可逆吸/放氢动力学性能,从而改善Mg2Ni基复合材料的储氢性能[7]。已有的研究已证实,钛和铌的氢化物/氮化物以及轻质储氢材料LiBH4等对Mg2Ni 合金的储氢性能有一定改善,而关于具有氢化分解特性的稀土氢化物载体对Mg2Ni 合金储氢性能影响方面的报道较少[8-10]。本文选取热力学稳定性较Mg2Ni合金更低的氢化物载体LaMg2Ni 为添加剂,考察了LaMg2Ni 含量对Mg2Ni基复合材料微观结构和储氢性能的影响,结果将有助于改善储氢材料的吸/放氢热力学和动力学性能并提升其储氢性能。
1 实验材料与方法
1.1 实验原料
实验原料包括感应熔炼法制备的Mg2Ni 和LaMg2Ni合金,机械破碎后过筛得到粒度小于150 μm的Mg2Ni 和LaMg2Ni 合金粉末。将Mg2Ni 合金粉末进行预处理:氢化处理(350 ℃、氢化压力和时间分别为3 MPa 和120 min)和动态真空处理(350℃、放氢),重复氢化处理和动态真空处理2次后进行真空密封保存。
1.2 Mg2Ni基复合材料的制备
将经过预处理的Mg2Ni合金粉末和LaMg2Ni合金粉末按照一定比例称量后,置于KQM-Z型高能球磨机中进行研磨,对磨材料为Φ6 mm的WC球,球料比为10∶1,球磨时间为120 min,制备得到Mg2Ni-x%LaMg2Ni复合材料(x%为质量分数),其中x=0、10、20、30。
1.3 测试方法
采用Empyrean锐影X射线衍射仪对Mg2Ni基复合材料进行相结构分析,Cu靶Kα辐射,扫描速度为2(°)/min;采用S-3400 型扫描电子显微镜对Mg2Ni基复合材料的显微形貌进行观察,并用附带能谱仪进行半定量成分分析;采用H-Sorb 2600 型PCT 测试仪对Mg2Ni 基复合材料进行压力-组成和温度(PCT)曲线测试[11],预先将复合材料在300 ℃、3 MPa氢气压力下吸氢1 h后在0.001 MPa氢气压力下放氢1 h,并重复上述吸氢和放氢步骤1 次;Mg2Ni 基复合材料的等温吸氢/放氢曲线[12]在PCT 测试仪上进行,吸氢和放氢过程中初始氢气压力分布为3 MPa和0.01MPa,测试温度分别为200 ℃和250 ℃。
2 实验结果与分析
2.1 物相组成和显微形貌
图1 为充分氢化后不同LaMg2Ni 含量的Mg2Ni基复合材料的XRD 谱图。当x=0 时,未添加LaMg2Ni 的Mg2Ni 在充分氢化后主要由Mg2NiH4和Mg2NiH0.3组成;当添加不同含量LaMg2Ni 后,x=10、x=20 和x=30 时Mg2Ni 基复合材料都主要由Mg2NiH4和LaH3组成,其中,氢化过程中反应式如下[13]:
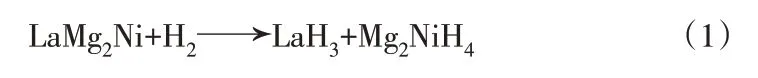

图1 充分氢化后不同LaMg2Ni含量的Mg2Ni基复合材料的XRD谱图Fig.1 XRD patterns of Mg2Ni matrix composites with different LaMg2Ni content after full hydrogenation
对比分析可知,添加LaMg2Ni 的复合材料在充分氢化后并未出现Mg2NiH0.3相,且随着LaMg2Ni 添加量的增加,Mg2Ni 基复合材料中LaH3衍射峰强度逐渐增大。由此可见,未添加LaMg2Ni的Mg2Ni在充分氢化后有部分转化为Mg2NiH0.3,而添加LaMg2Ni的Mg2Ni 在充分氢化后基本可以全部转化为Mg2NiH4,相同条件下后者氢化更为充分。
图2 为充分放氢后不同LaMg2Ni 含量的Mg2Ni基复合材料的XRD 谱图。当x=0 时,未添加LaMg2Ni 的Mg2Ni 在充分放氢后主要由Mg2Ni 组成,未见Mg2NiH4和Mg2NiH0.3相;当添加不同含量LaMg2Ni 后,x=10、x=20 和x=30 时Mg2Ni 基复合材料都主要由Mg2Ni 和LaH3组成。对比分析可知,充分放氢后,未添加LaMg2Ni的Mg2Ni在充分氢化后形成的Mg2NiH4和Mg2NiH0.3已全部转变为Mg2Ni,而添加LaMg2Ni 的复合材料在充分氢化后形成的Mg2NiH4已转变为Mg2Ni、LaH3依然存在且没有发现LaMg2Ni相,这主要是因为充氢过程中形成的LaH3具有较高的分解温度而无法在放氢过程中形成LaMg2Ni相[14]。

图2 充分放氢后不同LaMg2Ni含量的Mg2Ni基复合材料的XRD谱图Fig.2 XRD patterns of Mg2Ni matrix composites with different LaMg2Ni content after full dehydrogenation
图3 为充分放氢后不同LaMg2Ni 含量的Mg2Ni基复合材料的扫描电镜显微形貌。背散射电子形貌下,添加LaMg2Ni的Mg2Ni基复合材料中都弥散分布着白亮色细小颗粒,尺寸基本都在1 μm以下,且x=20 时白亮色细小颗粒分布最为均匀。表1 列出了图3 中不同区域的能谱分析结果。对比分析可知,亮白色区域(位置A、位置C和位置E)都含有较高含量的La,而颜色较暗的区域则主要含有Mg 和Ni 元素(La 元素含量相对较少)。结合图2 的XRD 谱图可知,亮白色区域主要为LaH3,而颜色较暗的区域主要为Mg2Ni 基体。此外,对比分析可知,随着Mg2Ni基复合材料中LaMg2Ni含量的增加,颜色较暗的Mg2Ni基体中的La元素含量逐渐增多(位置B、位置D和位置F),这也就说明球磨和吸氢/放氢过程中La 元素已经扩散至Mg2Ni 基体[15]。Mg2Ni 基复合材料中亮白色LaH3相的形成及Mg2Ni基体中扩散有La元素的结构有助于更好地发挥Mg2Ni基复合材料的催化性能[16]。

图3 充分放氢后不同LaMg2Ni含量的Mg2Ni基复合材料的SEM形貌Fig.3 SEM morphology of Mg2Ni matrix composites with different LaMg2Ni content after full dehydrogenation
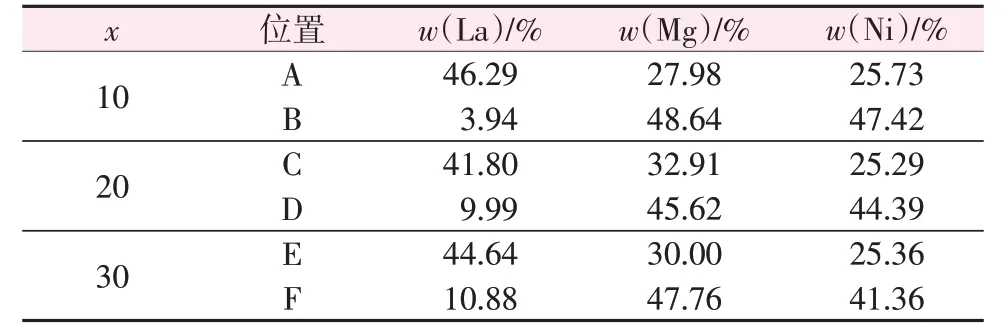
表1 图3中不同区域的能谱分析结果Table 1 Energy spectrum analysis results of different regions in Fig.3
2.2 储氢热力学与动力学性能
图4 为不同LaMg2Ni 含量的Mg2Ni 基复合材料的PCT曲线。当温度为250 ℃时,x=0、x=10、x=20和x=30 时复合材料的最大储氢容量分别为3.79%、3.66%、3.49%、3.28%,可见,Mg2Ni 基复合材料的最大储氢容量会随着LaMg2Ni 含量的增大而降低,这主要是因为添加LaMg2Ni 后Mg2Ni 基复合材料中的LaH3相不会参与吸氢和放氢反应[17],且由于LaMg2Ni含量越大Mg2Ni基复合材料中LaH3相越多,因此Mg2Ni 基复合材料的最大储氢容量会相应减小。当温度为200 ℃时,x=0、x=10、x=20 和x=30 时复合材料的可逆吸放氢容量分别为0.74%、2.42%、3.11%、2.19%,添加LaMg2Ni 的Mg2Ni 基复合材料的可逆吸放氢容量相对纯Mg2Ni 合金更大,且x=20 时Mg2Ni 基复合材料的储氢容量最大;此外,未添加LaMg2Ni 的Mg2Ni 基复合材料的最大储氢容量约为3.389%,而添加LaMg2Ni的Mg2Ni基复合材料的最大储氢容量都相对较低。

图4 不同LaMg2Ni含量的Mg2Ni基复合材料的PCT曲线Fig.4 PCT curves of Mg2Ni matrix composites with different LaMg2Ni content
根据范特霍夫方程可计算不同LaMg2Ni含量的Mg2Ni 基复合材料在不同温度下反应的平衡常数,表达式如下[18]:
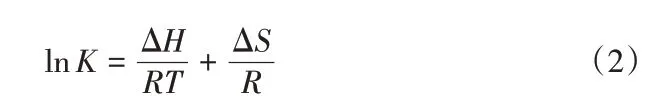
式中,K为平衡常数(放氢过程中为放氢平台压力);ΔH为焓变,kJ/mol;R为气体常数,8.314 J/(mol·K);T为温度,K;ΔS为熵变,J/(mol·K)。根据式(2)可线性拟合得到不同LaMg2Ni 含量的Mg2Ni 基复合材料的范特霍夫(Van't Hoff)曲线,见图5。x=0、x=10、x=20和x=30时,由式(2)和图5的数据,拟合得出Mg2Ni基复合材料的ΔH分别为64.49、58.14、59.32、60.19 kJ/mol,ΔS分别为122.9、83.67、86.22、87.86 J/(mol·K)。可见,添加LaMg2Ni的Mg2Ni基复合材料的ΔH和ΔS都小于纯Mg2Ni 合金,这主要是因为添加LaMg2Ni 后Mg2Ni 基复合材料中形成了能改善Mg2Ni 基复合材料吸氢/放氢热力学性能的LaH3相的缘故[19]。
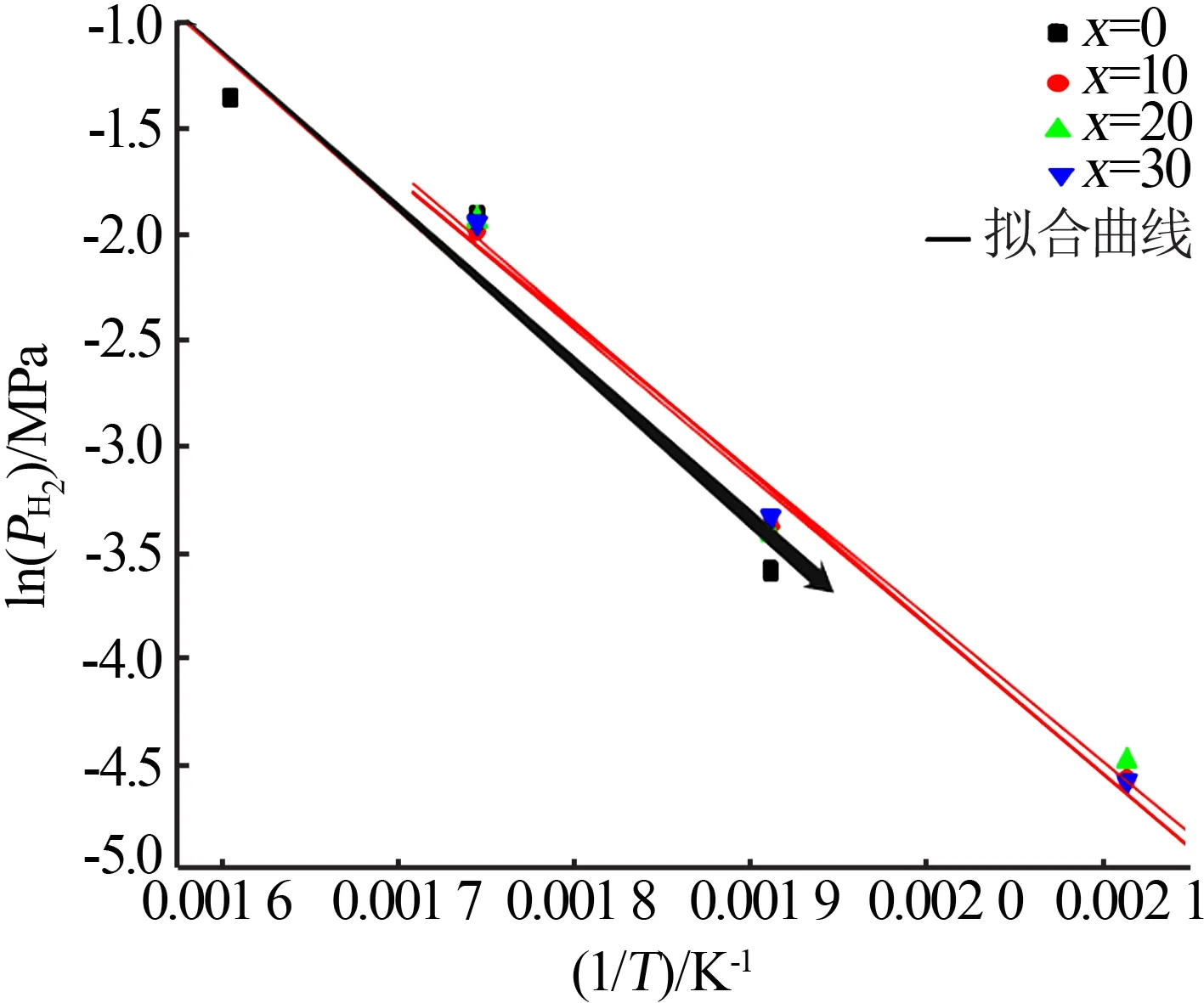
图5 不同LaMg2Ni含量的Mg2Ni基复合材料的范特霍夫(Van't Hoff)曲线Fig.5 Van't Hoff curve of Mg2Ni matrix composites with different LaMg2Ni content
图6 为不同LaMg2Ni 含量的Mg2Ni 基复合材料的等温吸氢/等温放氢曲线。从图6a 200 ℃等温吸氢曲线中可知,随着吸氢反应时间延长,不同LaMg2Ni 含量的Mg2Ni 基复合材料的吸氢容量都呈现先增加而后趋于稳定的趋势,在200 s内都已达到最大吸氢容量,且最大吸氢容量从小至大顺序为:x=30、x=20、x=10、x=0,即添加LaMg2Ni后Mg2Ni基复合材料的最大吸氢容量都相对纯Mg2Ni合金要小。从图6b 的250 ℃等温放氢曲线中可知,x=0、x=10、x=20、x=30 时Mg2Ni 基复合材料的最大放氢容量分别为0.48%、0.52%、0.57%、0.50%,最大放氢容量从大至小顺序为:x=20、x=10、x=30、x=0,即添加LaMg2Ni 后Mg2Ni 基复合材料的最大放氢容量都大于纯Mg2Ni合金,且x=20 时Mg2Ni 基复合材料具有最高的最大放氢容量。
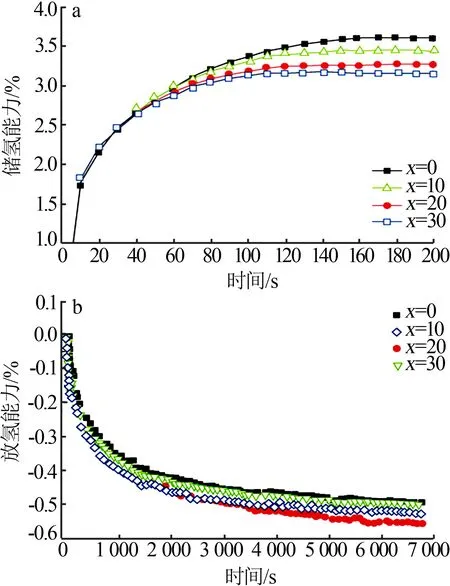
图6 不同LaMg2Ni含量的Mg2Ni基复合材料的等温吸氢/等温放氢曲线Fig.6 Isothermal hydrogen absorption/desorption curves of Mg2Ni matrix composites with different LaMg2Ni contents
图7为250 ℃下不同LaMg2Ni含量的Mg2Ni基复合材料的放氢Jander拟合曲线。通过Jander方程对Mg2Ni 基复合材料的放氢曲线进行三维扩散拟合[20],x=0、x=10、x=20 和x=30 时Mg2Ni 基复合材料的速率常数k分别为6.83×10-5、7.29×10-5、11.23×10-5和9.71×10-5。可见,随着LaMg2Ni 含量的增加,Mg2Ni 基复合材料放氢过程中的速率常数呈现先增加后减小的趋势,在x=20 时取得速率常数最大值。添加LaMg2Ni 的Mg2Ni 基复合材料的扩散性能都优于纯Mg2Ni 合金,这主要是因为添加LaMg2Ni 的Mg2Ni基复合材料会在充氢/放氢过程中形成提供氢扩散通道的LaH3相,且由于x=20时Mg2Ni 基复合材料中LaH3相分布相对x=10 和x=30 时更加均匀,其对Mg2Ni 基复合材料扩散性能的改善作用更为明显,速率常数k值相对更大。
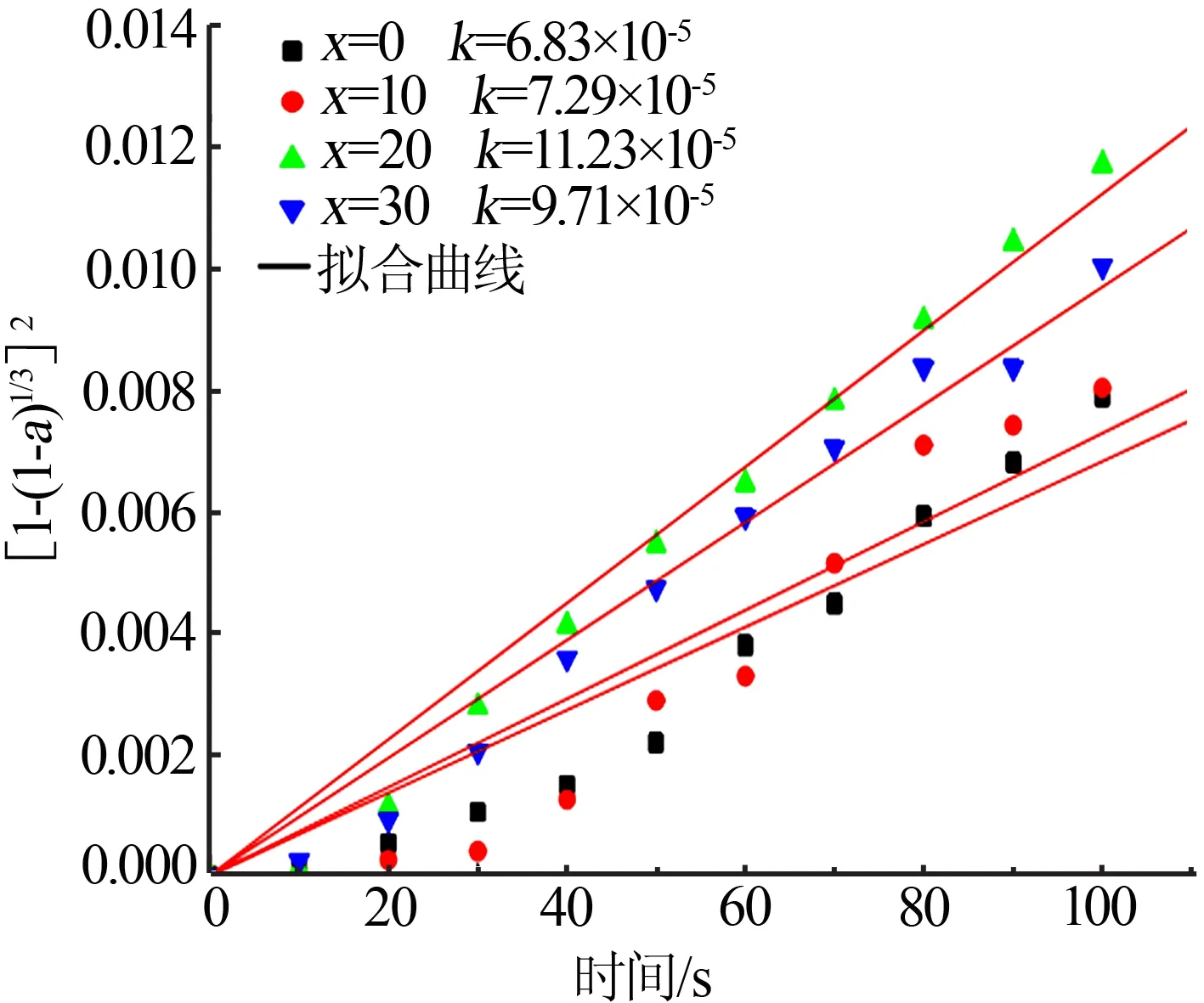
图7 250 ℃下不同LaMg2Ni含量的Mg2Ni基复合材料的放氢Jander拟合曲线Fig.7 Jander fitting curve of hydrogen evolution of Mg2Ni matrix composites with different LaMg2Ni content at 250 ℃
3 结论
1)充分吸氢后,未添加LaMg2Ni的Mg2Ni合金主要由Mg2NiH4和Mg2NiH0.3组成,而添加不同含量LaMg2Ni 的Mg2Ni 基复合材料都主要由Mg2NiH4和LaH3组成。充分放氢后,未添加LaMg2Ni的Mg2Ni合金主要由Mg2Ni 组成,添加不同含量LaMg2Ni 的Mg2Ni基复合材料主要由Mg2Ni和LaH3组成。
2)添加LaMg2Ni 的Mg2Ni 基复合材料中都弥散分布着白亮色LaH3颗粒,且x=20时白亮色细小颗粒分布最为均匀。随着Mg2Ni 基复合材料中LaMg2Ni含量的增加,颜色较暗的Mg2Ni 基体中的La 元素含量逐渐增多,表明球磨和吸氢/放氢过程中La 元素已经扩散至Mg2Ni基体。
3)Mg2Ni 基复合材料的最大储氢容量会随着LaMg2Ni 含量的增大而降低,添加LaMg2Ni 的Mg2Ni基复合材料的可逆吸放氢容量相对纯Mg2Ni合金更大。不同LaMg2Ni 含量的Mg2Ni 基复合材料的最大吸氢容量从大至小顺序为:x=0、x=10、x=20、x=30,最大放氢容量从大至小顺序为:x=20、x=10、x=30、x=0,即添加LaMg2Ni 后Mg2Ni 基复合材料的储氢性能得到改善,且x=20 时Mg2Ni 基复合材料具有最高的储氢容量。