新佐剂新流二联浓缩苗与常规新流二联苗肉鸡免疫效果比较
张 亚,段佳蕾,刘武杰,薛景景,胡小飞,田 辉,张盼涛 , 田克恭
(1.国家兽用药品工程技术研究中心,洛阳 471000;2.普莱柯生物工程股份有限公司,洛阳 471000)
鸡新城疫(newcastle disease, ND)是由鸡新城疫病毒(Newcastle disease virus, NDV)强毒株引起的一种急性、热性、高度接触性传染疾病,该病对养禽业造成巨大的经济损失,尤其对亚洲、中东和非洲的危害最为严重[1]。H9N2禽流感病毒(Avian influenza virus, AIV)是另一种对家禽危害严重,流行最为广泛的一种低致病性AIV[2],可引起蛋鸡产蛋数量和质量下降,与其他病原共感染时可造成较高的发病率和死亡率[3-6]。疫苗免疫是预防和控制鸡新城疫和H9亚型禽流感的有效措施之一。目前实际生产中普遍使用ND活疫苗和灭活疫苗对ND进行免疫防控,用于生产ND活疫苗的毒株有低毒力的HB1株、La Sota株、Clone30株、VG/GA株、V4/HB92克隆株,而灭活疫苗毒株主要是La Sota株[7],近年来也有NDV基因Ⅶ型相关灭活疫苗用于临床。H9亚型禽流感灭活疫苗的广泛应用使得该病的流行得到有效控制,由于禽流感病毒HA基因易变异[8-10],因此需根据流行趋势的变化,及时更新疫苗毒株。
基于矿物油为佐剂的常规鸡新城疫、H9亚型禽流感二联灭活疫苗是商品肉鸡养殖生产中应用最多的疫苗之一,对控制肉鸡ND和H9亚型AI发挥了重要作用。但因肉鸡的饲养周期短,尤其是快大型白羽肉鸡42日龄即可出栏,常规疫苗抗原浓缩倍数低,并且为了保持疫苗的稳定性,添加有一定比例的硬脂酸铝,因此免疫剂量大,疫苗粘度大,注射部位易出现较重的副反应,出栏屠宰时个别鸡只仍能在疫苗注射部位观察到未吸收疫苗。疫苗中不可代谢的矿物油佐剂成分不仅影响鸡肉品质,同时存在着一定的食品安全隐患[7]。本研究基于禽用新型无铝油性佐剂,结合高倍浓缩的NDV La Sota株和H9N2亚型禽流感SZ株抗原制备新型佐剂鸡新城疫-H9亚型禽流感二联浓缩灭活疫苗。该生产工艺制备的疫苗免疫剂量小,抗体产生快,吸收代谢快,更适合应用于商品肉鸡的疫病防控。
1 材料与方法
1.1 病毒株和检测抗原 鸡新城疫病毒La Sota株、H9亚型禽流感病毒SZ株均由国家兽用药品工程技术研究中心分离、鉴定、保存;鸡新城疫北京株强毒购自中国兽医药品监察所;鸡新城疫病毒血凝抑制试验抗原(HI)购自中国兽医药品监察所;禽流感病毒H9亚型血凝抑制试验抗原(SZ株),由国家兽用药品工程技术研究中心制备。
1.2 原辅材料 禽用新型无铝油性佐剂、常规白油佐剂、甲醛均由普莱柯生物工程股份有限公司GMP车间提供。
1.3 试验动物和试验场所 SPF鸡胚由购自济南斯帕法斯家禽有限公司的SPF鸡种蛋孵化。1日龄商品代AA白羽肉鸡购自洛阳周边某孵化场,于普莱柯生物工程股份有限公司禽用负压区动物房饲养至7日龄开展试验。
1.4 疫苗制备 鸡新城疫病毒La Sota株、H9亚型禽流感病毒SZ株利用无菌生理盐水分别进行10 000倍稀释,0.2 mL/胚接种10~11日龄的SPF鸡胚。接胚后收取72~96 h存活和死亡鸡胚的尿囊液,收获的两种病毒鸡胚尿囊液对1%鸡红细胞的血凝效价应不低于8log2,病毒含量应不低于108.0EID50/0.1 mL,每种鸡胚尿囊液利用超滤浓缩装置分别进行2倍和4倍浓缩。对浓缩后的鸡胚尿囊液使用终浓度为0.2%的甲醛溶液37℃水浴灭活18 h,灭活检验合格后用于疫苗制备。
疫苗的制备:新佐剂新流二联浓缩苗抗原部分由4倍浓缩的鸡新城疫抗原和H9亚型禽流感抗原等体积混合而成;常规新流二联苗抗原部分由4倍浓缩的鸡新城疫抗原和H9亚型禽流感抗原等体积混合而成;均按照96份抗原加入4份吐温-80混合均匀作为水相,水相和油相比例为1∶2乳化制备疫苗。新佐剂新流二联浓缩苗油相使用新型无铝油性佐剂,常规新流二联苗使用常规白油佐剂。
1.5 免疫分组及试验设计 140羽7日龄AA肉鸡分为三组,第1组和第2组均为50羽/组,第3组为40羽。第1组0.15 mL/羽免疫新佐剂新流二联浓缩苗,第2组0.3 mL/羽免疫常规新流二联苗,两种疫苗均为颈背部皮下免疫。第3组为空白对照组,不免疫任何疫苗。
1.6 疫苗安全性评价 免疫后每日观察并记录免疫鸡与对照鸡的精神、采食、饮水等状况,观察至试验结束。另外,每日随机抽取20羽免疫鸡,观察疫苗注射部位是否有肿胀、硬结、化脓等不良炎性反应,连续观察14 d。分别于疫苗免疫后第7、14、21、28 d,从免疫组和对照组中各随机抽取3羽剖杀,检查注射局部变化和疫苗吸收情况。
同时,为评价疫苗免疫对肉鸡生长性能的影响,分别于疫苗接种当日、免后第14 d、免后35 d随机从免疫组和对照组中各抽取15羽称重,并统计结果。
1.7 疫苗有效性评价 (1)抗体检测 免疫当日、免疫后第7 、10、14、21、35 d从免疫鸡和对照鸡中随机各取10羽采血并分离血清,分别检测NDV HI和H9 AIV HI抗体。(2)攻毒保护 于免疫后第7 d,从两个免疫组中各抽取10羽,从空白对照鸡中抽取5羽进行NDV攻毒保护效果评价,通过肌肉注射途径进行新城疫病毒北京株攻毒,105.0ELD50/羽,攻毒后连续观察14 d,当出现①死亡;②食欲明显下降,甚至废绝;③嗜睡、头颈、尾部节律性震颤等神经症状任一项症状即判为发病。攻毒后第5 d采集泄殖腔棉拭子接种10~11日龄SPF鸡胚进行病毒分离,每个样品按照0.1 mL/胚的剂量接种5枚鸡胚,接种后培养120 h,测定每胚尿囊液的HA效价。5枚鸡胚只要有1枚HA效价不低于1∶16(微量法),即可判定病毒分离阳性。对于病毒分离阴性的样品,应盲传1代后再进行判定。同时,从两个免疫组中各抽取10羽,从空白对照鸡中抽取5羽进行H9亚型禽流感攻毒保护效果评价,通过静脉注射途径进行禽流感病毒(H9亚型)SZ株攻毒,每羽接种107.0EID50/200 μL,H9N2亚型禽流感病毒属于低致病力病毒,感染SPF鸡后无任何临床症状,仅通过排毒检测评价疫苗的免疫攻毒保护效果。攻毒后第5 d采集喉头和泄殖腔棉拭子,每只鸡两种棉拭子混合后作为一个样品接种10~11日龄SPF鸡胚进行病毒分离,病毒分离方式及结果判定同新城疫病毒。
2 结果
2.1 疫苗安全性评价结果 7日龄AA肉鸡免疫新佐剂新流二联浓缩苗和常规新流二联苗后整个试验期内精神、采食、饮水与不免疫对照鸡均无明显差异。疫苗注射后14 d内,每日随机抽取20羽免疫鸡,检查注射部位均无硬结、肿胀和溃烂发生。免疫后第7、14、21、28 d从免疫组和不免疫对照鸡中各随机抽取3羽剖杀,检查疫苗注射部位均无硬结、脓肿、溃烂和坏死发生,新佐剂新流二联浓缩苗免疫后14 d疫苗即完全吸收,眼观无疫苗存在,而常规新流二联苗免疫后21 d仍有少量未吸收疫苗,免疫后28 d疫苗吸收完全。结果详见表1。于疫苗接种当日、免后14和35 d,从免疫鸡及对照鸡中随机各取15羽称重,结果显示,免疫鸡与对照鸡在同一时间点的体重无明显差异,表明鸡群在免疫后其生长性能均未受到影响,疫苗安全性良好。结果详见图1。
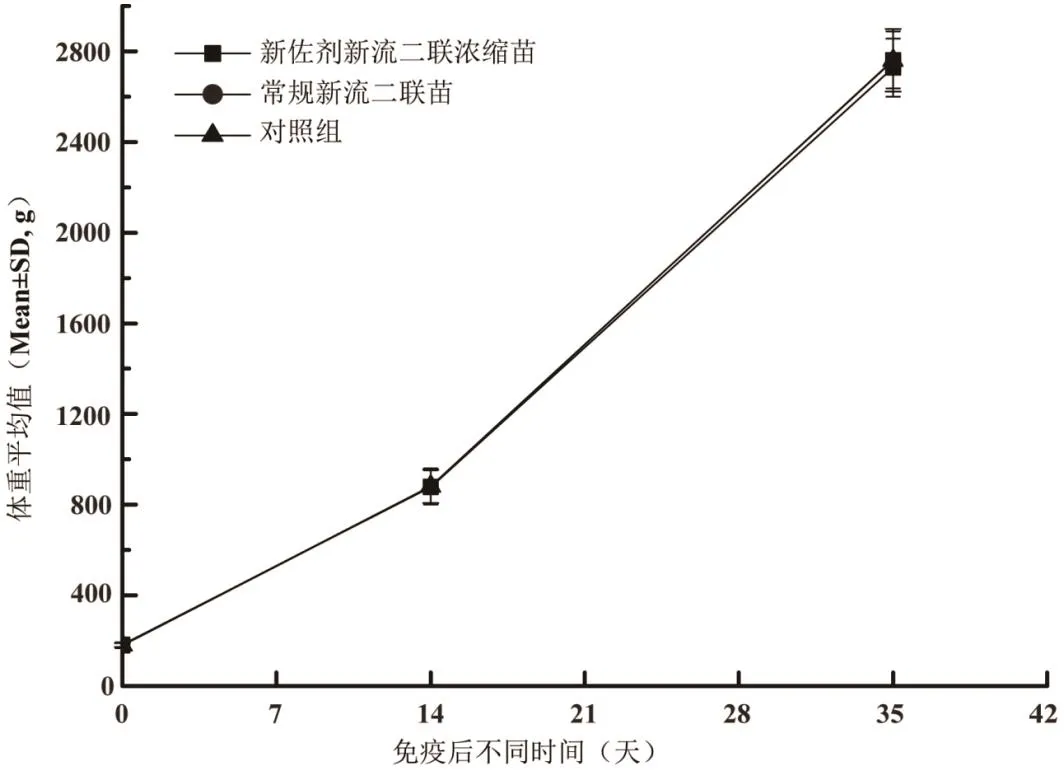
图1 AA肉鸡不同疫苗免疫后体重变化Fig.1 Body weight changes of AA broilers immunized with different vaccines

表1 AA肉鸡不同疫苗免疫后疫苗吸收情况Table 1 Absorption of AA broilers after immunization with different vaccines
2.2 抗体检测结果 免疫当日、免疫后第7、10、14、21、35 d从两种疫苗免疫鸡和对照鸡中各随机取10羽采血并分离血清,分别检测ND HI和H9亚型AI HI抗体。结果显示,不免疫对照组ND和H9 AI HI抗体免疫当天(7日龄)分别为4.2±1.4 log2和3.8±1.2 log2,随着日龄增大,母源抗体缓慢降低,21日龄时已低于2.0 log2。新佐剂新流二联浓缩苗和常规新流二联苗免疫组肉鸡免疫后ND和H9 AI HI抗体缓慢上升,免疫后第21 d(28日龄)抗体水平达到或接近高峰,并一直持续到42日龄(免疫后35 d)。新佐剂新流二联浓缩苗ND和H9 AI的HI抗体产生速度优于常规新流二联苗,前者免疫后第7 d ND和H9 AI的HI抗体分别为6.1±0.88 log2和6.8±0.63 log2,优于常规新流二联苗的4.7±1.2 log2和5.2±0.79 log2。疫苗免疫后21~35 d,新佐剂新流二联浓缩苗ND和H9 AI的HI抗体达到高峰,分别为8.4±0.7 log2和8.7±0.82 log2,高于常规新流二联苗的7.5±1.3 log2和8.1±1.0 log2。结果详见图2、图3。
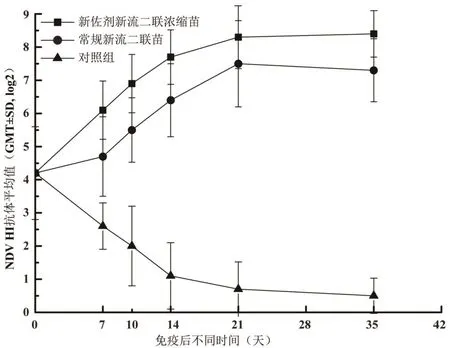
图2 肉鸡免后不同时间NDV HI抗体效价Fig.2 Titer of NDV HI antibody in broilers at different time after immunization

图3 肉鸡免后不同时间H9 AIV HI抗体效价Fig.3 Titer of H9 AIV HI antibody in broilers at different time after immunization
2.3 攻毒保护结果 免疫后第7 d,从两种疫苗免疫鸡中各随机抽取20只,连同对照鸡10只分别进行新城疫病毒北京株和禽流感病毒(H9亚型)SZ株攻毒保护试验,攻毒时每个病原免疫组攻10羽,不免疫对照组攻5羽。结果显示,新城疫攻毒后对照组全部死亡,新佐剂新流二联浓缩苗免疫组鸡无发病和死亡,病毒分离阳性率为0(0/10)。常规新流二联苗免疫组鸡无死亡,30%(3/10)表现出NDV特征性临床症状,病毒分离阳性率为60%(6/10)。同时,免疫后第7 d对两种疫苗免疫鸡进行H9亚型禽流感病毒攻毒,攻毒对照组病毒分离阳性率100%(5/5),新佐剂新流二联浓缩苗免疫组鸡病毒分离阳性率为0(0/10),常规新流二联苗免疫组鸡病毒分离阳性率为50%(5/10)。上述攻毒保护结果表明,新佐剂新流二联浓缩苗免疫后第7 d即可为免疫鸡提供针对NDV和H9亚型禽流感的完全攻毒保护,免疫效果优于常规新流二联苗。结果详见表2。
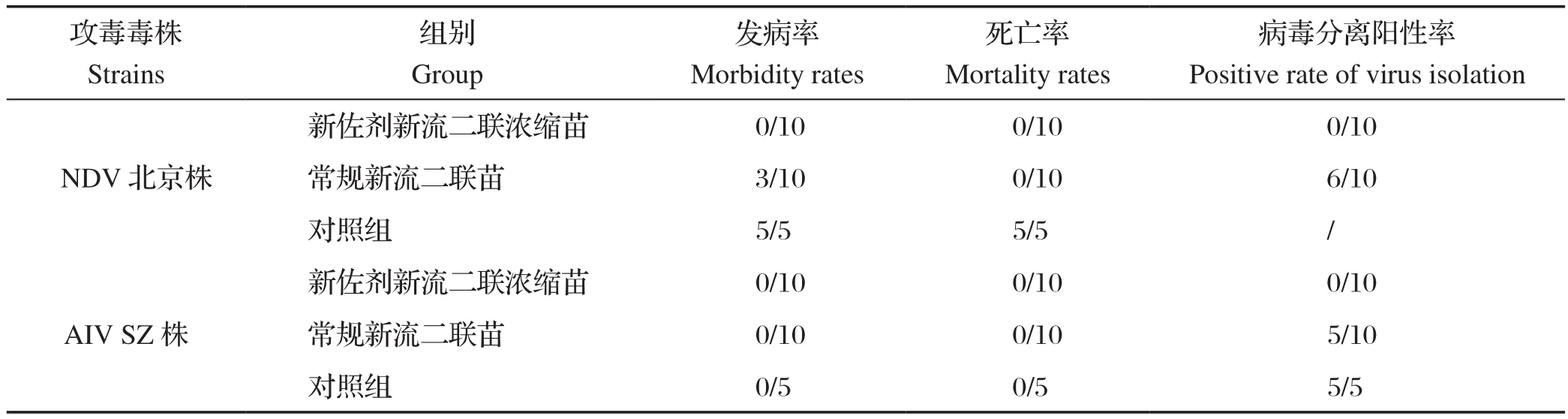
表2 AA肉鸡免后7 d NDV和H9N2 AIV攻毒保护效果Table 2 Protection effect of NDV and H9N2 AIV challenge on AA broilers 7 days after immunization
3 讨论
鸡新城疫和H9亚型禽流感是严重危害养禽业的重要疫病,疫苗免疫作为预防这两种疾病的重要措施被广泛应用。常规油乳剂鸡新流二联灭活疫苗抗原含量低,免疫剂量大,免疫后抗体产生速度慢、滴度低,尤其是针对快大型白羽肉鸡免疫效果更不理想。同时为了保持疫苗稳定性,常规油乳剂疫苗中添加有一定比例的硬脂酸铝[11-12],疫苗粘度可达50~100 cP,免疫应激大,接种部位易出现肉芽肿,引起肿胀、硬结和坏死,造成疫苗吸收慢,延缓抗体产生速度,增加疫苗免疫后的空白期。在目前尚无免疫效果理想的水佐剂可用于肉鸡灭活疫苗生产的情况下,常规的矿物油佐剂疫苗依然是肉鸡养殖生产的必需品,亟需对其免疫剂量、吸收速度、抗体产生速度进行改进。
抗原浓缩是提高疫苗单位体积内抗原含量的重要手段,使用浓缩苗可降低人力和物力,节省成本、较少应激、提高鸡群质量,并且浓缩苗抗体产生速度快、滴度高、持续时间长[13-15]。本研究使用“粗滤+超滤”的抗原浓缩工艺,实现了NDV La Sota株、H9 AIV SZ株抗原4倍的超强浓缩。为改善常规油乳剂灭活苗粘度大的问题,本研究用人工合成的异甘露醇单油酸脂替代硬脂酸铝,与硫酸葡聚糖、卵磷脂及矿物油等成分进行适当配比制备禽用新型无铝油性佐剂,该新型佐剂制备的鸡新流二联灭活疫苗粘度低至10~20 cP,解决了常规矿物油佐剂疫苗粘度高,易引起免疫副反应的不足,并可加快疫苗中抗原在机体内的释放速度,加快抗体产生速度,0.15 mL/羽的使用剂量,免疫后第7 d NDV和H9亚型禽流感的HI抗体即可达到6.1 log2和6.8 log2,抗体水平和均匀度均优于常规鸡新流二联苗。新佐剂鸡新流二联浓缩苗免疫后第7 d即可为免疫鸡提供针对NDV和H9N2禽流感病毒的完全攻毒保护,免疫鸡不发病、不排毒,攻毒保护效果明显优于常规鸡新流二联苗。
本研究由于免疫鸡数量少,常规油佐剂新流二联疫苗免疫后未出现硬结、肿胀等不良反应,新型无铝油性佐剂与高倍浓缩抗原制备的二联浓缩苗优势未能显现出来,但免疫剂量由0.3 mL/羽降低为0.15 mL/羽,免疫后第14 d疫苗即可吸收完全的优势对肉鸡生产意义重大。对饲养周期长的种鸡和蛋鸡,整个饲养期疫苗免疫次数可高达30余次,不仅造成鸡体应激反应大,同时耗时、费力、增加养殖成本。新型无铝油性佐剂与高倍浓缩抗原的有机结合和应用推广,可解决当前常规禽用油乳剂灭活疫苗存在的不足,推进养禽业的健康发展。

